漾濞泡核桃青皮中二芳基庚烷类成分研究
李冬梅++彭友伦++刘光明

[摘要]综合运用硅胶、Sephadex LH20、MCI等柱色谱方法对漾濞泡核桃青皮的乙酸乙酯部位化学成分进行了研究,并利用各种波谱技术(MS,1HNMR,13CNMR,2DNMR)对化合物结构进行了鉴定。结果从乙酸乙酯部位分离得到4个二芳基庚烷类化合物,分别鉴定为:二氢枫杨素(1),1(4′羟基苯基)7(3″甲氧基苯基) 3′,4″环氧3α庚醇(2),枫杨素(3)和1(4′羟基苯基)7(3″甲氧基4″羟基苯基)3α庚醇(4)。其中,化合物1(二氢枫杨素,dihydropterocarine)为新化合物,化合物2~4首次从该植物中分离得到。
[关键词]泡核桃;青皮;化学成分;二芳基庚烷类
Study on diarylheptanoids from green peel of Juglans sigillata
LI Dongmei*, PENG Youlun, LIU Guangming
(College of Pharmacy and Chemistry, Dali University, Dali 671000, China)
[Abstract]The chemical constituents from green peel of Juglans sigillata were isolated by column chomatographies over silica gel, Sephadex LH20, and MCI. Four diarylheptanoids were isolated and their structures were characterized as dihydropterocarine(1), 3′,4″epoxy1(4′hydroxyphenyl)7(3″methoxylphenyl)heptan3αol(2), pterocarine(3), and 1(4′hydroxyphenyl)7(3″methoxy4″hydroxyphenyl)heptan3αol(4) Compound 1 is a new compound, named as dihydropterocarine Compounds 24 were isolated from the plant of J. sigillata for the first time.
[Key words]Juglans sigillata; green peel; chemical constituents; diarylheptanoids
泡核桃Juglans sigillata D系胡桃科胡桃屬植物,又名茶核桃(云南)、铁核桃,产于云南、贵州、四川西部、西藏雅鲁藏布江中下游。胡桃属植物具有悠久的药用历史,胡桃楸青皮始载于宋《开宝本草》,后各代医家多以其清热解毒、祛风疗癣、止痛止痢等功效入药。核桃青皮又名青龙衣,为胡桃科植物的青果皮,未成熟时包裹在果实核外,果实成熟后自然脱落并变为褐色[12]。目前漾濞泡核桃青皮的研究报道相对较少,主要是对其化学成分及挥发性成分进行了研究[3 4]。漾濞泡核桃在大理州种植面积较广,泡核桃青皮产量较高、资源丰富,对其进行研究,可为进一步开发和利用该植物资源提供科学依据。
二芳基庚烷类化合物普遍存在于胡桃属植物中,是胡桃属植物中一类重要的抗肿瘤活性成分[58]。该类化合物的结构特点为:2个特征性很强的芳香环与七碳线型长链相连。根据其化学结构特点可分为3种结构亚类:即线型二芳基庚烷(Ⅰ型)、大环二芳基庚烷(Ⅱ型)和大环二芳基环氧庚烷(Ⅲ型),在胡桃属植物中目前发现的二芳基庚烷类主要为Ⅰ型和Ⅲ型[89]。
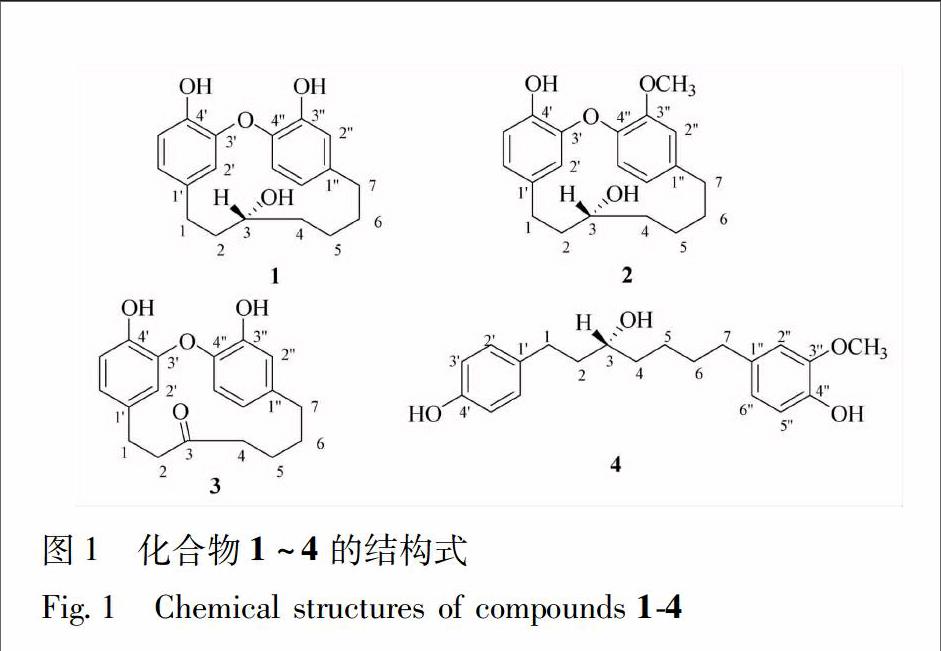
本课题组主要对漾濞泡核桃青皮乙酸乙酯部位的化学成分进行了研究,从中分离得到4 个二芳基庚烷类化合物,分别鉴定为:二氢枫杨素(1),1(4′羟基苯基)7(3″甲氧基苯基) 3′,4″环氧3α庚醇(2),枫杨素(3)和1(4′羟基苯基)7(3″甲氧基4″羟基苯基)3α庚醇(4)。其中,化合物1(二氢枫杨素,dihydropterocarine)为新化合物,化合物2~4为首次从该植物中分离得到,见图1。
1材料
梅特勒1/1万电子分析天平;旋转蒸发仪(BUCHI Rotavapor R210);低温冷却循环泵(巩义市予华仪器有限公司);Sephadex LH20(Amersham Biosciences,Sweden);MCIgel CHP20P(日本三菱化学公司)。所用试剂除石油醚、氯仿、丙酮、乙酸乙酯、甲醇为工业纯,经重蒸后使用外,其余均为分析纯。
实验用漾濞泡核桃青皮采自云南省大理州漾濞县,经大理大学药学与化学学院生药教研室周浓副教授鉴定为胡桃科胡桃属植物泡核桃J sigillata的青皮,样品标本保存于大理大学药学与化学学院有机药化教研室。
2提取与分离
干燥泡核桃青皮 10 kg,粉碎后用75%甲醇加热回流提取2次,每次2 h,提取液经减压浓缩后得到浸膏856 g。浸膏经硅胶柱色谱,依次用石油醚、乙酸乙酯和甲醇洗脱并分别回收溶剂,得到乙酸乙酯部位浸膏960 g。乙酸乙酯部位浸膏经丙酮溶解后,用2倍量硅胶拌样,20倍量硅胶(200~300目)装柱进行柱色谱,氯仿甲醇(20∶1~2∶1)梯度洗脱,洗脱液经TLC检测后合并相似组分,得P1~P10共10个组分。其中P2(123 g),经MCI柱色谱,50%~100%甲醇梯度洗脱并收集各个流分,经TLC检测后合并相似流分,得P21~P28共8个组分,其中P26经反复硅胶柱色谱,石油醚乙酸乙酯(10∶1~1∶1)梯度洗脱,分离得到化合物1(510 mg)和化合物2(151 mg)。P25经硅胶柱色谱,氯仿甲醇(20∶1~5∶1)梯度洗脱,洗脱液经TLC检测后合并相似组分,得P251~P257共7个组分,其中P252经硅胶柱色谱,石油醚乙酸乙酯(10∶1~1∶1)梯度洗脱,再经Sephadex LH20柱色谱(氯仿甲醇 1∶1)得化合物3(54 mg)。P253经硅胶柱色谱,石油醚乙酸乙酯(10∶1~1∶1)梯度洗脱,分离得到化合物4(65 mg)。endprint
3结构鉴定
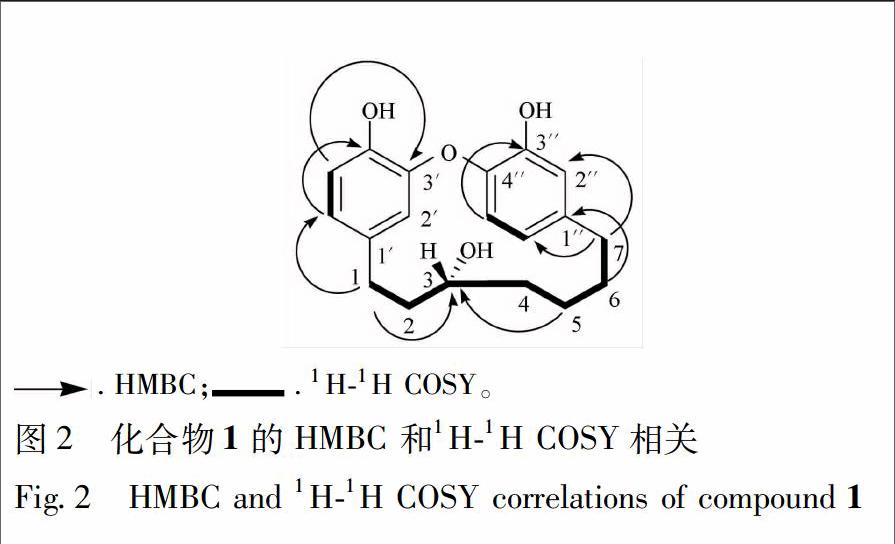
化合物1白色粉末,HRESIMS m/z 315151 5[M+H]+,分子式为C19H22O4。UV光谱在2825,2035 nm处有最大吸收,[α]163D-111(c 021,MeOH),IR谱提示有羟基(3 438,1 267 cm-1),苯环(2 929,1 598,1 514,1 503,1 500 cm-1)。10%硫酸乙醇溶液TLC顯色呈灰色。在化合物1的1HNMR谱(CD3COCD3)中,根据氢原子峰的裂分情况及偶合常数,推断化合物1结构中含有2个1,3,4三取代苯环[ δH:563(1H,d,J =18 Hz),658(1H,d,J=80 Hz),643[(1H,dd,J=80,18 Hz)]和[(δH:673(1H,d,J=18 Hz),685(1H,d,J=80 Hz),669(1H,dd,J=80,18 Hz)]。另外,在13CNMR和DEPT谱中,观测到有12个芳香碳原子信号(δC 110~150),6个亚甲基碳原子信号(δC 20~40)和1个叔碳原子信号(δC 717),分析13CNMR 和 DEPT 谱可知,化合物1结构中含有2个苯环,6个CH2和1个连氧叔碳原子,从而推测化合物1为二芳基庚烷类化合物。化合物1的波谱数据与文献[1011]报道的枫杨素对照发现,主要区别在于枫杨素中δ 210左右的羰基碳原子信号消失,而出现了1个δ 717的叔碳原子信号,因此该化合物应为枫杨素的还原产物,通过对化合物1的HSQC和HMBC分析,见图2,进一步证明了该化合物的结构为枫杨素3羰基的还原产物。
通过与已知化合物3′,4″epoxy1(4′hydroxyphenyl)7(3″methoxylphenyl)heptane3hydroxy[6]对比发现,该已知化合物与化合物1的区别仅仅只在C3″上的取代情况不同,化合物1的C3″上为羟基取代,而已知化合物3′,4″epoxy1(4′hydroxyphenyl)7(3″methoxylphenyl)heptane3hydroxy的C3″为甲氧基取代。同时,该已知化合物和化合物1的结构中都只存在1个手性碳原子,即C3的立体构型决定了2个化合物的绝对构型。该已知化合物
的旋光度为[α]25D-3907(c 024,MeOH),而化合物1的旋光度为[α]163D-111(c 021,MeOH),二者均为左旋光性,因此推断化合物1的绝对构型与已知化合物相同,即为R构型,3位为αOH。因此,将其结构鉴定为:(R)1(4′羟基苯基)7(3″羟基苯基)3′,4″环氧3α庚醇,并将其命名为二氢枫杨素(dihydropterocarine)。同时,通过对化合物1的HSQC和HMBC分析,见图2,对化合物1的波谱数据进行了归属,其波谱数据见表1。
化合物2浅黄色油状物,EIMS m/z 328 [M]+,分子式为C20H24O4。1HNMR(CDCl3,400 MHz)δ:285,281(2H,ddd,J=22,96,164 Hz,H1),143(2H,m,H2),320(1H,m,H3),182,145(2H,m,H4),150(2H,m,H5),196( 2H,m,H6),282,251(2H,m,H7),562(1H,d,J=20 Hz,H2′ ),667(1H,d,J=80 Hz,H5′),656(1H,dd,J=20,80 Hz,H6′),696(1H,d,J=20 Hz,H2″),703(1H,d,J=80 Hz,H5″),688(1H,dd,J=20,80 Hz,H6″),373(3H,s,3″OCH3),562(1H,br s,4′OH)。13CNMR(CDCl3,100 MHz)δ:282(C1),419(C2),78 4(C3),434(C4),201(C5),287(C6),363(C7),1339(C1′),1126(C2′),1479(C3′),1431(C4′),1152(C5′),1221(C6′),1402(C1″),1150(C2″),1524(C3″),1427(C4″),1240(C5″),1220(C6″),562(3″OCH3)。以上波谱数据与文献报道的3′,4″epoxy1(4′hydroxyphenyl)7(3″methoxylphenyl)heptane3hydroxy[6,10]对比,故化合物2鉴定为1(4′羟基苯基)7(3″甲氧基苯基) 3′,4″环氧3α庚醇。
化合物3白色粉末,EIMS m/z 312 [M]+,分子式为C19H20O4。根据化合物3的DEPT谱可知含有2个苯环,6个CH2和1个羰基碳,推断该化合物为二芳基庚烷类化合物。1HNMR(CD3COCD3,400 MHz)δ:266(2H,m,H1),215(2H,t,J=16 Hz,H2),173(2H,m,H4),137(2H,m,H5),146(2H,m,H6),253(2H,m,H7),545(1H,d,J=15 Hz,H2′),671(1H,d,J=81 Hz,H5′),642(1H,dd,J=80,15 Hz,H6′),678(1H,d,J=16 Hz,H2″),660(1H,dd,J=80,18 Hz,H5″),668(1H,dd,J=80,16 Hz,H6″)。13CNMR(CD3COCD3,100 MHz)δ:278(C1),412(C2),2098(C3),468(C4),194(C5),278(C6),361(C7),1340(C1′),1133(C2′),1489(C3′),1447(C4′),1160(C5′),1223(C6′),1408(C1″),1183(C2″),1490(C3″),1410(C4″),1236(C5″),1225(C6″)。以上波谱数据与文献报道的枫杨素[11]对比,故化合物3鉴定为1(4′羟基苯基)7(3″羟基苯基)3′,4″环氧3庚酮,即枫杨素(pterocarine)。endprint
化合物4白色粉末,EIMS m/z 33018[M] +,分子式为C20H26O4。1HNMR(CD3COCD3,400 MHz)δ:263(2H,m,H1),335(1H,m,H3),252(2H,t,J=75 Hz,H7),166143(8H,m,H2,4,6,5),702(2H,d,J=84 Hz,H2′,6′),674(2H,d,J=84 Hz,H3′,5′),679(1H,d,J=18 Hz,H2″),671(1H,d,J=80 Hz,H5″),662(1H,dd,J=80,18 Hz,H6″),379(3H,s,3″OCH3)。13CNMR(CD3COCD,100 MHz)δ:319(C1),407(C2),708(C3),382(C4),261(C5),328(C6),362(C7),1349(C1′),1301(C2′),1159(C3′),1563(C4′),1159(C5′),1301(C6′),1342(C1″),1129(C2″),1482(C3″),1454(C4″),1156(C5″),1215(C6″),562(3″OCH3)。以上波譜数据与文献[12]报道的1(4′hydroxyphenyl)7(3″methoxy4″hydroxyphenyl)heptane3αhydroxy对比,故化合物4鉴定为1(4′羟基苯基)7(3″甲氧基4″羟基苯基)3α庚醇。
漾濞泡核桃青皮具有丰富的植物资源,本课题组从漾濞泡核桃青皮的乙酸乙酯部位分离得到4个二芳基庚烷类化合物,二芳基庚烷类化合物是胡桃属植物中一类重要的抗肿瘤活性成分。本研究将为漾濞泡核桃青皮的进一步抗肿瘤活性研究奠定物质基础。
[参考文献]
[1]中国科学院中国植物志编委会中国植物志 [M] 北京:科学出版社,1979:31.
[2]全国中草药汇编编写组 全国中草药汇编[M] 北京:人民卫生出版社,1975:186.
[3]李冬梅,彭友伦,刘光明 漾濞泡核桃青皮化学成分的研究[J] 中草药,2015,46(7):962.
[4]李寅姗,李冬梅,刘熙,等. 漾濞泡核桃青皮中脂溶性成分的GCMS分析[J] 天然产物研究与开发,2012(24):28.
[5]Lee K S, Li G, Kim S H, et al. Cytotoxic diarylheptanoids from the roots of Juglans mandshurica[J] J Nat Prod, 2002, 65(11):1707
[6]Li G, Xu M L, Choi H G, et al. Four new diarylheptanoids from the roots of Juglans mandshurica[J] Chem Pharm Bull, 2003, 51(3):262
[7]李英春 胡桃楸叶的化学成分及其抗肿瘤活性的研究[D] 长春:吉林大学,2007.
[8]周媛媛, 王栋 胡桃属植物抗肿瘤作用化学成分研究进展[J] 中国药房, 2010,21(43):4119.
[9]Lakshmi N R V, Ravinder K, Srinivasulu M, et al. Two new macro eyelid diaryl ether heptanoids from Boswelliaova ovalifoliolata [J] Chem Pharm Bull(Tokyo), 2003, 51(9):1081.
[10]周媛媛, 王栋 青龙衣中二芳基庚烷类化学成分的研究[J] 时珍国医国药,2009,20(8):1936.
[11]刘红兵 中草药东京枫杨Pterocarya tonkinesis(Franch)Dode抗肿瘤活性成分的研究[D] 青岛:中国海洋大学,2004.
[12]Li G, Seo C S, Lee S H, et al. Diarylheptanoids from the roots of Juglans mandshurica [J]Bull Korean Chem Soc, 2004, 25(3):397.
[责任编辑丁广治]endprint

