医用透明质酸钠凝胶中钨含量的分析研究及其安全性评价*
刘莉莉,骆红宇,施燕平,潘华先,秦洋
(1. 山东省医疗器械产品质量检验中心,济南 2501012.山东省医疗器械生物学评价重点实验室,济南 2501013. 山东恒信检测技术开发中心,济南 250101)
1 引 言
医用透明质酸钠凝胶为生物可降解高分子聚糖类生物材料,具有良好的生物相容性及生物学活性。所形成的高分子网状结构具有特有的流变学特性,使其在手术中可作为手术工具和保护工具。医用透明质酸钠凝胶小包装一般采用预灌封包装设计,再封装于单包装容器(袋或塑料泡罩)内。
医用透明质酸钠凝胶作为一种可植入体内的特殊医疗产品,其质量优劣直接影响患者身体健康及生命安全。此类产品在生产过程中往往会引入微量金属元素,如果生产企业和医疗器械监管机构对此风险不加以控制,毒性较大的金属元素就会随着产品的植入在体内释放,对人体各组织器官造成不同程度的损伤。
在对医用透明质酸钠凝胶的金属元素检测中,发现此类产品中含有不同浓度的钨元素。追其原因是由于,预灌封注射器玻璃针筒顶部的内部通道成型工艺中会引入金属钨,金属钨在400℃时会被氧化为氧化钨,在800℃时,氧化钨会发生升华,在加工过程中变成蒸汽沉降在玻璃器皿表层[1-2]。
钨在预灌封注射器包装组件的加工工艺中引入,随着样品可直接进入人体,其安全风险应引起关注。本研究拟采用微波消解和ICP-MS法建立医用透明质酸钠凝胶产品中钨含量的分析方法,并对产品的迁入钨的安全性进行评价,以对产品标准的完善提供依据。
2 实验部分
2.1 仪器与材料
美国PE公司电感耦合等离子体质谱仪(NexlON 350D);美国CEM密闭微波消解系统(MARS-OMNI);德国Millipore公司超纯水机(Milli-Q®Advantage A10);硝酸(J.T.Baker,A.C.S. Reagent);双氧水(国药集团,优级纯);钨W标准溶液(1000 mg/L,国家有色金属及电子材料分析测试GSB 04-1760-2004);铼Re标准溶液(1000 mg/L,国家有色金属及电子材料分析测试GSB 04-1745-2004);12家市场可售医用透明质酸钠凝胶产品。
2.2 试验方法
2.2.1样品前处理 取样品0.5~1.0 g,加硝酸8 mL,H2O21 mL装入消解罐内,盖盖放置反应2 h,用微波消解仪进行前处理后于120℃赶酸至体积小于1 mL,用1%HNO3定容至50 mL,作为检验液,同法制备空白。微波消解具体条件见表1。
2.2.2仪器工作条件 ICP-MS工作条件:载气流量:0.75 L/min;射频功率:1600 W;雾化器及雾室:同心雾化器及玻璃旋流雾室;采样锥截取锥类型:铂锥;分析模式:标准模式;动态带宽调节:RPa=0,RPq=0.25。
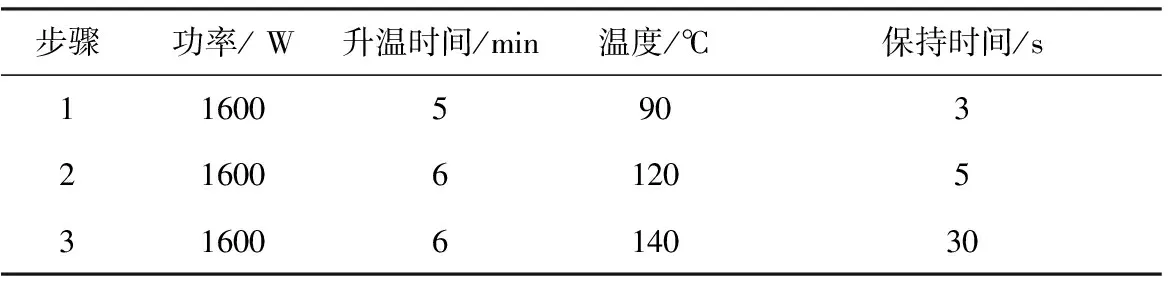
表1 微波消解条件
2.2.3测试方法 以铼187Re作为内标,采用市售标准物质W标准溶液(选用182W和184W),建立标准曲线。空白液和待测样品采用标准曲线定量。
3 结果
3.1 标准曲线及相关系数
取钨标准溶液,用1%HNO3稀释配制浓度为0、0.2、0.5、1、2、5、8、10 ug/L的标准溶液,1%HNO3将内标铼的浓度配制为10 ug/L,进样检测。

图1钨标准曲线图
Fig.1Tungstenstandardcurve
从图1可以看出,无论是仪器给出的检出限(DL)还是等效背景浓度(BEC),均是184W的数值较低,可优先选184W为定量曲线。对于184W的标准曲线,在0~10 ug/L浓度范围内,线性较好,相关系数R=0.9996。
3.2 检出限试验
重复进样空白溶液11 次,记录吸光度。以吸光度标准偏差的3 倍与标准曲线的斜率比值,计算得到仪器的检出限为0.006 ug/L,以吸光度标准偏差的10 倍与标准曲线的斜率比值,计算得到仪器的定量限为: 0.020 ug/L。若按取样量0.5 g,定容体积50 mL 计算,得方法检出限为0.0006 mg /kg,方法定量限为0.002 mg /kg。
3.3 精密度试验
取1份已处理好的供试品溶液,连续进样11次,测定吸光度,计算11 个结果的RSD 为2.4 %。
3.4 重复性试验
精密称取同批次医用透明质酸钠凝胶约0.5 g 6 份,按前述方法进行含量测试。结果为0.27、0.25、0.28、0.27、0.26、0.25 mg /kg,RSD为4.60%。
3.5 回收率实验
精密称取医用透明质酸钠凝胶约0.5 g,准确加入1 ug/mL 的钨标准储备液 0.1和0.3 mL,按前述方法进行含量测试,结果见表2。由表2可以看出,待测元素的加标回收率为95.23%和104.54%,表明采用本方法测定医用透明质酸钠凝胶中的钨元素,结果准确可靠。

表2 回收率试验(n=3)
3.6 样品分析
用上述方法,对12批市售医用透明质酸钠凝胶中的钨元素进行测定,结果见表3。从表3可以看出,医用透明质酸钠凝胶中钨的含量在0.03~4.56 ug/g之间。
4 讨论
因为医用透明质酸钠凝胶中钨的化合物主要来源于预灌封注射器的表层沉积,随着透明质酸钠凝胶的灌装而混入样品中。因此,钨的含量与质酸钠凝胶的体积和浓度无关,只与钨针在形成内部通道时的升华程度有关。这一点在表3的数据分布上也可以证明。
表3 12批供试样品铬含量测定结果
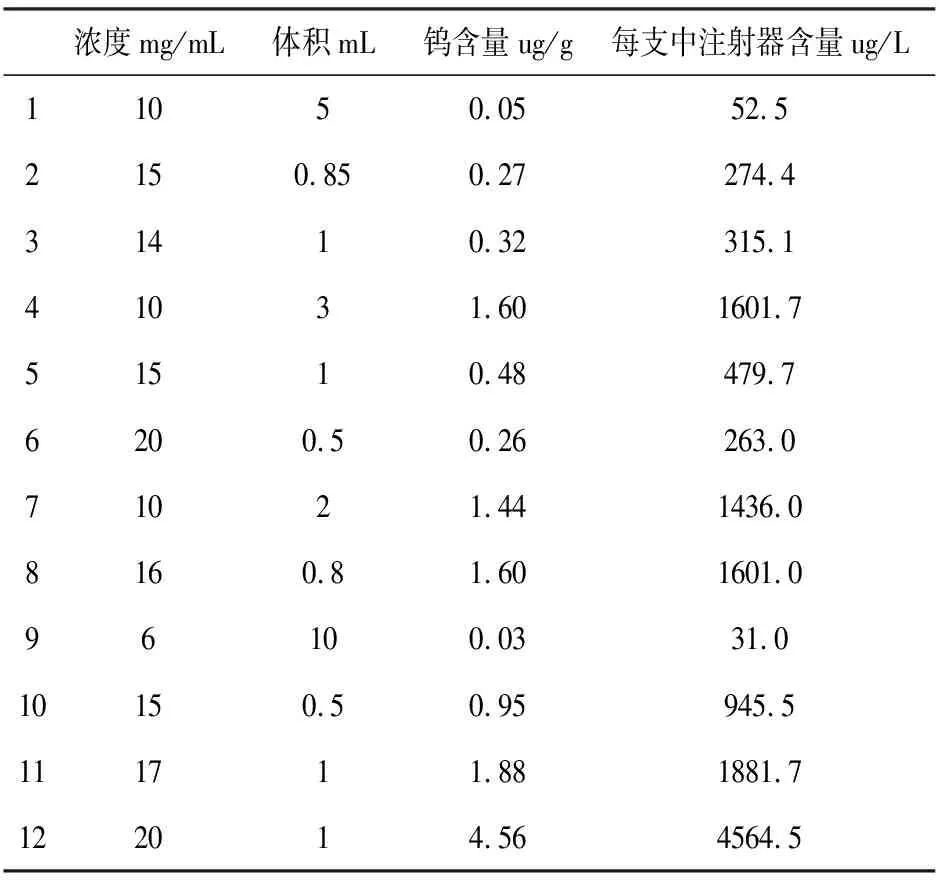
Table 3 Determination result of tungsten in 12 batches of samples
目前国际上关于金属元素的安全性评价大多参照美国药典<232药品元素杂质限度>,人用药物注册技术要求国际协调会议< ICH Q3D 元素杂质指导原则>以及EMEA关于金属催化剂或金属试剂残留量限度规定的指导原则。 但在USP 232及EMEA文件中,元素钨未出现在需要关注的元素列表之中[3-4],在ICH Q3D中也归类到其他元素杂质中(因其较低的毒性和/或在地方法规中的要求不同,其 PDE 还没有建立,在指南中并未说明)[5],因此无相关的PDE值可以参考。
金属元素钨的毒理机制的研究较少,缺少相关的毒理学数据。目前可查到的一些生态毒性实验,所有已知的数据集中在单一态钨酸盐,钨酸钠对小鼠和大鼠的LD50值分别为240 mg/Kg和1190 mg/Kg。但是在最近几年的研究中,研究人员发现尿液中钨含量高的人与高中风率之间存在关联。虽然没有记载钨单独作用并不会造成人体的健康问题,但有通过动物和细胞培养的实验表明它与癌症和肺部感染之间存在关联;另一些研究也显示了钨与心脏问题之间存在联系[6-10]。
国内标准中,查询器械类、食品类及环境保护类,均未有钨元素的限量值的相关标准。在国外的标准方面,在美国,除了职业暴露空气污染指数(难溶钨类为5 mg/m3,可溶钨类为1 mg/m3)外,没有针对钨的其他规定。钨污染指标在苏联首先建立起来,包括最大允许浓度(环境污染的一个定量指标)。MAC被定义在整个生命周期中某种化学物质影响人类健康的最低浓度。饮用水和渔业水库中钨的MAC值分别为0.05和0.0008 mg/L。起初,1966年的饮用水MAC值被定为0.1 mg/L。后来,当有研究发现在更低浓度的钨和钼共同作用下会对老鼠产生胚胎毒性时,MAC值被改为如今的0.05 mg/L[6]。
如若按照每个成人日均饮水量设定为1 500至1 700 ml[11],每日摄入的钨元素的量应控制在75 mg/d。医用透明质酸钠凝胶的临床日使用量假定为5支,则样品的钨摄入量见图2,远小于饮用水中的控制标准。
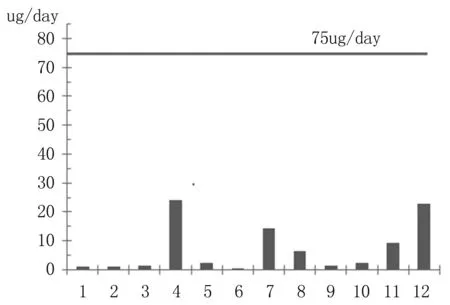
图2医用透明质酸钠凝胶中钨元素每日最大摄入量示意图
Fig2ThemaximumdailyintakeofTungsteninmedicalsodiumhyaluronategel
现在,有一种新型成型系统可以降低针头的处理温度,并在其表层形成一种保护层,以减少机械接触。从而可以使钨的残留含量大大降低,可浸出的金属钨平均残留量<250 ug/L[2]。按此数据,此次的供试样品除去5mL和10mL的体积较大的注射器外,其他批次都远大于此数值。因此,虽然钨的含量可满足人体的安全性评价要求,但是预灌封注射器的厂家还是可以通过工艺革新等措施减小人体钨的摄入量。

