UPLC-Q-Orbitrap HRMS同时检测水产品中磺胺和喹诺酮类药物残留
杨璐齐 李 蓉 高永清 张朋杰 张鹏云,
(1. 广东药科大学,广东 中山 528458;2. 中山出入境检验检疫局,广东 中山 528400)
UPLC-Q-Orbitrap HRMS同时检测水产品中磺胺和喹诺酮类药物残留
杨璐齐1,2李 蓉2高永清1张朋杰2张鹏云1,2
(1. 广东药科大学,广东 中山 528458;2. 中山出入境检验检疫局,广东 中山 528400)
建立了水产品中21种磺胺类(SAs)和12种喹诺酮类(QNs)药物残留的超高效液相色谱-四级杆/静电场轨道阱高分辨质谱(UPLC-Q-Orbitrap HRMS)多残留检测方法。样品经过乙腈提取,乙腈饱和正己烷脱脂,内标法定量。结果表明,33种目标化合物在质量浓度为0.1~100 ng/mL时线性关系良好,r2≥0.996 0,定量限(LQD)为2 μg/kg。平均加标回收率为54.3%~120.4%,相对标准偏差(RSDs)为1.7%~11.9%。该方法操作简便、灵敏度高、特异性强,可以满足日常检测要求。
高分辨质谱;水产品;磺胺类;喹诺酮类
Abstract: An Ultra-High Performance Liquid Chromatography-Quadrupole/Electrostatic Field Orbitrap High-resolution Mass Spectrometry method (UPLC-Q-Orbitrap HRMS)has been developed for the determinations of the drug residues of 21 SAs and 12 QNs in aquatic products.The sample was extracted by acetonitrile, cleaned up by acetonitrile saturated normal hexane and quantified in internal standard method.The results showed that 33 products presented a good linear relation in the range of 0.1~100 ng/mL.r2>0.996. The limits for qualitative detection was 2 μg/kg. The average recoveries at three spike levels ranged were 54.3%~120.4%, with RSDs ranging 1.7%~11.9%. The developed method was easy operation high sensitivity, which can meet the requirements of daily inspection.
Keywords: high-resolution mass spectroscopy; aquatic products; sulfonamides; quinlones
近年来,中国食品安全事件频发[1],食品安全问题关涉到每一个人的切身利益,直接影响着社会的和谐与稳定[2]。磺胺类(Sulfonamides,SAs)和喹诺酮类(Quinlones,QNs)药物为广谱抑菌药,具有抗菌谱广、高效、低毒、价格低廉等特点,在水产、畜牧养殖中被广泛使用[3-4]。同时SAs对人体肾脏和肝脏有毒副作用,破坏人的造血系统,从而引起溶血性贫血[5];QNs可发生严重的光敏反应和光毒性反应,对人体的中枢神经系统造成不良影响,导致重症肌无力、呼吸肌无力而危及生命,且具有潜在的致癌性和遗传毒性[6]。因此,国际食品法典委员会(CAC)和美国规定食品与饲料中SAs的最高残留限量为100 μg/kg[7];欧盟制定了可食动物肌肉[8]中磺胺类总量的最高残留限量(MRL)≤100 μg/kg;日本规定食品中不得检出SAs[5];中国规定磺胺类在所有食品动物肌肉中的最高残留限量为100 μg/kg,达氟沙星、恩诺沙星在除牛、羊、家禽等以外其他动物肌肉中的最高残留限量为100 μg/kg,沙拉沙星在鱼的“肌肉+皮”中的最高残留限量为30 μg/kg[9]。
近年来SAs与QNs的检测方法有酶联免疫法[10-11]、液相色谱法[12-13]、液相色谱-串联质谱法[14-16]、液相色谱-高分辨质谱法[16-18]等。酶联免疫法通常用于样品的快速筛查,该方法易受样品基质中类似物质干扰而产生假阳性[19]。液相色谱法的灵敏度较低,且无法提供目标物结构信息不能用于确证方法[20]。液相色谱-串联质谱法由于灵敏度高、结果准确,是目前检测兽药残留的常用标准方法[21-22]。随着人们生活水平的提高,对膳食结构的合理调整,水产品消耗量不断增大,目前尚未见文章报道采用高分辨质谱同时检测其中的SAs和QNs。本试验拟建立超高效液相色谱-四级杆/静电场轨道阱高分辨质谱同时检测水产品中21种SAs和12种QNs药物残留的检测方法,旨在为大批量水产品中磺胺与喹诺酮类兽药残留建立一种前处理简单、结果准确的检测方法。
1 材料与方法
1.1 仪器与试剂
高分辨质谱仪:Q-Exacitv型,配电喷雾离子源及Trace Finder 3.3 EFS数据处理系统,美国Thermo Fisher公司;
超高效液相色谱仪:Ultimate 3000型,美国Thermo Fisher公司;
离心机:SIGMA 2-16K型,德国Sartorius-sigma公司;
浓缩仪:BHCHI Synocre型,瑞士步琪公司;
纯水净化仪:Mili-Q 型,法国Milipore公司;
乙腈、正己烷、乙酸乙酯、甲醇:色谱级,美国默克公司;
鲩鱼:市购;
无水硫酸钠:分析纯,中国广州化学试剂厂(使用前在650 ℃的马弗炉内灼烧4 h);
22种兽药标准品、12种兽药内标标准品:德国Dr.Ehrenstorfer GmbH公司。
1.2 标准溶液配制
1.2.1 标准储备溶液 分别称取适量的上述标准品及内标于10 mL容量瓶中,用甲醇定容,配制成100 μg/mL的标准储备溶液,置于-18 ℃保存。
1.2.2 混合标准溶液 分别取一定量上述标准储备溶液用甲醇稀释成1 μg/mL的混合标准溶液,在2~4 ℃保存;分别取一定量上述内标标准储备溶液用甲醇配制成100 ng/mL的混合内标溶液,在2~4 ℃保存。临用前按需要混合稀释为标准工作溶液。
1.3 样品前处理
准确称取经搅拌器均质的水产品样品2.00 g至50 mL离心管中,添加浓度为100 ng/mL的混合内标溶液100 μL,加入10 mL乙腈,以14 000 r/min匀浆30 s,加入4 g无水硫酸钠涡漩30 s,以4 500 r/min离心5 min。准确吸取5 mL样品提取液至15 mL离心管中,在45 ℃下用氮气将试管内的溶剂吹干,残渣用体积比为10∶90的乙腈—0.1 %甲酸水溶液定容至1 mL,涡漩30 s,超声3 min,加入5 mL乙腈饱和正己烷,漩涡1 min,静置30 min,取下层液体1.5 mL转移至2 mL的高速离心管中,以12 000 r/min离心5 min,取下清液经0.22 μm滤膜过滤后上机。
1.4 仪器条件
1.4.1 液相色谱条件 色谱柱:WatersAcquity UPLC®BEH C18(2.1 mm×100 mm,1.7 μm);柱温:30 ℃;流动相:A(含0.1%甲酸的水溶液)和B(含0.1%甲酸的甲醇溶液);梯度洗脱程序见表1;流动相流速:0.3 mL/min;进样量:10 μL。
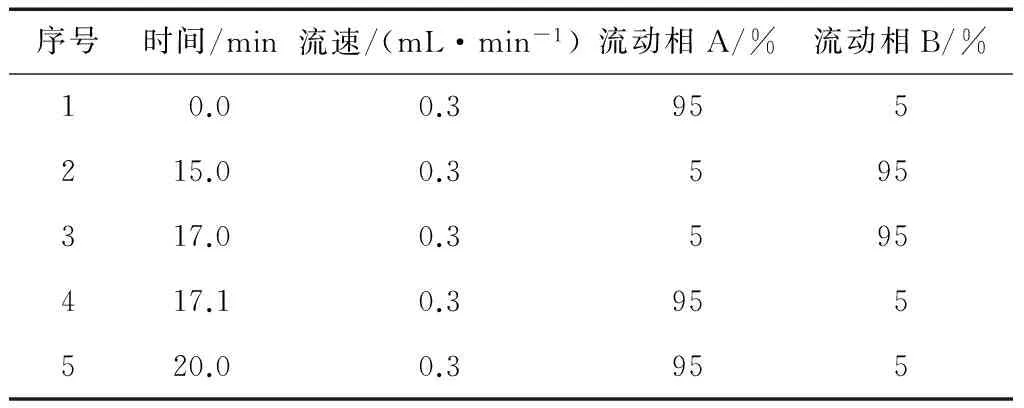
表1 液相色谱梯度洗脱程序
1.4.2 质谱条件 离子源:HESI;扫描模式:Full MS/ddMS2(Top1);全扫描范围(m/z):100~1 000;分辨率:一级全扫描70 000、二级17 500;质谱驻留时间(AGC): Full MS 1 e6、MS/MS 2 e5;归一化碰撞能:20,40,60;顶点激发:3~6 s;动态排除:6 s;喷雾电压: 3 200 V;鞘气流速(N2):0.276 MPa;辅助气流速(N2):0.069 MPa;加热温度:325 ℃;离子传输管温度:350 ℃;透镜电压:60 V;各化合物质谱信息见表2。
2 结果与分析
2.1 色谱条件的优化
对21种SAs和12种QNs兽药同时进行分析,因其药物极性差异较大,采用梯度洗脱。首先对比流动相中有机相分别为含0.1%甲酸的乙腈溶液、含0.1%甲酸的甲醇溶液、乙腈、甲醇时,发现在有机相中加入甲酸后响应值更高,可能是甲酸提供质子,离子源打碎目标物时提高了碎片的离子化程度。同时发现同分异构体SMD、SMP、SMM在流动相含有0.1%甲酸的水溶液和含0.1%甲酸的甲醇溶液条件下,分离效果较好。对比色谱柱Waters Acquity UPLC®BEH C18(2.1 mm×100 mm,1.7 μm)与Thermo Accucore RP-MS(2.1 mm×100 mm,2.6 μm),结果发现使用前者QNs峰型较好。最终选用Waters Acquity UPLC®BEH C18(2.1 mm×100 mm,1.7 μm)色谱柱,含0.1%甲酸的水溶液和含0.1%甲酸的甲醇溶液为流动相。图1 为添加浓度为10 ng/mL的33种目标物的提取离子流图。
2.2 质量准确度
使用高分辨质谱检测目标化合物的精确质量数对于同时准确定性和定量非常重要,本研究使用超高效液相色谱—四级杆/静电场轨道阱高分辨质谱所测的33种目标物均达到了良好的质量准确度。表3列举了其中6种物质的理论质荷比与实测质荷比,其质量准确度均小于±1×10-6,完全满足定性和定量要求。
2.3 前处理条件的选择和优化
因检测的目标物可以溶于非极性或中等极性溶剂,分别考察了有关文献报道的乙酸乙酯[23]、含1%甲酸的乙腈[5]、乙腈[24]、含2%甲酸的乙腈溶液的提取效果,见图2。由图2可知,4种提取液磺胺甲氧哒嗪的回收率均差异不大;STZ、SPD、SAA用含2%甲酸的乙腈溶液提取效率较低;乙腈具有较好的蛋白沉淀作用。因此,采用乙腈作为提取液。

表2 45种物质的质谱信息及保留时间
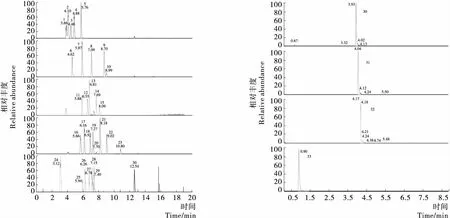
1. 磺胺嘧啶 2. 磺胺索嘧啶 3. 磺胺噻唑 4. 磺胺甲基嘧啶 5. 磺胺二甲嘧啶 6. 磺胺吡啶 7. 甲氧苄啶 8. 磺胺邻二甲氧嘧啶 9. 磺胺间二甲氧嘧啶 10. 噁喹酸 11. 磺胺甲噻二唑 12. 磺胺氯哒嗪 13. 磺胺甲恶唑 14. 磺胺苯酰 15. 司帕沙星 16. 磺胺甲氧哒嗪 17. 磺胺-5-甲氧嘧啶 18. 磺胺间甲氧嘧啶 19. 磺胺异恶唑 20. 加替沙星 21. 磺胺苯吡唑 22. 磺胺喹噁啉 23. 氟甲喹 24. 磺胺醋酰 25. 氟罗沙星 26. 氧氟沙星 27. 恩诺沙星 28. 双氟沙星 29. 沙拉沙星 30. 诺氟沙星 31. 环丙沙星 32. 达氟沙星 33. 磺胺胍

图1 鱼肉中添加回收21种SAs和12种QNs的提取离子流图
盐析剂在样品提取时可防止样品中的水分及杂质进入提取液,同时可以实现脱水和盐析,还可使蛋白质变性分散防止样品结块影响提取效率。对比使用无水硫酸镁和无水硫酸钠时,发现加入无水硫酸镁时或因其吸水放热提高了提取环境的温度,诺氟沙星等几种物质使用无水硫酸镁盐析的回收率明显低于使用无水硫酸钠的,见图3。进一步对比添加4,6,8 g无水硫酸钠,各目标物的添加回收率无明显差异,最终选择4 g无水硫酸钠作为盐析剂。

图2 提取液对目标物提取效率的影响

图3 盐析剂对提取效率的影响
2.4 线性范围与定量限的确定
配制质量浓度为0.1~200.0 ng/mL的系列标准溶液,在优化后的色谱和质谱条件下进行检测,对相对应化合物在质谱中的响应面积Y与目标化合物的标记浓度值X进行线性拟合,得到目标化合物的线性范围及其相对应的决定系数(r2)。结果显示,各化合物的r2值均≥0.996 0(见表4)。由于高分辨率质谱仪基线极低,信噪比不再适合于确定检出限和定量限[25],故本方法中定量限为化合物在线性范围内同时满足回收率值为60%~120%的最低浓度值2 μg/kg。该指标优于同类检测标准,满足所有国家和地区的限量要求。
2.5 方法的回收率与精密度
选取空白基质(阴性样品)鲩鱼,进行3个浓度水平的加标回收试验,考察方法的准确度。采用精确质量数、保留时间、同位素分布和二级碎片离子4个指标来对结果进行分析,方法定量时对有相应同位素内标的目标物采用内标法定量,其余采用外标法定量。方法的加标平均回收率为54.3%~120.4%,相对标准偏差为1.7%~11.9%,见表4,满足食品理化检测方法的技术要求。
2.6 方法应用
用建立的方法对收集的25个水产样品进行了检测。喹诺酮类药物均未检出;在其中1个南美对虾样品中检出磺胺邻二甲氧嘧啶(SDX),鲩鱼、北极贝、鳗鱼、罗非鱼4个样品中检出磺胺吡啶(SPD)。图4列举了标准溶液中的SDX和SPD与代表性阳性样品南美对虾中SDX和罗非鱼中SPD的对比图。阳性定量结果在2~3 μg/kg,均低于限量要求。说明此次收集的水产养殖鱼中磺胺类和喹诺酮药物残留处于安全水平。虽然本次试验所检测样品处于安全水平,但是食品安全直接关系到人们的生命健康,对严重危害食品安全的行为实行刑法规制是现代社会的必然选择[26]。
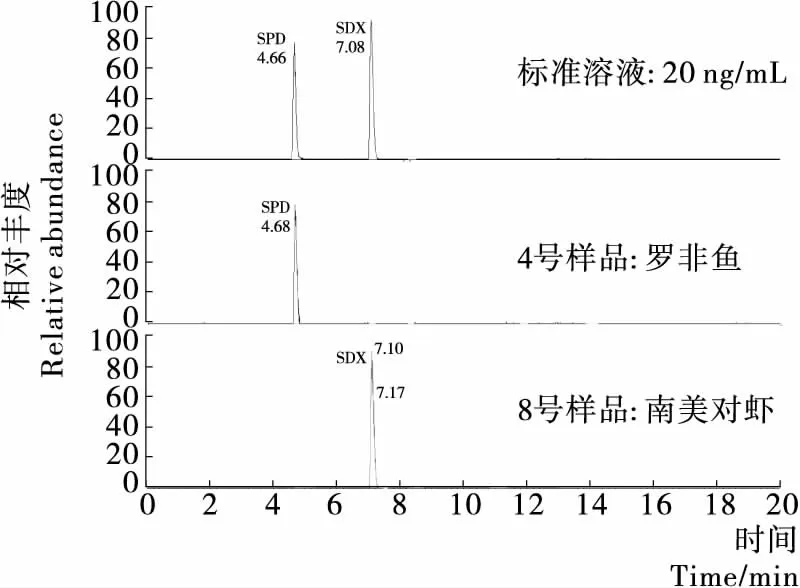
图4 SDX和SPD阳性样品的提取离子流图
3 结论
为了顺应兽药残留检测快速、简便、准确以及高通量的发展趋势,本研究将超高效液相色谱-四级杆/静电场轨道阱高分辨质谱仪与快速前处理方法结合,建立了水产品中21种SAs和12种QNs兽药残留同时检测的方法,样品只需进行简单的提取、浓缩、离心、过滤,即可上机检测。方法的测定低限满足国内外对水产品中SAs和QNs兽药残留的限量要求。该方法简便、灵敏、准确,满足日常检测和监管需求。

表4 空白基质中3个添加水平的平均回收率和相对标准偏差
[1] 李洪峰. 食品安全社会共治的现实困境与发展对策[J]. 食品与机械, 2016, 32(4): 234-236.
[2] 王立新. 中国食品安全问题的法律治理路径[J]. 食品与机械, 2014, 30(5): 107-109, 112.
[3] 李锋格, 苏敏, 李晓岩,等. 分散固相萃取-超高效液相色谱-串联质谱法测定鸡肝中磺胺类、喹诺酮类和苯并咪唑类药物及其代谢物的残留量[J]. 色谱, 2011(2): 120-125.
[4] GUIDI L R, SANTOS F A, RIBEIRO A C, et al. A simple, fast and sensitive screening LC-ESI-MS/MS method for antibiotics in fish[J]. Talanta, 2017, 163: 85-93.
[5] 孙伟红, 冷凯良, 王志杰, 等. HPLC-MS/MS内标法同时测定水产品中18种磺胺类药物残留量[J]. 食品科学, 2009(24): 294-298.
[6] 仲兆金. 喹诺酮类药物的毒性[J]. 国外医药: 抗生素分册, 2001(1): 31-33.
[7] Codex Alimentarius Commission. CAC/MRL 2-2015 Maximum Residue Limits (Mrls) and Risk Management Recommendations (Rmrs) for Residues of Veterinary Drugs In Foods [S/OL].(2015-08-12)[2017-08-20].http://down.foodmate.net/standard/sort/11/46551.html.
[8] European Union. Regulation (EC) No 470/2009 of the European parliament and of the council of 6 May 2009 laying down Community procedures for the establishment of residue limits of pharmacol-ogically active substances in foodstuffs of animal origin, repealing Council Regulation (EEC) No 2377/90 and amending Directive 2001/82/EC of the European Parliament and of the Council and Regulation (EC) No 726/2004 of the European Parliament and of the Council[S/OL].(2009-06-05)[2017-08-20].http://down.foodmate.net/standard/sort/44/28727.html.
[9] 中华人民共和国农业部. 动物性食品中兽药最高残留限量 中华人民共和国农业部公告第235号[S/OL].(2002-12-24)[2017-08-20]. http://www.moa.gov.cn/zwllm/tzgg/gg/200302/t20 030226_59300.htm.
[10] 张鸿雁, 崔小军, 耿金培, 等. 动物源性食品中磺胺类药物的多残留酶联免疫测定方法研究进展[J]. 食品研究与开发, 2008(9): 181-183.
[11] 于雪芝. 基于单链抗体的牛奶中21磺胺和20氟喹诺酮类药物残留生物发光免疫分析方法研究[D]. 北京: 中国农业大学, 2016: 52-74.
[12] 吴翠琴, 雷金妹, 李韵灵, 等. 基于离子液体的分散液液微萃取-柱前荧光衍生高效液相色谱法测定水样中8种磺胺类药物[J]. 色谱, 2014(12): 1 362-1 367.
[13] 张丽媛, 王颖, 张东杰. IL-HLLME-HPLC法测定酸奶中磺胺类抗生素[J]. 食品与机械, 2013, 29(6): 71-75.
[14] ZHANG Zhi-wen, LI Xiao-wei, DING Shuang-yang, et al. Multiresidue analysis of sulfonamides, quinolones, and tetracyclines in animal tissues by ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Food Chem, 2016, 204: 252-262.
[15] TIAN He, WANG Jia-qi, ZHANG Yang-dong, et al. Quantitative multiresidue analysis of antibiotics in milk and milk powder by ultra-performance liquid chromatography coupled to tandem quadrupole mass spectrometry[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2016, 1 033-1 034: 172-181.
[16] 孟哲, 石志红, 吕运开, 等. 超高效液相色谱-高分辨四级杆飞行时间质谱法快速筛查乳制品中磺胺类与氟喹诺酮类药物[J]. 分析化学, 2014(10): 1 493-1 500.
[17] 孔聪, 周哲, 汪洋, 等. 超高压液相色谱串联高分辨质谱筛查渔用投入品中禁限用药物[J]. 分析化学, 2017(2): 245-252.
[18] WANG Jian. Development and validation of a multiclass method for analysis of veterinary drug residues in milk using ultrahigh performance liquid chromatography electrospray ionization quadrupole orbitrap mass spectrometry[J]. Journal of Agricultural and Food Chemistry, 2015, 63(41): 9 175-9 187.
[19] 林品言, 杜红梅. 酶联免疫法快速检测水产品中磺胺类药物残留[J]. 当代水产, 2016(10): 94-95.
[20] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GBT 27404—2008 实验室质量控制规范食品理化检测[S]. 北京: 中国标准出版社, 2008: 27.
[21] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T 21316—2007动物源性食品中磺胺类药物残留量的测定方法液相色谱-质谱/质谱法[S]. 北京: 中国标准出版社, 2007: 1.
[22] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T20751—2006鳗鱼及其制品中十五中喹诺酮类药物残留量的测定液相色谱-串联质谱法[S]. 北京: 中国标准出版社, 2006: 2.
[23] 中华人民共和国农业部. 农业部985号公告-12-2007 水产品中磺胺类药物残留量的测定液相色谱[S]. 北京: 中国标准出版社, 2007: 5.
[24] 唐炜, 李龙飞. 固相萃取-HPLC法检测食品中四种磺胺类兽药残留[J]. 食品研究与开发, 2013(18): 62-65.
[25] 木合他拜尔, 严华, 徐姗, 等. QuEChERS-超高效液相色谱-高分辨串联质谱技术检测鸡肉中6种抗球虫药物[J]. 色谱, 2015(11): 1 199-1 204.
[26] 刘晓丹. 中国食品安全刑法规制的实践困境与完善路径[J]. 食品与机械, 2017, 33(1): 65-67.
Simultaneous determination of suIfonamides and quinIones infish by UPLC-Q/Orbitrap HRMS
YANG Lu-qi1,2LIRong2GAOYong-qing1ZHANGPeng-jie2ZHANGPeng-yun1,2
(1.GuangdongPharmaceuticalUniversity,Zhongshan,Guangdong528458,China;2.ZhongshanEntry-ExitInspectionandQuarantineBureau,Zhongshan,Guangdong528400,China)
10.13652/j.issn.1003-5788.2017.08.010
国家质检总局科技计划项目(编号:2015IK260);广东省省级科技计划项目(编号:2014A040401011,2015A050502010);中山市社会公益重大专项(编号:2015B2295)
杨璐齐,女,广东药科大学在读研究生。
李蓉(1969—),女,中山出入境检验检疫局研究员,学士。E-mail:lirong828@126.com 高永清(1958—),男,广东药科大学教授,硕士。 E-mail:yongqingg@163.com
2017—04—08

