铅锌烟灰为原料制备氯化锌和电铅工艺研究*
李晓乐,徐素鹏,汤长青,杨继鹏,程光辉
(济源职业技术学院,河南济源459000)
环境·健康·安全
铅锌烟灰为原料制备氯化锌和电铅工艺研究*
李晓乐,徐素鹏,汤长青,杨继鹏,程光辉
(济源职业技术学院,河南济源459000)
研究了炼铅厂铅锌烟灰作原料,以盐酸浸取并以高锰酸钾氧化Fe2+、Mn2+,电积法分段分离Cu2+、Pb2+、Cd2+,两步法生产氯化锌的新方法。以高的锌浸出率、低的铅浸出率,Fe2+、Mn2+、Cu2+、Pb2+、Cd2+除杂最彻底,处理成本最低为考察目标,确定了最佳的工艺条件:40 g铅锌烟灰、71 mL浓盐酸与130 mL水于30℃下酸浸50 min后,加高锰酸钾16.7 mg,10℃下继续反应2 h后过滤,滤液作阴极液分3段进行电沉积除Cu2+、Pb2+、Cd2+,每段电积时间控制为10 min,3段电积的电极电位分别控制为0.09、-0.37、-0.64 V,阴极液温度控制为 30℃,电积 30 min后,制得1.64 mol/L的氯化锌溶液。上述工艺中,锌的酸浸率达95.41%,用制备的氯化锌溶液生产氧化锌,产品杂质含量满足GB/T 19589—2004《纳米氧化锌》一级品的要求,浸出液中含量较多的金属离子通过分段电积回收,降低了锌灰浸出液除杂的成本,并使杂质离子实现了资源化,工艺更加绿色经济。
锌灰;酸浸;氧化;电积;氯化锌
Abstract:A new technology of preparing zinc chloride was studied.The technology taking zinc ash from a lead smelter as raw material applied a two-step method as below:leaching zinc ash by hydrochloric acid,oxidizing Fe2+and Mn2+by potassium permanganate,and separating Cd2+,Pb2+,and Cu2+by electrodeposition method.To get the high leaching rate of zinc,the low leaching rate of Pb and the thoroughly removing of Mn,Fe,Pb,Cd,and Cu elements,the optimum experimental acid leaching and purification conditions were as follows:after 40 g lead-zinc ash leached by the mixed acid including 71 mL concentrated hydrochloric acid and 130 mL water for 50 min at 30℃,0.017 g KMnO4was added into the solution to continue the reaction for 2 h at 10 ℃,and then electrodeposited Cu,Pb,and Cd on the potential of 0.09 V for 10 min,then-0.37 V for 10 min,and then-0.64 V for 10 min in the filtration,and finally the zinc chloride solution with the concentration of 1.64 mol/L was obtained.Under above conditions,the leaching rate of zinc was 95.41%,the impurity ion content in zinc chloride solution met the requirements of the first grade of Nano-sized Zinc Oxide,GB/T 19589—2004.The metal ions in the leaching solution were recovered by segmented electrodeposition,thus realized the cost reduction of impurity removal,changing impurity ions into resource,and the process being more green and economical.
Key words:zinc ash;acid leaching;oxidation;electrodeposition;zinc chloride
来自火法炼铅、锌矿焙烧车间的含铅锌灰是以PbO、ZnO 为主,兼有 FeO、MnO、CdO、CuO 及其他杂质的复杂混合物,若弃之不用,不仅造成污染,也是对锌资源的浪费。目前对铅锌烟灰的利用主要通过酸浸、氧化除铁锰、锌置换除铅铜镉的方式来实现。
生产企业通常用硫酸溶出锌灰中以氧化态形式存在的金属、高锰酸钾氧化除铁锰、锌粉置换铅铜镉等杂质金属离子后生产高纯氧化锌[1-3],用硫酸作酸浸剂,氧化锌前驱体所吸附的硫酸根离子需用大量水洗涤[4-5],且浸取成本较高,同时在铅铜镉置换过程中所用到的锌粉也是导致铅锌烟灰处理成本居高不下的一个主要因素。本文以氯碱企业当废物处理的盐酸为浸取剂,研究了盐酸加入量、浸取时间、温度等对铅锌烟灰浸取的影响,电解除杂工序中阴极电极电位对Pb2+、Cu2+等的脱除时间和脱除完全程度的影响,并对Mn的氧化脱除效果稳定性差[6]的原因进行了分析研究。研发出以锌灰为原料,通过酸浸、氧化、电还原制备氯化锌和电铅的新工艺。
1 实验部分
1.1 主要原料和实验原理
实验所用的含铅锌灰来自火法炼铅厂烟化炉,成分分析结果见表1。

表1 铅锌烟灰多元素分析表 %
实验原理:含铅锌灰中的ZnO、PbO、FeO等金属氧化物与盐酸反应,生成 ZnCl2、PbCl2、FeCl2,向酸浸液中加 KMnO4,Fe2+、Mn2+被氧化成 Fe(OH)3和MnO2沉淀后,过滤,由于Zn的标准电极为-0.763 V,而 Cu、Pb、Cd 分别为+0.337、-0.126、-0.403 V,可以采用控制合适的电极电位,对滤液中的Cu2+、Pb2+、Cd2+进行阴极电沉积而从滤液中除去,代替传统的锌粉置换,制得纯度符合要求的氯化锌溶液。三步法和两步法实验工艺流程图分别见图1和图2。

图1 实验工艺流程图(三步法)
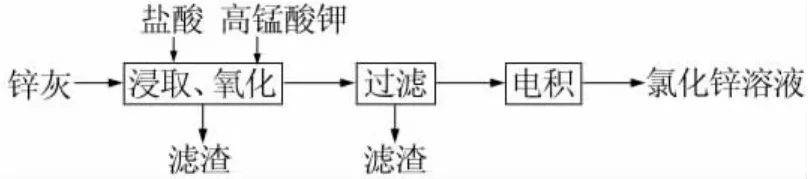
图2 实验工艺流程图(两步法)
1.2 实验步骤
1.2.1 盐酸浸取
质量为40 g含铅锌灰和一定浓度盐酸在250 mL的三口烧瓶中进行混合反应;通过电动搅拌保证固液接触充分,把烧瓶放在一定温度的水浴中控制酸浸反应温度,反应一段时间进行下一步操作。
1.2.2 氧化除杂
1)浸取过滤液氧化。酸浸结束后,用漏斗过滤反应液并洗涤滤渣,滤液和洗液转至250 mL的容量瓶并定容,测定锌、铅、铁等金属离子浓度,并计算锌的浸出率。
取200 mL锌灰酸浸液,加入一定量KMnO4,在一定温度、酸度下,反应一段时间后,过滤沉淀,测出滤液中 Fe2+、Mn2+浓度。
2)浸取氧化。浸取反应后,直接向三口烧瓶内加入一定量KMnO4,控制好酸度和温度,氧化一段时间, 过滤沉淀, 测定Zn2+浓度与 Fe2+、Mn2+、Cd2+、Pb2+等离子浓度。
1.2.3 还原除杂
1)锌粉置换。取200 mL脱除Fe2+、Mn2+的浸出液,在一定温度与酸度下,加锌粉进行铅、铜、镉离子的置换反应,反应一定时间过滤,测定滤液中铅、铜、镉离子浓度。
2)电积净化。用瓷隔膜把用环氧树脂制作的容器隔成阳极室和阴极室,取200 mL脱除铁、锰的浸取液,加入到阴极室,同样体积的氯化钠溶液加入到阳极室,以不锈钢板为阴极,石墨板为阳极,分段进行 Cu2+、Pb2+、Cd2+的阴极电沉积,并测定电积除杂后铅、铜、镉离子浓度。
2 实验结果
2.1 浸出率的影响因素
2.1.1 酸浸时间与固液比
酸浸时间和固液比对Zn2+、Pb2+等浸出率的影响通过预实验考察。结果显示,时间在40~100 min、液固质量比在(3~5)∶1范围内变化时,浸出率没有明显差异。
2.1.2 盐酸加入量
在温度为30℃下,将浓盐酸与130 mL蒸馏水配成一定浓度盐酸溶液与40g含铅锌灰反应50min,抽滤,酸浸液定容250 mL,将浸出的金属离子的浓度列于表2。由表2可知,酸浸液pH随浓盐酸用量的增加而减小,Zn、Fe、Mn、Pb、Cd、Cu 的浸出率随浓盐酸用量增加而增加,在浓盐酸用量超过71 mL、酸浸液pH小于3.94的条件下,锌的浸出率不再增加,Pb的浸出率仍随酸用量增加而增加,为此,确定40 g锌灰加盐酸71 mL为合适盐酸加入量,反应结束后,锌浸出率为95.4%。
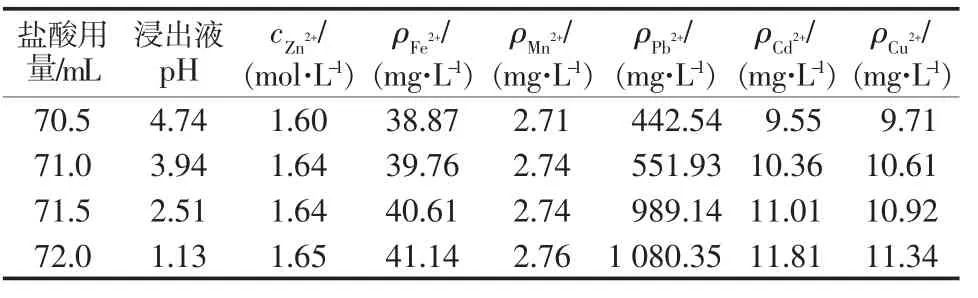
表2 浓盐酸用量对浸出率的影响
2.1.3 温度
浓盐酸71 mL和蒸馏水130 mL混合后,不同温度下,与40 g含铅锌灰酸浸反应50 min,浸出液定容250 mL,浸出的金属离子的浓度列于表3。由表3可知,30~60℃时锌的浸出率不随温度升高而大幅升高,而铅的浸出率随温度升高增加明显,铅的大量浸出会增加净化费用,因此,30℃下进行浸取反应是合适的。
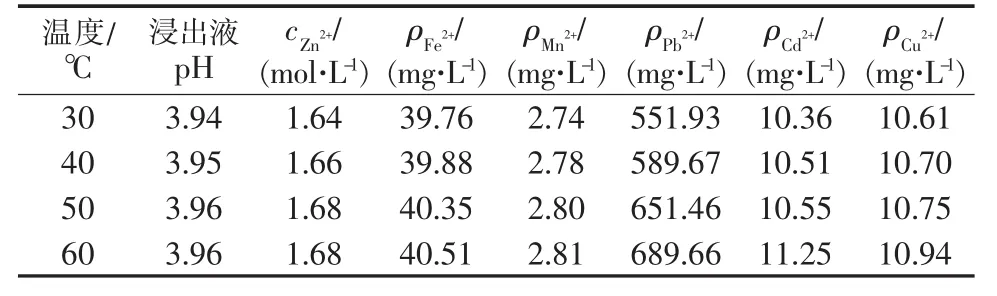
表3 温度对浸出率影响
2.2 高锰酸钾氧化脱除铁锰的影响因素
2.2.1 pH的影响
把 200 mL 浸取液(39.76 mg/L Fe2+,2.74 mg/L Mn2+,1.64mol/LZn2+)置于 10 ℃恒温水浴中,加 1.7 mL的高锰酸钾溶液(0.050 4 mol/L)氧化2.5 h,过滤掉Fe(OH)3和MnO2后,测定反应体系酸度对铁锰脱除的影响,结果见表4。从表4可见,溶液pH越高,氧化脱除后铁、锰离子浓度越低,脱除越彻底,这是因为体系pH越低,Fe3+越不容易生成Fe(OH)3沉淀,体系中Fe3+含量较高,导致Fe2+还原性减弱,高锰酸钾对Fe2+的氧化变得困难,同时酸性条件下,高锰酸钾更容易被还原为Mn2+,结果使得氧化脱除后体系中铁锰含量较高。文献[7]提到的高锰酸钾氧化脱除铁锰稳定性差的原因可能是因为没有关注体系pH所致。

表4 酸度对氧化除杂效果的影响
2.2.2 温度的影响
把 200 mL 浸取液(39.76 mg/L Fe2+,2.74 mg/L Mn2+,1.64 mol/L Zn2+)的 pH 调到 5,加 1.7 mL 的高锰酸钾溶液(0.050 4 mol/L),在不同温度下氧化2.5 h,过滤掉Fe(OH)3与MnO2后,测定反应体系温度对铁锰脱除的影响,结果见表5。表5所揭示的温度对铁锰脱除效果的影响规律与文献[8]不一致,表5显示,铁锰的除杂效果随温度升高而变差。这是由于2.5 h的氧化除杂反应已进行到反应平衡,而高锰酸钾氧化铁锰的反应是放热的,低温有利于平衡正向移动,铁锰脱除也就更加彻底。
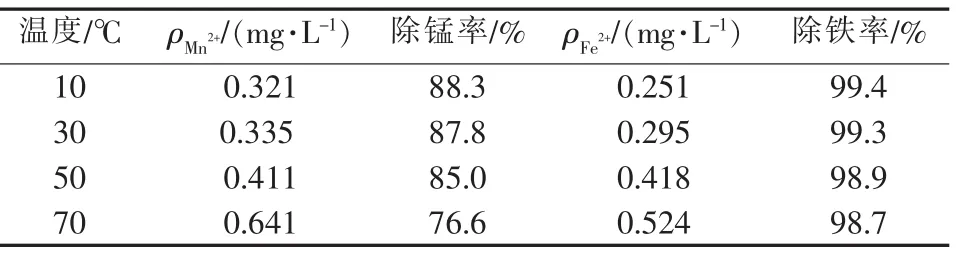
表5 温度对氧化除杂效果的影响
2.2.3 反应时间的影响
把 200 mL 浸取液(39.76 mg/L Fe2+,2.74 mg/L Mn2+,1.64 mol/L Zn2+)的 pH 调到 5,加 1.7 mL 的高锰酸钾溶液(0.050 4 mol/L),10℃下氧化一定时间,过滤掉Fe(OH)3与MnO2后,研究反应时间对铁锰脱除的影响,结果见表6。结果显示,10℃下,1~2 h范围内,脱除率随时间的延长而增加,反应时间超过2 h后,氧化除杂已达到平衡,脱除率不再增加,所以把氧化时间定为2 h。
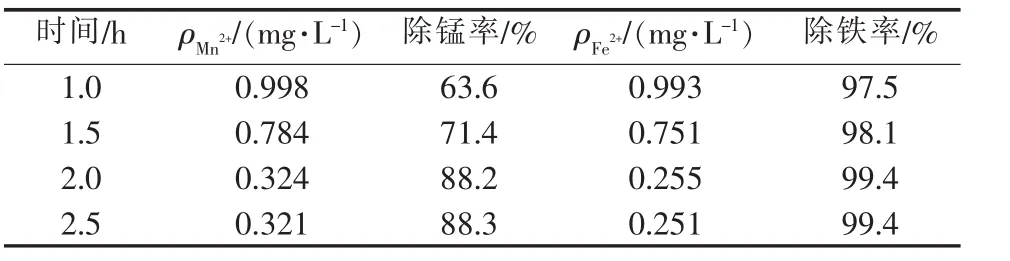
表6 时间对氧化除杂效果的影响
2.2.4 浸取氧化法脱铁、锰效果
浸取工艺条件为:铅锌烟灰40 g,71 mL浓盐酸+130mL水,反应温度为30℃,反应时间为50min。向浸取反应悬浮液中加浓度为0.050 4 mol/L的KMnO4溶液2.1 mL,反应温度控制为10℃,反应2 h后过滤,滤液定容到25 mL,测定金属离子浓度,结果见表7。由表7得知,对酸浸悬浮液直接进行氧化,可以缩短生产时间,且与浸取、氧化除杂两步法效果相当。
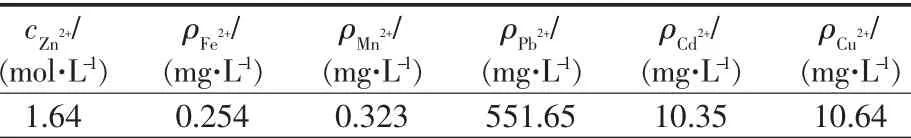
表7 锌灰酸浸液一次净化结果
2.3 还原除杂方法对比
2.3.1 锌粉置换
取脱除铁锰的净化液200 mL(10.64 mg/L Cu2+,551.65 mg/L Pb2+,10.35 mg/L Cd2+), 加 0.15 g Zn 粉,30℃下置换50 min后过滤沉淀,净化液中的Cu2+、Pb2+、Cd2+质量浓度降至 0.018、0.375、0.042 mg/L。
2.3.2 电积除杂
取脱除铁锰的净化液200 mL(10.64 mg/L Cu2+,551.65 mg/L Pb2+,10.35 mg/L Cd2+)作阴极液,控制温度为 30℃,控制阴极电极电位为 0.09 V,电积10 min后,测得Cu2+质量浓度降至0.01 mg/L;把阴极电极电位降至-0.37 V,电积10 min后,测得Pb2+质量浓度降至0.031 mg/L;把阴极电极电位降至-0.64 V,再电积10 min后,测得Cd2+质量浓度降至0.032 mg/L。
3 结论
1)30℃下,盐酸(71 mL 浓盐酸+130 mL 水)酸浸40 g锌灰50 min后,加16.7 mg高锰酸钾于10℃下氧化脱除铁锰工艺是可行的。锌灰中ZnO浸出率达 95.41%,Fe2+、Mn2+质量浓度降到 0.254、0.323 mg/L。2)脱除铁锰的锌灰酸浸液作阴极液,30℃下,阴极电极电位分段控制为0.09、-0.37、-0.64 V进行阴极电沉积30 min,可以把杂质Cu2+质量浓度降至0.01mg/L(电积 10min)、Pb2+质量浓度降至 0.031 mg/L(电积 10 min)、Cd2+质量浓度降至 0.032 mg/L(电积10 min),得到纯净氯化锌溶液和阴极上析出的有价值金属。3)盐酸替代硫酸浸取含铅锌灰,浸取、氧化合二为一,电积除铅铜镉代替锌粉置换生产氯化锌溶液,锌的浸出率高,用制备的氯化锌溶液生产氧化锌,产品杂质含量低(满足GB/T 19589—2004《纳米氧化锌》要求)。此法可以减少锌灰处理工序、降低处理成本、提高锌灰综合利用的程度。
[1] 曾鹏,范兴祥,王洪亮,等.利用次氧化锌粉制备活性氧化锌工艺研究[J].无机盐工业,2013,45(10):30-32.
[2] 邓桂花.锌灰制备活性氧化锌工艺的研究[J].贵州化工,2010,35(6):11-13.
[3] 吴军,宋祥莉,姜国敏.铜闪速炉烟灰硫酸化焙烧后焙砂浸出试验研究[J].有色金属:冶炼部分,2012(5):5-7.
[4] 范兴祥,高仕忠,汪云华,等.一种用初级氧化锌粉制备活性氧化锌工艺[J].无机盐工业,2007,39(2):36-37.
[5] 范兴祥,彭金辉,张利波,等.综合利用锌浮渣制备超细活性氧化锌的扩大试验研究[J].有色矿冶,2003,19(4):34-37.
[6] 童孟良.氧化锌矿制备活性氧化锌的工艺研究[J].矿冶工程,2006,26(4):43-45.
[7] 李国斌,杨明平.活性氧化锌生产中脱除铁锰杂质工艺研究[J].湘潭矿业学院学报,2001,16(4):39-41.
[8] 孙运泉,张志伟.碳酸铵法制备活性氧化锌[J].山东理工大学学报:自然科学版,2004,18(5):58-59.
Study on new technology of preparation of zinc chloride by acid leaching and purifying by electrodeposition method
Li Xiaole,Xu Supeng,Tang Changqing,Yang Jipeng,Cheng Guanghui
(Jiyuan V ocational and Technical College,Jiyuan 459000,China)
TQ132.41
A
1006-4990(2017)10-0053-04
省科技厅重点科技攻关课题(142102210347)。
2017-04-26
李晓乐(1978— ),男,硕士,讲师,研究方向为电化学,已发表论文13篇。
联系方式:xiaole-li@163.com

