船用钢板材料在淡水环境中初期腐蚀行为
郝张科,陈志飚,张东,潘莹,周学杰
船用钢板材料在淡水环境中初期腐蚀行为
郝张科1,2,陈志飚3,张东1,2,潘莹1,2,周学杰1,2
(1.武汉材料保护研究所,武汉 430030;2.特种表面保护材料及应用技术国家重点试验室,武汉 430030;3.中国船级社武汉规范研究所,武汉 430030)
目的研究船用钢板材料在长江淡水环境中的初期腐蚀行为。方法运用形貌分析、腐蚀质量损失、XRD、开路电位、极化曲线等方法研究Q235B和CCSA两种船用钢板材料在室外长江淡水环境中不同暴露方式(水面大气、半浸、全浸)及不同浸泡时间(0.5,1 a)腐蚀行为;室内长江淡水环境不同暴露方式(半浸、全浸)浸泡768 h内的腐蚀行为;室内长江淡水环境全浸泡下在不同时间(0~14 d)的电化学腐蚀行为。结果两种船用钢板材料在武汉长江淡水中腐蚀严重,半浸泡环境下腐蚀速率最大,达到100 μm/a,水面区大气腐蚀速率最小,腐蚀速率为30 μm/a左右,全浸区腐蚀速率为80 μm/a左右,1 a和0.5 a的腐蚀速率相近,CCSA耐蚀性优于Q235B。室内长江淡水浸泡环境下两种船用钢板材料腐蚀电位随时间而降低,2 d后趋于稳定;半浸泡环境下腐蚀速率大于全浸区;极化曲线说明浸泡2 d后,腐蚀速率降低且趋于稳定。结论 CCSA耐蚀性优于Q235B,半浸泡环境下腐蚀最严重,其次为全浸区,水面大气环境腐蚀最小。
船用钢板;淡水环境;腐蚀
我国开展材料水环境腐蚀试验已50年,但材料在江河湖泊中的腐蚀试验近10年才开始[1-2]。为了测定内河船用钢板材料在淡水环境中的腐蚀行为,开展了内河船用钢板材料环境腐蚀试验研究。选用两种常用钢板材料,在武汉长江淡水试验站进行实际淡水环境腐蚀试验,积累材料的腐蚀数据,为内河航运船舶用材及防腐蚀设计规范提供科学依据[3]。
1 试验
1.1 材料
试验材料选用CCSA和Q235B二种船用钢板,其化学成分见表1。试样尺寸规格为100 mm×200 mm。
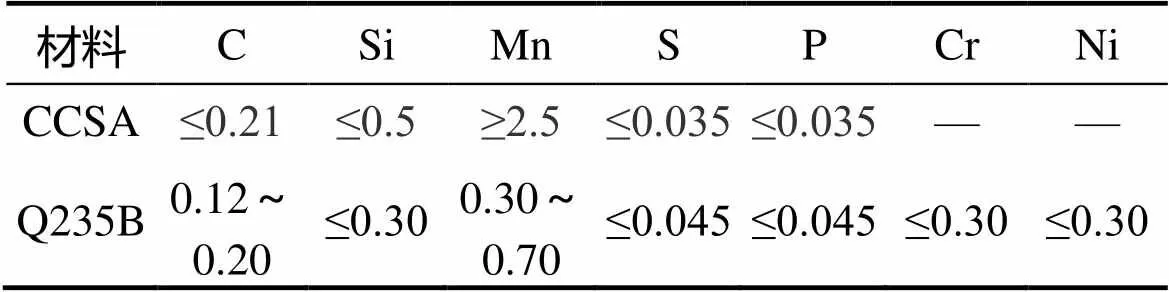
表1 CCSA和Q235B材料的化学成分
1.2 方法
1.2.1 长江淡水环境试验
试验参照GB/T 5776—2005《金属和合金的腐蚀金属和合金在表层海水中暴露和评定的导则》,在武汉淡水试验站进行腐蚀试验,试验区域包括水下全浸区,水面大气区和干湿交替水线区。同时在室内进行长江水浸泡试验,监测两种材料的腐蚀电位。
1.2.2 腐蚀速率测量
环境腐蚀试验后试样按照预定时间取出,用清水刷洗表面泥土,然后烘干拍照。除锈参照GB/T 16545—2005《金属和合金的腐蚀腐蚀试样上腐蚀产物的清除》,除锈的溶液见表2。试样除锈后,先用清水刷,然后用无水乙醇脱水处理,最后把试样放入烘箱中,在100 ℃下保温30 min,烘干的试样放入干燥器中24 h后,用电子天平称量,并计算材料的腐蚀速率。

表2 清除腐蚀产物所用化学清洗方法
1.2.3 形貌及物相结构分析
室外长江水浸泡试验后宏观形貌用数码相机拍照,将试样表面的腐蚀产物刮取下来,碾成粉末进行XRD检测,仪器型号为D8-Focus,40 kV,40 Ma,扫描速度每步0.05 s。
1.2.4 电化学试验
将试样材料切割成暴露面积为10 mm ×10 mm的试样,并焊上铜导线,然后将非工作面用环氧树脂封装。试验前,每个电极先用砂纸依次360#、800#和2000#逐级打磨,金刚石抛光剂抛光,用丙酮超声除油清洗。最后在冷空气流下干燥,放入干燥器中24 h后进行电化学测试。
电化学测试采用PARSTAT2273 电化学工作站,测量采用三电极体系,饱和甘汞电极(SCE)作为参比电极,石墨电极为辅助电极,测试所用电解液为长江淡水,室温。Tafel 极化曲线的测量参数:电位扫描范围±250 mV(相对于自腐蚀电位),扫秒速度为1 mV/s。
2 结果与讨论
2.1 室外长江淡水浸泡试验
2.1.1 宏观腐蚀形貌分析
0.5,1 a试验后两种碳钢材料的腐蚀形貌如图1—4所示,两种材料的腐蚀形貌相似,但在3个不同区域其腐蚀形貌完全不同。在水面大气区表面布满红褐色锈层,锈层均匀,且1 a较0.5 a的试样锈层更加致密,颜色变深,没有分层现象,其中Q235B锈层分布较CCSA致密。在全浸区,有瓜子状大小的贝类水生物附着,表面大部分区域布满褐色锈蚀,夹杂红色锈斑,锈层较厚,易脱落,少量区域还可见基体未腐蚀。其中1 a试样表面较0.5 a瓜子状大小的贝类水生物附着更多,锈层疏松且突起更加明显,有分层现象。半浸泡区试样,水面大气部分布满褐色锈层,水线附近的水下区域同水下试样,有瓜子状大小的贝类水生物附着,表面大部分区域布满褐色锈蚀,夹杂红色锈斑,锈层较厚,水线区锈层有明显突起且密集分布腐蚀严重。
0.5,1 a后表现出腐蚀的原因是由于水中氧气、微生物等综合作用。

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区
1)氧作为金属腐蚀过程中的去极化剂,它不仅影响淡水的基本水质,而且淡水中含有的氧是造成金属腐蚀的主要原因。试验结果表明,含氧量越大腐蚀越快[4]。
2)当金属表面存在微生物时,或结构表面堆积有含硫酸盐还原菌的泥沙时,由于细菌的新陈代谢作用,在金属局部区域分泌出无机酸或者有机酸。例如硫氧化菌能氧化元素硫、硫代硫酸盐等产生代谢产物硫酸,从而加速了钢铁的腐蚀破坏[5]。
两种材料经0.5,1 a暴露,试样去锈后的腐蚀形貌如图5—8所示。水面大气试样表面为均匀的麻点腐蚀,其中1 a分布较0.5 a致密,Q235B较CCSA腐蚀点密集。水下区域试样表面布满大小不一的腐蚀坑,其中1 a腐蚀坑较为明显。半浸泡试样上部如大气腐蚀为麻点腐蚀,下部区域为坑状腐蚀,水线附近腐蚀严重,腐蚀坑比全浸区大和深。对于碳钢而言,氧是腐蚀控制因素,氯离子是引起点蚀的主要因素[6],其腐蚀类型与碳钢在海水中的腐蚀类型一致[7]。长江淡水中含有少量具有强渗透能力的Cl-,腐蚀产物层难以阻挡Cl-的渗透,一旦坑蚀形成,其活性在局部增强致使点腐蚀深度增加[8]。

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区

a 水面大气区 b 水线区 c 水下区
2.1.2 XRD物相结构分析
对在两种材料1 a试样的水面大气暴露、半浸泡水线上、半浸泡水线下、全浸泡4种区域试样表面锈层进行X射线衍射分析,试验结果如图9和图10所示。
水面大气暴露试样锈层主要由FeOOH,Fe(OH)3和少量Fe2O3构成(见图9a、图10a),这和Evans提出的大气腐蚀机理相一致[9]。首先基体发生溶解,阳极反应:2Fe→2Fe2++4e,阴极反应:2H2O+O2+ 4e→4OH-。然后Fe2+和OH-发生溶解迁移结合,进一步氧化形成胶体氢氧化物Fe(OH)3,Fe(OH)3+ H2O→FeOOH或者2Fe(OH)3→Fe2O3+3H2O。半浸泡水线上方暴露大气面试样锈层主要由FeOOH,Fe2O3,Fe3O4构成,Q235B含有微量SiO2应为局部水花飞溅导致锈层中夹杂微小泥沙(图9b、图10b),
半浸泡试样,水线下浸水面表面锈层主要由FeOOH,Fe3O4构成(图9c、图10c),全浸泡试样表面锈层主要由FeOOH,Fe3O4和少量SiO2构成(图9d、图10d)。碳钢浸泡8 周以后,锈层主要为FeOOH,且主要电化学反应为3Fe3O4+4H2O=8FeOOH+Fe3O4。其中半浸泡试样锈层衍射峰强度明显大于水面大气暴露和全浸泡锈层衍射峰强度,主要锈层成分FeOOH,Fe3O4的含量较多,且腐蚀最明显。
2.1.3 腐蚀速率
0.5,1 a试验后两种碳钢材料的腐蚀速率见表3。结合锈层宏观形貌和XRD物相分析,两种材料具有相同的腐蚀规律,在水线区域腐蚀速率最大,水面大气腐蚀速率最小。对两种材料进行对比,CCSA的腐蚀速率小于Q235B,CCSA的具有较好的耐蚀性。其中两种材料在水面大气暴露、半浸泡中都表现出腐蚀速率增长的趋势且半浸泡增长率更明显。

表3 Q235B和CCSA 两种试样0.5,1 a腐蚀速率 μm/a
2.2 室内浸泡试验
2.2.1 开路电位随时间变化
开路电位每天定时测,参比电极为甘汞电极,测试结果如图11所示。两种材料于半浸泡状态下开路电位负于全浸泡状态下开路电位,且在第二天电位急剧下降,随后趋于平缓趋势。这和表面锈层的增厚导致锈层电阻的增加,和氧渗入困难从而减小阴极去极化作用有直接关系。浸泡初期,在金属锈层界面溶解氧的含量较高,溶解氧供应比较充足的情况下,阴极以氧还原为主,锈层不会参与阴极反应。比较腐蚀电位表明,半浸泡状态下铁活性更大,试样更易腐蚀。
2.2.2 腐蚀速率
表3显示Q2355B和CCSA分别在全浸和半浸环境下的平均腐蚀速率大小。在浸泡768 h后,结果表明,材料腐蚀速率在半浸泡环境下大于全浸泡的环境,这与开路电位变化的结果表现出一致性。这说明浸泡方式不同对腐蚀有显著的影响,主要是由于溶液与空气交界处氧气含量等因素造成的。氧是一种去极化剂,能加速金属的腐蚀过程,含氧浓度越高,电极电位越正,而含氧浓度较低的部位电位越负,从而可以形成一个腐蚀电池,含氧少的部位发生金属腐蚀这就是所谓的氧浓差电池[11-12]。

表3 试样浸泡768 h后腐蚀速率
2.3 电化学试验
2.3.1 浸泡时间的影响
图12为Q235B和CCSA在室内淡水中不同浸泡时间的极化曲线。用Tafel外推法可以求出在自腐蚀电位下的腐蚀电流密度[13],见表4和图13。由结果可知,随试验时间延长,极化曲线往左移动,说明随时间延长腐蚀速率减小。Q235B起始浸泡的自腐蚀电位为-0.660 V,在浸泡2 d后,自腐电位快速降到-0.723 V,随后电位缓慢变小并降至-0.726 V。CCSA起始浸泡的腐蚀电位为-0.468 V,2 d后电位降至-0.681 V,随后表现出与Q235B相一致的趋势缓慢降至-0.725 V。由此可知。两种船用钢板材料腐蚀速率在短期内表现出一个由快速下降到缓慢下降的过程,这和浸泡试验中所测开路电位变化趋势表现出一致性。

表4 Q235B,CCSA 在室内长江淡水中不同浸泡时间的极化曲线拟合值
从图12可以看出,阳极反应速度和斜率基本不变,表明锈层对阳极过程的影响不大。锈层下阳极过程仍然是铁溶解反应,但锈层对阴极过程有较大影响。其原因在于碳钢在淡水中的腐蚀属于电化学腐蚀,长江淡水含盐量少,一般呈中性。金属的腐蚀是氧去极化的电化学腐蚀,水中的溶解氧的含量或扩散影响阴极极化过程。淡水中含盐量低,导电性差,电化学腐蚀反应过程中的电阻比在海水中大,其腐蚀主要以微电池腐蚀为主。淡水下金属腐蚀按以下反应式进行:
阳极反应 2Fe→2Fe2++4e
阴极反应 2H2O+O2+4e→4OH-
总反应 2Fe+2H2O+O2→2 Fe(OH)2
上述腐蚀产物Fe(OH)2进一步受氧作用,生成Fe(OH)3和Fe2O3:4Fe(OH)2+2H2O+O2→4Fe(OH)3,Fe(OH)3脱水而形成铁锈:2Fe(OH)3→Fe2O3+3H2O。这是水中钢铁腐蚀的过程也是钢铁腐蚀电化学机理[14]。其中腐蚀速率减缓是由于腐蚀产物层覆盖在金属基体表面,并随时间延长增厚,延缓了介质中氧向金属基体扩散的速度。
3 结论
1)两种船用钢板材料在武汉长江淡水中腐蚀严重,半浸泡环境下腐蚀速率最大,达到100 μm/a。水面大气腐蚀速率最小,腐蚀速率接近30 μm/a,全浸区Q235B腐蚀速率0.5 a超过90 μm/a,CCSA仅为80 μm/a,耐蚀性能优于Q235B。
2)XRD结果说明,水面大气暴露试样锈层主要由FeOOH,Fe(OH)3和少量Fe2O3构成,半浸泡水线上方暴露大气面试样锈层主要由FeOOH,Fe2O3,Fe3O4和微量SiO2构成,半浸泡水线下浸水面表面锈层主要由FeOOH,Fe3O4构成,全浸泡试样表面锈层主要由FeOOH,Fe3O4和少量SiO2构成。
3)室内长江淡水浸泡的环境下两种船用钢板材料腐蚀电位随时间而降低,2 d后趋于稳定;半浸泡环境下腐蚀速率大于全浸区,与户外结果一致。极化曲线说明,浸泡2 d后,随表面腐蚀产物生成,腐蚀速率降低且趋于稳定。
[1] 颜民, 黄桂桥. 中国水环境腐蚀试验站网工作回顾与展望[J]. 海洋科学, 2005, 29(7): 73-76.
[2] 张小阳, 王占华, 张志修. 材料及防护涂层在淡水环境中的腐蚀试验研究[J]. 腐蚀与防护, 2006, 27(5): 240-243.
[3] 黄桂桥, 杨朝晖, 周学杰, 等. 钢铁材料在武汉长江中的现场腐蚀试验结果[J]. 腐蚀与防护, 2009(10): 675-677.
[4] 杨志宽. 钢制散热器腐蚀与控制[J]. 暖通空调, 2001, 31(1): 21-24
[5] GIBSON G R. Physiology and Ecology of the Sulphate- reducing Bacteria[J]. Journal of Applied Microbiology,1990, 69(6): 769-97.
[6] HU J, CAO S, HAN J, et al. Research on Corrosion Factors and Corrosion Prevention Measure of Carbon Steel in Produce Water of Reverse Osmosis in Power Plant[C]// Asia-Pacific Power and Energy Engineering Conference. IEEE Computer Society, 2011:1 - 4.
[7] 胡家元, 曹顺安, 谢建丽. 锈层对海水淡化一级反渗透产水中碳钢腐蚀行为的影响[J]. 物理化学学报, 2012, 28(5): 1153-1162.
[8] 夏兰廷. 铸铁材料在长江淡水中的腐蚀研究[J]. 铸造, 2008, 57(10): 1046-1051.
[9] 李晓刚. 金属大气腐蚀初期行为与机理[M]. 北京: 科学出版社, 2009.
[10] 邹妍, 王佳, 郑莹莹. 锈层下碳钢的腐蚀电化学行为特征[J]. 物理化学学报, 2010, 26(9):2361-2368
[11] 陈庆, 时黎霞, 腾玉华. 介质的成分、浓度和温度对金属材料电化学腐蚀的影响[J]. 吉林化工学院学报, 2000(1): 63-66.
[12] 王凤平, 康万利, 敬和民, 等. 腐蚀电化学原理、方法及应用腐蚀电化学原理方法及应用[M]. 北京: 化学工业出版社, 2008: 50-53
[13] 曹楚南. 腐蚀电化学原理[M]. 北京: 化学工业出版社, 2004: 56-65.
[14] 曹刚, 高翠, 甘复兴. 碳钢在淡水环境中的腐蚀行为[J]. 装备环境工程, 2006, 3(1): 46-51
Initial Corrosion Behaviors of Ship Steel Plate in Fresh Water Environment
HAO Zhang-ke1,2, CHEN Zhi-biao3, ZHANG Dong1,2, PAN Ying1,2, ZHOU Xue-jie1,2
(1.Wuhan Research Institute of Materials Protection, Wuhan 430030, China 2.State Key Laboratory of Special Surface Protection Materials and Application Technology, Wuhan 430030, China 3.Wuhan Institute of Specification of China classification society, Wuhan 430030, China)
Objective To study initial corrosion behaviors of ship steel plate material in fresh water environment of the Yangtze River. Methods Several methods including morphology analysis, weight loss analysis, XRD, open circuit potential and polarization curves were used to study corrosion behaviors of Q235B and CCSA in different exposure modes (surface water, semi immersion, full immersion) and different soaking time (0.5a, 1a) in outdoor fresh water environment of the Yangtze River; corrosion behaviors in different exposure conditions (semi immersion and full immersion) in indoor fresh water environment of the Yangtze River in 768h; electrochemical corrosion behaviors of indoor fresh water environment at different times (0-14 d). Results Two kinds of ship steel plate materials suffered from serious corrosions in the Wuhan Section of the Yangtze River. The corrosion rate in the semi immersion environment was the largest, which was up to100 μm/a; the corrosion rate in the water surface area was the smallest, which was about 30 μm/a and the whole immersion zone was about 80 μm/a; the corrosion resistance of CCSA was better than that of Q235B and the corrosion rate was similar between 1 and 0.5 years. The corrosion potential of two kinds of marine steel plates in the fresh water immersion environment of Yangtze River decreased with time, and tended to be stable 2 days later. The corrosion rate in the semi immersion environment was greater than that of the full immersion zone. The polarization curves showed that after 2 days of immersion, the corrosion rate decreased and tended to be stable. Conclusion The corrosion resistance of CCSA is better than that of Q235B.The corrosion is the most serious in the semi immersion environment, followed by the total immersion zone, and the minimum environmental corrosion in the water surface.
ship plate; freshwater environment; corrosion
10.7643/ issn.1672-9242.2017.09.015
TJ04;TG172
A
1672-9242(2017)09-0073-07
2017-05-27;
2017-06-20
国家科技基础条件平台项目(2005DKA10400)
郝张科(1990—),男,河南鹤壁人,硕士研究生,主要研究方向为金属腐蚀与防护。
周学杰(1965—),男,研究员,主要研究方向为材料腐蚀与防护。

