不同方法诱导THP-1细胞分化效果比较
彭卓颖,丛 喆,李 想,薛 婧,魏 强
(北京协和医学院比较医学中心,中国医学科学院医学实验动物研究所,卫生部人类疾病比较医学重点实验室,国家中医药管理局人类疾病动物模型三级实验室,新发再发传染病动物模型研究北京市重点实验室,北京 100021)
研究报告
不同方法诱导THP-1细胞分化效果比较
彭卓颖,丛 喆,李 想,薛 婧*,魏 强*
(北京协和医学院比较医学中心,中国医学科学院医学实验动物研究所,卫生部人类疾病比较医学重点实验室,国家中医药管理局人类疾病动物模型三级实验室,新发再发传染病动物模型研究北京市重点实验室,北京 100021)
目的优化不同方法刺激THP-1细胞定向分化为M1、M2巨噬细胞及DC细胞,为M1、M2和DC三种体外细胞模型研究奠定基础。方法首先用PMA和GM-CSF/M-CSF两种方法刺激诱导THP-1细胞分化,再分别添加不同细胞因子诱导其分化为M1、M2和DC细胞,观察细胞形态的变化,并用流式细胞术检测细胞表面分子的表达情况。结果两种方法刺激细胞CD分子表达的整体趋势基本一致。THP-1-M1细胞表面CD80和CD86表达量显著增加;THP-1-M2细胞高表达CD163和CD209;THP-1-DC细胞CD14表达量显著降低,高表达CD80、CD86和CD11c。PMA刺激后,M1、M2和DC细胞均贴壁生长;GM-CSF/M-CSF刺激后,只有DC细胞部分贴壁生长,M1和M2细胞仍呈悬浮生长。结论两种方法均能成功地诱导THP-1细胞向不同细胞亚型分化,但是诱导出来的细胞在形态上存在一定差异,可根据实验需求选择刺激方法。
THP-1;佛波酯;粒细胞巨噬细胞刺激因子/巨噬细胞集落刺激因子;M1巨噬细胞;M2巨噬细胞;树突状细胞;分化
单核细胞经细胞因子刺激后,细胞的形态和功能会发生不同的变化,可向不同方向分化成若干亚型巨噬细胞(macrophage,Mφ)及树突细胞(dendritic cell,DC)[1]。国际上多用佛波酯(phorbol 12-myristate 13-acetate,PMA)、粒细胞巨噬细胞刺激因子(granulocyte-macrophage colony-stimulating factor,GM-CSF)和巨噬细胞集落刺激因子(macrophage colony-stimulating factor,M-CSF)协同其他细胞因子刺激人单核细胞系THP-1细胞定向分化,作为体外细胞模型对巨噬细胞和树突状细胞开展相应研究[1, 2]。本文分别用以上方法刺激THP-1定向分化为M1、M2和DC细胞,比较不同细胞因子组合刺激分化出的同种细胞在形态和细胞表面CD分子表达方面的差异,以期为开展巨噬细胞和树突细胞的功能研究奠定基础。
1 材料和方法
1.1材料
人单核细胞系THP-1购自中国医学科学院基础所细胞中心;RPMI-1640培养基、胎牛血清、胰酶均购自Gibco公司;细胞因子GM-CSF、IL-6购自R&D公司,IFN-γ、M-CSF、IL-13和IL-4购自Peprotech公司,LPS、PMA购自Sigma公司;流式抗体PE Mouse Anti-Human CD14、FITC Mouse Anti-Human CD163和PerCP-CyTM5.5 Mouse Anti-Human CD209购自BD公司,APC Mouse Anti-Human CD11c、FITC Mouse Anti-Human CD80和PE Mouse Anti-Human CD86购自BioLegend公司;同型对照抗体PE Mouse IgG2a、FITC Mouse IgG1、PerCP-CyTM5.5 Mouse IgG2b、APC Mouse IgG1和PE Mouse IgG2b分别购自BD和BioLegend公司;IC Fixation Buffer和10×Permeabilization Buffer购自eBioscience公司。
1.2实验方法
1.2.1 细胞培养
THP-1为悬浮细胞,生长速度较快,在含10%胎牛血清的RPMI-1640完全培养基中培养,细胞浓度一般控制在5×105~ 1×106个/mL,置于37℃、5% CO2孵箱中培养。
1.2.2 PMA诱导THP-1 细胞定向分化为M1、M2和DC[1, 2]
取9×106个THP-1细胞接种于T25培养瓶内,定期向培养瓶内加入不同细胞因子(表1),PMA终浓度为50 ng/mL,其余细胞因子终浓度均为20 ng/mL,第6天收集细胞进行流式检测。
1.2.3 GM-CSF/M-CSF 诱导THP-1 细胞定向分化为M1、M2和DC[1]
取7×106个THP-1细胞接种于T25培养瓶内,定期向培养瓶内加入不同细胞因子(表2),其中刺激DC分化所使用的GM-CSF的终浓度为100 ng/mL,其余细胞因子终浓度均为20 ng/mL,第9天收集细胞进行流式检测。
1.2.4 流式细胞术检测细胞表面CD分子表达量的变化
培养瓶内的细胞经胰酶消化后,用PBS洗涤2次后重悬,调整细胞浓度为1×107个细胞/mL,轻轻混匀后加入流式管内,每管100 μL细胞悬液。
(1)胞外染色:每管细胞中加入相应抗体,4℃避光孵育30 min,PBS洗2次,细胞筛过滤后上机。
(2)胞内染色[3]:向每个流式管内加入200 μL IC fixation buffer,轻轻混匀后4℃避光孵育20 min,随后加入2 mL 1× permeabilization buffer洗2次,100 μL 1× permeabilization buffer重悬细胞后加入相应抗体,轻轻混匀后4℃避光孵育30 min,1× permeabilization buffer洗2次,PBS洗1次,细胞筛过滤后上机。

表1 PMA诱导THP-1细胞定向分化方案
1.3流式分析与数据统计
应用BD Accuri C6流式细胞仪进行样本检测,FlowJo v10进行数据分析,Graphpad 5软件作图和统计分析,不同组数据间进行方差分析,以P<0.05为差异有显著性。
2 结果
2.1THP-1细胞经不同细胞因子诱导分化后的形态学变化
正常THP-1细胞形态饱满、折光性好,为单个细胞悬浮生长(图1A)。
当THP-1被PMA刺激48 h后细胞全部贴壁,且发生明显聚团(图1B)。随后加入不同细胞因子诱导细胞定向分化,显微镜下观察发现THP-1-M1细胞形态具有多样性,部分细胞呈长梭形(图1D);THP-1-M2细胞为多边形,体积有所增加(图1E);THP-1-DC细胞贴壁较牢固,体积增大较明显,大多具有细长的树突状结构,LPS和IL-6的加入未对细胞形态产生影响(图1F)。
当THP-1被GM-CSF/M-CSF刺激4 d后细胞仍呈悬浮生长,部分发生聚团,其中GM-CSF所刺激的细胞表面出现非常细小的突起(图1C),而M-CSF所刺激的细胞表面未发生变化。随后加入不同细胞因子诱导细胞定向分化,显微镜下观察发现THP-1-M1细胞表面突起增多,胞膜出现褶皱(图1G);THP-1-M2细胞表面突起较THP-1-M1少,细胞多呈圆形(图1H);而THP-1-DC细胞大部分贴壁生长,形状不规则,伸出许多短小的树突样或伪足样突起,第8天加入LPS和IL-6后细胞形态未发生明显改变(图1I)。

表2 GM-CSF/M-CSF诱导THP-1细胞定向分化方案
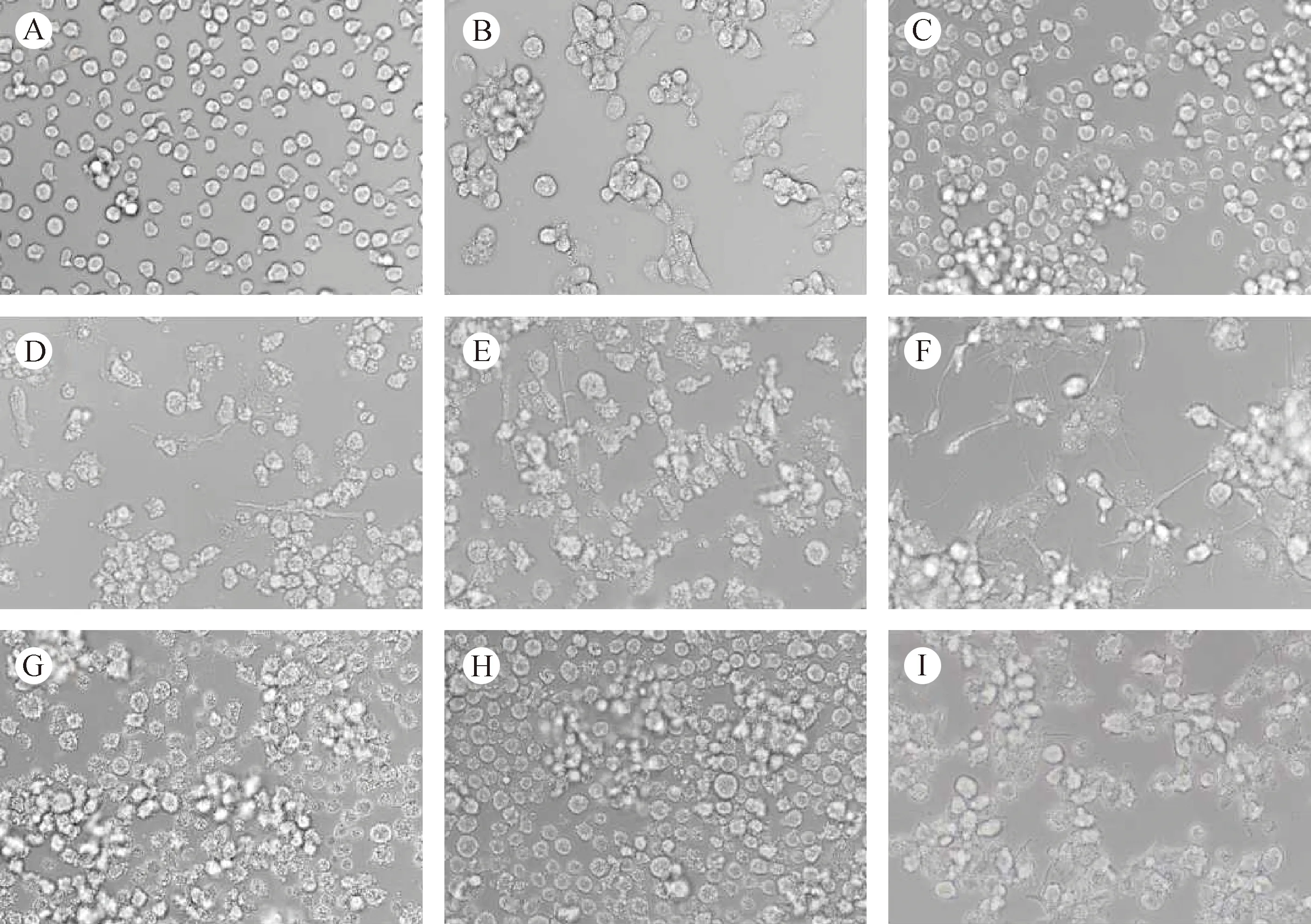
注:A:正常THP-1; B:PMA刺激后的THP-1; C:GM-CSF刺激后的THP-1; D:THP-1-M1(PMA);E:THP-1-M2(PMA); F:THP-1-DC(PMA); G:THP-1-M1(GM-CSF); H: THP-1-M2(M-CSF); I: THP-1-DC(GM-CSF)。图1 不同细胞因子刺激后THP-1细胞的形态学改变(×40)Note.A: Normal THP-1 cells; B: THP-1 cells stimulated by PMA; C: THP-1 cells stimulated by GM-CSF; D: THP-1-M1 (PMA) cells; E: THP-1-M2 (PMA) cells; F: THP-1-DC (PMA) cells; G: THP-1-M1 (GM-CSF) cells; H: THP-1-M2 (M-CSF) cells; I: THP-1-DC (GM-CSF) cells.Fig.1 Morphological changes of THP-1 cells stimulated by different cytokines
2.2THP-1细胞经不同细胞因子诱导分化后的细胞表面CD分子表达的差异
2.2.1 THP-1-M1细胞表面CD分子的表达
正常THP-1细胞表面低表达CD80[(11.27±2.73)%]。当PMA或GM-CSF刺激THP-1为THP-1-M1后,细胞表面的CD80显著升高,其表达量分别达到(77.05±7.28)%和(93.10±8.20)%,P值分别为0.0069和0.0055;两种方法所诱导的CD80的表达差异无显著性(P= 0.1744)。
正常THP-1细胞表面不表达CD86。而分化后的THP-1-M1细胞高表达CD86,其表达量分别高达(78.0±6.93)%和(49.65±6.72)%,P值分别为0.0043和0.0103;两种方法所诱导的CD86的表达量差异无显著性(P= 0.0534)(图2)。

注:“……”同型对照;“ ”CD分子。与THP-1组相比,*P<0.05,**P<0.01。图2 两种方法刺激THP-1分化为THP-1-M1细胞后CD分子的表达情况Note. “……”Isotype control; “”CD molecules. Compared with THP-1 group,*P<0.05,**P<0.01.Fig.2 Expression of CD molecules on THP-1-M1 cells stimulated by different cytokines
2.2.2 THP-1-M2细胞表面CD分子的表达
正常THP-1细胞胞内低表达CD163[(15.10±5.66)%]。当分化为THP-1-M2后,CD163的表达量显著升高,其表达量分别为(53.80±9.90)%和(67.15±4.60)%,P值分别为0.0408和0.0097;两种方法所诱导的CD163的表达量差异无显著性(P= 0.2258)。
CD209在正常THP-1细胞表面低表达[(25.30±7.07)%]。而THP-1-M2细胞则高表达CD209,其表达量分别达到(93.00±3.39)%和(72.70±11.88)%,P值为0.0066和0.0400;两种方法所诱导的CD209的表达量差异无显著性(P= 0.1458)(图3)。
2.2.3 THP-1-DC细胞表面CD分子的表达
正常THP-1细胞高表达CD14 [(89.70±1.41)%]、CD11c [(78.15±11.95)%]、CD80和CD86表达呈阴性。当PMA和GM-CSF刺激THP-1为THP-1-DC后,细胞表面的CD14显著降低,其表达量分别为(17.3±2.40)%和(20.85±7.28)% (P值分别为0.0007和0.0058)。CD11c的表达无明显变化,分别为(58.0±10.04)%和(74.95±6.01)%(P值分别为0.2094和0.7673)。CD80和CD86的表达量显著升高,CD80的表达量分别达到(39.41±7.48)%和(20.56±4.59)%(P值分别为0.0195和0.0302);CD86表达量分别为(78.35±4.88)%和(73.10±6.79)%(P值分别为0.0024和0.0049)。两种方法所诱导的CD分子的表达差异无显著性,P> 0.05(图4)。
3 讨论
一直以来,单核巨噬细胞和树突状细胞都是固有免疫系统中研究的重点。然而由于其数量少、分离困难[4,5],使得其研究工作受限。THP-1是来源于急性单核细胞性白血病患者的一种单核细胞系,高表达CD14分子[6],目前多用来代替原代单核细胞进行相关研究。对于巨噬细胞和树突状细胞,国际上较通用的方法为以GM-CSF/M-CSF为主,辅以IL-4、LPS等其他相关细胞因子刺激原代单核细胞进行分化,单核细胞系的分化则多用PMA进行诱导,然而GM-CSF/M-CSF刺激单核细胞系分化的研究比较欠缺。为了明确两种刺激方法诱导单核细胞系分化的差异,本文利用THP-1为单核细胞系模型,并在GM-CSF/M-CSF和PMA两种方法的基础上做了进一步优化[1],对其诱导THP-1细胞的分化效果进行对比。

注:“……”同型对照;“”CD分子。与THP-1组相比,*P<0.05,**P<0.01。图3 两种方法刺激THP-1分化为THP-1-M2细胞后CD分子的表达情况Note: “……”Isotype control; “”CD molecules. Compared with THP-1 group,*P<0.05,**P<0.01.Fig.3 Expression of CD molecules in THP-1-M2 cells stimulated by different cytokines

注:“…… ”同型对照;“”CD分子。与THP-1组相比,ns:差异无显著性;*P<0.05,**P<0.01,***P<0.001。图4 两种方法刺激THP-1分化为THP-1-DC细胞后CD分子的表达情况 Note.“…… ”Isotype control; “ ”CD molecules.Cmpared with THP-1 group, ns:not significant,*P<0.05,**P<0.01,***P<0.001.Fig.4 Expression of CD molecules on THP-1-DC cells stimulated by different cytokines
M1巨噬细胞表面较典型的分子为CD80和CD86[1]。当单核细胞分化为M1后,细胞表面的协同刺激因子CD80和CD86的表达量都会增加,此时细胞在免疫反应中对抗原的提呈能力增强[7]。研究结果发现,THP-1细胞经PMA与GM-CSF刺激诱导出的THP-1-M1均可高表达这两种CD分子,但是M1细胞的形态差异较大。PMA刺激后的细胞贴壁明显,可清晰观察到细胞表面的突起,形态上接近巨噬细胞,但是后期消化极度困难,易破碎,细胞不好再利用;GM-CSF刺激后的THP-1-M1细胞一直为悬浮生长,表面突起不明显,但细胞表面标志性的CD分子表达量正常,与PMA刺激的THP-1-M1细胞没有明显差异。
M2巨噬细胞高表达CD163和DC-SIGN[8]。CD163分子为清道夫受体蛋白,可参与机体多种免疫活动,对正常生理功能有非常重要的作用[9];DC-SIGN又被称作CD209,巨噬细胞表面的CD209可识别并结合病毒或细菌表面的病原相关分子模式受体[10]。本研究中PMA与M-CSF均可成功诱导出M2细胞,高表达CD163与CD209,但与M1细胞相同,两种方法刺激分化出的THP-1-M2细胞在形态上同样有很大差别。
DC细胞没有特征性的标志分子,一般会通过细胞表面CD14、CD80、CD86和CD11c等分子的表达来判断细胞的分化情况。研究结果显示,PMA与GM-CSF所刺激分化出的细胞表面分子的变化与文献中报道一致[11, 12],CD14明显下降,高表达CD80、CD86和CD11c。细胞贴壁生长,体积明显增大,大多具有细长的树突状结构。PMA刺激出的DC细胞整体形态及树突均偏细长,而GM-CSF刺激出的DC细胞偏多边形,树突短粗。
综上所述,GM-CSF/M-CSF和PMA两种方法均可诱导单核细胞系THP-1向M1、M2型巨噬细胞和DC细胞方向分化,所诱导的细胞表面分子的变化趋势较一致,但是在形态学方面差异较大。GM-CSF/M-CSF诱导出的M1和M2型巨噬细胞均为悬浮生长,DC细胞处于半贴壁状态,有利于细胞的获取再利用方面的研究,如流式细胞术检测;PMA所诱导出的M1、M2和DC细胞贴壁较牢固,消化困难,但其形态上更接近原代细胞,有利于细胞形态学方面的研究,如间接免疫荧光染色、激光共聚焦等。因此可以根据实验目的,针对性选择刺激方法,这将有助于我们更好地开展巨噬细胞和树突状细胞的功能研究。
[1] Zarif JC, Hernandez JR, Verdone JE, et al. A phased strategy to differentiate human CD14+monocytes into classically and alternatively activated macrophages and dendritic cells[J]. Biotechniques, 2016, 61(1): 33-41.
[2] Genin M, Clement F, Fattaccioli A, et al. M1 and M2 macrophages derived from THP-1 cells differentially modulate the response of cancer cells to etoposide[J]. BMC Cancer, 2015, 15: 577.[3] 吴芳新, 王卫, 丛喆, 等. 艾滋病猴特异性细胞免疫的胞内细胞因子检测方法优化与应用[J]. 中国实验动物学报, 2012, 20(1): 18-23.
[4] 孙晓梅, 曹春渝, 高家红, 等. 血细胞分离机大量采集实验猕猴外周血单核细胞方法探讨[J]. 中国实验动物学报, 2008, 16(6): 424-427.
[5] 桑明, 代明, 周立, 等. 恒河猴外周血单核巨噬细胞体外培养方法的建立[J]. 中国实验动物学报, 2015, 23(1): 18-24.
[6] Ziegler-Heitbrock L, Ancuta P, Crowe S, et al. Nomenclature of monocytes and dendritic cells in blood[J]. Blood, 2010, 116(16): 74-80.
[7] Konttinen Y T, Pajarinen J, Takakubo Y, et al. Macrophage polarization and activation in response to implant debris: influence by “particle disease” and “ion disease”[J]. J Long Term Eff Med Implants, 2014, 24(4): 267-281.
[8] Zhao M. Macrophage polarization and HIV infection[J]. Infect Dis Inf, 2011, 87(4): 599-608.
[9] 尚艳楠, 薛江东, 马德慧. CD163分子的研究进展[J]. 中国动物保健, 2015, 17(4): 68-70.
[10] Mcgreal EP, Miller JL, Gordon S. Ligand recognition by antigen-presenting cell C-type lectin receptors[J]. Curr Opin Immunol, 2005, 17(1): 18-24.
[11] Vogelsang P, Karlsen M, Brun JG, et al. Altered phenotype and Stat1 expression in Toll-like receptor 7/8 stimulated monocyte-derived dendritic cells from patients with primary Sjögren’s syndrome[J]. Arthritis Res Ther, 2014, 16(4): R166.
[12] Yang AX, Chong N, Jiang Y, et al. Molecular characterization of antigen-peptide pulsed dendritic cells: immature dendritic cells develop a distinct molecular profile when pulsed with antigen peptide[J]. PLoS One, 2014, 9(1):e86306.
ComparisonoftheeffectsofdifferenttreatmentsonTHP-1celldifferentiation
PENG Zhuo-ying, CONG Zhe, LI Xiang, XUE Jing*, WEI Qiang*
(Comparative Medicine Center, Peking Union Medical College (PUMC) & Institute of Laboratory Animal Sciences, Chinese Academy of Medical Sciences (CAMS) Medical; Key Laboratory of Human Disease Comparative Medicine, Ministry of Health; Key Laboratory of Human Disease Animal Models, State Administration of Traditional Chinese Medicine, Beijing Key Laboratory for Animal Models of Emerging and Remerging Infectious Diseases, Beijing 100021, China)
ObjectiveTo stimulate a human monocytic cell line THP-1 cells to differentiate into M1, M2 macrophages and dendritic (DC) cells by optimization of different methods, and lay the foundation for the study of M1, M2 and DC cell modelsinvitro.MethodsTHP-1 cells were stimulated by PMA and GM-CSF/M-CSF, respectively. Then, they were induced to differentiate into M1, M2 macrophages and DC cells by adding different cytokines, such as LPS, IL-6 and IFN-γ for M1 macrophages, IL-4, IL-13 and IL-6 for M2 macrophages, and IL-4 for DCs. Subsequently, the morphology of cells was observed and the expression of cell surface (CD) molecules was detected by flow cytometry.ResultsAfter stimulation with the two methods, the trends of CD molecules expression were basically the same. The expression of CD80 and CD86 on the THP-1-M1 cells were increased significantly, and CD163 and CD209 were highly expressed on the THP-1-M2 cells. For THP-1-DC cells, the expression of CD14 was significantly decreased, while the expression of CD80, CD86 and CD11c increased. M1, M2 macrophages and DC cells were adherent after stimulation with PMA. However, DC cells were partially adherent after GM-CSF/M-CSF treatment. M1 and M2 macrophages were also growing in suspension.ConclusionsBoth methods used in this study can successfully induce THP-1 cells to differentiate into different subtypes, but there are some differences in the morphology of the induced cells. Appropriate stimulation method can be selected according to the experimental requirements.
THP-1 cell line; Phorbol 12-myristate 13-acetate, PMA; GM-CSF/M-CSF; M1 macrophage; M2 macrophage; Dendritic cell; Differentiation
R-33
A
1671-7856(2017)09-0001-06
10.3969.j.issn.1671-7856. 2017.09.001
2016-12-28
国家自然科学基金青年科学基金项目(编号:81301437);科技部重大专项(编号:2014ZX10001001-001-004, 2014ZX10001001-002-006)。
彭卓颖 (1992- ),女,硕士研究生,从事实验动物病毒学研究工作。E-mail: 18810963239@163.com
薛婧 (1983- ),女,副研究员,硕士生导师,研究方向:病原生物学和免疫学,E-mail: xuejing@cnilas.org; 魏强 (1964- ), 男,研究员,博士生导师,研究方向:实验动物病毒学, E-mail: weiqiang0430@cnilas.org *共同通讯

