新亚特兰大标准下急性胰腺炎局部并发症的MRI评价
肖波
·图文讲座·
新亚特兰大标准下急性胰腺炎局部并发症的MRI评价
肖波
在急性胰腺炎(AP)2012年亚特兰大修订版分类和国际共识的新定义中,关于AP的主要局部并发症被重新定义和命名,包括急性胰周液体积聚、胰腺假性囊肿、急性坏死性积聚及胰腺包裹性坏死,每一种局部并发症又分为无菌性和感染性。影像学检查在对AP局部并发症的评价上有着举足轻重的作用,能为临床提供胰腺、胰周及胰外改变程度的客观依据,从而会影响到AP患者的治疗。尽管传统局部并发症的特征是依据增强CT表现而制定的,但在评价某些胰周积液的性质方面MRI更具有优势,即MRI能提供更多有价值的细节征象。本文就新亚特兰大诊断指南下AP局部并发症的MRI表现作一图文综述。
急性胰腺炎; 磁共振成像; 新亚特兰大分类; 局部并发症; 假性囊肿; 包裹性坏死
急性胰腺炎(acute pancreatitis,AP)是消化系统多发病,也是一种常见的急腹症。我国的急性胰腺炎以胆石症为病因的胆源性胰腺炎居多,但随着物质生活的日益富足和不健康生活方式的流行,大量或长期饮酒诱发的酒精性胰腺炎和肥胖症并发的高脂血症性胰腺炎日趋增多。在“急性胰腺炎2012年亚特兰大修订版分类标准和国际共识”的新定义中[1],将急性胰腺炎的主要局部并发症分为4种,包括急性胰周液体积聚(acute peripancreatic fluid collections,APFCs)、胰腺假性囊肿(pancreatic pseudocyst,PP)、急性坏死性积聚(acute necrotic collections,ANCs)和包裹性坏死(walled-off necrosis,WON)。其中,前2种局部并发症见于急性间质水肿性胰腺炎,后2种则见于急性坏死性胰腺炎,上述局部并发症的影像学表现在新的亚特兰大标准中是依赖增强CT的形态学特征[2-4]。不过,在临床工作中,笔者认为MRI在显示急性胰腺炎本身及胰周并发症的各种细节征象上更佳[5,6],故本文就新亚特兰大分类标准下急性胰腺炎的局部并发症的MRI表现作一图文综述。
与CT比较,对急性胰腺炎局部并发症的显示上,MRI有如下优势:①T1WI抑脂像可显示胰腺内部和胰腺外周的出血灶及范围,出血灶可呈斑片状、片状稍高信号影,是诊断急性坏死性胰腺炎的一项依据;②T2WI抑脂像对胰周渗出、胰周液性积聚物的显示十分敏感,且有利于显示高信号的液性积聚内部的等、低信号混杂成份,从而对后文提及的几种局部并发症的鉴别诊断有益;③磁共振胰胆管造影(magnetic resonance cholangiopancreatography,MRCP)系重T2WI,故对液性包裹物的整体形态和内部结构显示效果较好;④DWI图像对胰内及胰周包裹性液性积聚内的液体显示效果同样较好,但它不是鉴别几种局部并发症的优势序列(T2WI抑脂像最好),因为局部并发症的鉴别主要是依据内容物成份的复杂性。
MRI的不足之处在于对于胰周感染积气的显示不及CT,对胰周液性渗出或积聚物内的少量脂肪组织的显示也不及CT。
急性间质水肿性胰腺炎
1.急性胰周液体积聚
APFCs仅出现在急性间质水肿性胰腺炎,在新亚特兰大分类中,此型胰腺炎在发病4周以内影像学上可见胰腺周围的积液(常位于胰腺体尾部周围、左侧肾旁前间隙),呈游离性积液,且积液的性质单一,没有坏死组织位于其中[1-3]。其MRI表现为胰腺体积可正常,也可肿大,但实质信号均匀,平扫及增强图像上胰腺本身及胰周没有坏死灶;胰腺周围可见条带状、片状长T1、长T2液体信号影,积液可位于胰周(图1)、左侧肾旁前间隙(图2)、网膜囊等部位,呈“单纯的液体征象”;APFCs常受到正常胰周筋膜平面的限制(如左侧肾前筋膜)。APFCs不会与主胰管相连通,这类积液很少出现感染并发症。经临床内科治疗后,急性胰周液体积聚绝大多数在4周以内可自行吸收消失,在随访的MRI图像上可得以反映(图3),故该局部并发症预后良好。
2.胰腺假性囊肿
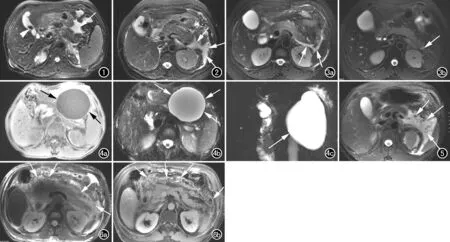
图1 男,47岁,上腹痛4天伴加重1天入院,急性胰腺炎伴急性胰周液体积聚。FSE T2WI抑脂像示胰腺体尾部前方片状液性稍高信号影,液体信号均匀(箭);胆囊内可见一枚结石影(箭头)。 图2 女,63岁,上腹痛1天入院,急性胰腺炎伴胰周急性胰周液体积聚。FSE T2WI抑脂像示左侧肾旁前间隙条片状液性稍高信号影,液体信号均匀(箭)。 图3 女,44岁,腹痛1天入院,急性胰腺炎伴急性胰周液体积聚。a) FSE T2WI抑脂像示胰腺实质信号均匀,胰尾周围、左侧肾旁前间隙条片状液性稍高信号影,液体信号均匀(箭); b) 治疗13天后、出院前MRI复查示急性胰周液体积聚完全吸收(箭)。 图4 男,55岁,急性胰腺炎后胰腺假性囊肿形成。a) GRE T1WI抑脂像示胰腺体部左前方一直径约6.5 cm的类圆形囊状低信号影,周边呈等信号环形薄壁(箭); b) FSE T2WI抑脂像示该病变呈囊状稍高信号影,囊壁呈环形低信号(箭); c) MRCP图像示该囊性占位为均质的水样信号影(箭),系胰腺假性囊肿形成,符合新亚特兰大标准的定义。 图5 男,47岁,腹痛1天入院,急性坏死性胰腺炎伴急性坏死性积聚。FSE T2WI抑脂像示胰腺尾部有坏死,左侧肾旁前间隙积液内见较多条絮状低信号影即坏死组织碎片(箭)。 图6 男,46岁,上腹疼痛2天入院,急性坏死性胰腺炎伴胰周急性坏死性积聚。a) FSE T2WI抑脂像示胰腺信号未见明显异常,胰周见大量液性渗出,累及腹膜后和肠系膜区脂肪组织,且胰周积液内见不规则条带状低信号影(箭),提示胰周组织坏死; b) 增强扫描静脉期示胰腺实质强化均匀,胰腺外周腹膜、系膜区见网格状、条索状炎性强化改变(箭),既往诊断术语为“胰周蜂窝组织炎”,在新亚特兰大分类中,应称为“急性坏死性胰腺炎(仅胰周坏死型)伴急性坏死性积聚”。
在新亚特兰大分类中,PP来源于 APFCs在4周之后未吸收而逐渐包裹而成,在CT上的形态学特征与1992年亚特兰大分类中的定义并没有发生变化[1],但有非常重要的3点更新,需引起影像科医生和临床医生的重视:①PP被定义为仅见于急性间质水肿性胰腺炎这一病理类型,发病超过4周以后见到的胰周包裹性积液。换言之,若CT/MRI诊断为急性坏死性胰腺炎,后期出现的胰周包裹性积液则不能称为“假性囊肿”;②PP的内容物被定义为仅含有胰酶的液体成份。凡胰周包裹性积液内部含有非液性物质影(不论多少),就不能称之为胰腺假性囊肿;③胰腺本身(胰腺内)的包裹性积液或累及到胰腺内(即胰腺内外)的包裹性积液,也不称之为胰腺假性囊肿,而被视作胰腺本身的坏死。基于上述的新定义标准,笔者对本院2006年1月-2016年1月的连续性急性胰腺炎住院患者的病例资料进行了回顾性分析[7],纳入急性胰腺炎发病后期因临床考虑“假性囊肿形成”而行MRI检查,并由MRI诊断为“胰腺假性囊肿形成”者,共搜集到113例连续性急性胰腺炎患者在病程后期行MRI检查,由MRI诊断为“胰腺假性囊肿”的病灶共计170个,病灶平均大小8.5 cm(1.5~24.5 cm),笔者发现MRI检出的这170个“胰腺假性囊肿”病灶(包裹性液性积聚影)按新亚特兰大分类标准有167个(98.2%)应改称为后面将介绍的“胰腺包裹性坏死灶”,仅3个(1.8%)真正满足PP的新分类要求。原因包括:后期有胰腺/胰周包裹性积液形成的113例急性胰腺炎病例中仅3例MRI表现属于急性间质水肿性胰腺炎,其余病例均存在胰腺和/或胰周不同程度的坏死灶;此外,本组167个(98.2%)包裹性液性积聚灶内见或多或少的非液性物质影,呈附壁或游离的飘带状、破絮状、斑片状、点结节状碎片影的MRI征象;仅3个(1.8%)包裹性液性积聚灶内为均匀的液体信号影,未见非液性物质信号(图4)。因此笔者认为真正符合新亚特兰大标准中定义的胰腺假性囊肿已相当罕见,绝大多数需用后面提及的胰腺包裹性坏死这一新术语替代;换言之,假性囊肿这一术语在急性胰腺炎中的使用应当很少了,甚至会被弃用。
急性坏死性胰腺炎
1.急性坏死性积聚
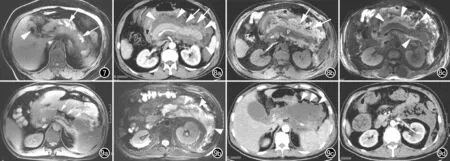
图7 女,65岁,腹痛3天入院,急性坏死性胰腺炎伴急性坏死性积聚合并出血。GRE T1WI抑脂像示胰周坏死性积液中见多发斑片状稍高信号影(箭),提示胰周出血灶,另胆囊内可见一枚结石影(箭头)。 图8 患者,男,63岁,急性坏死性胰腺炎(胰周脂肪坏死)伴胰周急性坏死性积聚。a) 发病后3天CT增强扫描示胰腺未见确切坏死区,胰腺周围大片状液体积聚(箭头),其内可见数个直径几毫米的小圆形脂肪密度影(脂泡影)位于胰周积液内(箭),提示胰周脂肪坏死; b) GRE T1WI抑脂像示胰腺(P)周围稍高信号的急性坏死性液体积聚中见斑点状、条状低信号影(箭),与上述CT表现类似,系胰周脂肪坏死; c) FSE T2WI抑脂像清晰显示胰周呈稍高信号的急性坏死性积聚(箭)。 图9 男,43岁,急性坏死性胰腺炎伴胰周急性坏死性积聚继发感染。a) MRI增强扫描静脉期示胰腺体部大片状低信号坏死灶(箭),坏死范围>50%; b) FSE T2WI抑脂像示左侧肾旁前间隙急性坏死性液体积聚(箭),其内见较多低信号坏死碎片;住院治疗期间体温突升至39℃故行CT增强检查; c) CT增强扫描动脉晚期示网膜囊区胰周积液出现“气泡征”(箭); d) CT增强扫描动脉晚期示左侧肾旁前间隙积液伴多发“气泡征”。
ANCs是指发生在急性坏死性胰腺炎这一病理类型,从患者发病起至4周以内出现的胰周和/或胰内液性积聚。在新亚特兰大分类中,急性坏死性胰腺炎包括仅胰腺坏死、仅胰周坏死、胰腺和胰周皆坏死3种亚型,其中胰腺和胰周皆坏死型占80%~90%[1-3]。急性坏死性积聚的积液特征是非单纯的液体,它还包括或多或少的胰腺坏死组织碎片(图5)、胰周脂肪组织等实性或半实性的成份位于其内(图6),且可合并出血即出血坏死性积液(图7)。在MRI上,该局部并发症表现为胰腺内可见不同程度未强化的坏死灶和/或胰周条片状长T2水样信号中见稍低信号的破絮状、斑片状、点结节状碎片影(提示胰周坏死)(图6),即胰周积液呈混杂性,有时在抑脂T1WI像上积液内出现斑片状、大片状稍高信号影,提示血性积液(图7)。该型积液的部位同样是以胰周、左侧肾旁前间隙、网膜囊等部位常见,呈游离性积液。值得一提的是,胰周脂肪坏死常表现为单个或数个、直径几毫米的小圆形脂肪密度影(脂泡影)位于胰周积液内,在MRI上需仔细观察,而CT上更易被识别(图8)。
急性坏死性积聚若积液量较少,经内科保守治疗后,大多可逐渐吸收消失,预后良好。若胰腺存在较大范围的坏死,尤其是坏死致“胰管中断综合征”,使得胰腺远端残存组织分泌的胰液持续经破裂的胰管处向胰外溢出,引起胰周积液持续存在或积液量不断增多,当病变趋于包裹后(从发病起计算常超过4周),应考虑外科介入治疗,如超声、CT引导下穿刺外引流术。此外,因为存在坏死底物,故急性坏死性积聚的积液较急性胰周液体积聚更易并发感染(图9),感染并发症的证据也是外科治疗的适应症[8]。在临床工作中,笔者发现一部分急性坏死性积聚的患者,经过临床综合治疗后,积液不会完全吸收,在左侧肾旁前间隙、网膜囊、胰周或盆腔等部位残余少量的包裹性积液,长期遗留,但不会影响患者的生活质量。
2.包裹性坏死
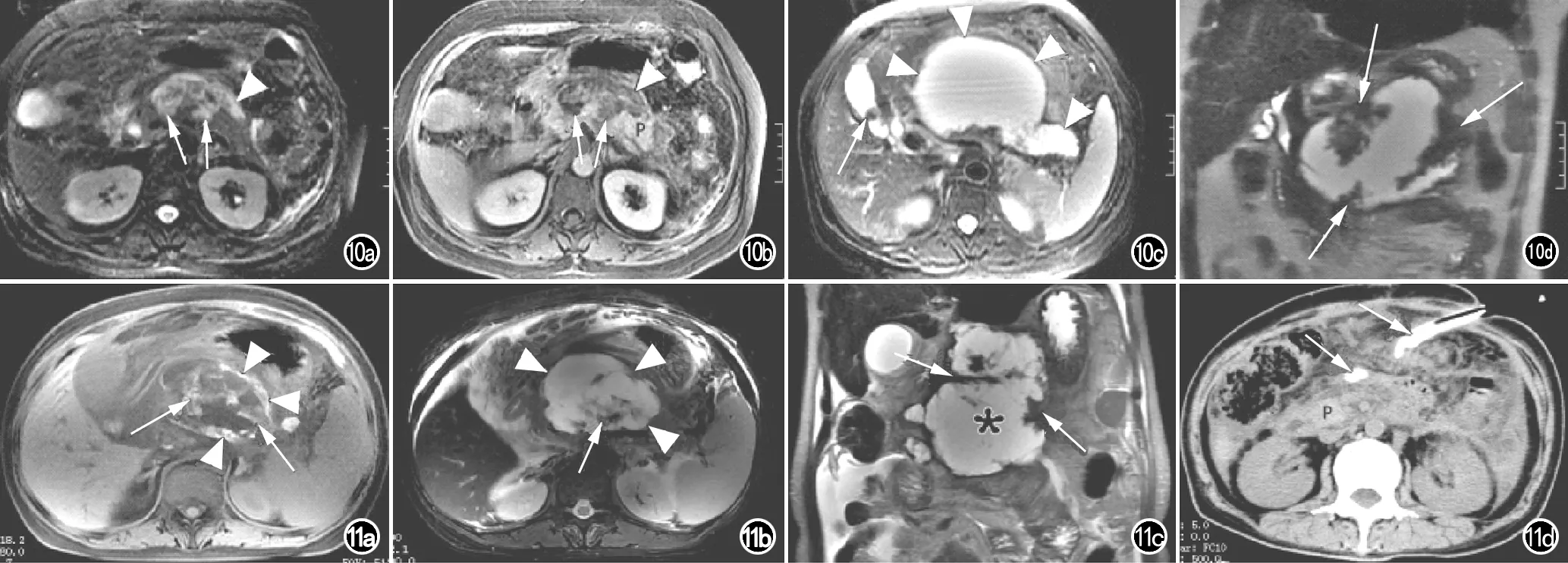
图10 患者,女,54岁,急性坏死性胰腺炎伴急性坏死性积聚演变至胰腺包裹性坏死。a) FSE T2WI抑脂像示胰腺头、颈、体大片状长T2信号影(箭)和胰周条带状长T2信号影(箭头),提示急性坏死性液体积聚; b) 增强扫描静脉期示胰内(箭)和胰周(箭头)病变区未见强化; c) 发病后1个多月复查,FSE T2WI抑脂像示胰周、网膜囊巨大WON形成(箭头),胆囊内见结石影(箭); d) 冠状面图像示巨大WON病灶的内部含条带状低信号坏死组织影(箭)。 图11 患者,女,44岁,急性坏死性胰腺炎伴胰体及网膜囊包裹性坏死形成。a) GRE T1WI抑脂像示网膜囊WON的环形壁厚薄不均,呈稍高信号影(箭头),病灶内见破絮状稍高信号影(箭); b) FSE T2WI抑脂像示网膜囊WON的环形壁呈低信号影(箭头),病灶内部见坏死组织碎片影(箭); c) 冠状面图像更好地显示上述WON(*)内容物含破絮状坏死组织碎片影(箭); d) 患者行胰体及网膜囊WON坏死组织清除术+外引流术后CT复查示胰腺(P)周围未见确切积液表现,局部可见引流管影(箭)。
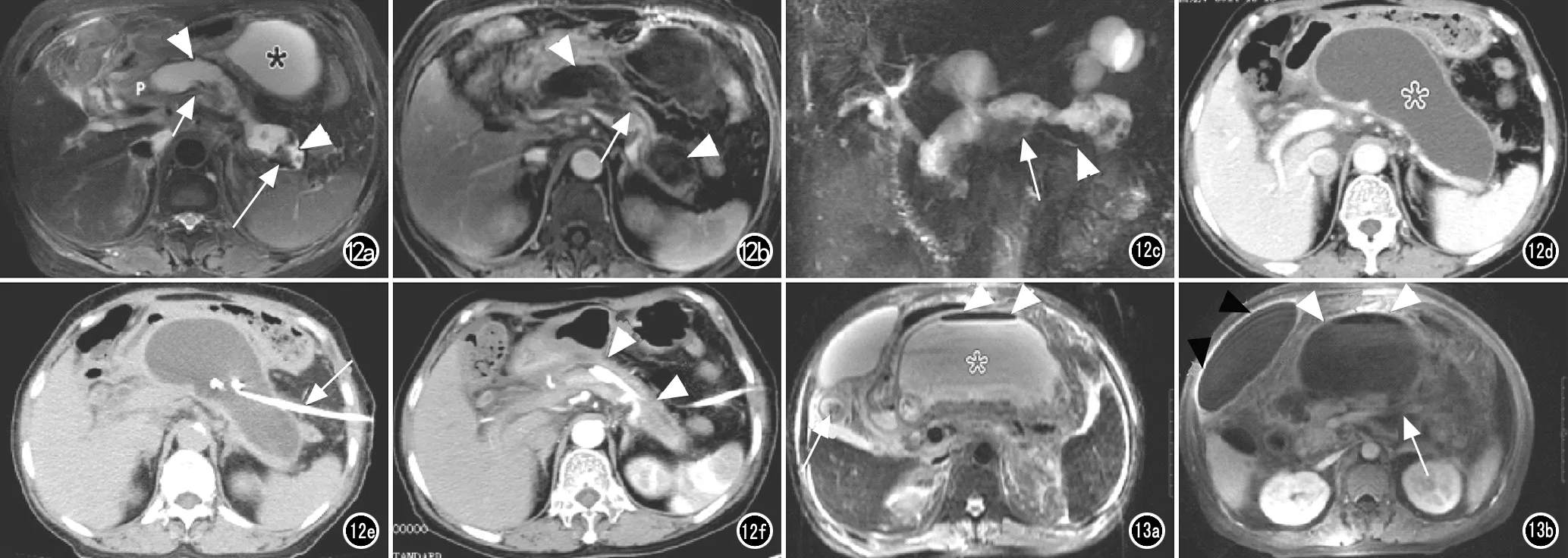
图12 患者,女,76岁,急性坏死性胰腺炎伴胰头颈、体尾WON形成。a) FSE T2WI抑脂像示胰腺(P)头颈、体尾区胰内WON形成(箭头),病变内含低信号的坏死组织影(长箭),胰头区主胰管中断(短箭),网膜囊另可见包裹性液性积聚(*); b) 增强扫描静脉期示胰腺头颈、体尾区胰内WON不强化(箭头),胰体部主胰管呈中断征(箭); c) MRCP示胰体的主胰管(箭头)走行至胰头颈病变处中断(箭); d) 发病后4个月CT复查示全胰腺区WON病变(*)明显增大; e) 行CT引导下穿刺外引流术后,CT平扫示引流管位于病灶中(箭); f) 术后3天复查,CT增强扫描动脉期示胰腺区WON病变(箭)几乎消失。 图13 患者,男,45岁,体温达40℃,重症急性胰腺炎,胰周WON伴感染。a) FSE T2WI抑脂像示胰腺前方、胃体后方即网膜囊大量包裹性坏死积液(*),病灶上缘见少量积气(箭头)形成一气液平;胆囊内可见结节状低信号结石(箭); b) 增强扫描静脉期示胰腺体尾部片状坏死(箭),网膜囊积液包裹性壁呈环形强化(白箭头),右上腹腔另可见一包裹性坏死积聚(黑箭头),患者行“胰周WON”切除术和外引流术,手术引出约3500mL的褐色脓性液体。
胰腺包裹性坏死是新亚特兰大分类中的一个新术语[1],指发生在急性坏死性胰腺炎的后期,通常在发病2周后开始形成、至发病4周以后在胰腺内、胰腺外周、胰内和胰周完全形成的包裹性液性积聚,它是由急性坏死性积聚迁延未愈并局限包裹而成(图10)。WON和假性囊肿的最大不同之处是除了大量的包裹性积液外,还含有前述的或多或少的非液性物质,这些非液性物质主要指坏死的胰腺组织碎块和胰周脂肪组织(图10)。尽管在增强CT上能显示出这些非液性物质,但笔者认为抑脂T2WI图像和MRCP图像更能清晰、逼真地显示出它们的细节特征。对此,笔者搜集了本院2010年1月-2015年6月间56例急性胰腺炎后期并发胰腺WON的患者[9],MRI图像上共发现WON病灶81个,单发者37例(66.1%)、多发者19例(33.9%);81个胰腺WON病灶中位于胰周36个(44.4%),胰周+胰内均受累25个(30.9%),胰内20个(24.7%)。胰周的WON以网膜囊受累最常见,胰周+胰内均受累的WON以网膜囊+胰头颈、体尾受累最常见,而胰内WON则以胰体尾部受累最常见。胰腺WON病灶呈圆形或卵圆形,均有“占位效应”(图11),本组病灶大小为1.5~24.5 cm,包裹性囊壁厚度为2~12 mm(平均3.6 mm);WON壁信号在抑脂T1WI上多呈等或稍低信号,少数呈稍高信号,抑脂T2WI上呈稍低或低信号,增强扫描WON壁呈轻-中度环形强化。所有WON病灶的内容物均呈“复杂性”征象,即以液体信号为主,同时内含破絮状、藕丝状、条带状坏死组织碎片影游离其中(图11)。WON内"坏死组织碎片影"在抑脂T1WI上可呈稍低、等、稍高多种信号,在抑脂T2WI上均呈低信号影,增强扫描不强化。由于胰腺WON病灶部分位于胰腺内或者位于胰周同时累及胰内,故MRI图像可以观察病变与主胰管的解剖关系,以指导临床治疗。本组发现81个胰腺WON灶中有19个(23.5%)与主胰管相关,分别为15个WON可见胰体尾主胰管走行至累及胰颈、胰体的WON病灶处“中断且相通”,即主胰管中断并通连征;4个WON可见主胰管贯穿累及胰颈或体的WON病灶呈“主胰管穿通征”。存在着这种“胰管中断综合征”表现的病例,有着非常重要的临床意义[10],即提示WON病灶会持续增大、长期存在,需要外科进一步处理(图12)。另一方面,胰腺WON因存在胰腺和胰周组织的坏死,同时又处在急性胰腺炎病程的后期,故易合并感染并发症[8]。WON一旦并发感染,则必须行外科引流或开腹手术治疗。笔者之前的研究中[9],56例胰腺WON患者后期临床诊断合并感染者37例(66.1%),由MRI和/或CT发现“气泡征”、“气液平”征象者21例(37.5%)(图13)。住院期间多数患者经临床外科治疗后影像学复查WON病灶明显缩小或消失,部分胰腺WON会长期遗留,并与后期新出现的其他局部并发症如胰源性门脉高压症、侧枝循环开放等相关。
综上所述,针对新亚特兰大分类下急性胰腺炎4种主要局部并发症,MRI均能进行很好地评价,笔者将重要的更新小结如下:①胰腺和胰周液性积聚内出现“非液性成份/实性成份”提示存在胰腺/胰周坏死,则为急性坏死性胰腺炎;若仅有胰周坏死,即诊断为急性坏死性胰腺炎(仅胰周坏死型);②胰周脂肪坏死在CT上表现为单个或数个、直径几毫米的小圆形脂肪密度影位于胰周积液内(脂泡影),在MRI上可通过抑脂与不抑脂T2WI进行对比观察,提示胰周脂肪坏死的表现为抑脂T2WI上腹腔/腹膜后单一或多发间隙液性积聚内含有低信号的非液性成份,增强扫描肠系膜、网膜、侧腹膜出现增厚伴炎性强化,腹膜后、肠系膜脂肪区内出现条索状、网格状炎性强化影[5,6];③在CT上发现的胰周液性积聚密度不均,在MRI上可能对胰周积液的异质性显示更佳,从而有助于坏死性液性积聚的诊断;④胰腺假性囊肿仅见于急性间质水肿性胰腺炎,起病4周之后出现的胰周包裹性均质液体积聚,但真正符合新亚特兰大分类假性囊肿定义的病变已很罕见,几乎均需用胰腺包裹性坏死这一新术语取代;⑤曾经被视为胰腺内假性囊肿的病变需更新诊断为胰内急性坏死性积聚或胰内包裹性坏死。⑥胰腺脓肿这一术语因只指包裹性的单纯脓液而已经被弃用,新的诊断术语为急性坏死性积聚合并感染或胰腺包裹性坏死合并感染,新术语突出了液化坏死物质(实性或半实性)的存在。
[1] Banks PA,Bollen TL,Dervenis C,et al.Classification of acute pancreatitis-2012:revision of the Atlanta classification and definitions by international consensus[J].Gut,2013,62(1):102-111.
[2] Thoeni RF.The revised atlanta classification of acute pancreatitis:its importance for the radiologist and its effect on treatment[J].Radiology,2012,262(3):751-764.
[3] Foster BR,Jensen KK,Bakis G,et al.Revised atlanta classification for acute pancreatitis:a pictorial essay[J].Radiographics,2016,36(3):675-687.
[4] 袁涛,全冠民,石伟,等.急性胰腺炎新分类相关术语和并发症及MCTSI评分[J].放射学实践,2015,30(10):1005-1010.
[5] Xiao B,Zhang XM.Magnetic resonance imaging for acute pancreatitis[J].World J Radiol,2010,2(8):298-308.
[6] Xiao B,Zhang XM,Tang W,et al.Magnetic resonance imaging for local complications of acute pancreatitis:a pictorial review[J].World J Gastroenterol,2010,16(22):2735-2742.
[7] 肖波,蒋志琼,蹇顺海.急性胰腺炎假性囊肿术语使用的临床探析[J].中华胰腺病杂志,2017,17(1):40-42.
[8] 肖波,蒋志琼,蹇顺海.急性坏死性液体积聚和包裹性坏死并感染的影像评价[J].影像诊断与介入放射学,2016,25(5):64-69.
[9] 肖波,蒋志琼,蹇顺海,等.急性坏死性胰腺炎:胰腺包裹性坏死(WON)的MRI表现和认识[J].影像诊断与介入放射学,2016,25(2):117-122.
[10] Sandrasegaran K,Tann M,Jennings SG,et al.Disconnection of the pancreatic duct:an important but overlooked complication of severe acute pancreatitis[J].Radiographics,2007,27(5):1389-1400.
R576; R445.2
A
1000-0313(2017)09-0918-05
2017-03-22)
637000 四川,川北医学院附属医院放射科,四川省医学影像重点实验室
肖波(1983-),男,四川南充人,博士研究生,主治医师,主要从事胰腺影像学研究工作。
10.13609/j.cnki.1000-0313.2017.09.005

