腹腔镜术后给予GnRH-a治疗卵巢巧克力囊肿的效果及对卵巢功能的影响
祝健婵 熊小琴 李 焱
(江门市人民医院妇科,广东 江门 529000)
腹腔镜术后给予GnRH-a治疗卵巢巧克力囊肿的效果及对卵巢功能的影响
祝健婵 熊小琴 李 焱
(江门市人民医院妇科,广东 江门 529000)
目的 探究在卵巢巧克力囊肿腹腔镜术后应用GnRH-a的疗效及其对卵巢功能的影响。方法 将2013年1月至2016年1月间68例卵巢巧克力囊肿腹腔镜术后患者分为实验组(34例)和对照组(34例),对照组予以常规术后治疗,实验组予以GnRH-a治疗,于术后第1、6、12月随访。观察指标为治疗效果和卵巢形态、功能(基础状态卵泡数、卵巢体积和FSH、E2及LH等水平)。结果 实验组显效率和总有效率均显著高于对照组,术后12月实验组基础状态卵泡数、卵巢体积和FSH、E2及LH等激素水平均显著高于对照组,差异均具有统计学意义(P<0.05)。结论 在卵巢巧克力囊肿腹腔镜术后应用GnRH-a的疗效优于常规术后治疗,并且可以显著改善卵巢的形态、功能和激素水平,值得推广。
子宫内膜异位;巧克力囊肿;腹腔镜;GnRH-a
子宫内膜异位(endometriosis,EMs)即子宫内膜的腺体和间质出现在子宫以外的部位,导致一系列的慢性炎症反应,是最常见的妇科疾病之一(患病率2%~10%),其中不孕症患者患病率达50%。卵巢巧克力囊肿是子宫内膜异位于卵巢而形成的囊肿,可对卵巢的正常形态和功能造成巨大影响,常引起腹部疼痛症状和不孕,严重影响患者生活质量。目前,腹腔镜是卵巢巧克力囊肿诊断的金标准和治疗的首选方式,但也存在较高的复发率和影响卵巢的功能等问题[1]。促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRH-a)是近年来新推出的生物治疗药物[2],体外实验取得了较好的效果,但在腹腔镜术后应用的疗效还存在一定争议。为探究在卵巢巧克力囊肿腹腔镜术后应用GnRH-a的疗效及对卵巢的影响,现将我院所做随机对照试验报告如下。
1 材料与方法
1.1一般资料 选择2014年11月至2015年11月间68例卵巢巧克力囊肿腹腔镜术后患者,随机分为实验组和对照组。其中,实验组34例,平均年龄(28.8±4.6)岁,病程(3.2±1.9)年,美国生殖医学学会(American Society for Reproductive Medicine,ASRM)分期:I期4例,II期10例,III期12例,IV期8例,单侧25例,双侧9例。对照组34例,平均年龄(28.1±5.0)岁,病程(3.5±1.6)年,ASRM分期I~IV期分别为5例、9例、13例和7例,单侧28例,双侧6例。所有患者均排除严重感染、心血管疾病和其他脏器严重疾病;两组一般资料间均无明显统计学差异,具有可比性(P>0.05)。
1.2治疗方法 对照组予以常规术后治疗;在常规术后治疗基础上,实验组联合GnRH-a(醋酸戈舍瑞林缓释植入剂,3.6 mg)3.6 mg皮下注射,每4周1次,5次。
1.3疗效评价 临床疗效判定标准:显效:原有症状、体征完全消失;部分缓解:原有症状、体征基本消失;无效:原有症状无明显改善;复发:原有症状再次出现或加剧,影像学发现肿瘤再次出现。卵巢功能指标包括基础状态卵泡数(AFC)、卵巢体积和卵泡刺激素(FSH)、雌二醇(E2)及黄体生成素(LH)等激素水平。于术后第1、6、12月随访。
1.4统计学处理 对计量资料以均数±标准差表示,组间比较采用t检验;计数资料采用χ2检验。采用SPSS 22.0进行数据处理,所有检验均为双侧假设检验,检验水准α=0.05。
2 结 果
2.1两组间临床疗效的比较 实验组显效率和总有效率显著高于对照组,复发率实验组显著低于对照组,差异均具有统计学意义(P<0.05),详见表1。
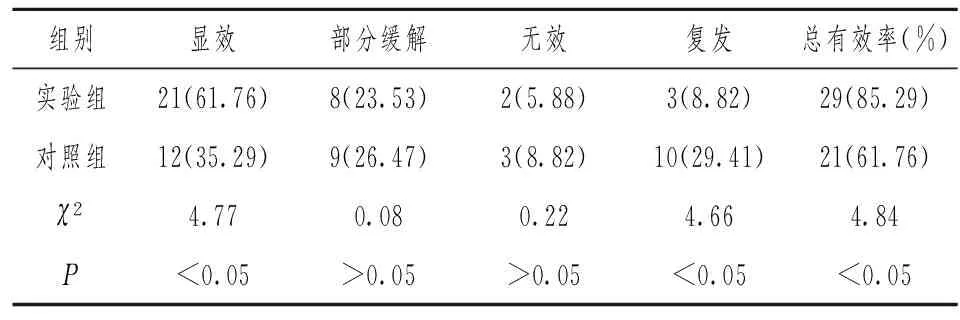
表1 两组间临床疗效的比较[n(%)]
2.2两组间基础状态卵泡数、卵巢体积的比较 两组间正常侧AFC和卵巢体积间无明显统计学差异(P>0.05);实验组术侧AFC和卵巢体积与对照组存在差异,且差异具有统计学意义(P<0.05),详见表2。

表2 两组间基础状态卵泡数、卵巢体积的比较
2.3两组间卵巢激素水平比较 治疗前两组间卵巢激素(FSH、LH和E2)水平均不存在明显的统计学差异;治疗后,实验组卵巢激素水平明显高于对照组,差异具有统计学意义(P<0.05),详见表3。

表3 两组间卵巢激素水平比较
3 讨 论
多种因素导致子宫内膜异位(经血逆流种植)至卵巢,发生浸润、反复出血进而形成的卵巢巧克力囊肿,具有病变部位广泛、形态多样以及具有较高的复发性,目前尚无完全治愈的方法,因此现有治疗中心是减轻症状以及改善生育[3]。
继发性、进行性加重的盆腔疼痛是卵巢巧克力囊肿的典型特点,是多数患者就诊的首要原因。本研究结果显示,两组治疗方式症状改善情况均较为明显,其中实验组显效率和总有效率分别为61.76%(21/34)和85.29%(29/34),显著高于对照组的35.29%(12/34)和61.76%(21),实验组复发率为8.82% (3/34)显著低于对照组的29.41% (10/34)。对于大多数子宫内膜异位症(包括卵巢巧克力囊肿)患者,都有较高的远期复发率,其复发的主要原因为病灶消除不充分,少量异位的子宫内膜组织在激素的作用下继续反复生长、浸润。鉴于异位组织具有高度的激素敏感性,通过调节患者的激素水平可以有效调节病变部位的异位组织生长。促性腺激素释放激素激动剂(GnRH-a)是一种生物合成的肽类,在首次应用后可以产生一过性的垂体-性腺系统的兴奋作用(激活作用),之后可以抑制垂体合成和释放促性腺激素,并可以下调垂体的功能,出现暂时性药物去势以及低雌激素水平;此外,GnRH-a还可以与外周的GnRH-a受体相结合,抑制异位子宫内膜细胞的活性。通过上述作用,异位组织处于抑制状态,显著改善了症状,降低了复发率[4]。
改善患者生育是治疗的重要目标之一。腹腔镜术为尽可能地切除病变组织,造成了卵巢体积的骤降和激素水平的不足,对卵巢形态和激素水平的恢复是改善患者生育条件的重要一环。与对照组相比,实验组术侧卵巢体积得到了有效恢复,其基础状态卵泡数也有显著提升;同时,实验组的卵巢激素水平也得到了一定程度的恢复。卵巢形态、功能得到良好的恢复,在适宜的激素水平下,卵巢巧克力囊肿患者术后2年的生育率可以达到80%左右。
此外,腹腔镜术后联合GnRH-a造成的雌激素波动,可引起类似围绝经期综合征的表现;有研究显示,在既不刺激异位组织又可以维持正常激素作用的剂量下(146~183 pmol/L),通过反向添加激素,可以进一步减少不良反应(如骨质疏松),提高生活质量,改善生育[5]。
综上所述,在卵巢巧克力囊肿腹腔镜术后应用GnRH-a的疗效优于常规术后治疗,并且可以显著改善卵巢的形态和功能,值得推广。
[1] 张清学, 李琳. 子宫内膜异位症合并不孕患者的助孕策略[J]. 国际生殖健康/计划生育杂志, 2014, 33(2): 77-79.
[2] 石一复, 李娟清, 舒淑娟, 等. 美国妇科腹腔镜协会第38届全球妇科微创年会有关子宫内膜异位症的综合介绍[J]. 国际妇产科学杂志,2010,37(2):144-146.
[3] 陈玉清, 裴慧慧, 常亚杰. 卵巢巧克力囊肿对卵巢储备功能的影响分析[J]. 中山大学学报:医学科学版, 2014,35(5):744-747.
[4] 叶丽虹, 方雅琴, 田国琴, 等. 腹腔镜卵巢子宫内膜异位囊肿剥除术联合使用GnRH-a对卵巢储备功能的影响[J]. 现代妇产科进展, 2014,23(3):171-174.
[5] 陈韦君, 周静, 梁笑倾. 子宫内膜异位症术后GnRH-α反向添加疗法的效果及其对性激素、骨密度的影响[J]. 中国妇幼保健, 2015,30(4):513-516.
祝健婵(1982—),女,广东肇庆人,主治医师,本科,主要从事妇科工作。
R711.3
:B
:1004-7115(2017)09-01058-02
10.3969/j.issn.1004-7115.2017.09.036
2017-06-13)
*

