超分子溶剂直提测定水中的多环芳烃
谈义萌, 唐 涛,, 杨三东, 夏明珠*, 王风云, 李 彤
(1. 南京理工大学工业化学研究所, 江苏 南京 210094; 2. 大连依利特分析仪器有限公司, 辽宁 大连 116023)
研究论文
超分子溶剂直提测定水中的多环芳烃
谈义萌1, 唐 涛1,2, 杨三东1, 夏明珠1*, 王风云1, 李 彤2
(1. 南京理工大学工业化学研究所, 江苏 南京 210094; 2. 大连依利特分析仪器有限公司, 辽宁 大连 116023)
超分子溶剂是两亲化合物通过分子间有序的自组装过程形成的具有纳米结构的胶束聚集体,是一种高效提取溶剂。该文以高效液相色谱-荧光检测法为测试手段,系统地对超分子溶剂组成及用量进行了优化,发展了一种直接提取、快速测定水中多环芳烃的方法,并进行了方法学验证及实际样品检测。结果表明,采用四氢呋喃和1-辛醇制备的超分子溶剂对4种多环芳烃的回收率为89.08%~102.47%,相对标准偏差(RSD,n=5)为1.38%~3.92%。 4种多环芳烃在一定范围内线性关系良好(相关系数R2>0.999),检出限为1.26~9.23 ng/L。该方法前处理过程简单,有利于实现快速分析;溶剂使用量少,符合绿色化学的发展趋势,具有一定的推广价值。
超分子溶剂;直接提取;高效液相色谱-荧光检测;多环芳烃;水
多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是一类广泛存在的环境污染物,普遍具有致癌、致突变和致畸形作用,危害生态环境和人类健康[1]。各国制定了相关法规来控制PAHs[2],如美国环境保护署(Environmental Protection Agency, EPA)列出16种PAHs(简称EPA-PAHs),要求其在水中总量不得大于0.2 μg/L;我国饮用水卫生标准也规定苯并[a]芘(benzo(a)pyrene, BaP)在水中的含量应小于0.01 μg/L。由于PAHs基体复杂且含量很低,所以传统的样品前处理方法(如液液萃取[3-6]、固相萃取[7-9])均需要繁杂的操作、较长的时间和大量的有毒试剂,对实验人员的健康和环境造成很大危害。因此,人们不断致力于开发省时省力、操作简便、对环境友好的新型样品前处理技术。
超分子溶剂(supramolecular solvent, SUPRAS)[10]通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的、具有纳米结构的胶束聚集体,在水溶液中形成后又与水相分离。超分子溶剂萃取是一种新型的萃取方法,由西班牙学者Rubio等[11,12]提出,具有安全环保、萃取效率高、简单快速等优点,已经被广泛应用到不同极性化合物的萃取中[13],如Rezaei等[14]用四氢呋喃(tetrahydrofuran, THF)/壬酸/水组成的超分子体系萃取了样品中的双氯芬酸和甲芬那酸,样品回收率为90.4%~103.8%。Ballesteros-Gómez等[15]用THF/癸酸/水组成的超分子体系萃取了水样中的7种致癌性多环芳烃,回收率为88%~95%,取样量仅为36 mL;用同样的超分子体系萃取茶水和咖啡中的BaP,回收率为90%~96%[16]。Feizi等[17,18]利用双子表面活性剂制取超分子溶剂提取水样和土样中的三氟氯氰菊酯和杀灭菊酯以及化妆品、饮料和水样中的对羟基苯甲酸酯,均取得了很好的回收效果。
本文以四氢呋喃和1-辛醇制取的超分子溶剂直接提取水样中的苯并[a]蒽(benzo(a)anthracene, BaA)、苯并[b]荧蒽(benzo(b)fluoranthene, BbF)、苯并[k]荧蒽(benzo(k)gluoranthene, BkF)及BaP,提取的超分子溶剂相直接进样分析,该方法样品前处理过程简单,溶剂使用量少,回收效果良好。
1 实验部分
1.1仪器和试剂
液相色谱系统由P1201高压恒流泵、S3100自动进样器、ZW1201色谱柱温箱、SinoPak C18柱(100 mm×4.6 mm, 3 μm)(大连依利特分析仪器有限公司)及岛津RF-20Axs荧光检测器(日本岛津公司)组成;QL-861涡旋仪(海门市其林贝尔仪器制造有限公司); 3K15离心机(德国Sigma公司)。
乙腈(色谱纯,美国Sigma-Aldrich公司);四氢呋喃(色谱纯,天津科密欧化学试剂有限公司); 1-辛醇(分析纯,百灵威科技有限公司); BaA、BbF、BkF和BaP标准品(纯度≥96%,百灵威科技有限公司)。
1.2标准储备液的配制
准确称取BaA、BbF、BkF及BaP各0.010 0 g,分别用乙腈溶解并定容至50 mL,配成质量浓度为200 mg/L的标准储备液,置于4 ℃冰箱内保存待用。
1.3样品处理
1.3.1预处理
选择海水、自来水和纯净水进行实验,水样经过0.45 μm水膜去除固体颗粒或不溶性杂质,于4 ℃冰箱保存。
1.3.2样品处理
取1 mL THF和250 μL 1-辛醇迅速注入10 mL离心管中,加入8 mL水样,涡旋30 s,混合均匀后以3 000 r/min的速度离心8 min,用注射器移除下层水相,上层有机相用乙腈定容至1 mL,经0.45 μm有机滤膜过滤后进样分析。
1.4色谱条件
色谱柱为SinoPak C18柱;柱温为30 ℃;进样量为10 μL;流动相为乙腈/水(76∶24, v/v);流速为1.0 mL/min;荧光检测器的激发波长Ex=290 nm,发射波长Em=410 nm。
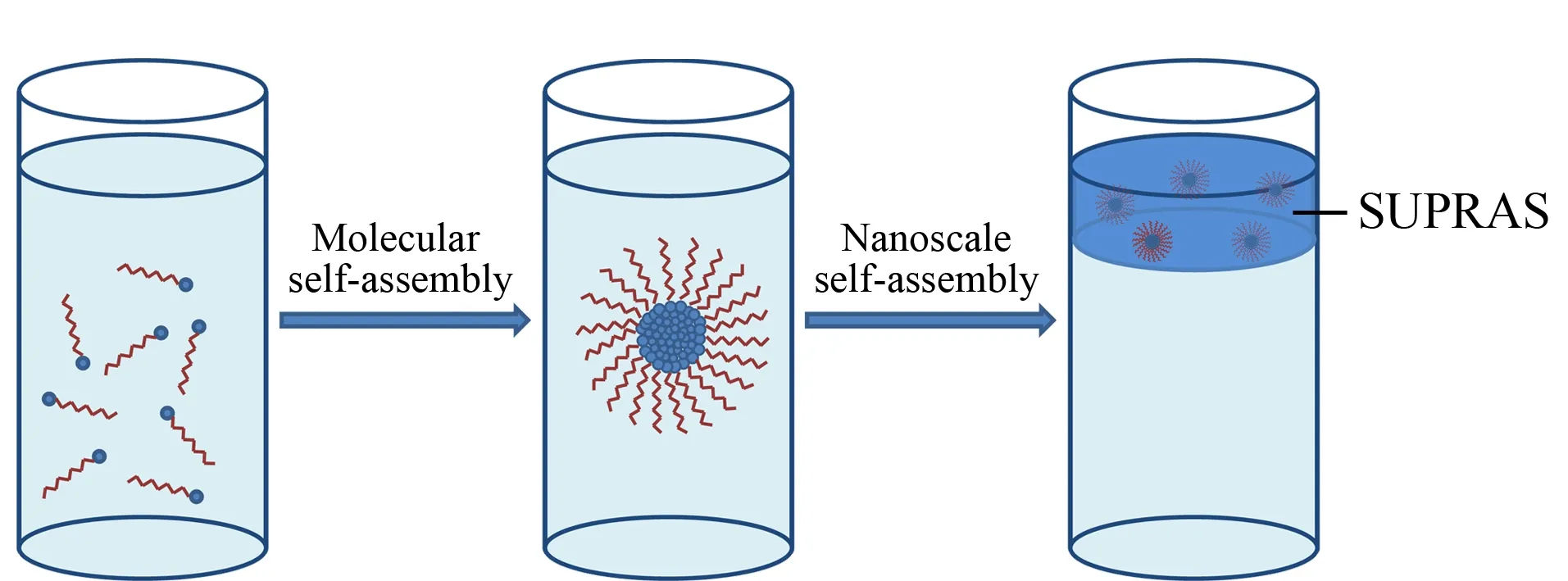
图 1 超分子溶剂自组装过程Fig. 1 Self-assembly processes in supramolecular solvent (SUPRAS) formation
2 结果与讨论
2.1超分子溶剂的制备
2.1.1组成溶剂的筛选
超分子溶剂自组装过程主要受组成物结构、环境、结合和驱动力等影响,典型的自组装过程如图1所示。选择具有两亲性质的THF分别与壬酸、癸酸、1-辛醇形成超分子基团,在相同条件下对多环芳烃进行萃取。结果表明,THF/壬酸/水体系提取4种多环芳烃的回收率为68.06%~69.41%, THF/癸酸/水体系提取4种多环芳烃的回收率为76.06%~78.20%, THF/1-辛醇/水体系提取4种多环芳烃的回收率为89.08%~96.05%, THF/1-辛醇/水体系对多环芳烃的提取效果最佳。其中,THF/1-辛醇/水超分子溶剂体系的光学显微镜图见图2。据Ballesteros-Gómez等[11]对SUPRAS属性的研究可知,SUPRAS的萃取作用力主要体现在烷基链提供的疏水相互作用和亲水头基提供的氢键作用。PAHs与SUPRAS主要以疏水相互作用结合,烷基醇比烷基酸的极性弱,因此THF与1-辛醇形成的SUPRAS对PAHs的萃取效果更好。本研究选取四氢呋喃/1-辛醇/水体系作为萃取多环芳烃的超分子溶剂。

图 2 THF/1-辛醇/水体系形成超分子凝聚体的光学显微镜图Fig. 2 Light microscopy micrograph of supramolecular coacervates prepared from tetrahydrofuran (THF)/1-octanol/water system
2.1.2THF用量的选择
在本实验中,作为超分子溶剂重要成分的THF是该体系的一个重要因素。本文考察了THF的用量分别为0.5、1.0、1.5、2.0和2.5 mL时样品的回收率,结果见表1。随着THF含量增大,回收率先升高后下降。当THF的用量为1.0 mL时,样品的回收率高且较稳定,满足检测的要求。因此在后续的研究中,选择加入1.0 mL THF作为最佳用量。
2.1.31-辛醇用量的选择
考察了1-辛醇用量为100、150、200、250、300和350 μL时样品的回收率,结果如表2所示。随着1-辛醇用量的增大,回收率逐渐升高,当1-辛醇用量大于或等于250 μL时,样品的回收率较高且稳定,满足检测的要求。因此在后续的研究中,选择250 μL 1-辛醇为最佳用量。
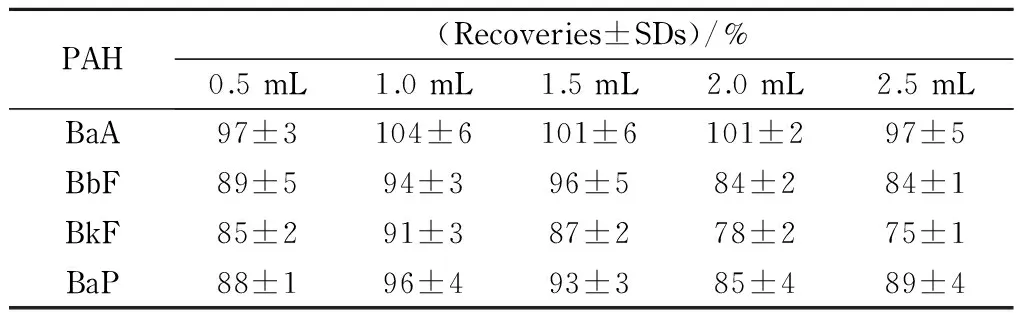
表 1 不同含量的THF提取PAHs的平均回收率及标准偏差(SDs)(n=3)Table 1 Mean recoveries and standard deviations (SDs) of the extraction of polycyclic aromatic hydrocarbons (PAHs) with different volumes of THF (n=3)
BaA: benzo(a)anthracene; BbF: benzo(b)fluoranthene; BkF: benzo(k)gluoranthene; BaP: benzo(a)pyrene. Spiked levels: BbF 1000 ng/L, BaA 100 ng/L, BkF 100 ng/L, BaP 100 ng/L. 1-Octanol: 250 μL.
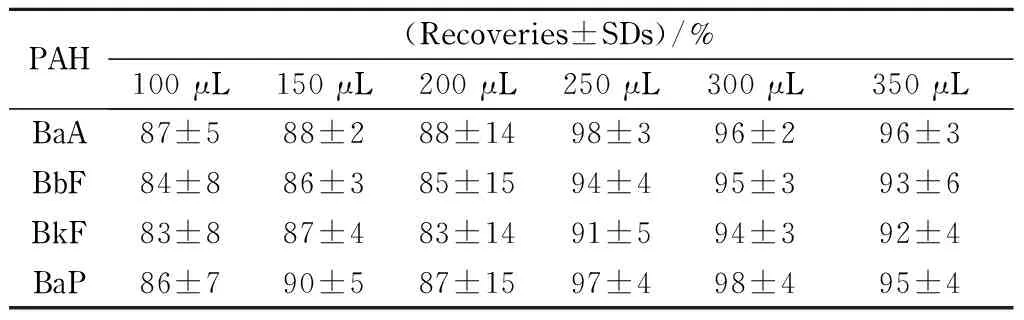
表 2 不同含量的1-辛醇提取PAHs的平均回收率及标准偏差(n=3)Table 2 Mean recoveries and SDs of the extraction of PAHs with different volumes of 1-octanol (n=3)
Spiked levels were the same as those in Table 1. THF: 1.0 mL.
2.2盐效应对回收率的影响
在常规的萃取过程中,离子强度扮演着十分重要的角色,为了考查离子强度对实验的影响,样品中分别加入了不同含量的NaCl(0~20%),按1.3节方法处理样品后进行HPLC测定,结果见表3。随着盐含量的增加,萃取效率逐渐下降,可能是因为随着盐的加入,弱极性化合物和盐离子之间的静电相互作用力增强,使多环芳烃进入到超分子溶剂相的能力减弱,导致回收率下降。因此,后续实验中不加盐。

表 3 不同含量NaCl提取PAHs的平均回收率及标准偏差(n=3)Table 3 Mean recoveries and SDs of the extraction of PAHs with different mass volume percentages of NaCl (n=3)
Spiked levels were the same as those in Table 1. 1-Octano: 250 μL; THF: 1.0 mL.
2.3方法学验证
2.3.1多环芳烃的典型分离色谱图
在1.4节色谱条件下,空白样品(THF/1-辛醇/水超分子溶剂体系)、4种多环芳烃标准品和典型加标样品的分离色谱图见图3。

图 3 (a)空白样品、(b)标准品与(c)加标样品的色谱图Fig. 3 Chromatograms of (a) a blank sample, (b) standards and (c) a spiked sample
2.3.2线性范围和检出限
用乙腈配制下列质量浓度的混合标准溶液:BaA 0.8 μg/L、BbF 8.0 μg/L、BkF 0.8 μg/L、BaP 0.8 μg/L。将上述标准溶液用去离子水依次稀释4倍、8倍、10倍、20倍和40倍,得到系列质量浓度的空白加标样品,按1.3节方法处理样品后进行HPLC测定。用峰面积(y)和各组分的质量浓度(x, μg/L)制作标准曲线,计算各组分的线性方程及相关系数(R2),结果见表4。各组分线性关系良好,相关系数均可达到0.999以上。

表 4 本方法的线性范围、线性方程、相关系数、 检出限和定量限Table 4 Linear ranges, linear equations, correlation coefficients (R2), limits of detection (LODs) and limits of quantitation (LOQs) of this method
y: peak area;x: mass concentration, μg/L.
2.3.3回收率和精密度
配制一定浓度的空白加标样品,按1.3节方法处理样品后进行HPLC测定,平行测定5组,计算出PAHs样品的回收率为89.08%~102.47%, RSD为1.38%~3.92%(见表5)。

表 5 本方法的加标回收率和相对标准偏差Table 5 Spiked recoveries and relative standard deviations (RSDs) of this method
2.4实际样品中PAHs的提取和定量分析
使用本方法测定了某品牌纯净水、自来水及黄海流域海水样本中PAHs的含量。检测结果显示,纯净水中没有检测出目标物,自来水及海水中发现了BaA和BaP,但含量均在定量限以下。
2.5前处理方法对比
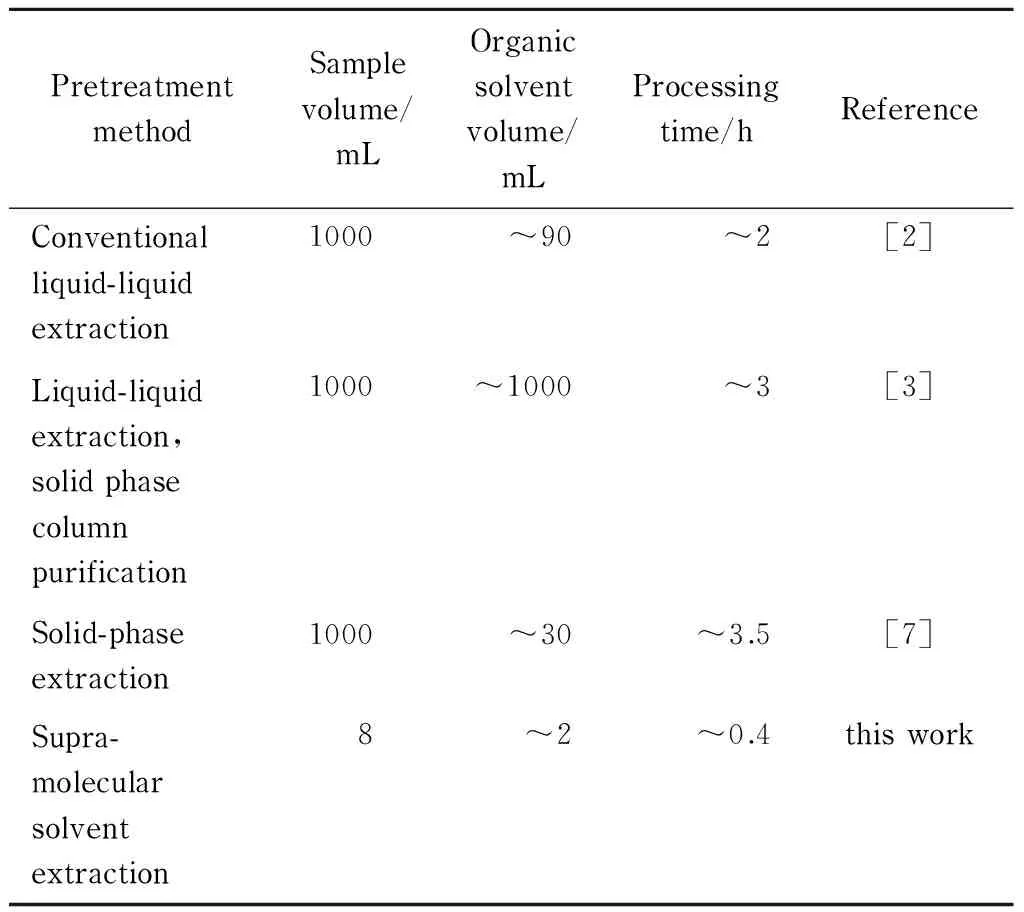
传统样品前处理和本文建立的样品前处理流程对比见图4,参数对比见表6。由图4可以看出,传统样品前处理过程需要经过液液萃取、固相净化、蒸馏浓缩等繁琐步骤,而本文建立的样品前处理方法仅需溶剂萃取一步便可得到被分析物。同样,由表6可以看出,传统的样品前处理方法取样量大,有机溶剂用量多,耗时长;而本方法仅需要约2 mL有机溶剂,减少了有机溶剂的使用,降低了实验成本,且取样量少,前处理速度快,大大方便了日常检测工作中对PAHs的分析。

图 4 传统样品前处理和本文建立的样品前处理流程对比Fig. 4 Comparison of pretreatment processes between traditional method and the established method
PretreatmentmethodSamplevolume/mLOrganicsolventvolume/mLProcessingtime/hReferenceConventionalliquid-liquidextraction1000~90~2[2]Liquid-liquidextraction,solidphasecolumnpurification1000~1000~3[3]Solid-phaseextraction1000~30~3.5[7]Supra-molecularsolventextraction8~2~0.4thiswork
3 结论
本文建立了超分子溶剂萃取直提测定水中4种致癌性多环芳烃的新方法。与传统前处理方法相比,超分子溶剂直提法简化了萃取步骤,仅需一步提取法,避免了消耗大量有机试剂以及固相萃取等繁琐步骤,操作简便。该方法重现性好,回收率稳定,可以满足日常水样检测工作中对多环芳烃定量分析的要求。
[1] Duan X L, Wei F S, Yang H B, et al. China Environmental Science, 2004, 24(5): 515
段小丽, 魏复盛, 杨洪彪, 等. 中国环境科学, 2004, 24(5): 515
[2] Li Y, Liu Y, Sun X W, et al. Environmental Chemistry, 2015, 34(8): 1460
李荫, 柳叶, 孙晓伟, 等. 环境化学, 2015, 34(8): 1460
[3] Cao B, Ma J, Li Y M Z. Rock and Mineral Analysis, 2010, 29(5): 539
曹攽, 马军, 李云木子. 岩矿测试, 2010, 29(5): 539
[4] Xue J. Geology of Fujian, 2012, 31(4): 358
薛佳. 福建地质, 2012, 31(4): 358
[5] Zhu B Q, Chen H, Li S Q. Chinese Journal of Chromatography, 2012, 30(2): 201
祝本琼, 陈浩, 李胜清. 色谱, 2012, 30(2): 201
[6] Song X, Li J, Liao C, et al. Chromatographia, 2011, 74(1): 89
[7] Tao J Q, Wang C Y, Li B F, et al. Chinese Journal of Chromatography, 2003, 21(6): 599
陶敬奇, 王超英, 李碧芳, 等. 色谱, 2003, 21(6): 599
[8] Wang A J, Guo Q. Sichuan Chemical Industry, 2008, 11(5): 36
王爱娟, 郭蔷. 四川化工, 2008, 11(5): 36
[9] Luo X P. Sichuan Environment, 2015, 34(2): 46
罗显平. 四川环境, 2015, 34(2): 46
[10] He W L. [MS Dissertation]. Kunming: Kunming University of Science and Technology, 2014
何文亮. [硕士学位论文]. 昆明: 昆明理工大学, 2014
[11] Ballesteros-Gómez A, Rubio S. Anal Chem, 2012, 84: 342
[12] Moradi M, Yamini Y. J Chromatogr A, 2012, 1229: 30
[13] Ballesterosgómez A, Sicilia M D, Rubio S. Anal Chim Acta, 2010, 677(2): 108
[14] Rezaei F, Yamini Y, Moradi M, et al. Talanta, 2013, 105(4): 173
[15] Ballesteros-Gómez A, Rubio S, Pérez-Bendito D. J Chromatogr A, 2008, 1203: 168
[16] Ballesteros-Gómez A, Rubio S, Pérez-Bendito D. J Chromatogr A, 2009, 1216: 530
[17] Feizi N, Yamini Y, Moradi M, et al. J Sol-Gel Sci, 2016, 39(17): 3400
[18] Feizi N, Yamini Y, Moradi M, et al. Anal Chim Acta, 2017, 953: 1
Supramolecular solvent-based direct extraction for the determination of polycyclic aromatic hydrocarbons in water
TAN Yimeng1, TANG Tao1,2, YANG Sandong1, XIA Mingzhu1*, WANG Fengyun1, LI Tong2
(1. Institute of Industrial Chemistry, Nanjing University of Science & Technology, Nanjing 210094, China;2. Dalian Elite Analytical Instruments Co., Ltd., Dalian 116023, China)
Supramolecular solvent (SUPRAS) is a nano-structured liquid generated from amphiphiles through a sequential self-assembly process. It is an efficient and excellent solvent for the sample extraction. In this paper, a method to directly extract and rapidly analyze polycyclic aromatic hydrocarbons (PAHs) in water samples by high performance liquid chromatography-fluorescence detection (HPLC-FLD) was developed. The composition and amount of SUPRAS were optimized and practical samples were tested. It indicated that the combination of tetrahydrofuran and 1-octanol was a suitable SUPRAS for the extraction of four PAHs with recoveries between 89.08% and 102.47% and relative standard deviations (RSDs) from 1.38% to 3.92% (n=5). Results showed a good linearity of four PAHs with the correlation coefficients (R2) more than 0.999. The limits of detection (LODs) ranged from 1.26 to 9.23 ng/L. The proposed pretreatment method greatly reduces the analysis time. And the solvent-less approach is in accordance with the development trend of green chemistry and of great application prospects.
supramolecular solvent (SUPRAS); direct extraction; high performance liquid chromatography-fluorescence detection (HPLC-FLD); polycyclic aromatic hydrocarbons (PAHs); water
10.3724/SP.J.1123.2017.06004
2017-06-01
.E-mail:863271491@qq.com.
国家自然科学基金项目(51472121);国家重大科学仪器设备开发专项(2012YQ12004403).
O658
A
1000-8713(2017)09-1003-05
Foundation item: National Natural Science Foundation of China (No. 51472121); National Key Scientific Instrument and Equipment Development Projects (No. 2012YQ12004403).
*