纳米Fe3O4表面聚合微粒制备及其尿样中二苯甲酮类化合物磁萃取应用
陈迪,罗晗,周胜兰,陈怀侠
(湖北大学化学化工学院,湖北 武汉 430062)
纳米Fe3O4表面聚合微粒制备及其尿样中二苯甲酮类化合物磁萃取应用
陈迪,罗晗,周胜兰,陈怀侠
(湖北大学化学化工学院,湖北 武汉 430062)

纳米Fe3O4;磁固相萃取;HPLC;二苯甲酮
0 引言

目前检测二苯甲酮类物质的方法有薄层色谱法(TLC)[7]、气相色谱法(GC)[8]、高效液相色谱法(HPLC)[9-10]、气相色谱-质谱法(GC-MS)[11-12]、液相色谱-质谱法(HPLC-MS)[13]等.液相色谱-质谱法联用能做到很高的灵敏度,但分析仪器成本高,后期的检修费用也不低,采用薄层色谱法的时候,实验操作比较繁杂,气相色谱-质谱法又要求具有较好的实验仪器,HPLC方法操作简便、测试费用低,是对二苯甲酮类物质分析的主流方法.
磁性聚合物微粒是采用一定的合成方法,将具有磁性的物质和高分子聚合物反应而制成的一种新型聚合物材料.磁性聚合物微粒具有超顺磁性,当被放置于磁场中时,可以迅速地与介质分离开.因此,磁性聚合物微粒逐渐被用作分离材料和介质,另外还被广泛用于核磁共振检查、环境污染物分析以及带有磁性的乳胶制品等领域[14-16].本文中主要合成了具有一定磁性,粒径分布均匀的Fe3O4磁性聚合物微粒,利用红外吸收光谱和色谱方法对磁性聚合物微球进行结构表征和萃取性能的考察.通过优化合成条件和萃取条件,建立了一种操作简单、快速、灵敏度高、适用于尿样中BPs残留检测的MSPE-HPLC分析方法.
1 实验
1.1 仪器与试剂 仪器:DIAMOND TG/DTA型热重分析仪(美国Perkin Elmer公司);LC-CT310型高效液相色谱仪(江苏天瑞仪器股份有限公司);UV310型紫外-可见检测器(江苏天瑞仪器股份有限公司);SMT-C18色谱柱(美国Supelco Technologies,DE);Kertone 型超纯水机(坷尔顿公司);JHX2H微型漩涡混合仪(京辉科技有限公司);XYH型真空干燥箱(南京百万机械仪器有限公司);可调式移液器(上海);CP213分析天平(上海五相仪器有限公司);超声仪(美国Branson200公司 );SPECTRUM ONE型红外光谱仪(美国Perkin Elmer公司).
试剂:2, 4-二羟基二苯甲酮(99.5%, BP-1)、二苯甲酮(99.5%,BP)、2-羟基-4-甲氧基二苯甲酮(99.5%,BP-3)、正硅酸乙酯(TEOS)、3-(甲基丙烯酰氧)丙基三甲氧基硅烷(MPS)(阿拉丁,上海);氯化亚铁(II)(FeCl2·4H2O,天津);氯化铁(FeCl3·6H2O,天津);2,2-偶氮-2-异丁腈(AIBN)(V-60,上海试剂四厂,分析纯);2-甲基-2-丙烯酸-1,2-乙二醇酯(EGDMA,美国Sigma公司,使用前用NaOH溶液多次处理,再用超纯水分多次萃取后用干燥剂进行干燥);甲基丙烯酸(MAA,天津,分析纯,使用前减压蒸馏);甲醇和乙腈(色谱纯,美国Tedia公司).
标准储备溶液的配制:先分别配置BP-1、BP、BP-3的标准溶液各1 mg/mL,再由上述浓度配成10 μg/mL 含3种目标物的甲醇混合储备液,各储备液都放置于冰箱的冷藏室中储存.
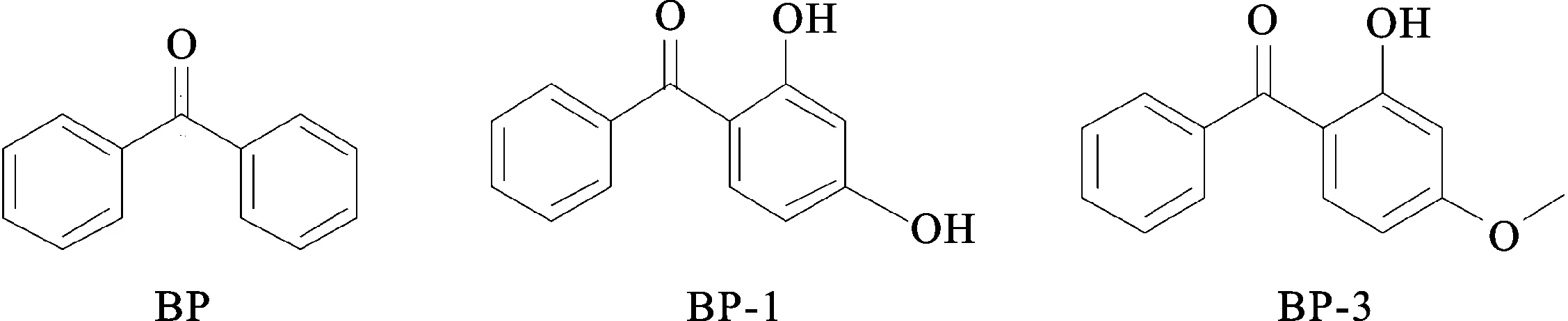
图1 BP、BP-1、BP-3的分子结
1.2 材料合成
1.2.1 合成Fe3O4纳米粒子[17]将1.72 g的FeCl2·4H2O和4.72 g的FeCl3·6H2O溶解在80 mL超纯水中,在氮气保护下高速搅拌(800 r/min). 随着温度升高到80 ℃,缓慢加入氨水10 mL,在该温度下反应30 min.将产品进行磁分离,以超纯水清洗纳米材料,60 ℃真空干燥.
1.2.2 合成Fe3O4@SiO2[18]称取0.3 g Fe3O4于50 mL三颈烧瓶中,加入50 mL乙醇和4 mL超纯水,超声15 min,加入5 mL 氨水和2 mL TEOS(正硅酸乙酯). 室温下搅拌反应24 h. 磁铁分离,用乙醇和超纯水冲洗磁材料,60 ℃真空干燥.
1.2.3 合成Fe3O4@SiO2@MPS[19]称取0.15 g Fe3O4@SiO2于100 mL三颈烧瓶中,加入30 mL无水甲苯和1 mL MPS,60 ℃水浴反应5 h,磁铁分离,并用乙醇清洗磁材料,60 ℃真空干燥.
1.2.4 合成Fe3O4磁性聚合微粒 称取0.1 g 上述合成的Fe3O4@SiO2@MPS悬浮在20 mL甲苯中(于50 mL三颈烧瓶中),搅拌1 h,加入170 mL MAA,继续搅拌1 h,加入1.9 mL EGDMA和0.08 g AIBN,60 ℃反应24 h,产物用磁铁分离,用乙醇洗净,60 ℃真空干燥,得到Fe3O4磁性聚合微粒.合成步骤如图2.
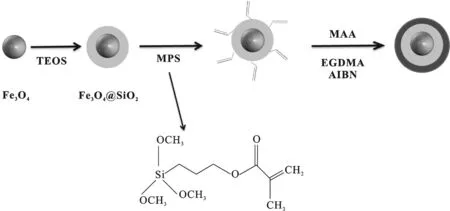
图2 纳米Fe3O4磁聚合微粒的合成步
1.3 色谱条件 流动相为甲醇的水溶液,V甲醇∶V水=85∶15;流速:1.0 mL/min;柱温:30 ℃;进样量:20 μL;测试波长:289 nm和256 nm.
1.4 磁固相萃取 磁固相萃取过程如图3所示,10 mg磁微粒置于25 mL的培养瓶中,加入1 mL甲醇活化后,倒掉甲醇,再往培养瓶中添加20 mL 200 ng/ mL的 BPs 标准溶液,将培养瓶置于超声仪中超声30 min,使材料分散在溶液中,并充分吸附目标物,再在外加磁场的条件下,倒掉上清液,加入1 mL洗脱剂(甲醇)洗脱目标物,过滤膜后进液相分析. 所有实验均采用回收率(ER)作为评价标准,其定义为:
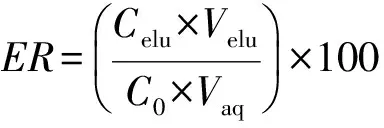
其中:Celu——洗脱液中分析物的浓度;C0——样品溶液中分析物的浓度;Velu——洗脱液的体积;Vaq——样品溶液的体积.
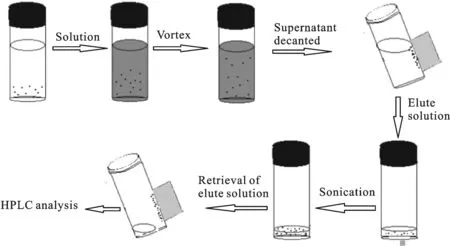
图3 磁固相萃
2 结果与讨论
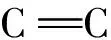
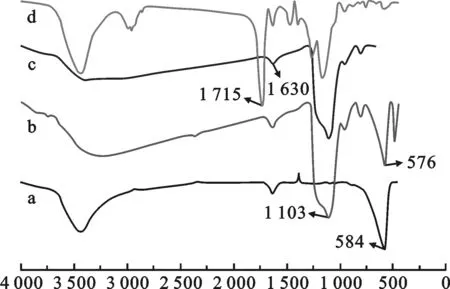
图

图5 磁性微粒热重(TGA)曲
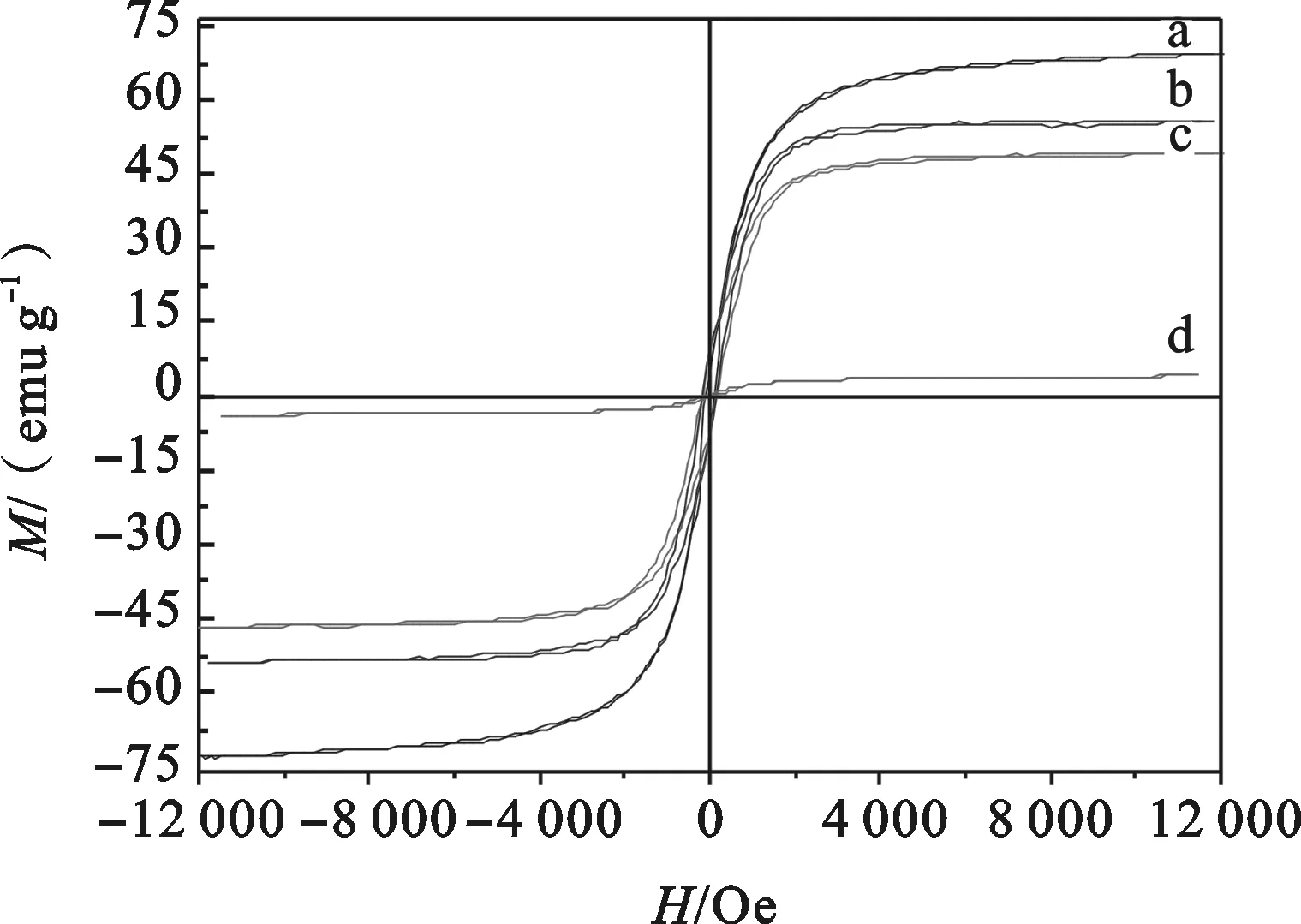
图
磁滞回线分析(VSM)用来考察合成磁性粒子的磁特性,Fe3O4(a)、Fe3O4@SiO2(b)、Fe3O4@SiO2@MPS(c)和磁性微粒(d)的磁滞回线如图6所示.从图中可以看出,4种物质的饱和磁强度分别为69.62、55.44、48.93和4.08 emu·g-1.这些磁性颗粒剩磁和矫顽力都为零,具有超顺磁性.与Fe3O4相比,磁微粒饱和磁化强度减少到4.08 emu·g-1,证明乙烯基和SiO2成功键合到Fe3O4表面.磁微粒在室温下仍保持磁性,外加磁场,可以快速从溶液中分开.2.2 磁固相萃取条件优化
2.2.1 洗脱剂种类选择 分别以1 mL的甲醇、乙腈和不同配比的甲醇和乙腈混合液为洗脱剂,对10 mL 200 ng mL-1的BP-1、BP、BP-3的混标溶液的磁萃取进行洗脱分析. 结果表明,V甲醇∶V乙腈=3∶7时洗脱效果较好,因此洗脱液甲醇和乙腈的体积比选择为3∶7.
2.2.2 吸附时间考察 分别考察吸附20、30、40、50、60和70 min时的萃取回收率,结果发现,随着吸附时间增加,回收率升高,在60 min以后趋于稳定,达到了吸附平衡,因此,吸附时间选择60 min.
2.2.3 洗脱液体积考察 选择0.4、0.6、0.8、1.0、1.2和1.4 mL的甲醇洗脱,结果发现,当洗脱液体积由0.4 mL增加到1.0 mL时,回收率随之升高,再增大洗脱液体积,回收率变化不大,可能是达到了解析平衡,因此洗脱液体积选择1.0 mL.


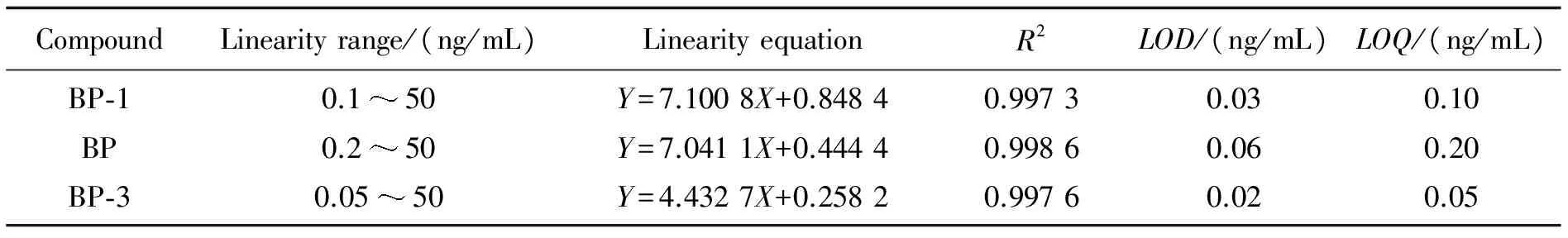
表1 BP-1,BP,BP-3的线性范围、检测限和定量限
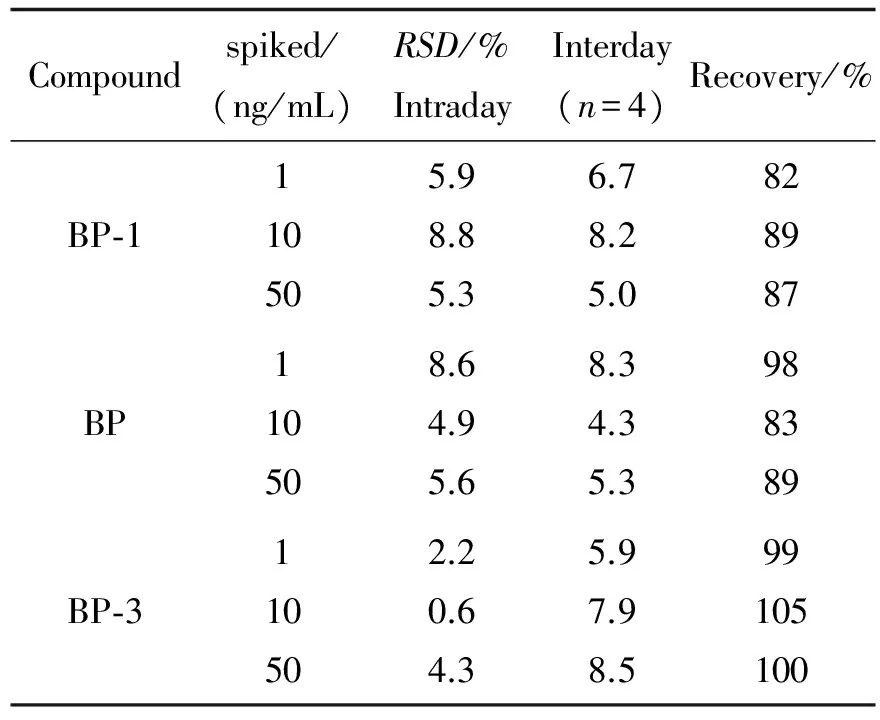
表2 加标回收率和精密度
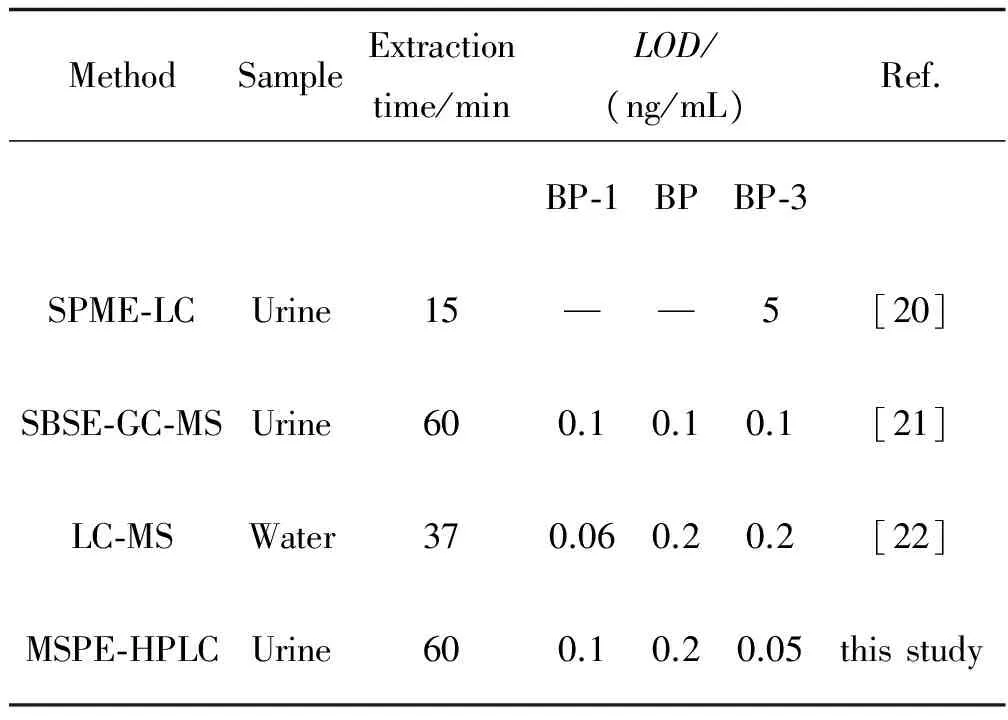
表3 本方法和其他分析方法的比较
将5 g防晒剂均匀涂抹在试验人皮肤上,每隔2 h取样,样品处理后,经材料吸附,洗脱后进HPLC检测,结果表明尿样中含有BP-3,见表4.
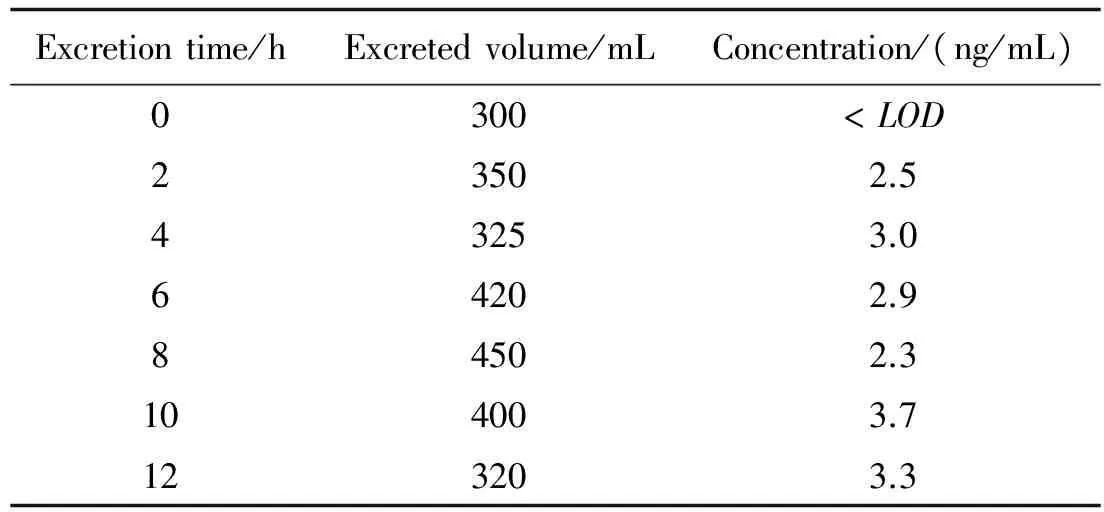
表4 不同取样时间尿样中的BP-3含量
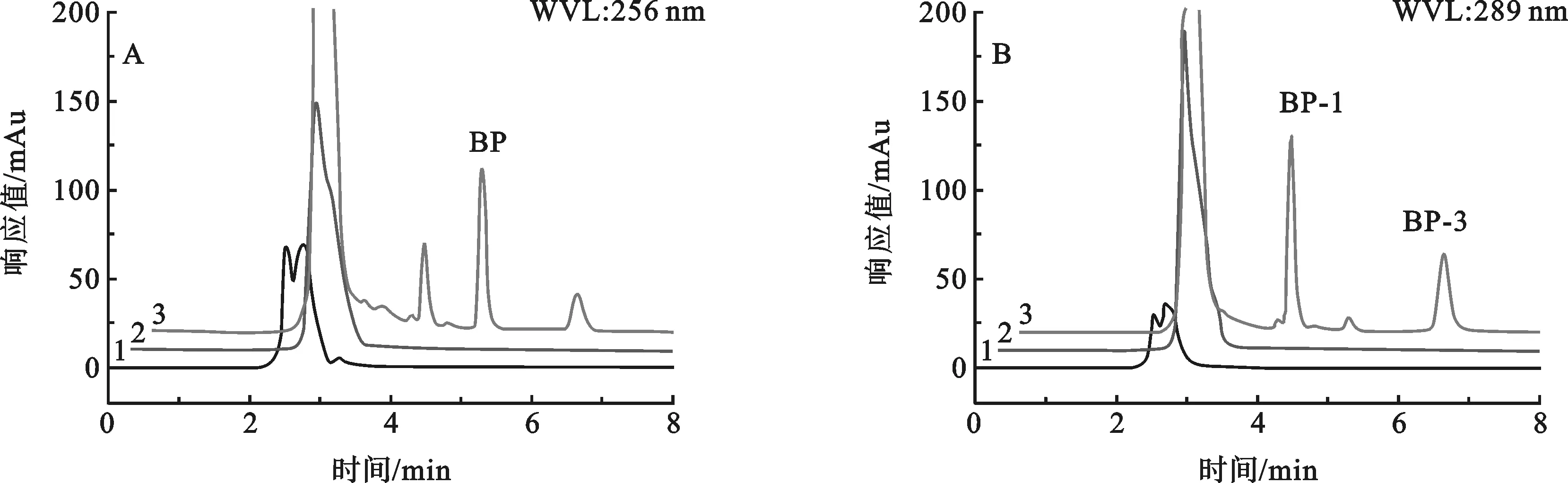
图7 256 nm(A)和289 nm(B)下空白尿样直接进样(1)、空白尿样加标50 ng/mL进样(2)、加标样品经MSPE富集(3)后的色谱
3 结论
以表面分散聚合法制备了Fe3O4聚合磁微粒,并进行材料结构、磁性、稳定性和吸附性能表征. 通过优化洗脱剂种类、体积、萃取时间、样品溶液酸度和离子强度等萃取条件,建立了尿样中3种常见二苯甲酮类物质的MSPE-HPLC分离分析方法.该方法操作简单、回收率高、灵敏度好,适用于实际尿样品中的二苯甲酮类的分析检测.
[1] 黄玮,由宏君,王世宏. 2,4-二羟基二苯甲酮的研究进展[J]. 辽宁化工,2003, 32(4): 158-160.
[2] 金颂良,骆丹.紫外线诱导的皮肤免疫抑制研究进展[J]. 中国美容医学,2006, 15(8): 987-989.
[3] 翟兴礼,史本林. 紫外线辐射对生物的影响[J]. 农业与技术,2000, 20(15): 44-45.
[4] Okereke C S, Barat S A, Abdel-Rahman M S. Safety evaluation of benzophenone-3 after dermal administration in rats[J]. Toxicol Lett, 1995, 80: 61-67.
[5] Rieger M M. Photostability of cosmetic ingredients on the skin : disposal of energy by photoactive molecules in sunscreens can adversely affect the sunscreens' function and safety[J]. Cosmetics and Toiletries, 1997, 112: 65-72.
[6] 中华人民共和国卫生部.化妆品卫生规范[S].北京:中华人民共和国卫生部,2007, 79-82.
[7] Vanoosthuyze K E, Van Poucke L S G, Deloof A C A. Development of a high-performance thin-layer chromatographic method for the multi-screening analysis of corticosteroids[J]. Anal Chin Acta, 1993, 275: 177-182.
[8] Ikeda K, Suzuki S, Watanabe Y. Determination of sunscreen agents in cosmetic products by gas chromatography and gas chromatography—mass spectrometry[J]. J Chromatogra A, 1990, 513: 321-326.
[9] Ye X, Kuklenyik Z, Needham L L, et al. Automated on-line column-switching HPLC-MS/MS method with peak focusing for the determination of nine environmental phenols in urine[J]. Anal Chem, 2005, 77 (16): 5407-5413.
[10] Wang S P, Lee W T. Determination of benzophenones in a cosmetic matrix by supercritical fluid extraction and capillary electrophoresis[J]. J Chromatogr A, 2003, 987: 269-275.
[11] Felix T, Hall B J, Brodbelt J S. Determination of benzophenone-3 and metabolites in water and human urine by solid-phase microextraction and quadrupole ion trap GC-MS[J]. Anal Chim Acta, 1998, 371: 195-203.
[12] Ro K W, Choi J B, Lee M H, et al. Determination of salicylate- and benzophenone-type sunscreen agents in cosmetic products by gas chromatography-mass spectrometry[J]. J Chromatogr A, 1994, 688: 375-382.
[13] Jeon H, Chung Y, Ryu J. Simultaneous determination of benzophenone-type UV filters in water and soil by gas chromatography-mass spectrometry[J]. J Chromatogr A, 2006, 1131: 192-202.
[14] 王胜林, 王强斌, 古宏晨.磁性微球的生物医学应用研究进展[J]. 化学世界, 2001(7): 384 -386.
[15] 谢钢,张秋禹,李铁虎.磁性高分子微球[J]. 高分子通报, 2001(6): 38-43.
[16] 王延梅,封麟先.磁性高分子微球的研究进展[J]. 高分子材料科学与工程, 1998, 5 (14): 6-8.
[17] Zhang M, Zhang Z, Liu Y. Preparation of core-shell magnetic ion-imprinted polymer for selective extraction of Pb(II) from environmental samples[J]. Chem Environ Sci, 2011, 178: 443-450.
[18] Kong X, Gao R, He X. Synthesis and characterization of the core-shell magnetic molecularly imprinted polymer (Fe3O4@MIPs) adsorbents for effective extraction and determination of sulfonamides in the poultry feed[J]. J Chromatogr A, 2012, 1245: 8-16.
[19] Karimi M, Aboufazeli F, Zhad H R. Determination of sulfonamides in chicken meat by magnetic molecularly imprinted polymer coupled to HPLC-UV[J]. Food Anal Chem, 2014, 7(1): 73-80.
[20] Felix T, Hall B J, Brodbelt J S. Estrogenic and antiandrogenic activities of 17 benzophenone derivatives used as UV stabilizers and sunscreens[J]. Anal Chim Acta, 1998, 371: 195-203.
[21] Kawaguchi M, Honda K, Okanouchi N. Miniaturized hollow fiber assisted liquid-phase microextraction and gas chromatography-mass spectrometry for determination of benzophenone and derivates in human urine sample[J]. Anal Sci,2008, 24:1509.
[22] Chisvert A, Vidal L, Canals A. Ionic liquid-based single-drop microextraction followed by liquid chromatography-ultraviolet spectrophotometry detection to determine typical UV filters in surface water samples[J]. Talanta, 2010, 81:549-555.
(责任编辑 胡小洋)
Preparation of nano Fe3O4magnetic polymer microspheres and theirapplication of magnetic solid phase extraction for benzophenones in urine
CHEN Di, LUO Han, ZHOU Shenglan, CHEN Huaixia
(College of Chemistry and Chemical Engineering, Hubei University, Wuhan 430062,China)
Fe3O4nanoparticles were synthesized by chemical co-precipitation of Fe3+and Fe2+under basic condition, and then were coated by SiO2by a modified Stober method. The composite was synthesized by dispersion polymerization. The structure and extraction performance of the magnetic polymer microspheres were evaluated by infrared spectrum and HPLC. Then this material was applied to separation and concentration of BPs in urine samples. By optimizing the extraction conditions, high selectivity analytical method for separation of benzophenones in urine had been developed. The experimental results showed that the linear ranges were 0.05—300 ng/mL for benzophenones in urine with the correlation coefficient of above 0.996 6. The detection limits (S/N=3) was 0.05 ng/mL.
nano Fe3O4; magnetic solid phase extraction; HPLC; benzophenone
2017-02-20
国家自然科学基金(2009CDB364)资助
陈迪(1992-),女,硕士生;陈怀侠,通信作者,教授,E-mail:hxch@hubu.edu.cn
1000-2375(2017)05-0474-06
TB383
A
10.3969/j.issn.1000-2375.2017.05.007

