优化高效液相色谱法检测万古霉素的血药浓度
张亮 陆磊 侯文洁 周秋云 丁红梓 王洁
·药物研究·
优化高效液相色谱法检测万古霉素的血药浓度
张亮 陆磊 侯文洁 周秋云 丁红梓 王洁
目的建立人血浆中万古霉素的高效液相色谱检测方法,为临床给药方案提供参考。方法采用6%高氯酸沉淀血浆中的蛋白,以乙腈-0.05 mol/L三氟乙酸(22∶3)为流动相,流速1 ml/min,检测波长280 nm。结果万古霉素在1.56~100 μg/ml范围内线性关系良好,批内、批间准确度的偏差<5%,批内、批间精密度<8%,在室温放置8、16、24 h及-20℃放置15 d后,万古霉素保持稳定,偏差小于5%。结论本方法测定万古霉素血药浓度具有准确和灵敏度高的特点,适合在治疗药物监测的应用中进行推广。
万古霉素;高效液相色谱法;药物浓度检测
万古霉素是当前治疗革兰氏阳性菌,特别是耐甲氧西林金黄色葡萄球菌(MRSA)最有效的药物之一。一直以来,万古霉素引起肾毒性是其在使用过程中最大的担忧。肾毒性是由于纯度较低导致的,随着制药工艺的优化和纯度的提高,毒性反应的发生率显著降低[1]。然而,临床实际中的情况是非常复杂的,患者往往合并有其它的基础疾病、老年患者还常常合用其他多种治疗药物。因此,对于万古霉素相关的肾毒性不可掉以轻心[2]。万古霉素属于治疗窗窄的药物,据报道,即使在治疗窗内也有相关肾毒性报道[3],若超过了治疗窗,则风险会大大增加。目前关于万古霉素药物浓度监测的报道虽然有很多[4,5],但在临床进行监测要求方法简单,操作简便。我们认为在已有的方法上依然有着进一步优化的空间。因此,本文参考了HPLC法检测万古霉素血药浓度的相关报道,在此基础上进行了方法学的改进,并成功用于临床患者。
1 材料与方法
1.1 仪器与试药 LC-20AB高效液相色谱系统(检测器为SPD-M20A,岛津,日本); 电子分析天平(EB224,0.1 mg,上海舜宇恒平科学仪器有限公司);高速离心机(TG1650-WS,上海卢湘仪);万古霉素对照品(中国药品生物制品检定所,批号:30360-200301);注射用盐酸万古霉素(Eli Lilly Japan K.K,规格:0.5g,批号:MW19231);乙腈(Merck,德国)为色谱纯,三氟乙酸(国药集团,中国)为分析纯,实验用水为MILLIPORE自制超纯水。
1.2 方法
1.2.1 色谱条件 色谱柱:CLC-ODS (250 mm×4.6 mm,5 μm,SMIMADZU,日本);流动相:乙腈-0.05 mol/L三氟乙酸(3∶22);柱温40℃;流速1 ml/min;检测波长280 nm;进样体积:20 μl。
1.2.2 血浆样品处理 取血浆样品500 μl于EP管中,加入6%高氯酸300 μl,涡旋震荡1 min,15 000 r/min离心3 min后,取上清液经0.45 μm滤膜过滤后进样分析。
2 结果
2.1 专属性试验 按“2.1”项下色谱条件,万古霉素保留时间在8.6 min左右,峰形良好,血浆内源性物质对分析无干扰,无杂质峰干扰检测。见图1。
2.2 标准曲线和定量下限 精密秤取万古霉素对照品适量溶于10 ml容量瓶中,加水溶解成1 mg/ml的标准储备液。在空白血浆中加入适量标准储备液,使血浆中药物浓度分别为1.56、3.125、6.25、12.5、25、50和100 μg/ml。按“2.2”项下的方法操作,记录下色谱图,以浓度为横坐标(X),峰面积为纵坐标(Y),通过加权最小二乘法进行回归运算,得到回归方程。试验结果表明万古霉素血药浓度在1.56~100 μg/ml范围内线性关系良好,定量下限(LLOQ)为1.56 μg/ml。
2.3 准确度与精密度试验 分别于500 μl空白血浆中加入标准储备液,配制成含低、中、高(2、10、80 μg/ml)3中不同的万古霉素血浆样品,每种浓度平行配制5份,再按“2.2”项下方法进行处理,依据标准曲线计算出万古霉素的血浆浓度,考察批内准确度和批内精确度;连续3 d重复相同的操作考察批间准确度和批间精确度。批内、批间准确度的偏差<5%,批内、批间精密度<8%。考察指标完全符合生物样品分析的要求。见表1、2。
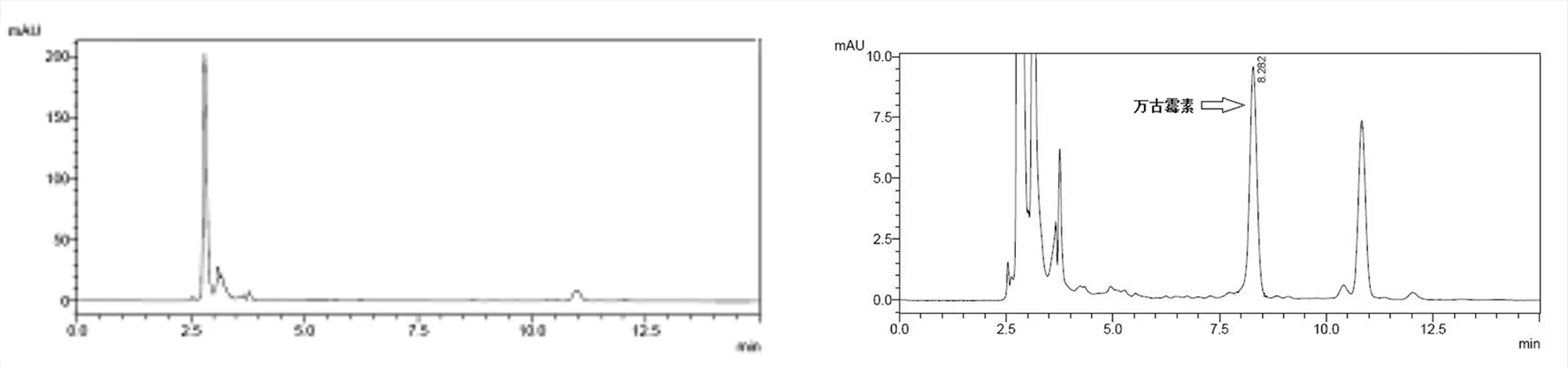
图1 HPLC色谱图

表1 批内准确度和精密度 n=5

表2 批间准确度和精密度 n=5
2.4 回收率试验 分别于500 μl空白血浆中加入标准储备液,精确配制成含低、中、高(2、10、80 μg/ml)3中不同的万古霉素血浆样品,每种浓度平行配制5份,按“2.2”项下方法处理后再进行分析,记录峰面积。800 μl流动相代替空白血浆配制相应的对照品溶液,每种浓度平行配制5份的样品,进样20 μl进行检测,每个浓度测5遍,按“2.2”项下方法处理后再进行分析,记录峰面积。以每种浓度两者峰面积之比计算提取回收率。绝对回收率大于90%。见表3。

表3 回收率试验 n=5
2.5 稳定性考察 血浆样品分别在室温放置8、16、24 h及-20℃放置15 d后进行分析。在这几个考察条件下,万古霉素的测定值均保持稳定,相对偏差小于5%。见表4。
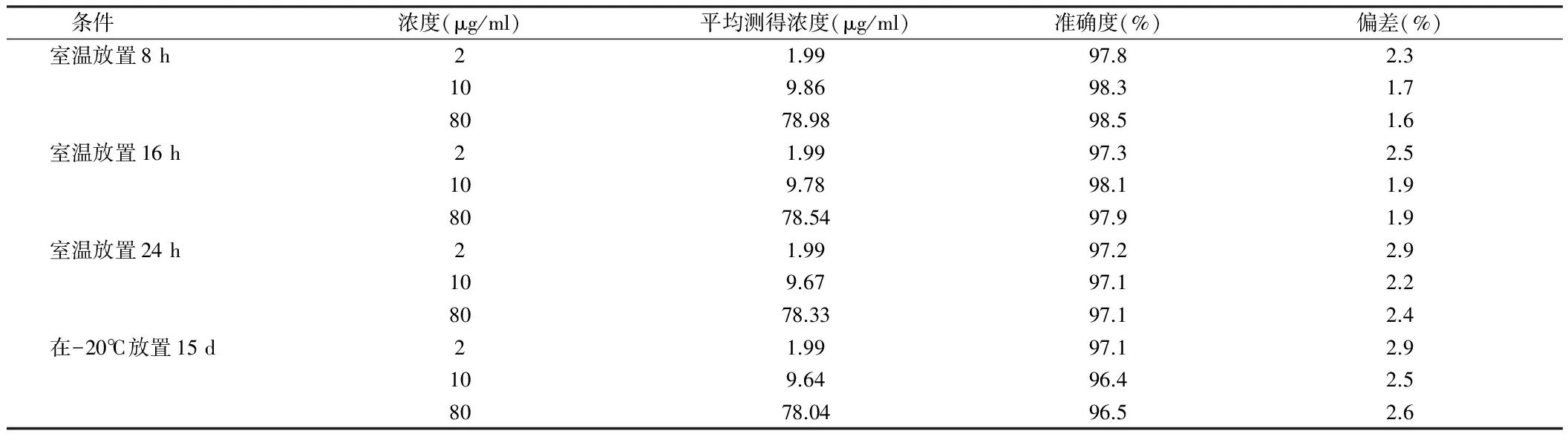
表4 稳定性试验 (n=5)
2.6 临床实际应用 本方法成功用于我院10例革兰氏阳性菌感染患者的血药浓度检测,检测对象大都是老年患者,用药为每8小时1 g或每12小时2 g。检测时间点为经4剂万古霉素治疗后,第5剂给药前30 min 的浓度。从测试结果看,患者的血浆中的药物浓度有差异,浓度在7.8~18.6 μg/ml,平均浓度(14.5±4.3)μg/ml。
3 讨论
早前由于万古霉素在临床上的使用受到很大程度的限制是由于其易引起毒性,相比较半合成青霉素更加安全。近些年(MRSA)感染率升高导致万古霉素的使用增加[6]。由于万古霉素的治疗窗窄,低浓度导致耐药和治疗不佳,高浓度导致治疗毒性。因此,对患者经行治疗药物检测是非常有必要的。美国感染病学在2009年万古霉素治疗指南中之处,其谷浓度应维持在10 mg/L以上,对于药敏结果提示最低抑菌浓度(MIC)达到1 mg/L需要将谷浓度维持在15~20 mg/L[7]。对于峰浓度来说由于没有发现其与毒性和疗效的之间有明确关系,所以不需要监测峰浓度。
目前主要有两种分析方法可以用来检测血浆中万古霉素浓度,一种是免疫法(包括放射免疫分析法和酶放大免疫检测法);另一种是色谱法[4,5]。免疫法的特点是简单、快速、有商业化的试剂盒可供使用。但是免疫法有难以克服的缺陷,一是成本过高;二是万古霉素相关物质(降解产物或生产过程中引入的物质)也会与试剂发生反应从而影响结果。大部分已报道检测万古霉素血药浓度的方法还是色谱法[8-10]。色谱法具有更高的灵敏度和特异度,在检测低浓度药物时更有优势。
由于万古霉素是水溶性抗生素,如果使用有机溶剂萃取就会导致药物回收率的降低。所以蛋白沉淀法是更能够确保准确性的方法。大部分已有的方法所使用高氯酸的浓度都在10%以上[11,12]。而本实验使用的是6%高氯酸。由于高氯酸属于有强腐蚀性的强酸,若长期使用浓度较高的酸会对色谱柱有损伤。我们在使用了6%、8%、10%和15%四种高氯酸作为沉淀剂进行试验后,发现对于10 μg/ml万古霉素的回收率并没有显示出差异。所以最终选用了6%的高氯酸。也有报道使用有机溶剂(甲醇或乙腈)沉淀蛋白的,我们经过反复试验认为使用有机溶剂会减少有效保留时间,而且有可能将保留在色谱柱上的弱极性杂质洗脱下来混进待测物中,对分析结果造成影响。所以,在准确度和精密度的前提下应该可以优先选择有机酸溶液。
在流动相方面,几乎所有研究中水相都使用了磷酸二氢钾缓冲盐。使用缓冲盐体系有很多缺陷:(1)对色谱柱损伤较大;(2)结束后需要长时间用高比例水冲洗,否则易堵塞色谱柱;(3)配制过程较为麻烦;(4)用高比例有机相进行分析时磷酸盐有析出的可能。在本试验中尝试使用0.05%三氟乙酸溶液做为水相,由于万古霉素的Pka为2.5~4.5,在偏酸性的流动相中待测物会以分子形式经过色谱系统,不会形成拖尾。经过试验比对,使用0.05%三氟乙酸溶液各项检测指标都能达到要求。
本试验具有简单、准确、经济的特点,使用15CM高保留C18柱即可获得很好的保留时间。能准确测定血浆中的万古霉素、特别适用于临床样本的检测。
1 George R,Baillie,Neal D,et al.Vancomycin Ototoxicity and Nephrotoxicity.Drug Safety,1988,3:376-386.
2 陈伯义,管向东,何礼贤,等.万古霉素临床应用中国专家共识(2011版).中国新药与临床杂志,2011,30:561-573.
3 李昕,李焕德,徐兵,等.万古霉素治疗细菌性肺炎患者时血药谷浓度与肾毒性相关性研究.中南药学,2009,7:352-356.
4 Oyaert M,Peersman N,Kieffer D,et al.Novel LC-MS/MS method for plasma vancomycin:comparison with immunoassays and clinical impact.Clin.Chim.Acta,2015,441:63-70.
5 Iwamoto T,Kagawa Y,Kojima M.Clinical efficacy of therapeutic drug monitoring in patients receiving vancomycin.Biol Pharm Bull,2003,26:876-879.
6 Rybak M,Lomaestro B,Rotschafer,et al.Therapeutic monitoring of vancomycin in adults summary of consensus recommendations from the American Society of Health-System Pharmacists,the Infectious Diseases Society of America,and the Society of Infectious Diseases Pharmacists.Pharmacotherapy,2009,29:1275-1279.
7 Cao YR,Yu JC,Chen YC,et al.Development and validation of a new ultra-performance liquid chromatographic method for vancomycin assay in serum and its application to therapeutic drug monitoring.Ther Drug Monit,2014,36:175-181.
8 华俊彦,田伟强,朱雅艳,等.万古霉素治疗耐甲氧西林金黄色葡萄球菌的疗效和血药浓度分析.中国临床药理学与治疗学,2010,15:673-677.
9 高稚婷,张锋英,王雷鸣,等.万古霉素血药浓度监测的临床应用.中国感染与化疗杂志,2014,14:526-531.
10 石秀锦,蔡郁,魏国义,等.老年肺部感染患者万古霉素血药浓度监测与疗效评价.中国临床药理学杂志,2012,28:803-805.
11 Cheng C,Liu SR,Xiao DQ,et al.LC-MS/MS method development and validation for the determination of polymyxins and vancomycin in rat plasma.J Chromatogr B,2010,15,878:2831-2838.
12 Bijleveld Y,Haan T,Toersche J,et al.A simple quantitative method analysing amikacin,gentamicin,and vancomycin levels in human newborn plasma using ion-pair liquid chromatography/tandem mass spectrometry and its applicability to a clinical study.J Chromatogr B,2014,951:110-118.
10.3969/j.issn.1002-7386.2017.18.039
项目来源:常州四药-南京药学会医院药学研究基金(编号:2014YX013)
210029 南京市,东南大学医学院附属南京胸科医院药学部
王洁,210029 南京市,东南大学医学院附属南京胸科医院药学部;
E-mail:xkyywj@163.com
R 917.1
A
1002-7386(2017)18-2861-03
2017-02-20)

