深部浸润型子宫内膜异位症的影像诊断研究进展
王曼頔戴 毅夏 宇陆菁菁
深部浸润型子宫内膜异位症的影像诊断研究进展
王曼頔1戴 毅2夏 宇3陆菁菁1
子宫内膜异位症;超声检查;磁共振成像;综述
深部浸润型子宫内膜异位症(deep in fi ltrating endometriosis,DIE)是子宫内膜异位症的一种特殊类型,是指子宫内膜异位病灶在腹膜下浸润深度>5 mm,多位于盆腔后部,包括直肠阴道隔、子宫直肠凹、子宫骶骨韧带、直肠及乙状结肠壁等,其他部位如膀胱、输尿管相对少见[1]。近来,DIE发病率呈明显上升趋势,且与疼痛、不孕密切相关,严重影响患者的生活质量[2]。本病的临床药物治疗效果不佳,且手术风险大、复发率较高,是妇科疾病治疗中的重点和难点。
临床诊断DIE主要依据临床症状结合妇科检查及影像学检查,而腹腔镜和病理检查是诊断盆腔子宫内膜异位症的“金标准”。妇科检查是一种重要的检查手段,但仅在某些特定的可触及部位上表现出较高的敏感度[3]。影像检查在DIE诊断方面具有较高的准确性,其价值得到越来越多的肯定。目前,经阴道超声(transvaginal sonography,TVS)是DIE首选的影像学检查,而MRI能够清晰地显示病变与周围组织结构的关系,在DIE诊断方面已经显示出越来越多的优势,在常规影像检查方法的基础上借助其他技术可提高诊断敏感度。本文对DIE的临床特点及分型进行综述,并着重阐述DIE的影像检查方法及其诊断研究进展。
1 DIE的临床特征与分型
DIE患者最突出且常见的症状为疼痛,主要临床表现为痛经、慢性盆腔痛、性交痛、肛门坠痛及不孕等。Dai等[4]对177例DIE患者调查发现,91.0%的患者有痛经症状,其中严重痛经者占43.5%。后盆腔的DIE患者中痛经的严重程度与2个独立因素有关,即直肠和阴道的浸润程度以及附件区粘连的范围[5]。位于膀胱的DIE常出现膀胱刺激症状伴周期性疼痛。肠道受累常合并排便痛、便秘或腹泻等。
DIE的分型主要根据病变的解剖部位,目前尚无明确统一的分型标准。Chapron等[6]按照解剖部位将其分为5型。I型:膀胱型,病灶累及膀胱固有肌层;II型:子宫骶骨韧带型,指病灶仅累及子宫骶骨韧带;III型:阴道型,病灶浸润子宫直肠凹、阴道后穹窿及两者之间的腹膜后区域;IV型:输尿管型,病灶累及输尿管壁或由其外部的DIE病灶压迫而导致的输尿管梗阻;V型:肠道型,病变累及肠管固有肌层。当同时存在多个部位的DIE病灶时,分型取决于最严重的病变部位,按照严重程度从低到高依次为子宫骶骨韧带、阴道、膀胱、肠道和输尿管。戴毅等[7]根据是否累及阴道穹窿和直肠提出了新的DIE分型方法,即单纯型、穹窿型和直肠型3种。单纯型:未累及穹窿或者直肠的病灶,包括子宫骶骨韧带、子宫直肠凹;穹窿型:浸润阴道穹窿的病灶;直肠型:后盆腔病灶累及直肠伴或不伴穹窿浸润。此种分型简洁清晰,对指导手术治疗有一定帮助。
2 影像学检查
2.1 超声检查 TVS和经腹部超声广泛应用于子宫内膜异位症的诊断。目前认为TVS是诊断DIE首选的影像检查方法,该法可探及子宫及其韧带、直肠阴道隔、子宫直肠凹、直肠及膀胱等盆腔内结构。经直肠超声及直肠内镜超声有助于发现直肠DIE病变,但临床上应用相对较少。
DIE在超声图像上多表现为异常的低回声线样增厚、结节或肿块,伴或不伴有不规则的边界,彩色多普勒超声常可见散在点状或短条状的不丰富血流信号[8]。不同部位DIE的超声特点分别为:子宫骶骨韧带DIE多为规则或不规则的结节状或线样低回声增厚;直肠阴道隔DIE常表现为宫颈后唇下缘水平以下的结节或团块状低回声;阴道受累则表现为阴道后穹窿增厚,伴或不伴圆形囊性无回声区;直肠、乙状结肠病变表现为不规则的低回声团块,伴或不伴有斑点状低/高回声浸润肠壁;膀胱受累时可见膀胱壁上的低回声结节或囊性病灶[3]。
超声诊断不同部位DIE的准确性并不一致,且与病变的浸润深度有关。Exacoustos等[9]对104例DIE患者进行术前TVS检查,得到诊断不同部位DIE的准确度为76%~97%。其中阴道DIE的敏感度和准确度最低,分别为59%和76%;诊断膀胱病灶和子宫直肠凹封闭的准确度最高,均为97%。经直肠超声和直肠内镜超声均可用于直肠DIE的诊断。Rossi等[10]通过回顾性研究发现直肠内镜超声可以准确评估浸润肌层的直肠病变,然而对于黏膜及黏膜下层的DIE病灶诊断准确性较低,其敏感度、特异度和准确度分别为89%、26%和58%。
在常规TVS检查的基础上,利用“触痛引导法”和“滑动征象”可提高诊断效能。Guerriero等[11]于2007年首次提出在检查中采用“触痛引导法”可提高DIE的诊断准确度,其敏感度和特异度分别达90%和95%。检查时超声探头表面用12 ml超声凝胶取代常规的4 ml,先将探头置于阴道后穹窿,边滑动按压边观察患者有无触痛,在触痛阳性处停止滑动仔细检查,有助于发现子宫直肠凹、子宫颈后方及直肠阴道隔DIE。也有操作者采用这种TVS方法检查直肠、乙状结肠DIE,并取得了与MRI相似的诊断效能,其中TVS的敏感度和特异度为73%、86%,MRI为73%、90%[12]。Guerriero等[13]将“触痛引导法”与三维超声技术相结合对202例患者进行研究,并与普通二维超声进行对照,结果显示三维超声在诊断除乙状结肠以外的后盆腔DIE中均有很高的准确度,如子宫骶骨韧带、阴道及直肠阴道隔处的病变,诊断后盆腔DIE的总敏感度为87%、特异度为94%。另有学者利用“滑动征象”预测子宫直肠凹封闭和直肠受累情况。TVS检查中的“滑动征象”阴性是指直肠与子宫、阴道后穹窿的位置相对固定,阳性为可以发生滑动,“滑动征象”为阴性者提示DIE,其诊断直肠DIE的敏感度、特异度和准确度分别达85%、96% 和 93%[14]。
此外,文献报道采用盐水对比经阴道超声,即通过导尿管向阴道注入盐水溶液的方法,其诊断准确性优于单纯TVS,并与MRI相比均具有较高的诊断价值[15]。与之类似,Bergamini等[16]采用直肠内盐水对比经阴道超声的方法观察直肠和乙状结肠的病变,并与传统检查方法比较发现,该方法在诊断直肠和乙状结肠DIE方面与经直肠超声的准确性一致;而在评估肠腔狭窄方面,与钡灌肠造影具有同样的效能。
2.2 MRI MRI可以全面观察盆腔内结构,包括腹腔镜下无法探及的部位,并且能够清晰地显示病变与周围组织结构的关系。对于发现不同部位的DIE病灶、周围组织的粘连及子宫直肠凹的封闭有较好的诊断价值。
根据病变部位和MRI特点可以将DIE分成3种类型。I型:实性深部浸润病灶;II型:子宫骶骨韧带和子宫颈旁病灶;III型:内脏器官病灶,主要包括膀胱和直肠壁[17]。实性深部浸润病灶在T1加权像上表现为低-中等信号伴斑点状高信号,斑点状高信号代表被实性纤维组织包绕的出血性病灶,T2加权像上则表现为均一的低信号(图1)。子宫骶骨韧带、阴道后穹窿和子宫直肠凹DIE在T2加权像上可表现为高信号,这是因为病灶多由大量的腺体伴有少量纤维化成分组成,增强扫描实性腺体成分可见强化。在缺乏典型的斑点状出血灶时,当出现子宫骶骨韧带增厚(>9 mm)、双侧或非对称受累、韧带内结节征象时更有助于DIE的诊断(图2)。膀胱DIE病灶表现为膀胱壁的局灶性或弥漫性增厚,绝大多数病例可见异常增厚的膀胱壁内出现点状高信号,位于膀胱子宫凹的病灶常可侵犯膀胱壁(图3)。MRI对发现直肠DIE病灶具有一定的局限性,直肠壁增厚伴有T2上低信号和有时出现的T1上斑点状高信号出血灶可有助于诊断。有学者提出直肠、乙状结肠T2上的“蘑菇帽”征是诊断DIE的特征性表现,即在高信号的黏膜层及黏膜下层覆盖下,可见增厚的固有肌层内不均匀低信号[18]。
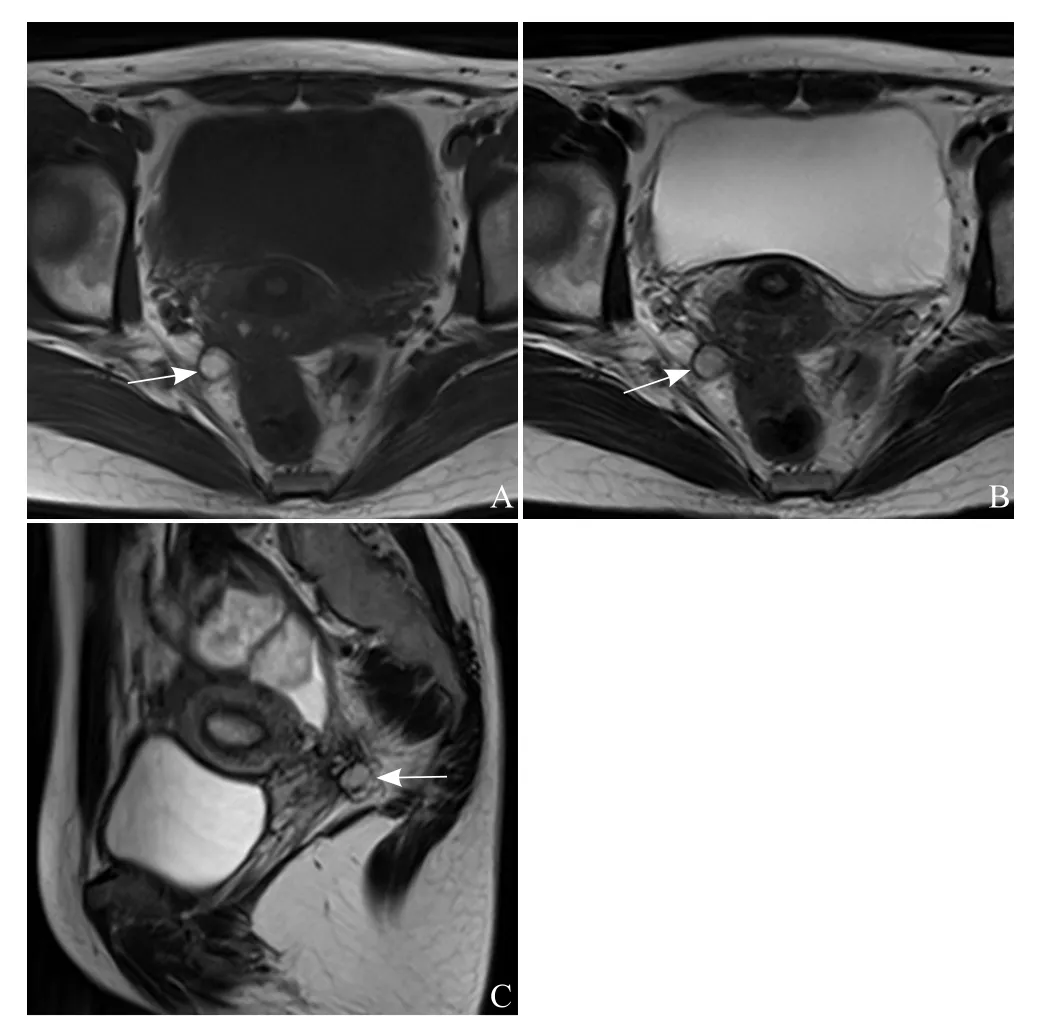
图1 27岁,直肠阴道隔DIE。轴 位 T1WI(A) 及 T2WI(B)示宫颈右后方、直肠右前方结节影(箭),T1WI(A)呈高信号,T2WI(B)呈稍高信号,矢状位T2WI(C)示宫颈与直肠之间稍高信号结节影(箭)
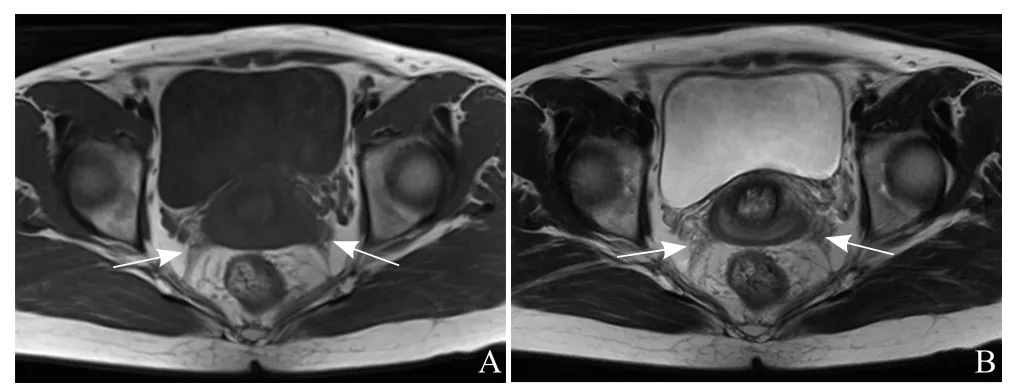
图2 32岁,子宫骶骨韧带DIE。轴位T1WI(A)及T2WI(B)示双侧子宫骶骨韧带不规则增粗(箭),T1WI(A)以等信号为主,T2WI(B)以稍高信号为主,其内均可见点状高信号
DIE常侵犯子宫直肠凹,导致该部位的粘连、封闭。Macario等[19]总结了5种高度提示子宫直肠凹封闭的征象,分别是子宫后屈、子宫和直肠之间的纤维病灶、原有的盆腔积液移位、阴道后穹窿抬高及与周围肠管粘连。其中盆腔积液移位的征象最具有临床价值,其诊断DIE所致的子宫直肠凹封闭的准确度高达93.1%。阴道后穹窿、直肠阴道隔的病变向后方延伸也会导致子宫直肠凹的封闭;而腹腔镜可能会遗漏该部位病灶。MRI可协助该部位病灶的显示,其重要性更加突出[20]。
MRI扫描技术是清晰显示和准确评价DIE的关键。临床常用的1.5T和3.0T场强的MRI设备均可满足盆腔扫描需求。在扫描序列方面,Siegelman等[21]认为所有女性盆腔MRI均推荐使用T1加权脂肪抑制序列。因为这样可将子宫内膜异位症与含脂肪的成熟囊性畸胎瘤相鉴别,并且可以凸显非脂肪成分的T1高信号病变,提高诊断小的腺肌瘤和DIE的敏感度。子宫骶骨韧带是DIE最常受累的部位。有文献报道采用3 mm薄层的斜轴位扫描方式有助于发现该处的病变。若矢状位T2加权像上可见一侧或双侧子宫骶骨韧带,该斜轴位平面应沿子宫骶骨韧带走行的方向;当子宫骶骨韧带不可见时,斜轴位平面应与宫颈垂直[22]。
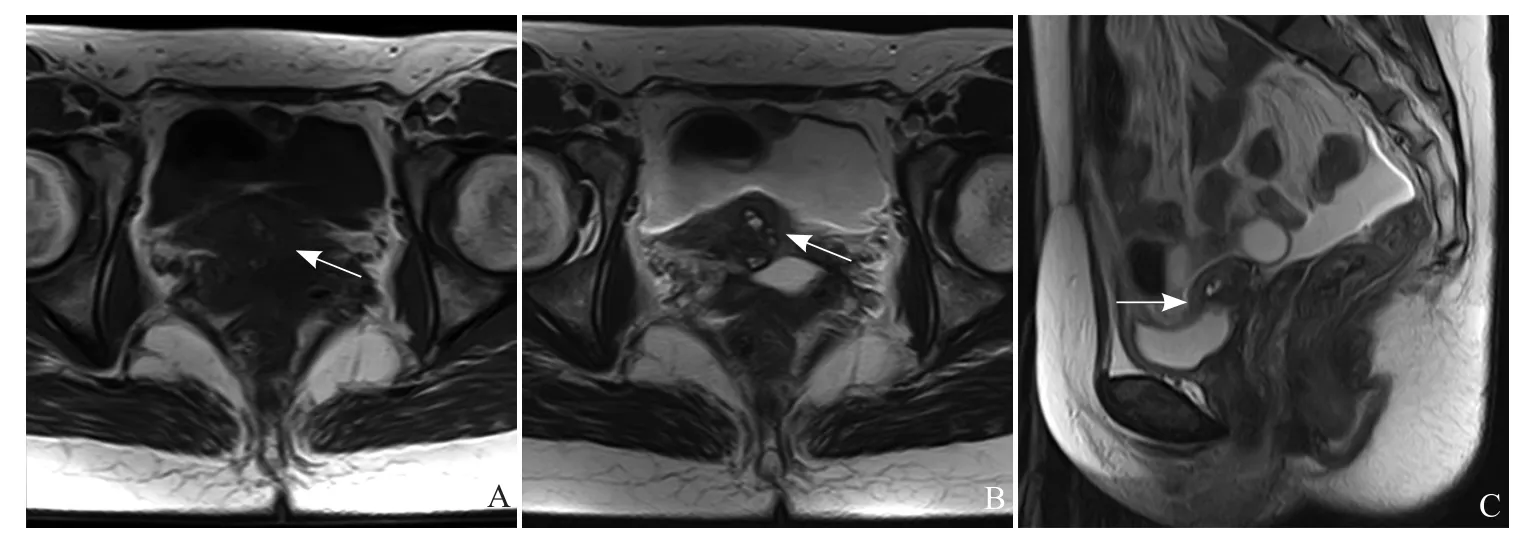
图3 36岁,子宫及双附件切除术后膀胱DIE。轴位T1WI(A)及T2WI(B)示膀胱后壁外不规则异常信号影(箭),T1WI(A)呈等信号,T2WI(B)呈稍高信号,其内均可见多发斑点状高信号,矢状位T2WI示膀胱后上壁上方异常信号影(箭),病灶累及膀胱壁(C)
随着三维成像技术的不断发展与成熟,三维T2加权MRI可明显缩短扫描时间,并能够得到与普通二维成像相同的诊断准确性[23]。三维重建MRI可以发现子宫直肠凹、膀胱子宫凹及直肠阴道隔的DIE病灶。文献报道其总敏感度和准确度分别为83%和86%,可在术前对病灶进行准确定位并描述其体积大小,尤其适用于乙状结肠或膀胱的浸润性病变,有助于指导手术[24]。
为提高MRI诊断DIE的敏感性,许多学者在常规扫描的基础上采用其他辅助手段。Fiaschetti等[25]的一项前瞻性研究中,采用阴道注入凝胶的方法对63例临床怀疑为DIE的患者行MRI检查发现,未注入凝胶的敏感度为67.8%,而注入凝胶后为90.8%,尤其在直肠阴道隔、子宫骶骨韧带和阴道后穹窿,诊断敏感度明显提高。直肠内注入凝胶同样有助于显示病变,Nathaile等[26]应用3.0T MRI并采用直肠内凝胶填充的方法,得到的诊断敏感度、特异度和准确度分别高达93.3%、100.0%和97.6%。由于TVS无法评估乙状结肠以上的肠管,MRI显示出其独特的优势。Rousset等[27]采用口服甘露醇小肠MRI重建的方法,结果证实MRI在诊断直肠、乙状结肠交界以上的肠道DIE有良好的准确性,阳性预测值高达100%,可直观显示小肠及结肠的病变范围及粘连情况,在一定程度上决定手术方案,指导手术治疗。
TVS和MRI是诊断DIE最重要的影像学检查,运用图像融合技术可将2种检查的图像进行空间配准融合。有学者将磁场传感器安装到超声探头上组成新型的实时虚拟超声成像设备,可以在TVS检查中将已获取的MRI图像传输到超声设备上,从而产生超声和MRI的多模态融合图像,这种融合图像整合了超声和MRI的优势,可以更好地显示部分主要解剖部位的DIE病变[28]。该方法的临床实用价值还需进一步验证。
综上所述,DIE是严重影响育龄期妇女健康和生活质量的一种疾病,临床诊断主要依据病史、妇科检查及多种影像学检查。TVS和MRI作为最重要的2种影像检查方法,在诊断和评估DIE病变方面具有重要作用,其诊断效果取决于操作者的经验和对不同部位病变的认识程度。在常规影像方法的基础上采用其他辅助手段和扫描技术可以提高诊断效能,为术前诊断及评估DIE提供更多帮助。
[1] Kinkel K, Frei KA, Balleyguier C, et al. Diagnosis of endometriosis with imaging: a review. Eur Radiol, 2006, 16(2): 285-298.
[2] Koninckx PR, Ussia A, Adamyan L, et al. Deep endometriosis:de fi nition, diagnosis, and treatment. Fertil Steril, 2012, 98(3): 564-571.
[3] Bazot M, Lafont C, Rouzier R, et al. Diagnostic accuracy of physical examination, transvaginal sonography, rectal endoscopic sonography, and magnetic resonance imaging to diagnose deep in fi ltrating endometriosis. Fertil Steril, 2009, 92(6): 1825-1833.
[4] Dai Y, Leng JH, Lang JH, et al. Anatomical distribution of pelvic deep infiltrating endometriosis and its relationship with pain symptoms. Chin Med J (Engl), 2012, 125(2): 209-213.
[5] Chapron C, Fauconnier A, Dubuisson JB, et al. Deep in fi ltrating endometriosis: relation between severity of dysmenorrhoea and extent of disease. Hum Reprod, 2003, 18(4): 760-766.
[6] Chapron C, Chopin N, Borghese B, et al. Deeply infiltrating endometriosis: pathogenetic implications of the anatomical distribution. Hum Reprod, 2006, 21(7): 1839-1845.
[7] 戴毅, 冷金花, 郎景和, 等. 后盆腔深部浸润型子宫内膜异位症的临床病理特点及腹腔镜手术治疗效果. 中华妇产科杂志,2010, 45(2): 93-98.
[8] Bazot M, Thomassin I, Hourani R, et al. Diagnostic accuracy of transvaginal sonography for deep pelvic endometriosis. Ultrasound Obstet Gynecol, 2004, 24(2): 180-185.
[9] Exacoustos C, Malzoni M, Di Giovanni A, et al. Ultrasound mapping system for the surgical management of deep in fi ltrating endometriosis. Fertil Steril, 2014, 102(1): 143-150.
[10] Rossi L, Palazzo L, Yazbeck C, et al. Can rectal endoscopic sonography be used to predict infiltration depth in patients with deep in fi ltrating endometriosis of the rectum? Ultrasound ObstetGynecol, 2014, 43(3): 322-327.
[11] Guerriero S, Ajossa S, Gerada M, et al. Tenderness-guided.transvaginal ultrasonography: a new method for the detection of deep endometriosis in patients with chronic pelvic pain. Fertil Steril, 2007, 88(5): 1293-1297.
[12] Saba L, Guerriero S, Sulcis R, et al. MRI and "tenderness guided"transvaginal ultrasonography in the diagnosis of recto-sigmoid endometriosis. J Magn Reson Imaging, 2012, 35(2): 352-360.
[13] Guerriero S, Saba L, Ajossa S, et al. Three-dimensional ultrasonography in the diagnosis of deep endometriosis. Hum Reprod, 2014,29(6): 1189-1198.
[14] Hudelist G, Fritzer N, Staettner S, et al. Uterine sliding sign: a simple sonographic predictor for presence of deep infiltrating endometriosis of the rectum. Ultrasound Obstet Gynecol, 2013,41(6): 692-695.
[15] Saccardi C, Cosmi E, Borghero A, et al. Comparison between transvaginal sonography, saline contrast sonovaginography and magnetic resonance imaging in the diagnosis of posterior deep in fi ltrating endometriosis. Ultrasound Obstet Gynecol, 2012, 40(4):464-469.
[16] Bergamini V, Ghezzi F, Scarperi S, et al. Preoperative assessment of intestinal endometriosis: a comparison of transvaginal sonography with water-contrast in the rectum, transrectal sonography, and Barium enema. Abdom Imaging, 2010, 35(6):732-736.
[17] Del Frate C, Girometti R, Pittino M, et al. Deep retroperitoneal pelvic endometriosis: MR imaging appearance with laparoscopic correlation. Radiographics, 2006, 26(6): 1705-1718.
[18] Yoon JH, Choi D, Jang KT, et al. Deep rectosigmoid endometriosis:"mushroom cap" sign on T2-weighted MR imaging. Abdom Imaging, 2010, 35(6): 726-731.
[19] Macario S, Chassang M, Novellas S, et al. The value of pelvic MRI in the diagnosis of posterior cul-de-sac obliteration in cases of deep pelvic endometriosis. Am J Roentgenol, 2012, 199(6): 1410-1415.
[20] 梁文华, 陆菁菁, 冯逢, 等. 深部浸润型子宫内膜异位症MRI表现. 临床放射学杂志, 2014, 33(1): 63-67.
[21] Siegelman ES, Oliver ER. MR imaging of endometriosis: ten imaging pearls. Radiographics, 2012, 32(6): 1675-1691.
[22] Bazot M, Gasner A, Ballester M, et al. Value of thin-section oblique axial T2-weighted magnetic resonance images to assess uterosacral ligament endometriosis. Hum Reprod, 2011, 26(2):346-353.
[23] Bazot M, Stivalet A, Daraï E, et al. Comparison of 3D and 2D FSE T2-weighted MRI in the diagnosis of deep pelvic endometriosis:preliminary results. Clin Radiol, 2013, 68(1): 47-54.
[24] Giusti S, Forasassi F, Bastiani L, et al. Anatomical localization of deep in fi ltrating endometriosis: 3D MRI reconstructions. Abdom Imaging, 2012, 37(6): 1110-1121.
[25] Fiaschetti V, Crusco S, Meschini A, et al. Deeply infiltrating endometriosis: evaluation of retro-cervical space on MRI after vaginal opaci fi cation. Eur J Radiol, 2012, 81(11): 3638-3645.
[26] Hottat N, Larrousse C, Anaf V, et al. Endometriosis: contribution of 3.0T pelvic MR imaging in preoperative assessment-initial results.Radiology, 2009, 253(1): 126-134.
[27] Rousset P, Peyron N, Charlot M, et al. Bowel endometriosis:preoperative diagnostic accuracy of 3.0T MR enterography-initial results. Radiology, 2014, 273(1): 117-124.
[28] Millischer AE, Salomon LJ, Santulli P, et al. Fusion imaging for evaluation of deep infiltrating endometriosis: feasibility and preliminary results. Ultrasound Obstet Gynecol, 2015, 46(1): 109-117.
R711.22;R445.1
2017-01-20
2017-03-03
(本文编辑 闻 浩)
10.3969/j.issn.1005-5185.2017.08.018
1.中国医学科学院 北京协和医院放射科 北京100730;2.中国医学科学院 北京协和医院妇产科 北京100730;3.中国医学科学院 北京协和医院超声诊断科北京 100730
陆菁菁 E-mail: cjr.lujingjing@vip.163.com

