利用白酒丢糟制备蛋白发泡剂
王宇鹏,赵华*
(天津科技大学生物工程学院,天津300457)
利用白酒丢糟制备蛋白发泡剂
王宇鹏,赵华*
(天津科技大学生物工程学院,天津300457)
使用白酒丢糟为原料制备蛋白发泡剂。以蛋白发泡剂的发泡性能为评价指标,优化白酒丢糟的水解条件和蛋白发泡剂的制备条件,确定最适的水解条件为:选用氧化钙和氢氧化钠组成的复合水解剂,其中氧化钙用量为丢糟质量的6%,并添加氢氧化钠使得pH值为12.5,固液比为1∶4(g∶m L),温度120℃,时间3 h。此外蛋白发泡剂最佳制备条件为:脱钙率50%,浓缩前后蛋白液的pH均为7,浓缩温度和蛋白含量分别为36℃和3%,黄原胶添加量为0.15%。在此最佳条件下,最终得到蛋白发泡剂起泡体积为330m L,稳泡体积为255m L。
白酒丢糟;蛋白发泡剂;发泡体积;稳泡体积
发泡剂又称为起泡剂或者沫泡剂,是一种能使其水溶液在机械作用引入空气的情况下产生大量泡沫的物质,多是指表面活性剂或者表面活性物质。发泡剂的种类主要有松香型、合成类表面活性剂、蛋白质型及复合型发泡剂等[1]。在这些发泡剂中,蛋白发泡剂具有泡沫稳定性好、可降解无污染等优点,成为近年来的研究热点。
蛋白发泡剂广泛应用于食品行业,建筑行业的混凝土制备及消防领域的泡沫灭火器的制备中。食品行业中,MARINEZT K D等[2]以大豆为原料,经过酶促反应,并添加黄原胶等表面活性多糖,研究多糖对大豆蛋白及其水解产物的发泡性能的影响,确定了工业中用于提高蛋白发泡剂发泡性能的蛋白质—多糖的最佳比例。LOMOLINOG等[3]以富含蛋白质的马铃薯为原料,通过在相同压力和时间下向发泡液体中喷射不同的气体来研究影响蛋白发泡剂性质的原因,从而制备出可用于食品行业的蛋白发泡剂。在建筑行业方面,孙萌等[4]通过理论研究确定发泡剂种类,以发泡剂的发泡倍数和泡沫稳定性试验确定发泡剂的最佳用量,最终以动物蛋白发泡剂制备出低密度泡沫混凝土。姜松等[5]采用α-烯基磺酸钠(alpha-olefin sulfonate,AOS)、十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、十二烷基苯磺酸钠等阴离子表面活性剂以及硅树脂聚醚乳液、十二醇、羟乙基纤维素等稳泡剂对混凝土用蛋白质发泡剂进行复配改性,制备出优异的泡沫混凝土。而在消防领域方面,毕波[6]提出了一种利用碱—醇法从酒糟中提取蛋白质从而制备蛋白泡沫灭火剂的方法。何越等[7]公布了一种利用植物蛋白为原来制备泡沫灭火剂的方法,其发泡倍数高、贮存时间长、沉淀物少、黏度小、蛋白质不易变质。
白酒是中国传统的饮料酒。然而,每生产1 t白酒,约产生3 t的丢糟。我国每年白酒产量约为1 226.20万kL,白酒丢糟作为白酒生产中主要副产物,其年产鲜酒糟近2100万t[8]。白酒丢糟量大、集中,并且酸度较高、易腐败变质,若不及时处理,必然会对环境造成严重的污染;另外,由于白酒丢糟中营养成分含量较高,干物质中粗蛋白的含量达20%左右,若不能使白酒丢糟得到充分合理的利用,还会浪费这些资源[9]。因此,本研究选用白酒丢糟制备蛋白发泡剂,通过对白酒丢糟的复合碱水解、离心、脱钙、浓缩并添加黄原胶制备而成,通过该制备方法不仅有效地解决了白酒丢糟的利用问题,为某些用酒糟制备饲料或土壤添加剂不经济的地区提供一种新的酒糟处理措施,并为蛋白发泡剂提供了一种廉价易得的原料。
1 材料与方法
1.1 材料与试剂
酱香型白酒丢糟(含水量60.0%):天津市宁河酒厂酱香型酒糟;氢氧化钠、醋酸(均为分析纯):天津市化学试剂一厂;氧化钙(分析纯):国药集团化学试剂北京有限公司;无水碳酸钠(分析纯):天津市北方天医化学试剂厂;蔗糖(分析纯):天津市三江赛瑞达科技有限公司;明胶(分析纯):天津大学科威公司;黄原胶(食品级):淄博中轩生化有限公司。
1.2 仪器与设备
SYQ-DSX-280B医用灭菌锅:上海申安医疗器械厂;2152型罗氏泡沫仪:上海银择仪器设备有限公司;KON-2C自动凯氏定氮仪:上海纤检仪器有限公司;LD5-2A离心机:北京医用离心机厂;RE-52AA旋转蒸发仪:上海雅荣生化仪器设备有限公司。
1.3 实验方法
1.3.1 白酒丢糟的水解及蛋白发泡剂的制备
取白酒丢糟60 g(含水量60%),按照1∶4~1∶7(g∶m L)加水,添加水解剂进行水解,维持pH 11~13[10],水解温度为80~120℃,水解时间1~6 h。将所得的白酒丢糟水解液放入离心机,控制转速8 000 r/m in离心5min,取上清蛋白液,测定所得蛋白液中的钙含量,然后添加过量碳酸钠对水解液进行脱钙并再次测定蛋白液中的钙含量,计算蛋白液的脱钙率,维持脱钙率10%~90%,为防止蛋白液进一步水解,向其中添加醋酸,使得水解液的pH近中性,使用旋转蒸发仪在36~51℃对蛋白液进行浓缩,使蛋白液的蛋白含量为3%~12%,再次使用醋酸调节pH近中性,并添加0.05%~0.20%的添加剂制备成蛋白发泡剂。
1.3.2 水解剂对蛋白发泡剂泡沫性能的影响
通过水解作用,酒糟中的蛋白质部分水解,一部分侧链基团暴露出来,有利于增加蛋白发泡剂的泡沫性能,然而酸性水解剂水解时易造成蛋白质过度水解,使蛋白质变为小分子的肽或进一步水解为氨基酸,影响蛋白液泡沫的稳定性[10],其水解性能往往不如碱性水解剂,因此选择碱性水解剂,其中碱性水解剂常选择氧化钙或氢氧化钠。
取白酒丢糟60 g(含水量60%),以水解剂为单一变量,分别使用氢氧化钠、氧化钙及碱性复合水解剂作为水解剂(其中使用单一水解剂时,分别添加氢氧化钠和氧化钙,使得水解液的pH为12;使用复合水解剂时,添加氧化钙用量固定为6%,并添加氢氧化钠使得pH为12),制备蛋白发泡剂并测定其发泡性能。
1.3.3 各因素对蛋白发泡剂泡沫性能的影响[12-13]
取60 g白酒丢糟(含水量60%),分别使用氢氧化钠调节pH值为11.5、12.0、12.5、13.0,加入2%、4%、6%、8%、10%的氧化钙,固液比为1∶4、1∶5、1∶6、1∶7(g∶m L),水解温度为60℃、80℃、100℃、120℃、140℃,水解时间为1 h、2 h、3 h、4 h、5 h、6 h,控制脱钙率为0、25%、50%、75%、100%,浓缩温度为36℃、41℃、46℃、51℃,分别控制蛋白含量为3%、6%、9%、12%,分别以蔗糖、明胶、黄原胶为添加剂,并控制添加量为0、0.05%、0.10%、0.15%、0.20%,制备蛋白发泡剂并测定其发泡性能。
1.3.4 钙含量及脱钙率的测定
使用乙二胺四乙酸(ethlene diam ine tetraacetic acid,EDTA)滴定法测定溶液中的钙含量[14]。脱钙率计算公式如下:

1.3.5 蛋白含量的测定
使用自动凯氏定氮仪测定蛋白质含量[15]。
1.3.6 蛋白发泡剂泡沫性能测定
采用罗氏泡沫仪测定蛋白液的泡沫性能,以最终蛋白发泡剂的起泡体积和稳泡体积分别代表待测蛋白液的起泡能力和稳泡能力。具体操作步骤为:量取300m L左右的蛋白浓缩液加入到大烧杯中,放在30℃水浴锅内保温15~20m in后,取50m L的待测蛋白液,倒入罗氏泡沫仪的刻度管内,再取200m L的蛋白液加入到泡沫移液管。整个操作过程需缓慢地进行,并且要避免泡沫的生成。
将200m L的蛋白液从毛细管中自由流下,冲击刻度管内的蛋白液,此时刻度管内将产生大量泡沫,形成泡沫柱。在200m L的蛋白液刚流完时开始计时,同时读取刻度管内的泡沫体积,即为起泡体积(V0),并在5m in后再次读取刻度管内的泡沫体积,记为稳泡体积(V1)。每个待测蛋白液样品做3次实验并以结果的平均值作为最终的实验结果,重复测定结果之间的误差不得超过5m L[16-17]。
2 结果与分析
2.1 白酒丢糟的水解条件优化
2.1.1 水解剂对泡沫性能的影响
水解剂对制备蛋白发泡剂的泡沫性能影响结果如表1所示。
由表1可知,使用氢氧化钠作为水解剂时,水解剂的用量少,但是蛋白发泡剂的泡沫性能较差,此时蛋白发泡剂的起泡体积为151m L,稳泡体积为70m L;使用氧化钙作为水解剂时,蛋白发泡剂的泡沫性能最好,此时的蛋白发泡剂的起泡体积为333m L,稳泡体积为248m L,但是氧化钙的用量较大,而氧化钙作为水解剂后不能再回收或进一步利用,后续的处理困难,这就造成资源的浪费;而使用复合水解剂水解时,氧化钙用量适中,而且可以达到较好的水解效果,此时蛋白发泡剂的起泡体积为320m L,稳泡体积为251m L。因此,综合蛋白发泡剂的泡沫性能和氧化钙用量,选择水解剂为碱性复合水解剂。

表1 碱性水解剂对蛋白液泡沫性能的影响Table 1 Effect of alkaline hydrolysis agent on foam p roperties of protein solution
2.1.2 水解pH对泡沫性能的影响
水解pH对蛋白发泡剂泡沫性能的影响结果如图1所示。
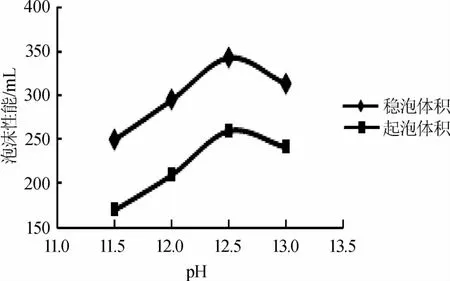
图1 pH值对蛋白液泡沫性能的影响Fig.1 Effect of pH value on foam properties of protein solution
由图1可知,随着蛋白液的pH在11.5~12.5范围内逐渐升高,制备出的蛋白发泡剂的泡沫性能也逐渐增加;当pH值为12.5时蛋白发泡剂的起泡体积为343m L,稳泡体积为260m L;当pH>12.5时,泡沫性能逐渐降低。因此本实验选用水解pH值为12.5。
2.1.3 氧化钙用量对蛋白发泡剂发泡性能的影响
氧化钙用量对蛋白发泡剂泡沫性能的影响结果如图2所示。
由图2可知,随着氧化钙用量在2%~6%范围内增加,蛋白发泡剂的发泡性能逐渐增加;当氧化钙用量为6%时,此时蛋白发泡剂的起泡体积为315m L,稳泡体积为242m L;当氧化钙用量>6%时,泡沫性能的增长趋于平缓。综合发泡剂的发泡性能和氧化钙用量考虑,选用氧化钙用量为6%。
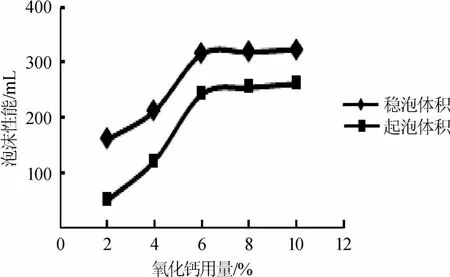
图2 氧化钙用量对蛋白液泡沫性能的影响Fig.2 Effect o f calcium oxide addition on foam properties o f protein solution
2.1.4 固液比对蛋白发泡剂发泡性能的影响
固液比对蛋白发泡剂泡沫性能的影响结果如图3所示。

图3 固液比对蛋白液泡沫性能的影响Fig.3 Effect of solid-liquid ratio on foam properties of protein solution
由图3可知,随着固液比在1∶4~1∶7(g∶m L)范围内增加,其蛋白发泡剂的起泡体积缓慢降低,稳泡体积缓慢增加,然而浓缩时间的增长会增加生产过程中所需的热能、增加生产成本。而且当固液比为1∶3(g∶m L)时,由于加水量较小而不能充分反应,本实验不予不考虑。因此,综合考虑固液比对蛋白发泡剂的泡沫性能的影响及对经济效益和生产成本的影响,固液比选用1∶4(g∶m L)为宜,此时蛋白发泡剂的起泡体积为325m L,稳泡体积为245m L。
2.1.5 水解温度及水解时间对泡沫性能的影响
水解温度和水解时间对蛋白发泡剂泡沫性能的影响结果如图4所示。
由图4A可知,随着水解温度在60~140℃范围内升高,其起泡体积和稳泡体积逐渐增加,水解温度>120℃后逐渐趋于平缓。然而,升高温度无疑造成更大的能耗。因此,选择水解时的最适温度为120℃,此时起泡体积为315m L,稳泡体积为240m L。由图4B可知,在水解时间为1~6 h范围内,蛋白液的泡沫性能随着水解时间的增加先升高后降低;当水解时间为3h时,蛋白液的起泡体积和稳泡体积最大此时蛋白发泡剂的起泡体积为315m L,稳泡体积为245m L;当水解时间>3h之后,蛋白液的泡沫性能逐渐减小。因此,本实验中选择最适水解时间为3 h,此时蛋白液的起泡体积为315m L,稳泡体积为245m L。

图4 水解温度(A)及水解时间(B)对蛋白液泡沫性能的影响Fig.4 Effect of hydrolysis temperature(A)and time(B)on foam properties of protein solution
2.2 蛋白发泡剂制备条件优化
2.2.1 脱钙对蛋白液泡沫性能的影响
脱钙对蛋白发泡剂的泡沫性能的影响结果如图5所示。
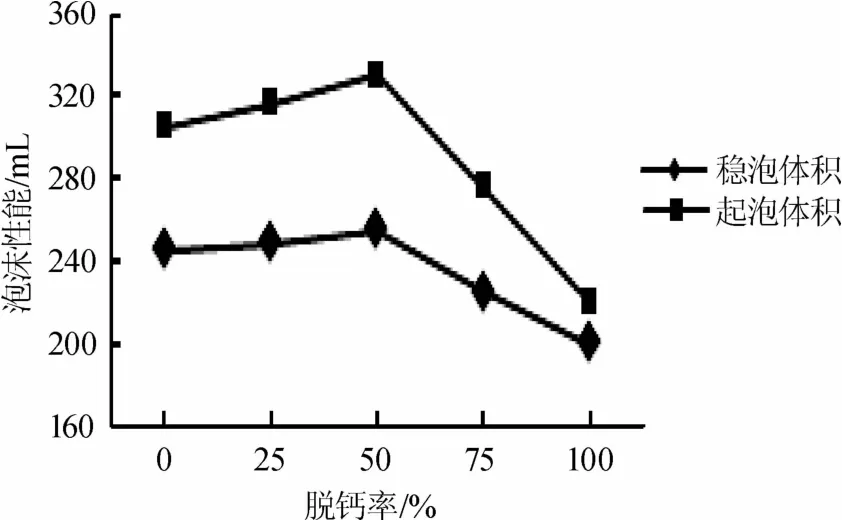
图5 脱钙对蛋白液泡沫性能的影响Fig.5 Effect of decalcification on foam properties of protein solution
由图5可知,随着脱钙率在0~100%范围内的增大,制备出的蛋白液的泡沫性能先增大再减小;当脱钙率为50%时,蛋白液的起泡体积和稳泡体积达到最大,此时蛋白发泡剂的起泡体积为330m L,稳泡体积为255m L;当脱钙率>50%时,蛋白液的起泡体积和稳泡体积随之减少。这可能是因为脱钙时加入了碳酸钠,溶液中引入了较多的钠离子,而高浓度的盐会影响可溶性蛋白的含量,蛋白液的泡沫性能又与蛋白液中的可溶性蛋白有关,因此钠离子的含量过多时,会对蛋白液的泡沫性能造成不利影响。因此,可以根据所需的蛋白液的泡沫性能进行适当的脱钙。因此,选择脱钙率为50%。
2.2.2 浓缩温度对蛋白液泡沫性能的影响
浓缩温度对蛋白发泡剂泡沫性能的影响结果如图6所示。
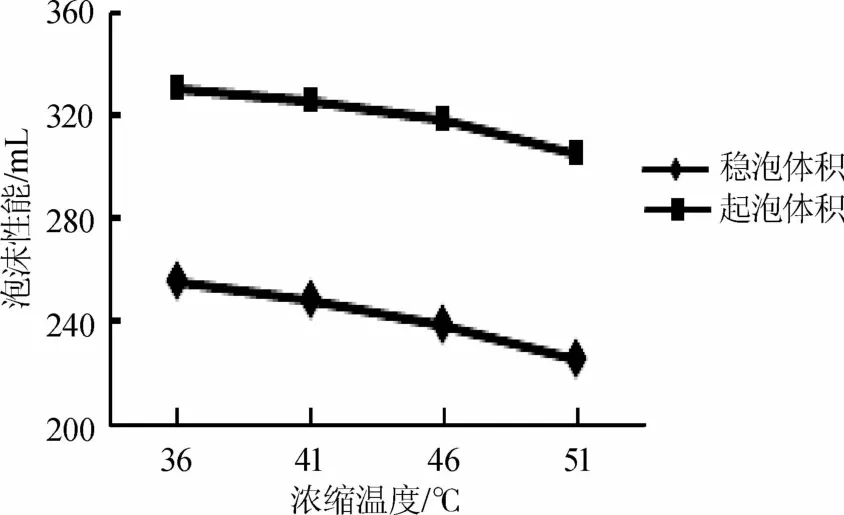
图6 浓缩温度对蛋白液泡沫性能的影响Fig.6 Effect o f concentration tem perature on foam properties of p rotein so lution
由图6可知,随着浓缩温度在36~51℃范围内升高,制备出的蛋白液的起泡体积和稳泡体积均下降,并且在实验中观察到当浓缩温度为36℃时,水解液在浓缩的过程中几乎不会起泡沸腾;当温度继续升高时,水解液在浓缩过程中开始有起泡沸腾现象,当浓缩温度为51℃时,水解液在浓缩过程中会有大量泡沫产生,而这些泡沫可能是由蛋白等活性物质产生的,由此可见,浓缩温度的升高会降低蛋白液的泡沫性能。虽然浓缩温度越高所需的浓缩时间越短,但是随着浓缩温度的提高,制备出的蛋白液的泡沫性能也会降低。因此,浓缩温度仍选择36℃为宜,此时蛋白发泡剂的起泡体积为330m L,稳泡体积为255m L。
2.2.3 蛋白含量对蛋白液泡沫性能的影响
蛋白含量对蛋白发泡剂泡沫性能的影响结果如图7所示。

图7 蛋白含量对蛋白液泡沫性能的影响Fig.7 Effect of protein content on foam properties of p rotein so lution
由图7可知,蛋白液中蛋白含量为3%~12%时,起泡体积和稳泡体积都有所上升,然而上升的幅度都很小。泡沫性能提高的原因主要可能有:(1)浓缩液中蛋白含量的增多会降低泡沫液膜的表面张力、提高表面强度和表面弹性,增加了泡沫的抗冲击的能力,从而提高了泡沫的稳定性;(2)随着蛋白含量的提高,在冲击作用下所产生的泡沫量会增大,也就是说泡沫的质量会增加,而泡沫质量的提高会使气泡的半径减小、排液的速度减慢,从而提高泡沫的稳定性。因此,蛋白液中的蛋白含量选3%为宜,此时蛋白液的起泡体积为329m L,稳泡体积为249m L。
2.2.4 添加剂对蛋白液泡沫性能的影响
添加剂对蛋白发泡剂泡沫性能的影响结果如图8所示。
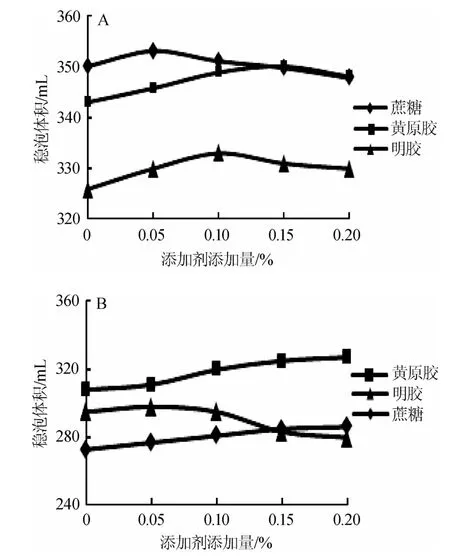
图8 添加剂及其添加量对蛋白液起泡体积(A)及稳泡体积(B)的影响Fig.8 Effect of additives and their addition on foam ing volume(A) and foam volum e(B)of p rotein so lution
由图8可知,当添加相同量的添加剂时,以蔗糖为添加剂所得的蛋白发泡剂起泡体积较大,稳泡体积最小;而以黄原胶为添加剂所得的蛋白液起泡体积较大,而稳泡体积最大;以明胶为添加剂时,起泡体积最小,而稳泡体积居中,因此本实验选择的添加剂为黄原胶。以黄原胶为添加剂时,随着添加量在0~0.20%范围内逐渐增加,起泡体积在添加量为0.15%时达到最大,此时气泡体积为350m L,添加剂添加量>0.15%后趋于平缓,而稳泡体积逐渐增加。因此,选择的黄原胶添加量为0.15%,此时蛋白发泡剂的起泡体积为350m L,稳泡体积为324.9m L。
3 结论
本实验以蛋白发泡剂的发泡性能为评价指标来优化白酒丢糟的水解条件和蛋白发泡剂的制备条件,确定最适的水解条件为:选用氧化钙和氢氧化钠组成的复合水解剂,其中氧化钙用量为丢糟质量的6%,并添加氢氧化钠使得pH值为12.5,固液比为1∶4(g∶m L),水解温度120℃和时间3 h。此外蛋白发泡剂最佳制备条件为:脱钙率50%,浓缩前后蛋白液的pH值均为7,浓缩温度和蛋白含量分别为36℃和3%,黄原胶添加量为0.15%。在此最佳条件下,最终得到蛋白发泡剂起泡体积为330m L,稳泡体积为255m L。
[1]胡涛,钟世云.混凝土蛋白质发泡剂改性研究[J].粉煤灰综合利用,2016(5):41-44.
[2]MARTINEZK D,FARIASM E,AMRP.Effectsof soy protein hydrolysisand polysaccharidesaddition on foaming properties studied by cluster analysis[J].Food Hydrocolloid,2011,25(7):1667-1676.
[3]LOMOLINO G,VINCENZIS,GAZZOLA D,et al.Foaming properties of potato(Solanum tuberosum)proteins:A study by the gas sparging method[J].Colloid Surface A,2015,475(1):75-83.
[4]孙萌,陈巧志.低密度泡沫混凝土发泡剂的研究[J].城市道桥与防洪,2014(6):297-299.
[5]姜松,王路明,冯扣宝.混凝土用蛋白质发泡剂的复配改性研究[J].功能材料,2015(9):9056-9061.
[6]毕波.利用酒糟生产蛋白泡沫灭火剂的研究[J].消防科学与技术,2014,33(1):92-95.
[7]何越,潘来东.一种植物蛋白泡沫灭火剂:CN104984508A[P].2015-10-20.
[8]宋书玉.中国酒业协会白酒分会、市场专业委员会2013年工作报告[J].酿酒科技,2014(6):1-9.
[9]谢正军,曹镜明,万建华.白酒糟饲用价值分析与应用探讨[J].饲料工业,2014,35(12):51-53.
[10]欧阳云凤.剩余活性污泥水解工艺的研究[D].天津:天津大学,2008. [11]邓塔,李军生,阎柳娟,等.可溶性丝蛋白的制备及性能研究[J].日用化学工业,2013,43(2):114-118.
[12]郑浩.污泥蛋白发泡剂的制备与泡沫性能研究[D].天津:天津大学,2010.
[13]于淼,任保增.油田发泡剂的稳定性能改良的研究[J].河南化工,2012(17):43-44.
[14]中华人民共和国国家质量监督检验总局,中国国家标准委员会.GB/T 19281—2014碳酸钙分析方法[S].北京:中国标准出版社,2014.
[15]中华人民共和国国家质量监督检验总局,中国国家标准委员会.GB 5009.5—2010食品安全国家标准食品中蛋白质的测定[S].北京:中国标准出版社,2010.
[16]中华人民共和国国家质量监督检验总局,中国国家标准委员会.GB/T 13173—2008表面活性剂洗涤剂试验方法[S].北京:中国标准出版社,2008.
[17]岳秀伟,张卫江,徐娇,等.污泥微生物蛋白发泡剂的改性[J].化工进展,2011,30(6):1316-1319.
Preparation of protein foam ing agentby Baijiu vinasse
WANG Yupeng,ZHAO Hua*
(College ofBiotechnology,Tianjin University ofScience&Technology,Tianjin 300457,China)
The protein foaming agentwas prepared by Baijiu vinasse.Using the foamability as evaluation index,the hydrolysis conditions of Baijiu vinasseand preparation conditionsof protein foaming agentwereoptimized.Theoptimum hydrolysis conditionswere determined as follows:calcium oxide and sodium hydroxide as compound hydrolysis agent,calcium oxide addition 6%of Baijiu vinassemass,and pH 12.5 adjusted by sodium hydroxide,solid-liquid ratio 1∶4(g∶m l),temperature 120℃and time3 h.Theoptimum preparation conditionsof protein foam ing agentwere decalcification rate 50%,the pH of the protein solution(beforeand after concentration)7,concentration temperature 36℃,protein concentration 3%,xanthan gum addition 0.15%.Under the optimum conditions,the foaming volume and foam volume of protein foam ing agentwere 330 m l and 255 m l, respectively.
Baijiu vinasse;protein foam ing agent;foam ing volume;foam volume
TS261.9
0254-5071(2017)08-0085-05
10.11882/j.issn.0254-5071.2017.08.019
2017-03-29
王宇鹏(1994-),男,硕士研究生,研究方向为现代酿造技术。
*通讯作者:赵华(1963-),男,教授,博士,研究方向为现代酿造技术。

