磁性壳聚糖糖用澄清剂的制备及结构表征
范松林,张佳欣,宋小荣,梁欣泉
(广西大学 轻工与食品工程学院,南宁 530004)
磁性壳聚糖糖用澄清剂的制备及结构表征
范松林,张佳欣,宋小荣,梁欣泉*
(广西大学 轻工与食品工程学院,南宁 530004)
以壳聚糖(CTS)为原料,通过化学共沉淀一步法制备出磁性壳聚糖(MCTS),以取代糖业传统澄清剂SO2。用该产物澄清糖厂甘蔗汁,并以清汁脱色率和纯度差为评价指标,通过单因素实验与正交实验优化制备工艺条件,利用扫描电镜(SEM)、傅里叶红外变换光谱仪(FT-IR)、X射线衍射仪(XRD)和振动样品磁强计(VSM)对其进行结构表征及性能分析。实验结果表明:在NaOH质量分数为20%、戊二醛质量分数为1%、交联时间为2 h及壳聚糖的添加量为1.25 g的条件下,所制备出的磁性壳聚糖的澄清效果最好,脱色率可达55.55%,纯度差可达2.80%。通过与糖厂传统澄清剂SO2的澄清效果进行比较,认为可以用磁性壳聚糖取代SO2应用于甘蔗汁的澄清过程。
磁性壳聚糖;蔗汁;脱色率;纯度差
我国的甘蔗糖厂绝大部分都使用亚硫酸法制糖,其中主要以糖业传统的澄清剂SO2对蔗汁进行脱色和澄清处理,但是用该方式所产白糖存在残硫量高的问题,近年来许多国家对白糖残硫量进行了更为严格的监控及检测,这对中国的制糖企业造成了一定的冲击。因此,寻求一种新型的糖用澄清剂以取代SO2已成为制糖行业科研工作者的研究热点[1-4]。
磁性壳聚糖是将壳聚糖与磁性粒子结合而成的一种新型高分子物质,具有尺寸粒径小、表面积大、吸附性能强等优良特性。在外加磁场的作用下可快速地分离与移动,该物质还含有大量的氨基和羟基活性基团,可吸附分离金属离子、蛋白质、明胶及多酚等物质,广泛应用于食品、生物医疗、化学工业等领域[5-7],但将其应用于蔗汁的澄清处理却未见报道。
本文采用化学共沉淀一步法制备出磁性壳聚糖[8],并用该产物对甘蔗混合汁进行澄清处理,以清汁的脱色率和纯度差作为评价指标,通过单因素实验与正交实验优化制备工艺条件,开发出适合于糖厂甘蔗汁澄清处理的澄清剂。利用其具有的氨基和羟基活性基团吸附去除蔗汁中胶体、蛋白质、酚类等非糖成分,为探索出无硫糖的生产提供实践与理论依据。同时采用扫描电镜(SEM)、X射线衍射仪(XRD)、傅里叶红外变换光谱仪(FT-IR)对其进行结构表征及性能分析[9]。
1 材料与方法
1.1 材料、试剂与仪器
1.1.1 材料与试剂
壳聚糖(AR);甘蔗混合汁(购于广西南宁明阳糖厂,过200目筛网待用);亚硫酸(AR)、絮凝剂PAM(日本T1150)、氯化铁(AR)、硫酸亚铁(AR)、戊二醛(AR)等;其余所用试剂均为分析纯。
1.1.2 主要仪器
数字式阿贝折光仪 日本ATAGO公司;WZZ-T2自动旋光仪 上海精密科学仪器有限公司;岛津UV-2501PC紫外分光光度计 日本岛津公司;S-3400N扫描电镜 日本日立公司;FT-IR傅里叶红外光谱仪 美国赛默飞世尔公司;DX-2700A-X射线衍射仪 丹东浩元仪器有限公司。
1.2 磁性壳聚糖的制备
配制50 mL 2%的乙酸溶液,使用电子天平准确称量一定量的壳聚糖,将上述壳聚糖溶解于装有50 mL配制好的乙酸溶液的250 mL三角瓶中,并将其置于60 ℃的震荡水浴锅中使其完全溶解。随后加入4 g FeCl3·6H2O和3 g FeSO4·7H2O,并且FeSO4·7H2O稍微过量,目的是防止FeSO4·7H2O被氧化,机械搅拌30 min。将上述溶液滴加到90 mL一定质量分数的NaOH溶液中,置于加热磁力搅拌器在温度为50 ℃的条件下搅拌1 h。随后加入75 mL一定质量分数的戊二醛溶液中,交联反应1~3 h,产物最后经蒸馏水、乙醇洗涤各3次,用磁铁收集产物于70 ℃下真空干燥,研磨成粉待用。
1.3 磁性壳聚糖的制备工艺实验
1.3.1 制备工艺单因素实验
通过单因素实验考察NaOH的质量分数、戊二醛的质量分数、交联反应的时间及壳聚糖的添加量等因素在适宜的范围内制备磁性壳聚糖,将所制备出的产物对甘蔗混合汁进行澄清处理,并以澄清后清汁的脱色率(ΔIU)和纯度差(ΔG.P)为评定指标,以此来评定磁性壳聚糖的最佳制备工艺条件。
1.3.2 制备工艺条件的优化
在单因素实验的基础上,采用L9(34)四因素三水平进行正交实验[10],并以磁性壳聚糖对甘蔗混合汁澄清的脱色率和纯度差为评价指标,优化磁性壳聚糖的制备工艺条件,因素水平表见表1。

表1 正交实验因素水平表Table 1 Factors and levels of orthogonal test
1.4 磁性壳聚糖对甘蔗混合汁的澄清实验
取250 mL混合汁于300 mL三角瓶中,添加磷酸300 mg/L,石灰乳调节pH为7.0±0.2,第1次加热到60 ℃,取30%的蔗汁机械制泡10 s,蔗汁混合后添加一定量的磁性壳聚糖微粒,摇匀,加入PAM 3 mg/L,摇匀后,置于90 ℃的恒温水浴锅中保温上浮25 min,过滤得到清汁,进行实验指标分析。
1.5 纯度、色值的测定与计算
甘蔗混合汁与清汁的重力纯度、色值的测定与计算参照文献[11]。
纯度差的计算:
ΔG.P=清汁的重力纯度-混合汁的重力纯度。
脱色率的计算:
脱色率=(IU混合汁-IU清汁)/IU混合汁×100%。
1.6 电镜扫描(SEM)分析
用扫描电镜对磁性壳聚糖和壳聚糖进行表面形貌扫描,观测两者表面形貌情况。
1.7 傅里叶红外光谱分析
将磁性壳聚糖和壳聚糖样品进行FT-IR扫描分析。
1.8 X射线衍射分析
采用X射线衍射仪(XRD)对Fe3O4和磁性壳聚糖进行晶型结构的分析。
1.9 磁性能分析
采用振动样品磁强计(VSM)进行磁性能分析。
2 结果与讨论
2.1 磁性壳聚糖制备工艺单因素实验
采用化学共沉淀一步法制备磁性壳聚糖是采用液相壳聚糖与液相磁核物质直接进行沉淀反应,可以避免或减轻产品团聚、产品微粒不均匀、表面活性剂难清除等缺陷。因此,本研究采用化学共沉淀一步法制备磁性壳聚糖,通过考察NaOH质量分数、交联剂戊二醛质量分数、交联时间与壳聚糖用量4个因素在适宜范围内,制备出的磁性壳聚糖对甘蔗混合汁的纯度和色值的影响为评定指标,以此优化制备工艺条件。
2.1.1 NaOH质量分数对蔗汁的脱色率和纯度差的影响
固定壳聚糖的用量0.75 g,戊二醛的质量分数1%,交联时间2 h,考察NaOH的质量分数分别为15%,20%,25%,30%,35%时对实验产生的影响,实验结果见图1。

图1 NaOH质量分数对脱色率和纯度差的影响Fig.1 Effect of sodium hydroxide mass fraction on decolourization ratios and purity differences
2.1.2 戊二醛质量分数对蔗汁的脱色率和纯度差的影响
固定壳聚糖的用量0.75 g,NaOH的质量分数20%,交联时间2 h,考察戊二醛的质量分数分别为0.5%,1%,1.5%,2%,2.5%时对实验产生的影响,实验结果见图2。

图2 戊二醛质量分数对脱色率和纯度差的影响Fig.2 Effect of glutaraldehyde mass fraction on decolourization ratios and purity differences
由图2可知,在戊二醛的质量分数为0.5%~2.5%,蔗汁的脱色率先降低后略微升高,最低值达41.16%,当戊二醛的质量分数为0.5%时,此时蔗汁的脱色率最高,可达50.02%; 而蔗汁纯度差随着戊二醛质量分数的变化呈现波动式的变化,当戊二醛的质量分数为1%时,纯度差达到最大值,为3.27%,此时的脱色率为46.53%,脱色效果较好。因此,选定戊二醛的质量分数为1%作为后续单因素的试验水平。
2.1.3 交联时间对蔗汁的脱色率和纯度差的影响
固定壳聚糖的用量1 g,NaOH的质量分数20%,戊二醛的质量分数1%,考察交联时间分别为1,1.5,2,2.5,3 h时对实验产生的影响,实验结果见图3。

图3 交联时间对脱色率和纯度差的影响Fig.3 Effect of crosslinking time on decolourization ratios and purity differences
由图3可知,交联时间在1~3 h的范围内时,蔗汁的脱色率呈现波动式的变化;交联时间为1.5 h时,脱色率为最高值,可达57.91%;交联时间为2 h时,脱色率最低,为44.63%;当交联时间为1.5 h时,纯度差为最大值,可达3.25%,此时的脱色率也为最优值,综合生成效率问题,选定1.5 h作为后续单因素实验的最佳水平。
2.1.4 壳聚糖用量对蔗汁的脱色率和纯度差的影响
固定NaOH的质量分数20%,交联时间1.5 h,戊二醛的质量分数1%,考察壳聚糖的用量分别为0.5,0.75,1,1.25,1.5 g时对实验产生的影响,实验结果见图4。
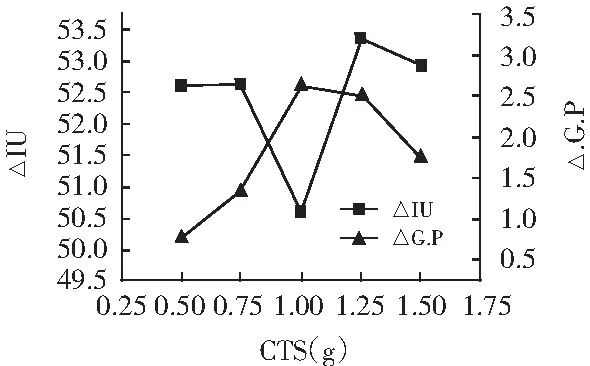
图4 壳聚糖质量对脱色率和纯度差的影响Fig.4 Effect of chitosan mass on decolourization ratios and purity differences
由图4可知,壳聚糖的质量为0.5~1.5 g时,蔗汁的脱色率总体上变化不大,最低值为50.63%,最高值为53.35%;纯度差的变化较为明显,当壳聚糖的添加量为1 g时,纯度差可达最大值,为2.64%,此时的脱色率为50.63%,脱色效果较好。
近年来,随着政策的出台和制度的完善,大同市农业科技推广取得了长足的发展。在优化农业生产格局,提升农业经济发展水平,带动区域经济发展等方面具有显著的作用。就整体而言,其发展趋势表现在以下几个方面。
2.2 磁性壳聚糖制备工艺条件的优化
在单因素实验的基础上,采用L9(34)四因素三水平进行正交实验,并以磁性壳聚糖对甘蔗混合汁澄清的脱色率和纯度差为评价指标,优化磁性壳聚糖的制备工艺条件,进而确定最佳工艺参数,结果见表2。

表2 正交实验结果Table 2 Results of orthogonal experiments
由表2极差分析结果可知,影响磁性壳聚糖澄清甘蔗混合汁脱色率的因素主次顺序为C>B>A=D,其最佳工艺条件是A3B1C3D2;影响纯度差的因素主次顺序是C>D>A>B,其最佳工艺条件是A2B2C3D3。

表3 脱色率正交实验结果方差分析Table 3 The variance analysis result of decolorization ratio orthogonal experiment

表4 纯度差正交实验结果方差分析Table 4 The variance analysis result of purity difference orthogonal experiment
由表3和表4方差分析结果可知,F均小于F临界值,所以4个因素对脱色率和纯度差的影响均不显著。
2.3 验证实验
将正交实验结果得出的最佳组合条件A3B1C3D2,A2B2C3D3和传统亚硫酸法工艺分别进行3次平行试验,试验结果见表5。
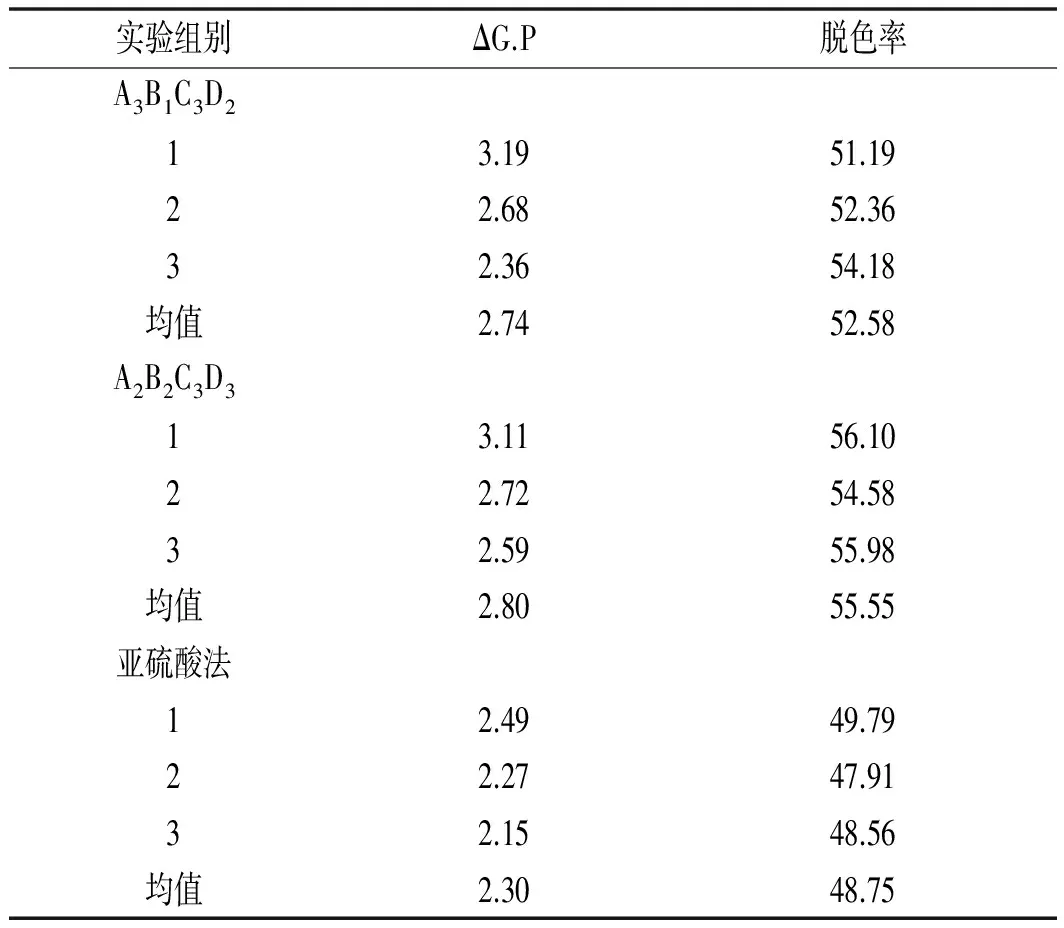
表5 平行试验结果Table 5 Parallel test results %
由表5可知,通过3次平行试验,A2B2C3D3的脱色率和纯度差分别为55.55%,2.80%,均高于A3B1C3D2和传统的亚硫酸法工艺。因此,可以采用A2B2C3D3即NaOH质量分数为20%、戊二醛质量分数为1%、交联时间为2 h及壳聚糖的添加量为1.25 g制备工艺生产磁性壳聚糖,用以替代传统的亚硫酸法澄清工艺。
2.4 壳聚糖和磁性壳聚糖的电镜扫描(SEM)表征分析
壳聚糖和磁性壳聚糖的电镜扫描图见图5。

图5 壳聚糖和磁性壳聚糖的电镜扫描(SEM)图(×6800)Fig.5 SEM photograph of chitosan and magnetic chitosan(×6800)
由图5可知,采用化学共沉淀一步法制备出的磁性壳聚糖表面具有非常独特的类蜂窝多孔状结构,孔径直径大约2 μm,与表面较为光滑的壳聚糖相比,磁性壳聚糖具有更好的吸附蔗汁中的大分子有机物(多酚、果胶、蛋白质)的性能,进而具有更好的澄清效果。
2.5 磁性壳聚糖和壳聚糖的傅里叶红外光谱的表征分析
傅里叶表征结果见图6。

图6 壳聚糖(a)、磁性壳聚糖(b)、Fe3O4 (c)傅里叶红外光谱图Fig.6 FT-IR pattern of chitosan a,magnetic chitosan b and Fe3O4 c
由图6可知,在4000~500 cm-1的范围内,壳聚糖和磁性壳聚糖的吸收峰比较接近,但也存在一些差异。由图6(a)可知,在3436 cm-1处有较宽的吸收峰是由于壳聚糖中含有的-OH和-NH2的伸缩振动引起的,在1656 cm-1和1367 cm-1分别对应着N-H和C-OH的伸缩振动。由图6(c)可知,在576 cm-1附近有着非常明显的吸收峰,这与Fe3O4在580 cm-1的Fe-O键的吸收峰吻合。而图6(b)的吸收峰位置与a,c均有较大的重合性,此外,在1630 cm-1处有较宽的吸收峰是由于戊二醛的交联作用生成新的亚胺键(N=C)引起的振动。因此,可以证明制备出的物质为具有壳聚糖和Fe3O4特性的磁性壳聚糖。
2.6 X射线衍射分析
磁性壳聚糖和Fe3O4的X射线衍射图,见图7。

图7 Fe3O4(a)和MCTS(b)的X射线衍射图Fig.7 XRD pattern of Fe3O4(a)and MCTS(b)
由图7可知,磁性壳聚糖(b)在30.72,35.38,43.72,53.64,57.24,62.86处均出现了与图7中Fe3O4(a)中一致的衍射峰,分别对应立方相 Fe3O4中的晶体(220),(311),(400),(422),(511),(440)上的晶面,这与参考文献[12]基本一致,说明在制备过程中并未改变 Fe3O4的晶型结构。
2.7 磁性能分析
磁性壳聚糖的磁性能分析图见图8。

图8 MCTS的磁滞回线图Fig.8 The magnetic hysteresis chart of MCTS
由图8可知,曲线呈S型,并且通过原点,这说明矫顽力和剩余磁场强度都接近零,无剩磁产生,由此说明所制备出的MCTS具有超顺磁性,饱和磁场强度为43.4 emu/g。
3 结论
以壳聚糖为原料、戊二醛为交联剂,采用化学共沉淀一步法制备磁性壳聚糖的最佳工艺条件是:NaOH质量分数为20%、戊二醛质量分数为1%、交联时间为2 h及壳聚糖的添加量为1.25 g,此时甘蔗混合汁的脱色率和纯度差分别可达55.55%,2.80%;通过对比亚硫酸法的澄清生产工艺实验,认为磁性壳聚糖可以取代SO2作为糖用澄清剂。
将制备出的样品利用SEM,FT-IR,XRD和VSM表征分析,结果发现:磁性壳聚糖具有独特的类蜂窝多孔状结构,磁核物质是Fe3O4,使用交联剂戊二醛,使得磁核和壳聚糖成功地交联在一起,磁性微粒具有超顺磁性,饱和磁场强度可达43.4 emu/g。本研究为探索无硫澄清工艺提供了新的理论和实践依据。
[1]何惠欢,谢志荣,刘继栋,等.羧甲基壳聚糖糖用澄清剂的制备及结构表征[J].食品工业科技,2015(6):117-121.
[2]Laksameethanasana P,Somla N,Janprem S,et al.Clarification of sugarcane juice for syrup production[J].Procedia Engineering,2012,32:141-147.
[3]Saha N K,Balakrishnan M,Ulbricht M.Fouling control in sugarcane juice ultrafiltration with surface modified polysulfone and polyethersulfone membranes[J].Desalination,2009,249(3):1124-1131.
[4]梁欣泉,何惠欢,谢志荣,等.季铵化壳聚糖糖用澄清剂的制备及结构表征[J].广西大学学报(自然科学版),2014(3):544-551.
[5]Fan L,Li M,Lv Z,et al.Fabrication of magnetic chitosan nanoparticles grafted with β-cyclodextrin as effective adsorbents toward hydroquinol[J].Colloids and Surfaces B: Biointerfaces,2012,95:42-49.
[6]Li L,Fan L,Sun M,et al.Adsorbent for chromium removal based on graphene oxide functionalized with magnetic cyclodextrin-chitosan[J].Colloids and Surfaces B:Biointerfaces,2013,107:76-83.
[7]范松林,任勤,张佳欣,等.磁性壳聚糖微球在食品工业中的应用研究进展[J].食品工业,2017(2):249-253.
[8]Wang P,Ma Q,Hu D,et al.Removal of Reactive Blue 21 onto magnetic chitosan microparticles functionalized with polyamidoamine dendrimers[J].Reactive and Functional Polymers,2015,91-92:43-50.
[9]Funes A,de Vicente J,de Vicente I.Synthesis and characterization of magnetic chitosan microspheres as low-density and low-biotoxicity adsorbents for lake restoration[J].Chemosphere,2017,171:571-579.
[10]李利华.正交试验法优化超声辅助提取大蒜多糖工艺[J].中国调味品,2014,39(7):70-73.
[11]李墉,郑长庚.甘蔗制糖化学管理分析方法[M].广州:中国轻工总会甘蔗糖业质量监督检测中心,1995.
[12]王鹏.磁性壳聚糖基复合微粒的制备及对两种阴离子染料的吸附性能研究[D].哈尔滨:东北林业大学,2015.
Preparation and Structural Characterization of MagneticChitosan as Sugarcane Juice Clarifying Agent
FAN Song-lin, ZHANG Jia-xin, SONG Xiao-rong, LIANG Xin-quan*
(College of Light Industry and Food Engineering, Guangxi University, Nanning 530004, China)
To prepare a new clarifying agent to replace traditional SO2in sugarcane industry, magnetic chitosan composite microparticles(MCTS) are prepared using a one-step chemical co-precipition method. The optimal preparation conditions of magnetic chitosan are evaluated by the decolourization ratio and the purity difference to sugarcane juice clarification, the process conditions are optimized by single factor experiment and orthogonal experiment and the product is analyzed by scanning electron microscope (SEM), fourier transform infrared spectrum (FT-IR), X-ray diffraction(XRD) and vibrating sample magnetometer. The results indicate that under the treatment of sodium hydroxide concentration of 20%, glutaraldehyde concentration of 1%, crosslinking time of 2 h and chitosan additive amount of 1.25 g, the product is proved to be magnetic chitosan with the best clarifying effect. The decolourization ratio and the purity differenc to sugarcane juice clarification are 55.55% and 2.80% respectively.Compared with the traditional sugar clarification agent effect, the results indicate that magnetic chitosan could replace SO2in sugarcane juice clarification.
magnetic chitosan;sugarcane juice;decolourization ratio;purity difference
2017-02-12 *通讯作者
糖蜜酒精精馏过程节能技术开发及应用示范(AE120094);广西区特色本科专业建设项目——食品科学与工程(制糖工程)
范松林(1992-),男,江西赣州人,硕士,研究方向:糖品过程强化理论与技术; 梁欣泉(1966-),男,广西南宁人,教授,博士,研究方向:糖品过程强化理论与技术。
TS202.3
A
10.3969/j.issn.1000-9973.2017.08.007
1000-9973(2017)08-0030-06

