壳聚糖活性污泥复合吸附剂处理铅、镉废水研究
赵佐平,段 敏,刘智峰,汤 波,同延安
(1.陕西理工大学化学与环境科学学院,陕西 汉中 723001;2.陕南秦巴山区生物资源综合开发协同创新中心,陕西 汉中 723001;3.西北农林科技大学资源环境学院,陕西 杨凌 712100)
壳聚糖活性污泥复合吸附剂处理铅、镉废水研究
赵佐平1,2,段 敏1,2,刘智峰1,2,汤 波1,2,同延安3①
(1.陕西理工大学化学与环境科学学院,陕西 汉中 723001;2.陕南秦巴山区生物资源综合开发协同创新中心,陕西 汉中 723001;3.西北农林科技大学资源环境学院,陕西 杨凌 712100)
研究了壳聚糖活性污泥复合吸附剂(SCTS)对废水中Pb2+和Cd2+的吸附性能,通过单因素试验分析了温度、SCTS投加量、pH值、搅拌转速和重金属离子浓度对SCTS吸附性能的影响,正交试验确定了影响因素的主次顺序及最优组合水平。结果表明:影响 SCTS 吸附废水中Pb2+的因素从大到小依次为 pH值、SCTS投加量、Pb2+初始浓度和搅拌转速,吸附 Pb2+的最优组合为 pH值=2、SCTS 投加量为10 g·L-1、ρ(Pb2+)初始值为50 mg·L-1、搅拌转速130 r·min-1,Pb2+去除率达95.76%。影响 SCTS 吸附废水中Cd2+的因素作用力大小依次为pH值、Cd2+初始浓度、转速和SCTS投加量,吸附Cd2+的最优组合为 pH值2、SCTS 投加量2.5 g·L-1、ρ(Cd2+)初始值60 mg·L-1、转速130 r·min-1,此时Cd2+的去除率为96.08%。
壳聚糖;复合吸附剂;镉;铅;废水;吸附
由于铅和镉被广泛应用于电镀等领域,已成为污水中的重要污染物,对人体健康和生态环境构成了严重威胁[1]。铅在自然界中难以转化,易在土壤及动植物体内累积,致人体急性或慢性中毒[2];镉能够牢固地累积在生物体内,导致肾功能衰竭、骨伤害、癌症和高血压等疾病的产生[3]。
目前,对含铅和镉废水的处理方法主要有:电解法、化学沉淀法、活性炭吸附法、离子交换法、生物吸附法、反渗透法、电渗析法等[3],但均具有处理量小、选择性差、易造成二次污染等缺点[4]。目前在剩余污泥资源化方面的研究报道较多[5]。王士龙等[6]研究表明,在废水pH值为4~9、ρ(Pb2+)≤100 mg·L-1时,投加活性污泥进行处理,Pb2+去除率达99%以上。彭立凤[7]研究发现,ρ(Cd2+)为20~40 mg·L-1时,在电解液中采用脱乙酰度为66%的壳聚糖,去除率达99.9%。敖晓奎等[8]研究表明,在活性污泥微生物细胞的表面含有大量羟基、羧基等基团,它们对重金属离子形成络合物有着非常重要的作用。由此可见,污泥对去除铅和镉有很好的效果,是一个具有可行性和发展前景的研究方向。
壳聚糖是甲壳素在脱乙酰化反应下得到的一种天然高分子有机物[9-10]。甲壳类动物的外壳和很多植物的细胞壁内都含有甲壳素,因而资源比较丰富,属于廉价易得的材料[11]。壳聚糖具有耐碱、耐腐蚀、无毒、无味以及对环境友好等特点[12],在其分子内含有大量氨基、羟基和氢键等[13],易与重金属离子形成比较稳定的螯合物[14],从而达到去除重金属离子的目的。使用壳聚糖处理重金属离子副作用较小且处理效果较好,故壳聚糖可以作为包埋固定活性污泥的载体以达到提高污泥细胞吸附重金属离子能力的目的[15]。笔者采用壳聚糖活性污泥复合吸附剂(SCTS)为载体,探寻其对废水中Pb2+和Cd2+的吸附性能,以期为城市污水厂剩余污泥的资源化利用和工业废水的处理提供理论基础。
1 材料与方法
1.1 主要试剂
壳聚糖(上海蓝季生物,RT)、活性污泥(取自陕西省汉中市污水处理厂)、冰乙酸(CH3COOH)、碳酸氢铵(NH4HCO3)、氢氧化钠(NaOH)、环氧氯丙烷(ECH)、硝酸铅〔Pb(NO3)2〕、硝酸(HNO3)、磷酸二氢钾(KH2PO4)、磷酸氢二钠(Na2HPO4)、硝酸镉〔Cd(NO3)2·4H2O〕、硫酸(H2SO4)和盐酸(HCl)。
1.2 主要仪器
SHB-Ⅲ循环水式多用真空泵、WGLL-230BE电热鼓风干燥箱、SHA-C水浴恒温振荡器、pH计、火焰原子吸收光谱仪(岛津AA-6880,日本)、电子天平。
1.3 壳聚糖活性污泥复合吸附剂(SCTS)的制备
(1)壳聚糖溶液的制备:称取3.0 g壳聚糖粉末,溶于体积分数为1%醋酸溶液中,配制成质量分数为3%的壳聚糖溶液。壳聚糖溶解时可在低温水浴锅里适当加热,加热过程中不断搅拌直到完全溶解,此时溶液呈现淡黄色且均匀透明,有一定黏度。
(2)试验污泥的制备:活性污泥取自陕西省汉中市污水处理厂,经淘洗除去脏杂物,再自配营养液在室温下培养,试验期间污泥性质稳定。污泥活性指标为:污泥沉降比VS30min=34%,污泥容积指数ISV=118 mL·g-1,混合液挥发性悬浮固体/混合液悬浮固体(MLVSS/MLSS)=0.71。使用时污泥经清水淘洗3次,抽滤浓缩,使得污泥干重占总质量的85%,试验活性污泥用量均以干重计。
(3)发泡剂的添加:称取1 g发泡剂NH4HCO3加入步骤(2)所得的泥浆中搅拌均匀。
(4)SCTS的制备:取适量的泥浆与壳聚糖均匀混合后,将其滴加到含有交联剂(环氧氯丙烷)的固化液NaOH溶液中,滴加过程中要不断地搅拌,一方面可以加快固化速度,另一方面可以防止吸附剂沉于烧杯底部。滴加完成后,将烧杯置于水浴锅中加热,加热过程中不断搅拌,将水温设置为45 ℃,交联4 h,最终获得SCTS固体小球[15]。
(5)复合吸附剂的干燥:将得到的固体小球用大量清水反复冲洗直至中性,再用纯水浸泡1 h。浸泡后将小球平铺于培养皿中,置于60 ℃条件下烘烤,烘干一段时间后称质量,再放在烘箱中烘,直至恒重;由于水分流失,吸附剂体积将会减小,此时将会得到粒径较小的复合吸附剂。烘干后将小球置于100 ℃环境中受热,使小球内部的发泡剂受热分解产生气体,从而得到带孔的复合吸附剂。
1.4 试验设计
1.4.1 壳聚糖活性污泥复合吸附剂(SCTS)吸附Pb2+和Cd2+单因素试验设计
(1)pH值对SCTS吸附Pb2+和Cd2+的影响
分别称取0.75和0.5 g SCTS 置于150 mL锥形瓶中,再分别取100 mL初始ρ(Pb2+)为 100 mg·L-1和ρ(Cd2+)为60 mg·L-1的溶液,调节 pH值分别为 2.0、3.0、4.0和5.0,温度40 ℃,转速 130 r·min-1,振荡吸附 20 h。
(2)初始浓度对SCTS吸附Pb2+和Cd2+的影响
分别称取0.75和0.5 g SCTS置于150 mL锥形瓶中,再分别取 100 mL初始ρ(Pb2+)分别为 10、50、100、150和200 mg·L-1和初始ρ(Cd2+)分别为 20、40、60、80和100 mg·L-1的溶液置于5组锥形瓶中,用缓冲溶液调节 pH 值为3.0,温度 40 ℃,转速130 r·min-1,振荡吸附20 h。
(3)温度对SCTS吸附Pb2+和Cd2+的影响
分别称取0.75和0.5 g SCTS置于150 mL锥形瓶中,再分别取100 mL初始ρ(Pb2+)为 100 mg·L-1和ρ(Cd2+)为60 mg·L-1的溶液,调节pH值为 3.0,设定温度分别为 30、40、50和60 ℃,转速130 r·min-1,振荡吸附 20 h。
(4)吸附剂投加量对SCTS吸附Pb2+和Cd2+的影响
分别取100 mL初始ρ(Pb2+)为 100 mg·L-1和ρ(Cd2+)为60 mg·L-1的溶液置于锥形瓶中,调节 pH值为 3.0,设定 SCTS 用量分别为 0.25、0.5、0.75、1.0、1.25 g,温度40 ℃,转速 130 r·min-1,振荡吸附 20 h。
(5)搅拌转速对SCTS吸附Pb2+和Cd2+的影响
称取 0.75和0.5 g SCTS置于150 mL锥形瓶中,分别取100 mL初始ρ(Pb2+)为 100 mg·L-1和ρ(Cd2+)为60 mg·L-1的溶液,调节 pH值为3.0,温度 40 ℃,转速分别设置为 110、130、150和170 r·min-1,振荡吸附 20 h。
1.4.2 正交试验
通过单因素试验结果分析,选择4个主要因素进行3水平的正交试验,确定4个因素对SCTS吸附废水中重金属离子能力的影响次序并给出最优水平组合。
1.5 吸附性能评价标准
用火焰原子吸收光谱仪测定处理后废水中Pb2+和Cd2+浓度,计算去除率。
(1)
(2)
式(1)~(2)中,ω为重金属离子的去除率,%;ρ0为溶液的初始浓度,mg·L-1;ρ为吸附后的溶液浓度,mg·L-1;q为吸附剂吸附量,mg·g-1;V0为溶液体积,100 mL;m为吸附剂质量,g。
2 结果与分析
2.1 不同因素对壳聚糖活性污泥复合吸附剂(SCTS)吸附废水中Pb2+和Cd2+的影响
2.1.1 pH值对SCTS吸附Pb2+和Cd2+的影响
pH值对壳聚糖和微生物细胞吸附重金属的影响较大[16-17]。改变溶液pH值,Pb2+和Cd2+的去除率如图1所示。当pH值在2~3之间时,去除率呈上升趋势,对Pb2+的去除率较高且均在80%以上,这与KATSUTOSHI等[18]用 EDTA 改性壳聚糖对重金属的吸附发生在pH值为0~2范围内的研究结果相一致。当pH值=3 时出现极大值,去除率高达 93.76%。而当pH值>3时,随着pH值的增大吸附率逐渐降低,然后稳定在82%~83%。
王林[19]研究发现在较低 pH值条件下,EDTA 改性壳聚糖(ETC)对水溶液中重金属Pb2+和Cd2+都有较好的吸附效果。pH值对Cd2+去除率的影响总体呈下降趋势。当pH值<3时,去除率小幅上升并稳定在93%~94%。当pH值=3 时出现极大值,去除率最高达到 94.32%。而当pH值>3时,去除率呈明显下降趋势。因而,pH值是影响SCTS吸附性能的主要因素之一。该试验pH值对SCTS吸附Pb2+和Cd2+的最佳试验条件均为3。
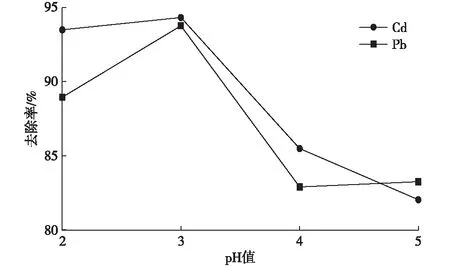
图1 pH值对吸附Pb2+和Cd2+的影响
2.1.2 初始浓度对SCTS吸附Pb2+和Cd2+的影响
重金属离子的初始浓度也是影响吸附的主要因素之一[20]。改变重金属离子初始浓度后Pb2+和Cd2+的去除率如表1所示。随着Pb2+初始浓度的增大,吸附量也增加,但是当ρ(Pb2+)>150 mg·L-1时吸附量的增长明显变缓。由图2可知,SCTS对Pb2+的去除率随着Pb2+初始浓度的增大呈下降趋势。当ρ(Pb2+)≤100 mg·L-1时去除率缓慢下降,而当ρ(Pb2+)≥150 mg·L-1时去除率明显下降,最低达53.61%。当ρ(Pb2+)为100 mg·L-1时,吸附量为9.93 mg·g-1,去除率达74.88%,此时为最佳去除浓度。
表1 初始浓度对SCTS吸附Pb2+和Cd2+的影响
Table 1 The influence of initial concentration of Pb2+and Cd2+on SCTS adsorption

重金属离子初始ρ/(mg·L-1)吸附量/(mg·g-1)最终ρ/(mg·L-1)去除率/%Pb2+101.0602.0779.34505.04012.2177.381009.93025.5274.8815013.82646.3069.1320014.29692.7853.61Cd2+203.0214.9075.52406.6226.8982.786010.1829.0984.858013.22113.9082.6310013.86930.6569.35

图2 初始浓度对吸附剂吸附Pb2+的影响
随着初始ρ(Cd2+)的增加,SCTS对Cd2+的吸附量也增加,但是当ρ(Cd2+)>80 mg·L-1时吸附量增长变缓。如图3所示,去除率随ρ(Cd2+)的增长呈阶梯性变化,ρ(Cd2+)≤40 mg·L-1时缓慢上升;而当40<ρ(Cd2+)<80 mg·L-1时较为稳定,维持在82%~84%之间;当ρ(Cd2+)≥80 mg·L-1时去除率迅速下降。这与处理含Pb2+废水结果相似。究其原因可能是因为重金属离子初始浓度增大,使其跟活性基团接触的概率增加,有利于对重金属离子的吸附,但是吸附剂的量是一定的,所以溶液中活性吸附位点也一定,当溶液中Pb2+、Cd2+与活性位点充分结合后,Pb2+和Cd2+的初始浓度越高,溶液中残留的越多,导致其去除率下降[20-22]。因此,该试验选择60 mg·L-1为Cd2+去除率的最佳浓度。
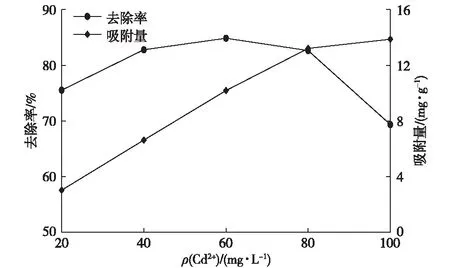
图3 初始浓度对吸附剂吸附Cd2+的影响
2.1.3 温度对SCTS吸附Pb2+和Cd2+的影响
温度不同对重金属的吸附效果也不一样[23]。改变温度,Pb2+和Cd2+的去除率如图4所示。在整个试验过程中Pb2+去除率一直保持在 87%~92%之间,随着温度的增加去除率上升,当温度为30~40 ℃ 时上升速度较快,40 ℃后上升速度缓慢。

图4 温度对吸附Pb2+和Cd2+的影响
Cd2+去除率一直保持在 87%~91%之间,随着温度的不断增加去除率缓慢上升,之后达到稳定。当温度为30~40 ℃时去除率上升速度较快,40 ℃后小幅下降,随即恢复平缓。因而,温度对SCTS吸附Pb2+和Cd2+的影响并不明显,这说明温度并不是影响SCTS吸附性能的主要因素。后续试验温度选取40 ℃。
2.1.4 SCTS投加量对其吸附Pb2+和Cd2+的影响
吸附剂的投加量一般要考虑经济效益,不仅要达到预期效果还要用量最省[16]。改变吸附剂的投加量,废水中重金属离子的去除率如图5所示。随着 SCTS 投加量的增加,Pb2+去除率也呈逐渐增加趋势。这是因为吸附剂投加量的增加导致反应体系中的活性基团数量增加,有更多的活性位点与重金属离子相结合,最终使得吸附剂对重金属离子的吸附率提高,这和王林[19]用 EDTA 改性壳聚糖吸附重金属离子的研究结果相一致。SCTS对Pb2+的吸附在投加量为2.5~7.5 g·L-1内增加迅速,随后趋于平稳,因此SCTS投加量选取7.5 g·L-1。
随着 SCTS 投加量的增加,Cd2+去除率呈阶梯性变化。当SCTS投加量为2.5~7.5 g·L-1时去除率大幅上升,之后去除率的变化有下降趋势,但趋于稳定,去除率在84%~87%之间。这同样可能是因为吸附剂投加量的增加导致反应体系中活性基团数量增加,有更多的活性位点与重金属离子相结合,使去除率提高。从经济角度出发,SCTS投加量在处理含Cd2+废水时选取5 g·L-1为宜。

图5 SCTS投加量对吸附Pb2+和Cd2+的影响
2.1.5 搅拌转速对SCTS吸附Pb2+和Cd2+的影响
李永明等[13]研究表明搅拌会对重金属离子的吸附产生影响。改变试验过程中的搅拌转速,废水中重金属离子的去除率如图6所示。
随着转速的增加,Pb2+去除率有一个明显的先升后降的过程。当转速<130 r·min-1时,去除率随着转速增大而缓慢上升,达到85%以上。在转速为130 r·min-1时出现极大值,去除率最高,达 94.93%。转速>130 r·min-1时去除率迅速下降。

图6 搅拌转速对吸附Pb2+和Cd2+的影响
搅拌转速对Cd2+去除率见图6。当转速较小时去除率缓慢上升,达84%以上。在转速为130 r·min-1时出现极大值,达95.51%。而当转速超过130 r·min-1时去除率缓慢下降并趋于稳定。这可能是由于转速增加提高了溶液中重金属离子与活性基团碰撞的机会,有利于吸附的进行,然而吸附固定在吸附剂表面的重金属离子Pb2+和Cd2+并非全都是牢固的,转速过高会导致Pb2+和Cd2+重新释放到溶液中,进而导致去除率降低。因而可以判定转速是影响SCTS吸附性能的主要因素之一。控制转速为130 r·min-1时效果最好。
2.2 SCTS吸附Pb2+和Cd2+的正交试验
2.2.1 SCTS吸附Pb2+的正交试验
根据各单因素试验结果,同时考虑到实际经济因素,分别取适当条件做4因素3水平正交试验,试验结果见表2~3。
表2 SCTS吸附Pb2+的正交试验设计及试验结果
Table 2 The orthogonal experiment design and test results of SCTS adsorption on Pb2+
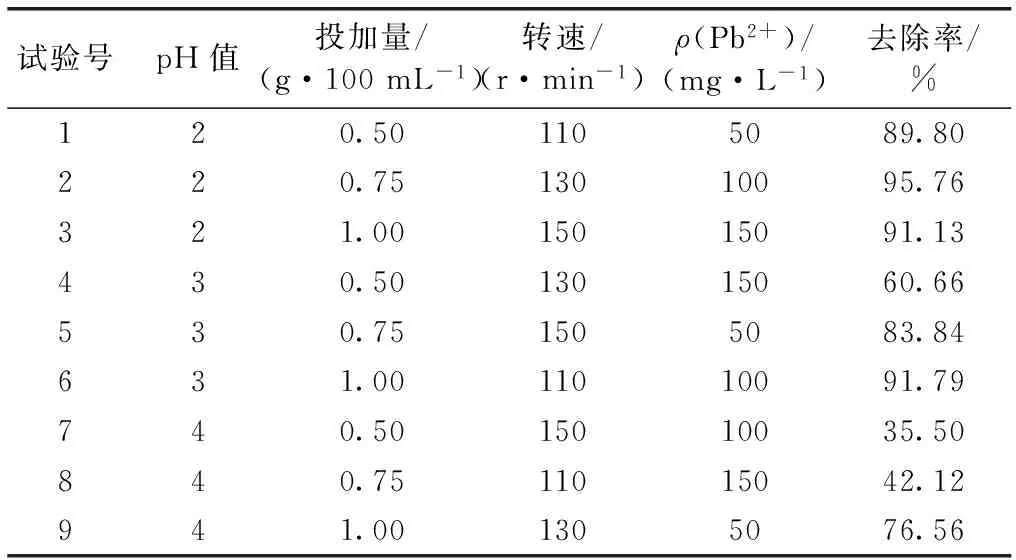
试验号pH值投加量/(g·100mL-1)转速/(r·min-1)ρ(Pb2+)/(mg·L-1)去除率/%120.501105089.80220.7513010095.76321.0015015091.13430.5013015060.66530.751505083.84631.0011010091.79740.5015010035.50840.7511015042.12941.001305076.56
表3 各因素对SCTS吸附Pb2+的正交试验结果极差分析
Table 3 The orthogonal test results and range analysis of SCTS adsorption on Pb2+
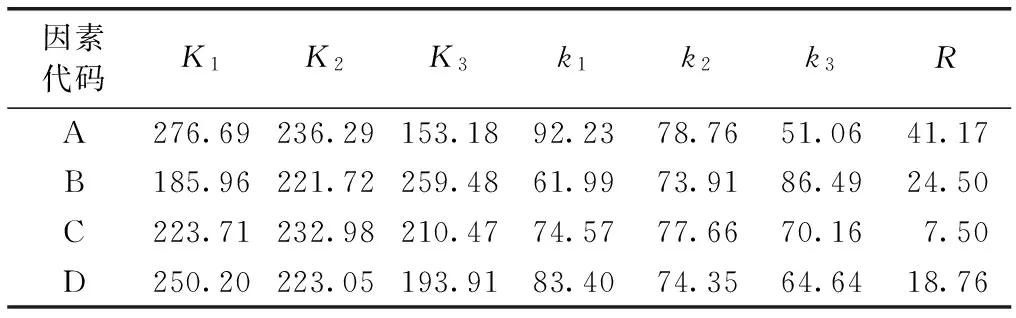
因素代码K1K2K3k1k2k3RA276.69236.29153.1892.2378.7651.0641.17B185.96221.72259.4861.9973.9186.4924.50C223.71232.98210.4774.5777.6670.167.50D250.20223.05193.9183.4074.3564.6418.76
K为因素试验结果之和;k为因素试验结果之和的均值。
以上研究证实了外界因素对SCTS吸附 Pb2+的过程存在着不同程度的影响,影响 SCTS 吸附的因素作用力大小依次为pH值、SCTS投加量、Pb2+初始浓度和转速。SCTS吸附Pb2+的最佳条件是pH值为2,SCTS投加量为10 g·L-1,转速为130 r·min-1,ρ(Pb2+)初始值为50 mg·L-1,此时Pb2+的去除率为95.76%。
2.2.2 SCTS吸附Cd2+的正交试验
根据各单因素试验结果,取适当条件做4因素3水平正交试验,试验结果见表4~5。
由表中极差项可知,影响SCTS吸附能力的因素作用力大小依次为pH值、Cd2+初始浓度、转速和SCTS投加量。其中,pH值的影响是最大的,是吸附的主要控制条件,Cd2+初始浓度、转速和投加量是次要控制条件。SCTS吸附Cd2+的最佳条件是 pH值为2,SCTS 投加量为2.5 g·L-1,ρ(Cd2+)为 60 mg·L-1,转速为130 r·min-1,Cd2+去除率为96.08%。
表4 SCTS吸附Cd2+正交设计及试验结果
Table 4 The orthogonal experiment design and test results of SCTS adsorption on Cd2+

试验号pH值投加量/(g·100mL-1)转速/(r·min-1)ρ(Pb2+)/(mg·L-1)去除率/%120.251104087.84220.501306096.08320.751508087.29430.251308075.72530.501504053.98630.751106077.78740.251506086.33840.501108074.39940.751304082.65
表5 各因素对SCTS吸附Cd2+的正交试验结果极差分析
Table 5 The orthogonal test results and range analysis of SCTS adsorption on Cd2+
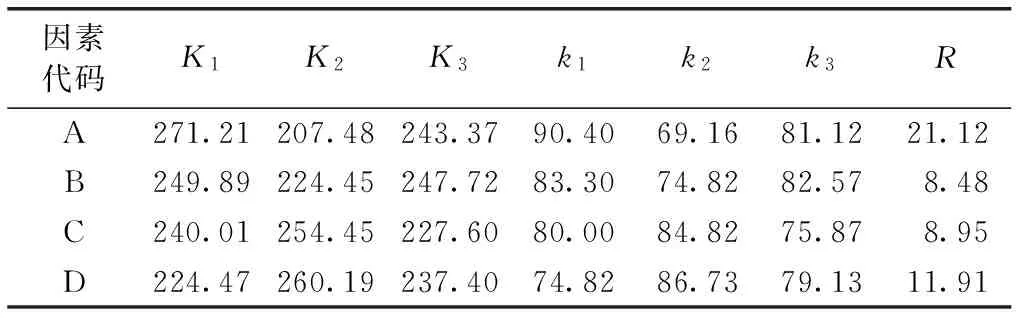
因素代码K1K2K3k1k2k3RA271.21207.48243.3790.4069.1681.1221.12B249.89224.45247.7283.3074.8282.578.48C240.01254.45227.6080.0084.8275.878.95D224.47260.19237.4074.8286.7379.1311.91
K为因素试验结果之和;k为因素试验结果之和的均值。
3 讨论
正交试验结果显示,不论是SCTS处理废水中Pb2+还是Cd2+,pH值是影响SCTS吸附重金属离子过程中最主要因素。ZHOU等[2]研究发现,pH值可以影响微生物分子的结构、表面特征和重金属离子在水中的存在形态。FABRIS等[16]发现,pH值会对壳聚糖和金属离子的络合产生影响。张艳雅等[23]研究表明,壳聚糖的糖残基上官能团的特殊结构使它们在一定的 pH 值条件下对具有一定离子半径的金属离子形成螯合作用。
重金属离子初始浓度、转速和SCTS投加量均显著影响其吸附能力。王菲等[5]研究表明,污泥对废水具有一定的处理效果,且可以得到很好的经济效益。王岚等[24]研究了用活性污泥制备的颗粒污泥对废水中铅的吸附,发现这种吸附剂对低浓度Pb2+的吸附平衡时间为 30 min。孙胜玲等[10]用从蚕蛹中提取的壳聚糖作为吸附剂,其对重金属Pb2+离子有良好的吸附效果,在壳聚糖脱乙酰度为55%、pH值为4~4.5的条件下,吸附率高达99%。程珊珊等[20]研究了壳聚糖对废水中Pb2+的吸附特性,在吸附时间为30 min、pH值为5~6、Pb2+浓度为10-4mol·L-1条件下,去除率达98%。但是这种由活性污泥或壳聚糖单独处理含铅、镉废水后,吸附剂无法回收再利用,从一定程度上增加了处理成本,故复合吸附剂的制备势在必行。向文英等[15]在0.4 g·L-1STPP 固化溶液、w为10%的NH4HCO4、污泥与壳聚糖用量比值0.5、发泡温度100 ℃条件下制得SCTS,处理ρ为10 mg·L-1的含铬废水,吸附率达97.3%。
综上所述,尽管处理废水中Pb2+和Cd2+的方法很多,但各方法或多或少存在着这样或那样的缺点[25],如果在提高SCTS吸附Pb2+和Cd2+等重金属离子吸附率的同时提高复合吸附剂的重复使用率,那么SCTS 处理含重金属离子废水将是一种较为理想的且有发展前景的方法之一[26]。
4 结论
(1)试验中制得的SCTS 吸附废水中Pb2+的影响因素作用力大小依次为 pH值、SCTS投加量、Pb2+初始浓度和搅拌转速,在废水pH值为2、SCTS 投加量为10 g·L-1、初始ρ(Pb2+)为 50 mg·L-1、搅拌转速130 r·min-1条件下,Pb2+去除率可达95.76%。
(2)SCTS 吸附废水中Cd2+的影响因素作用力大小依次为pH值、初始ρ(Cd2+)、搅拌转速和SCTS投加量,当含Cd2+废水pH值为2、SCTS 投加量为2.5 g·L-1、ρ(Cd2+)初始值为60 mg·L-1、转速为130 r·min-1时,Cd2+去除率可达96.08%。
[1] 孙艳芳,刘芸.壳聚糖的交联改性及其吸附铜和铅离子的研究[J].西安交通大学学报,2013,47(11):127-132.[SUN Yan-fang,LIU Yun.Adsorption of Pb(Ⅱ) and Cu(Ⅱ) Ions by Cross-Lonked Chitosan Beads[J].Journal of Xi′an Jiaotong University,2013,47(11):127-132.]
[2] ZHOU L M,WANG Y P,LIU Z R,etal.Characteristics of Equilibrium,Kinetics Studies for Adsorption of Hg(Ⅱ) and Cu(Ⅱ) and Ni(Ⅱ) Ions by Thiourea-Modified Magnetic Chitosan Microspheres[J].Journal of Hazardous materials,2009,161(2/3):995-1002.
[3] NGAH W S,FATINATHAN S.Pb(Ⅱ) Biosorption Using Chitosan and Chitosan Derivatives Beads:Equilibrium,Ion Exchange and Mechanism Studies[J].Journal of Environmental Sciences,2010,22(3):338-346.
[4] ROGERIO L,THIAGO G,BRUNO S,etal.Adsorption and Desorption of Cu(Ⅱ),Cd(Ⅱ) and Pb(Ⅱ) Ions Using Chitosan Crosslinked With Epichlorohydrin-Triphosphate as the Adsorbent[J].Journal of Hazardous Materials,2010,183(1):233-241.
[5] 王菲,杨国录,刘林双,等.城市污泥资源化利用现状及发展探讨[J].南水北调与水利科技,2013,11(2):99-103.[WANG Fei,YANG Guo-lu,LIU Lin-shuang,etal.Research on Development and Utilization of Municipal Sewage Sludge[J].South-to-North Water Transfers and Water Science & Technology,2013,11(2):99-103.]
[6] 王士龙,张虹,朱孔秀,等.用活性污泥处理含铅废水的试验研究[J].材料保护,2002,35(4):53-56.[WANG Shi-long,ZHANG Hong,ZHU Kong-xiu,etal.The Study of Activated Aludge Treatment of Wastewater Containing Lead[J].Materials Protection,2002,35(4):53-56.]
[7] 彭立凤.壳聚糖的制备及其在废水处理中的应用[J].化学世界,1999(4):8-11.[PENG Li-feng.The Preparation of Chitosan and Its Application in Waste Water Treatment[J].Chemical World,1999(4):8-11.]
[8] 敖晓奎,罗琳,关欣,等.废弃茶叶渣对铅离子的吸附研究[J].农业环境科学学报,2008,27(1):372-374.[AO Xiao-kui,LUO Lin,GUAN Xin,etal.Adsorption of Lead Ion by Waste Tea[J].Journal of Agro-Environment Science,2008,27(1):372-374.]
[9] 朱巨建,周衍波,张永利,等.壳聚糖的改性及在印染废水处理中的应用[J].生态环境学报,2016,25(1):112-117.[ZHU Ju-jian,ZHOU Yan-bo,ZHANG Yong-li,etal.Modificaton of Chitosan and Its Application in Wastewater Treatment[J].Ecology and Environmental Sciences,2016,25(1):112-117.]
[10]孙胜玲,王爱勤.铅模板交联壳聚糖对Pb(Ⅱ)的吸附性能[J].中国环境科学,2005,25(2):192-195.[SUN Sheng-ling,WANG Ai-qin.Adsorption Properties of Pb(Ⅱ) Template Chitosan by Cross-Linked With Glutaraldehyde[J].China Environmental Science,2005,25(2):192-195.]
[11]SANDHYA B,TONNI A K.Study on Cr (VI) Removal From Contaminated Wastewater Using Natural Zeolite[J].Journal of Ion Exchange,2003,14:289-292.
[12]郭敏杰,刘振,李梅.壳聚糖吸附重金属离子的研究进展[J].化工环保,2004,24(4):262-265.[GUO Min-jie,LIU Zhen,LI Mei.Research Progresses on Adsorbing Heavy Metal Ions With Chitosan[J].Environmental Protection of Chemical Industry,2004,24(4):262-265.]
[13]李永明,于水利,唐玉霖.壳聚糖絮凝剂在水处理中的应用研究进展[J].水处理技术,2011,37(9):11-14.[LI Yong-ming,YU Shui-li,TANG Yu-lin.Research and Application of Chitosan and Its Derivatives in Water Treatment[J].Technology of Water Treatment,2011,37(9):11-14.]
[14]孙昌梅,曲荣君,王春华,等.基于壳聚糖及其衍生物的金属离子吸附剂的研究进展[J].离子交换与吸附,2004,20(2):184-192.[SUN Chang-mei,QU Rong-jun,WANG Chun-hua,etal.Progress in Adsorbents for Metal Ions Based on Chitosan and Its Derivatives[J].Ion Exchange and Adsorption,2004,20(2):184-192.]
[15]向文英,张志明.壳聚糖活性污泥复合吸附剂的制备研究[J].环境科学学报,2014,34(11):2792-2797.[XIANG Wen-ying,ZHANG Zhi-ming.Preparation of Composite Adsorbent With Chitosan and Activated Sludge[J].Acta Scientiae Circumstantiae,2014,34 (11):2792-2797.]
[16]FABRIS R,CHOW C W,DRIKAS M.Evaluation of Chitosan as a Natural Coagulant for Drinking Water Treatment[J].Water Science & Technoloy,2010,61(8):2119-2128.
[17]沈祥信,李小明,曾光明,等.活性污泥吸附重金属离子的研究进展[J].工业用水与废水,2006,37(4):7-11.[SHEN Xiang-xin,LI Xiao-ming,ZENG Guang-ming,etal.Development of Research on Adsorption of Heavy Metal Ions by Activated Sludge[J].Industrial Water & Wastewater,2006,37(4):7-11.]
[18]KATSUTOSHI I,YOSHIZUKA K,OHTO K.Adsorptive Separation of Some Metal Ions by Complexing Agent Types of Chemically Modified Chitosan[J].Analytica Chimica Acta,1999,388(1/2):209-218.
[19]王林.EDTA-壳聚糖的制备及对Cd2+、Pb2+的吸附研究[D].广州:广东海洋大学,2013.[WANG Lin.Study on the Preparation of EDTA-Chitosan and Adsorption of Cd2+and Pb2+[D].Guangzhou:Guangdong Ocean University,2013.]
[20]程珊珊,杨锡洪,章超桦,等.壳聚糖对镉铅混合离子吸附作用的研究[J].现代食品科技,2011,27(3):257-261,274.[CHENG Shan-shan,YANG Xi-hong,ZHANG Chao-hua,etal.Adsorption of Mixed Cadmiun and Plumbum Ions by Chitosan[J].Modern Food Science and Technology,2011,27(3):257-261,274.]
[21]杨家添,韦庆敏,谢秋季,等.花状BiOBr催化剂制备及对废水底物降解的光催化特性[J].生态与农村环境学报,2016,32(5):818-825.[YANG Jia-tian,WEI Qing-min,XIE Qiu-ji,etal.Preparation of Floriform BiOBr and Its Photocatalytic Characteristics in Degrding Wastewater Substrate[J].Journal of Ecology and Rural Environment,2016,32(5):818-825.]
[22]ALEXANDRE T P,MARCOS R G,ADRIANO V R,etal.Capacity of Adsorption of Pb2+and Ni2+From Queous Solutions by Chitosan Produced From Silkworm Chrysalides in Different Degrees of Deacetylation[J].Journal of Hazardous Materials,2007,147:139-147.
[23]张艳雅,马启敏.壳聚糖改性吸附剂的制备及其吸附性能研究[J].中国海洋大学学报(自然科学版),2006,36(5):153-156.[ZHANG Yan-ya,MA Qi-min.Adsorbent Prepared From Modified Chitosan Derivatives and Study of Its Adsorption Behavior[J].Periodical of Ocean University of China,2006,36(5):153-156.]
[24]王岚,王龙耀.生物吸附剂及其应用研究进展[J].天津化工,2006,20(5):5-8.[WANG Lan,WANG Long-yao.Progress of Biosorbent and Its Applications[J].Tianjin Chemical Industry,2006,20(5):5-8.]
[25]MOISSAVI G,BARIKBIN B.Biosorption of Chromium(VI) From Industrial Waste Water Onto Pistachio Hull Waste Bimass[J].Chemical Engineering Journal,2010,162(3):893-900.
[26]姚瑞华,孟范平,张龙军,等.改性壳聚糖对重金属离子的吸附研究和应用进展[J].材料报道,2008,22(4):65-70.[YAO Rui-hua,MENG Fan-ping,ZHANG Long-jun,etal.Study and Application of Adsorption of Heavy Metal Ions by Modified Chitosan[J].Materials Review,2008,22(4):65-70.]
(责任编辑: 陈 昕)
Research on Adsorption Performance of Chitosan-Activated Sludge Composite Adsorbent to Cadmium and Lead in Wastewater.
ZHAOZuo-ping1,2,DUANMin1,2,LIUZhi-feng1,2,TANGBo1,2,TONGYan-an3
(1.College of Chemical and Environment Science, Shaanxi University of Technology, Hanzhong 723001, China;2.Qinba Mountains Bio-Resource Collaborative Innovation Center of Southern Shaanxi Province, Hanzhong 723001, China;3.College of Natural Resources and Environment, Northwest A&F University, Yangling 712100, China)
The adsorption performance of the chitosan-activated sludge composite adsorbent on cadmium and lead in wastewater was examined, and the influencing factors, such as temperature, SCTS addition, pH, rotate speed and the concentration of heavy metals were investigated in a single factor experiment, thus the order of influencing factors and the optimal combination were determined in an orthogonal experiment. The results show that the factors affecting the adsorption of lead followed the order of pH > SCTS addition > initial concentration of Pb2+> rotate speed. The optimal adsorption of Pb2+could be reached with the pH of 2, SCTS addition of 10 g·L-1, Pb2+initial concentration of 50 mg·L-1, and rotate speed of 130 r·min-1, and the removal rate of Pb2+reached 95.76%. The factors influencing the adsorption of cadmium followed the order of pH > initial concentration of Cd2+>rotate speed > SCTS addition. The optimal adsorption of Cd2+could be reached with the pH of 2, SCTS addition of 2.5 g·L-1, Cd2+initial concentration of 60 mg·L-1, and rotate speed of 130 r·min-1, and the removal rate of Cd2+reached 96.08%. The composite adsorbent explores a new way for reutilization of sludge and provides a new method for wastewater treatment.
chitosan; composite adsorbent; cadmium; lead; wastewater; adsorption
2016-08-19
国家公益性行业科研专项(201203045);陕西省2011协同创新中心项目〔QBXT-Z(P)-15-5〕;2016年国家级大学生创新创业训练计划(201610720009)
X2
A
1673-4831(2017)08-0730-07
10.11934/j.issn.1673-4831.2017.08.008
赵佐平(1982—),男,陕西旬阳人,博士,主要从事环境监测等方面的研究。E-mail: zhaozuoping@126.com
① 通信作者E-mail: tongyanan@nwsuaf.edu.cn

