超细胆道镜在经皮经肝途径胆管肿瘤活检中的应用*
金 浩 刘会春 李宗狂 王 勇 满忠然 黄 伟
(蚌埠医学院第一附属医院肝胆外科,蚌埠 233004)
·临床研究·
超细胆道镜在经皮经肝途径胆管肿瘤活检中的应用*
金 浩 刘会春**李宗狂 王 勇 满忠然 黄 伟
(蚌埠医学院第一附属医院肝胆外科,蚌埠 233004)
目的 探讨超细胆道镜在经皮经肝胆管肿瘤活检中的应用价值。 方法 2014年12月~2016年9月,对21例行经皮经肝胆道引流(percutaneous transhepatic cholangial drainage,PTCD)联合胆道支架置入的胆管肿瘤,应用超细胆道镜取活检。 结果 10例获得明确病理结果(腺癌),5例倾向于癌诊断,1例上皮内瘤变,3例乳头状增生伴重度不典型增生,2例病理结果为炎症。无严重并发症。 结论 超细胆道镜可以应用于胆管肿瘤经皮经肝途径活检。
胆管癌; 经皮经肝胆道引流; 经皮经肝胆道支架置入; 超细胆道镜; 活检
胆管癌发病隐匿[1],早期诊断困难,手术是主要治疗措施,但是由于胆管毗邻肝动脉及门静脉,解剖位置特殊,手术根治性切除率低[2]。对于胆管癌非外科手术获得病理诊断的方法包括经皮经肝胆道镜活检、十二指肠镜细胞刷或活检钳在透视下活检。对于不能根治性切除的胆管癌致梗阻性黄疸,我们应用经皮经肝胆道引流(percutaneous transhepatic cholangial drainage,PTCD)联合胆道支架置入治疗[3~5]。在此基础上,2014年12月~2016年9月,我们在21例PTCD术中应用超细胆道镜进行肿瘤活检,获得良好的效果,报道如下。
1 临床资料与方法
1.1 一般资料
本组21例,男13例,女8例。年龄48~86岁,平均68.9岁。20例主要症状为皮肤巩膜黄染,其中2例伴寒战、发热等胆管炎症状,1例伴上腹部疼痛;1例主要症状为上腹部疼痛。病程2~60 d,平均22 d。均行彩超、CT、MRCP检查,临床诊断为胆管占位,其中肝门胆管占位15例,胆管中段占位2例,胆管下段占位4例。胆管梗阻长2.5~8 cm,平均4.1 cm。直接胆红素升高20例,11.7~420 μmol/L,平均179.4 μmol/L。转氨酶均升高,丙氨酸氨基转移酶(ALT)63~573 U/L,平均156.5 U/L;天冬氨酸氨基转移酶(AST)34~396 U/L,平均130.2 U/L。CA19-9升高14例,64.5~1200 IU/ml,平均531.1 IU/ml。其中1例行经皮经肝胆道支架置入术后3月余再次出现黄疸。
病例选择标准[6]:以皮肤巩膜黄染为主要症状,实验室检查提示以直接胆红素升高为主的梗阻性黄疸,血CA19-9升高,彩超、增强CT和MRCP检查提示胆管占位,因以下情况不能行根治性手术切除:①按肝门胆管癌Bismuth分型[6],术前CT、MRCP检查提示为Bismuth Ⅳ型肝门胆管癌;②术前增强CT检查提示肿瘤侵犯门静脉或肝动脉不宜行根治性切除;③高龄或有心、肺、肾功能障碍不能耐受手术切除。
1.2 方法
应用Olympus CB-30L超细胆道镜,外径2.7 mm。常规PTCD留置引流管,在透视下经引流管造影证实引流管在胆管内,并判断胆管占位导致梗阻所在位置(图1),置入导丝,拔出引流管。经导丝置入鞘管入肝内胆管,通过导丝置入造影导管,导丝和造影导管配合通过梗阻部位,退出造影导管,经导丝通过鞘管置入超细胆道镜(图2),胆道镜可通过梗阻部位至梗阻远端正常胆管,退出导丝,通过胆道镜直接观察胆管内病变(图3),活检钳取组织行病理检查(图4)。获得活检的组织单个直径约1 mm,可根据活检钳单次钳夹的组织大小,多次钳取,通常获得3~4块组织。通过导丝置入金属胆道支架[南京微创医学科技有限公司自膨式记忆合金支架,8 mm×60 mm、8 mm×80 mm、8 mm×100 mm、10 mm×60 mm、10 mm×80 mm、10 mm×100 mm,国食药监械(准)字2012第3460992号],重新置入PTCD管,观察PTCD引流的量及性状,以观察可能出现的胆管内出血及感染,支架置入术后1周复查生化常规提示直接胆红素下降,患者体温正常,夹管24 h无不适,拔除PTCD管。术后常规抗感染、保肝、补液治疗。
2 结果
2.1 活检病理诊断结果
10例获得明确阳性病理结果(腺癌)(图5、6);5例镜下提示核大深染,倾向于癌诊断;1例上皮内瘤变;3例乳头状增生伴重度不典型增生;2例未获得肿瘤病理诊断,其中1例病理报告个别核大细胞,另1例为胆管黏膜上皮稍增生,分化尚好,管壁见少量炎性细胞浸润。其中1例胆道支架置入后3个月余再次出现黄疸者,胆道镜见支架头端新生物导致支架梗阻,再次活检证实胆管腺癌。
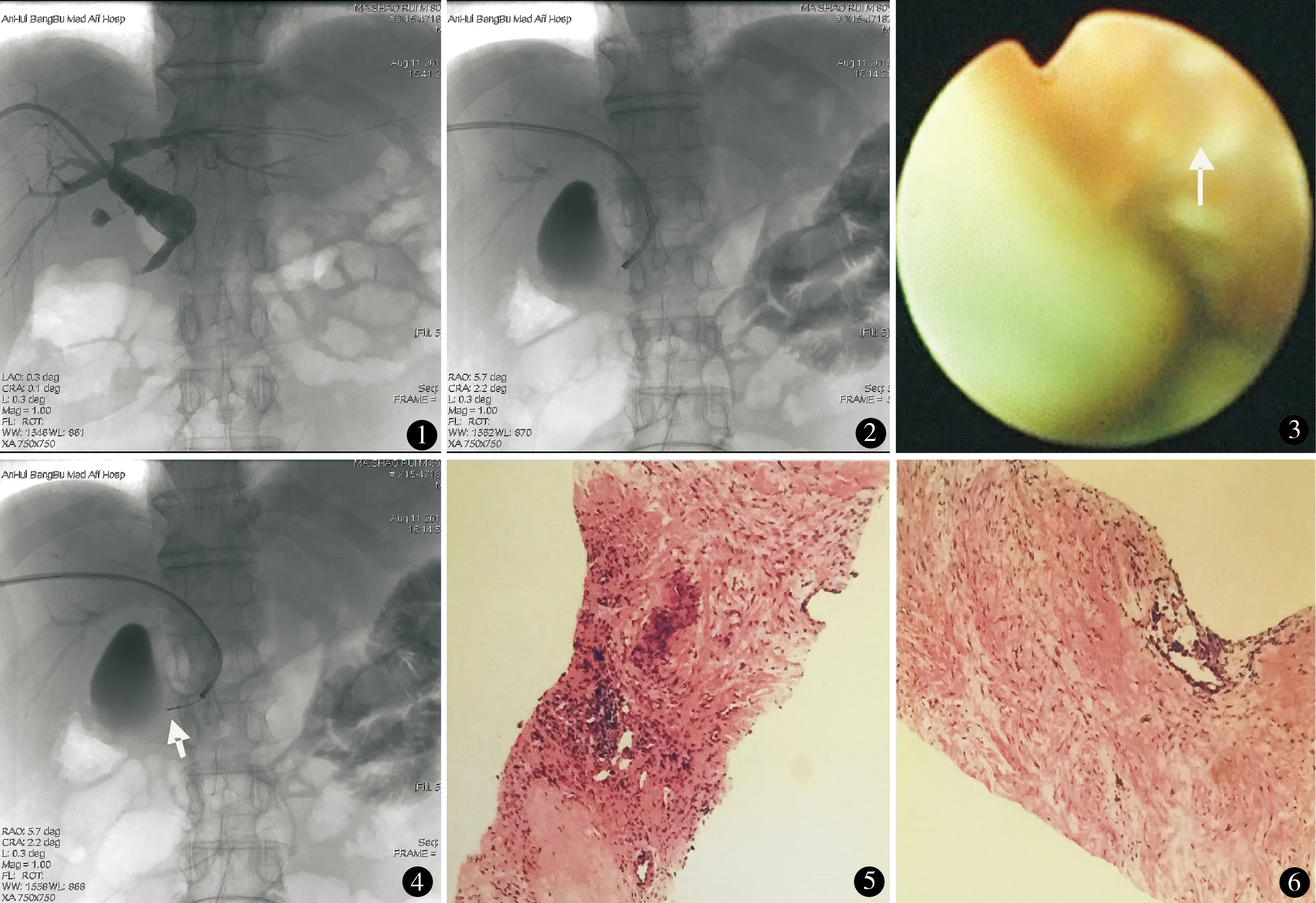
图1 造影提示梗阻位于胆管下段 图2 超细胆道镜经PTCD管窦道进入 图3 镜下胆管内黏膜毛糙 图4 活检钳活检 图5、6 病理诊断腺癌(HE染色 ×100)
2.2 并发症
胆管穿孔1例,活检后造影发现造影剂局部外漏,行支架置入并胆管内放置PTCD管引流。活检后局部少量出血1例,支架置入压迫结合药物止血。
3 讨论
对于胆管肿瘤的诊断,目前主要依靠彩超[7]、CT[8]、MRI[9]及肿瘤标志物CA19-9[10,11],但是即使是敏感性较高的CA19-9在胆管炎患者中也可能升高[12],需要动态观察[13]。手术切除是获得病理诊断的确切方法,但因肿瘤不能完全切除,或患者全身情况不允许手术,导致手术无法实施,对于这些患者获得病理诊断成为难题。胆管良性肿瘤或非肿瘤病变也可以表现为胆管占位性病变[14],如硬化性胆管炎、自身免疫性胆管炎等。对于这些疾病,治疗的策略及原则与胆管癌完全不同。获得胆管占位病变的病理诊断,对治疗方案的制定意义重大。
胆管癌的诊断通常依靠临床资料得出临床诊断。如何获得病理诊断一直是个难题,尤其对于无法根治切除的病例,既不能像体表肿瘤那样行切除活检,也不能像腹腔内实体肿瘤那样行穿刺活检。ERCP时通过细胞刷或活检钳在透视下取标本存在盲目性,且敏感性不高[15];经皮经肝胆道镜(percutaneous transhepatic cholangilscopy,PTCS)已应用于胆管癌的活检,且确诊率较高[16,17],但由于PTCD窦道较细,不能直接置入胆道镜,需要通过逐级更换PTCD管扩张窦道才能完成,需较长时间,容易延误治疗。我们将超细胆道镜应用于PTCS下行胆管癌活检,可同时获得病理结果。
对于无法根治性切除或患者全身情况不适合手术的胆管肿瘤,可以应用腔内粒子置入行局部放疗、全身化疗、生物免疫治疗等综合措施[18],然而没有明确的病理诊断,这些针对恶性肿瘤的措施不能合理应用,因此我们通过超细胆道镜活检获取病理诊断对不能根治切除的胆管癌的姑息治疗有重要的指导价值。
胆管癌行PTCD联合经皮经肝胆道支架置入术后一段时间可再次出现胆管梗阻,导致梗阻最多的原因是肿瘤通过支架网眼或支架头端生长[19],也可能是支架头端由于支架的刺激导致肉芽组织增生或胆泥淤积[20]。常规的处理方法是再次置入支架。本组1例胆管癌行胆道支架联合放射性粒子腔内治疗后3月余再次黄疸,超细胆道镜见支架头端有新生物,取活检病理提示重度不典型增生,癌变可能性很大,再次置入胆道金属支架并置入放射性粒子行腔内放射治疗。如果胆道镜发现为胆泥淤积,可在胆道镜下应用导丝疏通并反复冲洗,从而避免盲目置入支架。
胆管癌起病隐匿,早期诊断困难,我们经皮经肝途径应用超细胆道镜活检的初步经验表明,超细胆道镜可以获取标本,明确病理诊断,指导晚期胆管癌的综合治疗。本组仅10例明确获得癌诊断,确诊率仍需提高,其可能的原因为:①技术开展初期,操作技术不熟练;②超细胆道镜直径较细,其清晰度和普通胆道镜有差距;③超细胆道镜直径较细,可置入的活检钳较小,导致每次钳取的组织量较小,可能不能钳取到肿瘤组织。这些原因也是2例穿孔和出血并发症的原因。通过改善操作技术,规范流程,提高团队协作能力,可使操作更加精细,提高确诊率,减少并发症,拓宽适用范围。
1 Razumilava N,Gores GJ.Cholangiocarcinoma.Lancet,2014,383(9935):2168-2179.
2 Saxena A,Chua TC,Chu FC,et al.Improved outcomes after aggressive surgical resection of hilar cholangiocareinoma:a critical analysis of recurrence and survival.Am J Surg,2011,202(3):310-320.
3 范恒伟,刘会春,李宗狂,等.经PTCD途径胆道金属支架置入术治疗恶性梗阻性黄疸137例临床疗效分析.肝胆外科杂志,2013,21(2):94-97.
4 王 勇,刘会春,李宗狂,等.经皮胆道支架联合125I粒子腔内植入治疗恶性梗阻性黄疸的初步研究.中华放射学杂志,2014,48(5):403-407.
5 费圣贤,刘会春,孙 喆,等.胆道支架联合125I粒子腔内治疗胆管癌恶性黄疸的疗效评价.中国肿瘤临床,2015,45(11):564-569.
6 国际肝胆胰学会中国分会,中华医学会外科学分会肝脏外科学组.胆管癌诊断与治疗外科专家共识.中国实用外科杂志,2014,34(1):1-5.
7 Sungkasubun P,Siripongsakun S,Akkarachinorate K,et al.Ultrasound screening for cholangiocarcinoma could detect premalignant lesions and early-stage diseases with survival benefits:a population-based prospective study of 4,225 subjects in an endemic area. BMC Cancer,2016,16:346.
8 Dickson PV,Behrman SW.Distal cholangiocarcinoma.Surg Clin North Am,2014,94(2):325-342.
9 Valls C,Ruiz S,Martinez L,et al.Radiological diagnosis and staging of hilar cholangiocarcinoma.World J Gastrointest Oncol,2013,5(7):115-126.
10 杨 晨,张 捷,林圯昕,等.肝内胆管结石合并肝内胆管癌发病危险因素及预测指标分析.四川大学学报(医学版),2014,45(4):628-632.
11 Lumachi F,Lo Re G,Tozzoli R,et al.Measurement of serum carcino-embryonic antigen,carbohydrate antigen 19-9,cytokeratin-19 fragment and matrix metalloproteinase-7 for detecting cholangiocarcinoma:a preliminary case-control study.Anticancer Res,2014,34(11):6663-6667.
13 Khan SA,Davidson BR,Goldin RD.Guidelines for the diagnosis and treatment of cholangiocarcinoma: an update.Gut,2012,61(12):1657-1669.
14 Menias CO,Surabhi VR,Prasad SR,et al.Mimics of cholangiocarcinoma:spectrum of disease.Radiographics,2008,28(4):1115-1129.
15 刘素丽,王鼎鑫,邢国璋,等.内镜下胆管癌组织活检方法研究.中国内镜杂志,2009,15(5):456-457.
16 Kim HM,Park JY,Kim KS,et al.Intraductal ultrasonography combined with percutaneous transhepatic cholangioscopy for the preoperative evaluation of longitudinal tumor extent in hilar cholangiocarcinoma.J Gastroenterol Hepatol,2010,25(2):286-292.
17 Kim EH,Kim HJ,Oh HC,et al.The Usefulness of percutaneous transhepatic cholangioscopy for identifying malignancies in distal common bile duct strictures.J Korean Med Sci,2008,23(4):579-585.
18 Pu LZ,Singh R,Loong CK,et al.Malignant biliary obstruction:evidence for best practice.Gastroenterol Res Pract,2016,2016:3296801.
19 陆其明,王晓光,倪全法,等.经内镜胆道支架置入内引流术治疗恶性梗阻性黄疸的疗效分析及其对细胞免疫功能的影响.肿瘤学杂志,2013,19(6):484-487.
20 谭志刚,郭奕彤.胆道金属支架再狭窄原因及支架置入的治疗展望.中国组织工程研究与临床康复,2010,14(9):1669.
(修回日期:2017-05-10)
(责任编辑:王惠群)
Application of Percutaneous Transhepatic Ultrafine Choledochoscopy in the Biopsy of Cholangiocarcinoma
Jin Hao, Liu Huichun, Li Zongkuang, et al.
Department of Hepatobiliary Surgery, The First Affiliated Hospital of Bengbu Medical College, Bengbu 233004, China
Liu Huichun, E-mail:doctorlhc2000@aliyun.com
Objective To investigate the application value of percutaneous transhepatic ultrafine choledochoscopy in the pathological examinations of cholangiocarcinoma. Methods A combination of percutaneous transhepatic cholangial drainage (PTCD) and biliary stent placement was performed in 21 patients with cholangiocarcinoma from December 2014 to September 2016. During the surgery, a ultrafine choledochoscope was used for biopsy. Results Definite positive pathological results (adenocarcinoma) were obtained in 10 patients. And there were 5 cases inclined to diagnosis of carcinoma under microscope showing deep-dyed big nucleolus, 1 case of intraepithelial neoplasia, 3 cases of papillary hyperplasia with severe atypical hyperplasia, and 2 cases of inflammation. No severe complications occurred. Conclusion Percutaneous transhepatic ultrafine choledochoscopy can be applied in the biopsy of cholangiocarcinoma.
Cholangiocarcinoma; Percutaneous transhepatic cholangial drainage (PTCD); Percutaneous transhepatic stent placement; Ultrafine choledochoscope; Biopsy
安徽省科技攻关基金(编号:1501041155);蚌埠医学院科技发展基金(编号:BYKF1404)
A
1009-6604(2017)08-0698-03
10.3969/j.issn.1009-6604.2017.08.007
2016-11-08)
**通讯作者,E-mail:doctorlhc2000@aliyun.com
——导丝概述及导丝通过病变技巧

