无需全身麻醉、经胸超声心动图引导的改良经皮左心耳封堵术的初步经验
陈良龙 陆林祥 方军 鄢晓平 黄煜 李金国 孙旭东 钟玲
·临床研究·
无需全身麻醉、经胸超声心动图引导的改良经皮左心耳封堵术的初步经验
陈良龙 陆林祥 方军 鄢晓平 黄煜 李金国 孙旭东 钟玲
目的 初步探讨经胸超声心动图(TTE)替代经食管超声心动图(TEE)引导、无全身麻醉的改良经皮左心耳封堵术(PLAAO)的可行性及安全性。方法 对14例符合入选标准的患者以TTE替代TEE引导、无全身麻醉进行PLAAO,术后定期临床随访,观察PLAAO相关主要不良事件。结果 所有患者术中器械操作均获成功、无封堵相关严重并发症发生,即刻封堵成功率100%。住院及随访期间无PLAAO相关主要不良事件发生。本组14例患者改良局麻下TTE引导PLAAO患者手术时间及手术费用(不含麻醉及封堵器费用)分别为75~150(108±22)min及14601~33083(22491±5984)元。局麻患者较全身麻醉(全麻)患者每例节约麻醉费用960元。X线透视时间8~32(15.8±7.6)min。结论 初步证实TTE替代TEE引导、无全身麻醉的改良PLAAO是安全有效的,这种方法简化了手术过程、有利于PLAAO的推广应用,但仍需更多病例加以验证。
经皮左心耳封堵术; 经胸超声心动图; 全身麻醉
经皮左心耳封堵术(percutaneous left atrial appendage occlusion,PLAAO)是有效预防心房颤动(房颤)血栓栓塞事件的新技术[1-2]。除X线外,标准的PLAAO术中尚需经食管超声心动图(transesophageal echocardiography, TEE)引导、全身麻醉、气管插管、机械通气[1, 3]。若能以经胸超声心动图(transthoracic echocardiography, TTE)替代TEE,则可大幅简化手术流程、减少插管及全身麻醉相关并发症、降低手术费用、缩短手术及术后恢复时间。本文总结14例TTE替代TEE引导、无全身麻醉的改良PLAAO的初步经验,探讨其可行性。
1 对象与方法
1.1 研究对象
入选2015年12月至2017年1月,在福建医科大学附属协和医院心内科接受TTE引导PLAAO治疗患者14例。其中,男性10例,女性4例;年龄47~80(64.8±10.4)岁,年龄≥65岁10例;持续性房颤13例,阵发性房颤伴脑栓塞1例,病程半年至10年。使用CHA2DS2-VASc评分评估血栓栓塞风险[4],HAS-BLED评分评估抗凝出血风险[5]。入选标准[6-7]:CHA2DS2-VASc评分≥2分房颤患者,同时具有下列情况之一:(1)不适合长期口服抗凝者,如华法林禁忌、耐受不良、依从性不好;(2)服用华法林,国际标准化比值(INR)达标的基础上仍发生卒中或栓塞事件者;(3)HAS-BLED评分≥3分者。纳入14例患者中,CHA2DS2-VASC评分≥2分,平均3.2分。高血压病是最常见的危险因素(10例),其他主要危险因素为女性、年龄;全部患者HAS-BLED评分≥3分,平均3.7分。高血压病、年龄和INR不稳定是出血的主要危险因素。1例患者5年前行心脏永久起搏器植入术,起搏器程控功能正常。1例患者15年前曾行经皮动脉导管未闭封堵术。
1.2 研究方法
PLAAO手术步骤:用2%利多卡因局部麻醉,穿刺右股静脉,沿普通导丝送房间隔穿刺系统至上腔静脉,穿刺房间隔。确认穿刺成功后于鞘管内注射普通肝素100 U/kg、控制活化凝血时间在 200~300 s。送加硬导丝至左上肺静脉,撤出房间隔穿刺系统,沿加硬导丝送14 F输送鞘及扩张管至左心房。撤出扩张管,经输送鞘沿加硬导丝送6 F猪尾导管至左上肺静脉。撤出加硬导丝,送猪尾导管至左心耳,沿猪尾导管送输送鞘至左心耳。右前斜30°、+头20°及+足20°猪尾导管左心耳造影,观察其形态并测量口部、颈部最大直径。撤出猪尾导管,沿输送鞘经12 F输送系统送WATCHMANTM左心耳封堵器(boston Scientific Ireland Limited)封堵左心耳。经12 F输送系统造影,TTE观察封堵器位置、形态、周围残余裂隙及血流,测量封堵器压缩比。对于符合左心耳封堵器通过释放标准者,予以释放封堵器[8];否则调整封堵器位置或考虑更换之。
TEE法:术前常规TTE和TEE检查以明确心脏结构与功能、左心耳解剖结构,排除左心房及左心耳血栓。改良PLAAO术中以TTE结合X线引导,具体方法如下:(1)探查体位。患者取平卧位,必要时(透声差)可取左侧或浅左侧卧位。(2)观察切面。首先,将探头置于胸骨左缘第2~3肋间,获得胸骨旁大动脉短轴切面,微调探查切面方向以充分显示左心耳主体全貌;随后,探头逆时针旋转约90°、获得胸骨旁大动脉短轴正交切面,仔细调整探查切面方向以充分显示左心耳及其分叶,必要时可增加心尖部及剑突下探查切面。(3)观察指标。封堵器到位前,观察左心耳解剖结构(形态与分叶),测量左心耳开口、颈部(封堵器着陆区)的宽度及其深度并取均值,以此作为选择封堵器的参考;封堵器到位后及释放后,重点观察封堵器张开的形态、是否占位效应(挤压、覆盖周围结构或干扰其功能)、封堵器周围是否有裂隙及残余血流,并测量压缩比。
封堵后抗栓方案:按本中心常规方式处理,术后6 h皮下注射治疗量低分子肝素2~3 d;同时开始PLAAO术后45 d的口服药物抗凝方案,随后改为双联抗血小板治疗,即阿司匹林100 mg、每日1次,氯吡格雷75 mg、每日1次[1]。
1.3 随访与观察指标
术后每月进行定期临床随访,观察PLAAO相关主要不良事件发生情况,包括心源性死亡、封堵器脱落、血栓、栓塞、心包积血或心脏压塞及感染性心内膜炎等;术后翌日、出院前、随后每月TTE,术后1~3个月TEE复检观察封堵器位置、形态、压缩比、周围裂隙及残余血流、心包积血等。PLAAO成功定义:即刻封堵成功,指术中器械操作成功、无≥5 mm残余裂隙或残余血流、无封堵治疗相关并发症;短期临床成功,指住院及随访期间无PLAAO相关主要不良事件发生。
1.4 统计学分析
2 结果
2.1 左心耳形态特征与器械选择情况
术前超声心动图及术中造影显示:左心耳呈仙人掌形8例、菜花形4例、风向标形及鸡翅形各1例。左心耳颈部最大直径18~28(23.2±3.3)mm,所选封堵器大小27~33(29.6±2.6)mm。其中,1例封堵器过大,由33 mm换用30 mm封堵器成功封堵。
2.2 即刻封堵效果及短期随访结果
14例患者术中器械操作均获成功、无封堵相关主要不良事件发生,即刻封堵成功率100%。术中造影及TTE测量封堵器压缩比分别为(21.8±5.5)%和(22.1±5.9)%。封堵器位置良好、形态正常、无≥5 mm裂隙或残余血流、未干扰周围结构及功能。术后第1~2天TTE复查仍维持良好封堵效果,住院期间无PLAAO相关主要不良事件发生。
本组随访1~12个月,中位随访时间3个月。术后1~3个月,全部患者复查TTE未见封堵器移位、脱落及对周围结构的占位效应。术后3~6个月,7例TEE复查见封堵器位置正常、未见表面血栓附着,其中3例可见细小残余裂隙血流(<3 mm)。随访期间无PLAAO相关主要不良事件发生,短期临床成功率也为100%。
2.3 术后抗凝及抗栓治疗情况
9例患者服用华法林,按INR调整剂量;2例服用利伐沙班10 mg,每日1次;2例服用达比加群150 mg,每日2次。以上治疗方案45 d,随后改为双联抗血小板治疗。服药及随访期间无严重出血及血栓事件,仅1例服用利伐沙班者牙龈出血。
2.4 手术时间、透视时间及费用
本组14例患者改良局麻下TTE引导PLAAO手术时间及手术费用(不含麻醉及封堵器费用)分别为75~150(108±22)min及14601~33083(22491±5984)元。局麻患者较全麻患者每例节约麻醉费用960元。X线透视时间8~32(15.8±7.6)min。
2.5 同期实施的其他介入手术
本组14例患者中,1例症状性持续性心房颤动患者,同期先行导管射频消融治疗,再行PLAAO;1例合并短暂脑缺血发作的卵圆孔未闭患者,同期先行PLAAO,再行卵圆孔未闭封堵术。
3 讨论
房颤是临床上最常见的心律失常之一。血栓栓塞特别是脑栓塞是其致死、致残的主要原因。传统的预防栓塞事件方法是使用华法林抗凝,但需终身服药及长期监测。 华法林抗凝有效窗窄,易受食物和药物影响、INR达标率低、出血风险大。在非瓣膜性房颤患者中,约90%的血栓源自左心耳[9]。因此,左心耳成为干预的靶点。WATCHMANTM是最早经临床试验证实有效的左心耳封堵器。研究证实,采用WATCHMANTM封堵器进行左心耳封堵,其预防脑卒中的疗效不劣于口服华法林[1,10],在预防不良心血管事件复合终点发生方面优于华法林[11]。PLAAO已成为长期口服抗凝治疗禁忌证、卒中高危患者的治疗选择[12]。
目前,标准的PLAAO术通常采用TEE实时监测,结合X线透视引导左心耳封堵器置入[1, 10-11]。本中心首先尝试改良PLAAO是基于以下考虑:(1)术中TEE的作用主要在于封堵器释放后确认其位置、形态及是否存在残余裂隙与残余血流,这些大多通过X线透视和造影即可实现,TEE的作用只是再次确认。(2)封堵器置入左心耳后,由于其金属骨架的强回声,易被TTE检出;即使存在一些影响透声的因素,如肥胖、肺气肿等,仍可通过改变体位或超声探查位置检出封堵器的位置、大小与形态。(3)以TTE代替TEE既可避免全身麻醉、减轻患者痛苦、缩短手术及恢复时间,又可避免食管与气管插管可能造成的额外损伤及并发症。实践表明,本组14例患者经改良PLAAO即刻封堵及短期临床成功率均达100%,初步结果提示TTE代替TEE进行PLAAO术中监测是安全可行的,由此可避免食管与气管插管及全麻、实现了简化手术流程的目标。
通过本组14例成功的PLAAO,我们积累了TTE代替TEE进行术中监测的初步经验:(1)胸骨旁大动脉短轴切面及其正交切面是显示左心耳及封堵器的最佳切面。前者相当于TEE切面方位30°~45°、左心耳造影右前斜位30°+头20°,而后者则相当于TEE切面方位120°~135°、左心耳造影右前斜位30°+足20°。必要时(肺气肿或垂位心),可增加心尖部四、五腔心切面显示左心耳,这组切面相当于TEE切面方位90°、左心耳造影右前斜位30°。(2)封堵器置入前,胸骨旁大动脉短轴切面左心耳呈“倒三角形”或“风袋状”,该切面可较好地显示、测量左心耳深度的最大径线;而其正交切面在透声较佳时则可显示左心耳形态(鸡翅状、分叶状、菜花状);两组切面均可显示左心耳开口、颈部(封堵器着陆区)及深度,相应部位径线的超声测值可作为选择封堵器的参考值。(3)封堵器置入后,胸骨旁大动脉短轴切面可见封堵器金属骨架强回声,形态多呈“梯形”或“水母状”;而其正交切面则多呈“卵圆形”或“类圆形”。 (4)在上述切面上,除了观察封堵器的形态、位置和大小(压缩比)外,尚可观察封堵器对周围结构(左上肺静脉、二尖瓣)的影响,但TTE对不完全堵闭裂隙及残余血流的敏感度显著低于TEE。图1为1例TTE引导PLAAO典型病例。
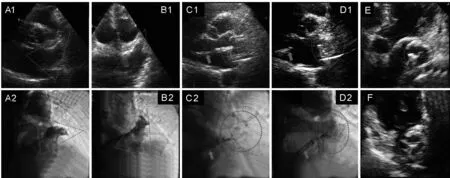
图1 经胸超声心动图(TTE)引导、无全身麻醉的改良PLAAO典型病例 本例术前造影示左心耳颈部着陆区直径27 mm,选用33 mm WATCHMANTM封堵器封堵左心耳。上行(A1~D1)与下行(A2~D2)分别为封堵前、后TTE与左心耳造影图像。A、B:封堵前,TTE大动脉短轴及其正交切面分别可见左心耳呈“风袋状”(A1)及“仙人掌状”(B1)回声,分别与右前斜位30°+头位20°及右前斜位30°+足位20°造影所示左心耳形态相一致(A2、B2分别与A1、B1对应,见三角形轮廓线所示)。C、D:封堵器到位后,TTE大动脉短轴及其正交切面可见封堵器位于左心耳内,分别呈草莓形及卵圆形,金属骨架呈“梯形”回声,铆钉(C1、D1三角形所示)及推送杆(C1、D1箭头所示)清晰可见,两个切面分别为封堵器长轴及接近短轴切面,分别与术中右前斜位30°+头位20°及右前斜位30°+足位20°透视所示封堵器及输送鞘(C2、D2箭头所示,三角形箭头示铆钉)相对应(C2、D2分别与C1、D1对应,见圆形及椭圆形轮廓线所示);长轴切面可见推送杆与铆钉相连,短轴切面示推送杆与铆钉不在同一切面。E、F:术后第一天复查,TTE大动脉短轴及其正交切面分别可见封堵器长轴(纵轴)切面(E,封堵器呈草莓形)及短轴(横轴)切面(F,封堵器呈圆形,铆钉居中);与术后透视下左心耳封堵器形态相对应(C2、D2圆形及椭圆形轮廓线内)。星形所示为左上肺静脉,提示左心耳封堵器未压迫左上肺静脉及影响血流(C1、D1、E星形所示)。
不可否认,较之TTE,TEE可更清晰地显示左心耳结构及其与封堵器的位置关系,特别是在显示封堵后残余裂隙及残余血流方面更具优势。因此,对于经验不足者或在患者胸部透声条件较差时,TEE仍是目前PLAAO的常规影像引导方式。
综上所述,我们首次采用TTE引导、无全身麻醉的改良PLAAO术,术中及术后随访无明显残余裂隙血流、未发生PLAAO相关性主要不良事件,即刻封堵成功率及短期临床成功率高,初步证实其安全性及有效性。改良PLAAO术简化了手术过程、有利于PLAAO的推广应用,但仍需更多病例加以验证。
[1] Reddy VY, Doshi SK,Sievert H, et al. PROTECT AF investigators. percutaneous left atrial appendage closure for stroke prophylaxis in patients with atrial fibrillation: 2.3-year follow-up of the PROTECT AF (watchman left atrial appendage system for embolic protection in patients with atrial fibrillation) trial. Circulation, 2013,127(6):720-729.
[2] 苏晞. 左心耳封堵治疗的现状和进展. 中国介入心脏病学杂志, 2016, 24(8):458-461.
[3] Wunderlich NC, Beigel R, Swaans MJ, et al. Percutaneous interventions for left atrial appendage exclusion: options, assessment, and imaging using 2D and 3D echocardiography. JACC Cardiovasc Imaging,2015,8(4):472-488.
[4] Lip GY, Nieuwlaat R, Pisters R, et al. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest, 2010,137(2):263-272.
[5] Pisters R, Lane DA, Nieuwlaat R, et al. A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey. Chest, 2010,138(5):1093-1100.
[6] Meier B, Blaauw Y, Khattab AA, et al. Document reviewers. EHRA/ EAPCI expert consensus statement on catheter-based left atrial appendage occlusion. Europace, 2014,16(10):1397-1416.
[7] 中华医学会心电生理和起搏分会, 中华医学会心血管病学分会, 中国医师协会心律学专业委员会. 左心耳干预预防心房颤动患者血栓栓塞事件:目前的认识和建议. 中国心脏起搏与心电生理杂志, 2014,18(4):471-486.
[8] Möbius-Winkler S, Majunke N, Sandri M, et al. Percutaneous left atrial appendage closure: Technical aspects and prevention of periprocedural complications with the watchman device. World J Cardiol,2015,7(2):65-75.
[9] Odell JA,Blackshear JL,Davies E,et al. Thoracoscopic obliteration of the left atrial appendage: potential for stroke reduction.Ann Thorac Surg, 1996,6l:565-569.
[10] Reddy VY, Möbius-Winkler S, Miller MA, et al. Left atrial appendage closure with the Watchman device in patients with a contraindication for oral anticoagulation: the ASAP study (ASA Plavix Feasibility Study With Watchman Left Atrial Appendage Closure Technology). J Am Coll Cardiol,2013,61(25):2551-2556.
[11] Reddy VY,Sievert H,Halperin J,et al. PROTECT AF steering committee and investigators. Percutaneous left atrial appendage closure vs warfarin for atrial fibrillation: a randomized clinical trial. JAMA, 2014,312(19):1988-1998.
[12] Kirchhof P, Benussi S, Kotecha D, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J,2016,37(38):2893-2962.
The preliminary experience of modified percutaneous left atrial appendage occlusion under transthoracic echocardiographic guidance without general anesthesia
CHENLiang-long,LULin-xiang,FANGJun,YANXiao-ping,HUANGYu,LIJin-guo,SUNXu-dong,ZHONGLing.
Departmentofcardiology,fujianmedicaluniversityunionhospital.Fuzhou350001,China
Correspondingauthor:CHENLiang-long,Email:lianglongchen@126.com
Objective To investigate the feasibility and safety of modified percutaneous left atrial appendage occlusion( PLAAO ) under transthoracic echocardiographic (TTE) guidance without general anesthesia instead of transesophageal echocardiographic guidance. Methods A total of 14 patients who met the inclusion criteria underwent modified PLAAO guided by TTE instead of TEE without general anesthesia. Regular clinical follow-up observations of PLAAO-related major adverse events were done in the perioperative period. Results All patients were successfully implanted with left atrial appendage occluder device (Watchman) without device-related serious complications. Immediately occlusion success rate was 100%. No major adverse events occurred during hospitalization and follow-up.The mean operation time was 108±22 min(range 75-150 min)and the mean radiation exposure time was 15.8±7.6 min(range 8-32 min).Conclusion Modified PLAAO guided by TTE instead of TEE without general anesthesia may be safe and effective. This method simplifies the operation process and is favorable for PLAAO application. But this modified PLAAO is still needed to be validated in more patients.
Percutaneous left atrial appendage occlusion; Transthoracic echocardiography; General anesthesia
10.3969/j.issn.1004-8812.2017.06.005
福建省医学创新课题资助计划(2014-CX-12)
350001 福建福州,福建医科大学附属协和医院心内科 福建省心脏医学中心 福建省冠心病研究所
陈良龙, Email:lianglongchen@126.com
R654.2
2017-03-13)

