子宫肌瘤超声造影定量灌注特征预测超声消融的效果
王 勇,陈锦云*,陈文直,胡 亮,李俊书,王 熙
(1.重庆医科大学生物医学工程学院,省部共建国家重点实验室培育基地—重庆市超声医学工程重点实验室,重庆市生物医学工程学重点实验室,重庆市微无创医学协同创新中心,重庆 400016;2.重庆医科大学附属第一医院超声消融治疗中心,重庆 400042)
子宫肌瘤超声造影定量灌注特征预测超声消融的效果
王 勇1,陈锦云1*,陈文直1,胡 亮1,李俊书1,王 熙2
(1.重庆医科大学生物医学工程学院,省部共建国家重点实验室培育基地—重庆市超声医学工程重点实验室,重庆市生物医学工程学重点实验室,重庆市微无创医学协同创新中心,重庆 400016;2.重庆医科大学附属第一医院超声消融治疗中心,重庆 400042)
目的 探讨子宫肌瘤超声造影定量参数预测超声消融效果的价值。方法 对63例子宫肌瘤患者术前行超声造影检查,采用JC型超声消融治疗系统内置灰度测量软件获得子宫肌瘤血流灌注定量参数。术后根据增强MRI分为消融满意组(消融率≥70%)和部分消融组(消融率<70%),比较2组造影参数差异,分析造影参数与消融率的关系,并采用ROC曲线评价造影参数对消融效果的预测价值。结果 2组到达时间(AT)、达峰时间(TTP)、增强时间(ET)、增强强度(EI)、增强速率(ER)差异均有统计学意义(P均<0.01);AT、TTP、ET与消融率呈正相关(P均<0.01),EI、ER与消融率呈负相关(P均<0.001)。AT、TTP、ET、EI、ER的ROC曲线下面积(AUC)均>0.7,其中ER的预测价值最高(AUC=0.935)。以ER=5.23作为截点值,其预测消融效果的敏感度为80.0%、特异度为95.8%。结论 子宫肌瘤的超声消融效果与超声造影定量参数存在一定相关性,ER可作为预测消融效果的较好指标。
子宫肌瘤;高强度聚焦超声消融;造影剂
高强度聚焦超声(high intensity focused ultrasound, HIFU)主要利用超声的热效应使靶组织局部温度升高到60℃以上,使病灶发生凝固性坏死[1-5],从而达到治疗的目的。研究[6-7]表明血液供应是影响超声消融能量沉积的重要因素,因此了解子宫肌瘤血流灌注特征对临床超声消融治疗子宫肌瘤有重要意义。超声造影剂(ultrasound contrast agent, UCA)是良好的血管显像剂,在体内血流动力特征与红细胞相似,其到达脏器组织的数量和速度可反映该组织血流灌注特征。本研究采用第三代造影剂声诺维[8](SonoVue)及超声造影匹配成像技术(contrast tuned imaging, CnTI)观察HIFU治疗前子宫肌瘤造影特征,并定量评价子宫肌瘤血流灌注特征,探讨其与HIFU消融效果的关系及其对预测超声消融效果的价值。
1 资料与方法
1.1 一般资料 选取2015年1月—2016年9月于我院超声消融中心接受治疗的子宫肌瘤患者63例,年龄26~52岁,平均(39.5±6.7)岁。纳入标准:①临床及影像学(超声及MRI)确诊为单发子宫肌瘤;②病灶位于子宫前壁,且为肌壁间肌瘤;③患者能配合超声造影检查,造影时移动度小,图像清晰;④无超声造影检查禁忌证;⑤术前模拟定位焦点运行范围可完全覆盖病灶,且声通道无骨骼和肠道遮挡。本研究获得重庆医科大学伦理委员会批准,患者均知情同意。
1.2仪器与方法 采用Esaote MyLab 70XV彩色多普勒超声诊断仪,CA430E探头,频率2.5~5.0 MHz,配备CnTI成像软件,机械指数0.12。造影剂采用SonoVue,与5 ml生理盐水混合并振荡成微泡混悬液。
患者取俯卧位,经腹矢状位行超声检查,扫查整个子宫肌瘤病灶后,移动探头至病灶最大切面,启动CnTI程序进入造影显像模式。抽取1.5 ml微泡混悬液,经肘前静脉快速团注,随即注入5 ml生理盐水。同时启动计时器,待造影剂充填整个病灶并开始逐渐消退时,观察病灶其他切面的增强情况。造影结束10 min后,行HIFU治疗。
HIFU治疗采用JC型高强度聚焦超声治疗系统(重庆海扶医疗科技股份有限公司)。靶区出现团块状或整体灰度变化且覆盖计划治疗区为治疗终点。根据术中监控超声图像实时灰度变化情况及患者治疗反应,调整声波发射功率、发射时间和冷却时间。存储所有动态影像资料于仪器硬盘。
根据术前拟治疗区范围勾画ROI(图1),采用消融治疗系统内置灰度测量软件,测量增强开始灰度值及增强最大灰度值,同时记录到达时间(arrival time, AT):造影剂注入至其到达ROI的时间;达峰时间(time to peak, TTP):造影剂注入至增强灰度最大值的时间;增强时间(enhancement time, ET):达峰时间-到达时间;增强强度(enhancement intensity, EI):增强最大灰度值-增强开始灰度值;增强速率(enhancement rate, ER):增强强度/增强时间。
1.3 效果评价 术后第2天行增强MR检查观察消融效果,于T2WI脂肪抑制序列图像上测量子宫肌瘤长径(D1)、前后径(D2)、横径(D3),计算肌瘤体积(V):V=D1×D2×D3×0.523 3;相同方法于增强MR测量非增强肿瘤体积(non-perused volume, NPV)。计算消融率:消融率=NPV/V×100%。根据研究[9]设定消融率≥70%为达到治疗效果,为消融满意组,消融率<70%为部分消融组。

2 结果
63例患者体质量指数(21.88±2.75)kg/m2,肌瘤最大径(5.43±1.07)cm,肌瘤体积(80.10±40.01)cm3。子宫肌瘤超声造影的典型表现为肌瘤周边首先呈环状增强(图2),之后内部出现不规则树枝样63例患者均顺利完成HIFU治疗,术后肌瘤体积平均(82.38±46.20)cm3,增强MRI显示NPV为(64.98±39.53)cm3,消融率(79.22±14.34)%。其中消融满意组48例(48/63,76.19%),部分消融组15例(15/63,23.81%)。部分消融组AT、TTP、ET均短于消融满意组(P均<0.01),EI、ER大于消融满意组(P均<0.001),见表1。
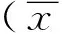
表1 消融满意组与部分消融组超声造影定量参数比较±s)

图1 造影前后ROI内的变化 A.子宫肌瘤造影开始前ROI区未见明显造影剂充填; B.造影开始后20 s,ROI区造影剂充填明显 图2 子宫肌瘤超声造影图 A.造影早期肌瘤周边出现环状高增强; B.增强达峰后肌瘤边界清晰
或点状增强,随后整个肌瘤逐渐增强,呈均匀或不均匀增强,并与周围正常子宫肌层有明显分界。AT为(15.92±3.92)s,TTP为(25.50±5.67)s,ET为(9.58±2.70)s,EI为37.55±24.16,ER为4.33±3.52。
AT、TTP、ET与消融率呈正相关(r=0.325、0.453、0.480,P均<0.01),EI、ER与消融率呈负相关(r=-0.631、-0.724,P均<0.001)。
根据ROC曲线(图3),以AT=13.50 s、TTP=20.50 s、ET=9.50 s、EI=34.55、ER=5.23为预测消融效果最佳截点值,各参数诊断效能见表2。

表2 子宫肌瘤各造影定量参数预测消融效果的 截点值及诊断效能
3 讨论
HIFU利用超声波的方向性、组织内穿透性和可聚焦性,通过超声换能器将体外低能量超声波聚焦于靶组织内,利用热效应、机械效应、空化效应使靶组织局部温度瞬时升高至60℃以上,发生凝固性坏死,从而达到治疗的目的。因此,HIFU治疗的关键在于热量的累积,即增加热量沉积,减少热量散失。研究[6-7]表明血流是影响能量沉积的重要因素。流动的血液可迅速将部分热量带走导致局部温度下降,从而降低超声消融的效果[10-11]。因此了解子宫肌瘤血流灌注特征对临床超声消融治疗子宫肌瘤有重要意义。本研究旨在通过造影参数定量描述子宫肌瘤造影灌注特征,分析其与肌瘤消融效果的关系及其对预测消融效果的临床价值。
本研究对63例患者进行HIFU消融治疗,术后部分消融组AT、TTP、ET明显短于消融满意组(P<0.01),造影的时间参数[12]反应微泡灌注的速度,时间越短,提示灌注速度越快,即部分消融组的血流灌注速度明显大于消融满意组,表明血流速度越快,消融效果越差;部分消融组EI、ER明显大于消融满意组 (P<0.001),病灶增强强度与微泡含量相关[13],而微泡含量则反映组织血流灌注量,增强强度越大,血流灌注越丰富,即本研究中部分消融组血流灌注量明显大于消融满意组,提示肌瘤血流灌注越丰富,消融效果越差。陈建科等[14]发现超声造影呈高增强的肌瘤HIFU后易发生肌瘤残存,治疗效果较差,与本研究结果类似。
通过对子宫肌瘤造影定量参数与肌瘤消融率的相关性分析发现,AT、TTP、ET与消融率呈正相关,EI、ER与消融率呈负相关,并且发现ER与消融率的相关程度最高(r=-0.724,P<0.001)。ER为增强强度与增强时间的比值,该参数综合血流灌注量及血流速度的信息,可更好地反映子宫肌瘤的灌注特征与消融效果的关系。

图3 超声造影参数的ROC曲线图
另外,本研究通过ROC曲线比较各造影参数对消融效果的预测价值,结果显示AT、TTP、ET、EI及ER的AUC分别为0.806、0.820、0.767、0.841、0.935,其中ER的AUC值最大,提示ER对消融效果的预测准确率最高。以ER=5.23作为预测消融满意的截点值,其敏感度为80.0%、特异度为95.8%,提示增强速率可作为预测消融效果的较好指标。
本研究的不足:由于造影晚期切面的移动,未能收集到子宫肌瘤超声造影晚期的定量参数特征;由于临床使用超声仪器品牌众多,以及采用的造影成像技术的不同、配套的定量分析软件的差异等因素,可能会对不同研究间截点值的结果带来一定的变异。有研究[15]报道VueBoxTM软件可对不同品牌仪器获得的造影序列进行定量分析,今后有必要采用统一的软件对造影结果标准化,从而减少变异,提高研究的可重复性及可推广性。
总之,本研究结果显示子宫肌瘤不同消融效果之间超声造影特征存在显著差异,子宫肌瘤的血流灌注特征与消融效果关系密切。术前对子宫肌瘤的超声造影进行定量评价,对预测HIFU消融效果有重要意义。
[1] 陈文直,唐良萏,杨武威,等.超声消融治疗子宫肌瘤的安全性及有效性.中华妇产科杂志,2010,44(12):909-912.
[2] Quinn SD, Vedelago J, Gedroyc W, et al. Safety and five-year re-intervention following magnetic resonance-guided focused ultrasound (MRgFUS) for uterine fibroids. Eur J Obstet Gynecol Reprod Biol, 2014,182:247-251.
[3] Chen J, Chen W, Zhang L, et al. Safety of ultrasound-guided ultrasound ablation for uterine fibroids and adenomyosis: A review of 9 988 cases. Ultrason Sonochem, 2015,27:671-676.
[4] 王智亮,熊正爱,陈骊,等.高强度聚焦超声消融治疗围绝经期子宫肌瘤的初步研究.中国超声医学杂志,2014,30(1):55-58.
[5] 任小龙,周晓东,张军,等.高强度聚焦超声治疗子宫平滑肌瘤的病理变化及其超声随访研究.中国超声医学杂志,2006,22(9):714-716.
[6] 刘芳,邹建中,艾慧坚,等.猪肝脏灌流对脉冲高强度聚焦超声辐照致热沉积的影响.中国介入影像与治疗学,2013,10(6):369-372.
[7] 陈锦云,陈文直,朱丽,等.子宫肌瘤的血液供应特征对超声消融剂量的影响.中华妇产科杂志,2011,46(6):403-406.
[8] 何蒙娜,姜玉新,吕珂.超声造影剂Sonazoid与SonoVue的物理特征及临床特定比较.中国医学影像技术,2015,31(2):306-309.
[9] 秦娟,陈文直,陈锦云,等.超声消融子宫肌瘤后残余瘤组织的核磁共振影像学转归.中国肿瘤临床,2013,40(2):111-115.
[10] Kennedy JE. High-intensity focused ultrasound in the treatment of solid tumours. Nat Rev Cancer, 2005,5:321-327.
[11] Zhou P, Zhou P, He W, et al. The influence of blood supply on high intensity focused ultrasound a preliminary study on rabbit hepatic VX2 tumors of different ages. Acad Radiol, 2012,19(1):40-47.
[12] 燕翠菊,黄备建,王文平,等.肾良恶性占位超声造影定量参数分析的初步研究.中华超声影像学杂志,2012,21(4):312-315.
[13] Tang MX, Mulvana H, Gauthier T, et al. Quantitative contrast-enhanced ultrasound imaging: A review of sources of variability. Interface Focus, 2011,1(4):520-539.
[14] 陈建科,刘学明,张闻,等.子宫肌瘤超声造影增强类型与高强度聚焦超声治疗疗效的关系.中国介入影像与治疗学,2010,7(4):428-431.
[15] Tranquart F, Mercier L, Frinking P, et al. Perfusion quantification in contrast-enhanced ultrasound (CEUS)—ready for research projects and routine clinical use. Ultraschall Med, 2012,33(Suppl 1):S31-S38.
Quantitative perfusion characteristics of contrast-enhanced ultrasound of uterine fibroids in predicting effect of ultrasound ablation
WANGYong1,CHENJinyun1*,CHENWenzhi1,HULiang1,LIJunshu1,WANGXi2
(1.StateKeyLaboratoryofUltrasoundEngineeringinMedicineCo-FoundedbyChongqingandtheMinistryofScienceandTechnology,ChongqingKeyLaboratoryofUltrasoundinMedicalandBiomedicalEngineering,ChongqingCollaborativeInnovationCenterforMinimally-InvasiveandNoninvasiveMedicine,CollegeofBiomedicalEngineering,ChongqingMedicalUniversity,Chongqing400016,China; 2.UltrasoundAblationCenter,theFirstAffiliatedHospitalofChongqingMedicalUniversity,Chongqing400042,China)
Objective To investigate the value of quantitative parameters of CEUS in predicting the effect of ultrasound ablation of uterine fibroids. Methods Sixty-three patients with uterine fibroids underwent CEUS before operation. The software of gray level measurement in JC HIFU system was used to obtain quantitative parameters of uterine fibroids perfusion. According to postoperative enhanced MR examination, the results were divided into satisfactory group (ablation rate≥70%) and partial ablation group (ablation rate<70%). CEUS parameters of two groups were compared, and the correlation between parameters and ablation rate were analyzed. The predictive value was evaluated by ROC curve. Results There were significant differences in the time of arrival (AT), time to peak (TTP), enhancement time (ET), enhancement intensity (EI) and enhancement rate (ER) between the two groups (allP<0.01). The AT, TTP and ET were positively correlated with the ablation rate (allP<0.01), and the EI and ER were negatively correlated with the ablation rate (bothP<0.001). The area under the curve (AUC) of AT, TTP, ET, EI, ER were all greater than 0.7, among which ER had the highest predictive value (AUC=0.935). Using ER=5.23 as the cut-off point, the sensitivity of predicting ablation effect was 80.0%, specificity was 95.8%. Conclusion There is a certain correlation between the ultrasound ablation effect of uterine fibroids and the quantitative parameters of CEUS. ER can be used as a good predictor of ablation effect.
Uterine fibroids; High intensity focused ultrasound ablation; Contrast media
国家“十二五”科技支撑计划课题项目(2011BAI14B01)、国家重点基础研究发展计划(973计划)项目(2011CB707900)。
王勇(1991—),男,安徽阜阳人,在读硕士。研究方向:子宫肌瘤的超声消融治疗。E-mail: 964260703@qq.com
陈锦云,重庆医科大学生物医学工程学院 省部共建国家重点实验室培育基地—重庆市超声医学工程重点实验室 重庆市生物医学工程学重点实验室 重庆市微无创医学协同创新中心,400016。E-mail: chenjinyun2006@126.com
2017-03-17
2017-05-27
R737.33; R445.1
A
1672-8475(2017)07-0404-04
10.13929/j.1672-8475.201703023

