丁酮3s里德堡态的超快光解动力学研究∗
罗金龙 凌丰姿 李帅 王艳梅 张冰
1)(昆明学院物理科学与技术系,昆明 650214)
2)(中国科学院武汉物理与数学研究所,波谱与原子分子物理国家重点实验室,武汉 430071)
丁酮3s里德堡态的超快光解动力学研究∗
罗金龙1)凌丰姿2)李帅2)王艳梅2)张冰2)†
1)(昆明学院物理科学与技术系,昆明 650214)
2)(中国科学院武汉物理与数学研究所,波谱与原子分子物理国家重点实验室,武汉 430071)
(2016年9月12日收到;2016年11月1日收到修改稿)
本文采用195.8 nm飞秒激光将丁酮分子激发到S2(n,3s)里德堡态,在800 nm探测光的作用下获得时间分辨的飞行时间质谱.对实验结果的分析表明,由于丁酮α位置具有一个甲基和一个乙基,使得Norrish I型解离反应表现出丰富的动力学特征.母体离子瞬态衰减的时间常数为(2.23±0.02)ps.丙酰基离子瞬态衰减与母体类似,只有一个为(2.15±0.02)ps的时间常数,说明丙酰基离子来自于母体的解离性电离.乙酰基离子的时间曲线拟合得到四个时间常数:τ1=(2.40±0.15)ps,τ2=(1.10±0.25)ps,τ3=(0.08±0.02)ps,τ4=(17.72±0.80)ps,分别对应于S2→S1的内转换,S1态生成CH3CO()的初步解离,CH3CO()快速内转换为CH3CO(),以及CH3CO()基态上的二次解离.丁酮分子α-C-C键的解离存在分子内振动能量再分配(IVR)与势垒解离两种竞争的解离通道,但在该实验条件下,我们认为是通过分子内振动能量再分配通道发生解离的结果.
时间分辨质谱,超快动力学,泵浦-探测,光解离
1 引 言
脂肪酮作为一类重要的有机化合物,数十年来被进行了广泛深入的研究[1-20].脂肪酮含有化学性质活泼的羰基,容易光解或与OH自由基发生反应[1,2].主要的光解过程是nπ∗轨道上的电子被激发后,与羰基相邻的C-C键发生解离,这类反应也称为Norrish I型反应[3,4].随着飞秒化学的发展,酮类分子的Norrish I型反应机理得到了进一步研究[5-12].目前对丁酮分子的Norrish I型反应研究报道相对较少[5-8],而事实上丁酮分子的α位置具有一个甲基和一个乙基,在Norrish I型反应中,能够完全分辨分子中与羰基相邻的两个α-C-C键,对于认识酮类分子的α-C-C键的解离反应机理具有积极作用.
丁酮的真空紫外吸收谱显示[13],丁酮在180-200 nm范围内存在一个对应于第二电子激发单重态S2(n,3s)态跃迁的吸收带.该吸收带明显的振动结构意味着S2(n,3s)并非直接解离态,而是存在预解离过程.研究丁酮分子S2(n,3s)激发态的弛豫动力学,有助于探明Norrish I型光解反应的断键机理.我们的实验通过飞秒时间分辨的飞行时间质谱技术[14,15]实时跟踪了丁酮初始态和中间体的演化,研究S2态的光解动力学特征.在真空环境下,195.8 nm的飞秒激光将丁酮分子泵浦到S2态,然后用800 nm的飞秒激光作为探测光,相对于泵浦光经过一定的时间延迟后作用到S2态的丁酮分子上将其电离,形成的离子通过一个无场飞行管到达探测器.通过监测离子信号强度随延迟时间的变化,从而获得激发态的衰减寿命等动力学信息.
2 实 验
实验中使用的激光器是一套自锁模钛:蓝宝石飞秒激光系统(Coherent Int.,美国),中心波长为800 nm,最大单脉冲能量为4.5 mJ,线宽8.6 nm,带宽100 fs,频率1 kHz.该激光器配置了TOPAS(traveling wave optic parametric amplifier system)系统(Coherent Int.,美国),在单脉冲能量约为1 mJ的飞秒激光泵浦下,输出波长在240-2600 nm范围内可调的激光.实验时调节TOPAS产生260 nm的输出光,与800 nm的基频光通过BBO晶体混频后产生195.8 nm的和频光,将其作为泵浦光,单光能量为每脉冲0.2µJ,实验光路如图1所示.探测光则直接使用800 nm的基频光,单光能量为每脉冲50µJ.泵浦光与探测光皆为竖直偏振,平行于探测器表面.泵浦光和探测光通过合束片合并后直接进入束源室作用在分子束上.泵浦和探测脉冲之间的时间延迟由计算机控制的线性精密平移台(PI,M-126.GG1,德国)改变光路中平移量Δx的值进行精确控制.此外,根据实验的需要,在泵浦和探测光路中加入衰减片,适当地衰减光强,不仅能够减小背景信号,也有利于调节泵浦与探测光之间的强度比例,获得更好的信噪比.
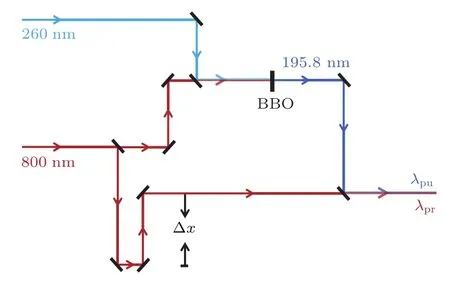
图1 实验光路示意图 TOPAS产生260 nm的输出光,与800 nm的基频光和频产生195.8 nm的泵浦光,探测光是800 nm的基频光Fig.1.Diagram of the experimental pump-probe light path.The pump pulse at 195.8 nm is obtained by the sum frequency mixing of the compressed optical parametric amplifier(OPA)output at 260 nm with the fundamental pulse at 800 nm.The probe pulse is 800 nm fundamental laser.
实验装置包括真空系统、超声分子束装置、飞行时间质谱仪,和一个二维位置敏感探测器[16,17].实验样品分子丁酮(99%纯度),使用前无需进一步纯化.丁酮经氦气携带通过孔径为0.5 mm的脉冲阀(Parker,general valve,美国)绝热膨胀产生脉冲超声分子束.分子束经skimmer限束和准直后进入电离室,与泵浦和探测激光束垂直相交,激光作用后产生的离子通过µ金属屏蔽的自由飞行区(360 mm),被二维位置敏感探测器接收,通过光电倍增管采集荧光屏上的光信号,输送到示波器上获得质谱信号,由计算机进行监控和处理.
丁酮经过超声膨胀后,极易形成团簇[18],实验中调节分子束的时序,使激光作用于分子束的前沿,能够有效避免产生团簇离子.整个系统的时序控制利用一台多通道时序控制器(DG535,stanford research systems)实现.
3 结果与讨论
图2为丁酮分子的双光作用下的飞行时间质谱. 从质谱图上看出,在双光共同作用下,出现较强的母体离子(72 aum)和光解碎片离子CH3CH2CO+(57 aum),CH3CO+(43 aum)信号.如此高的双光增益表明,195.8 nm泵浦光确实将丁酮分子激发到了3s里德堡态,与195.2 nm的理论计算值相符[19],并且所反映的都是单光子泵浦到3s态的动力学过程,因为丁酮的电离势为9.54 eV[19],195.8 nm的能量为6.33 eV,如果是双光子泵浦,分子就直接电离了.CH3CH2CO+和CH3CO+的出现势分别为9.9[20]和10.32 eV[21],这意味着195.8 nm激发丁酮到S2(n,3s)里德堡态后,在不少于3个探测光子的作用下出现这些瞬态离子.

图2 195.8和800 nm双光作用下丁酮的飞行时间质谱Fig.2.The time-of-flight mass spectrometry(TOFMS)of butanone by 195.8 and 800 nm.
图3给出了双光作用下母体及典型碎片离子随泵浦-探测时间延迟的变化曲线及拟合结果.如图3(a)所示,母体瞬态可拟合为单指数衰减,时间常数τa=(2.23±0.02)ps,是S2态到第一电子激发单重态S1态内转换(IC)的时间,表示丁酮S2态带源寿命.而且,母体瞬态单一指数的衰减意味着S2→S0态内转换以及S2→T1系间窜越(ISC)在该实验结果的分析中可以忽略.图3(b)中丙酰离子相对强度迅速增加,得到的时间常数τb=(2.15±0.02)ps与母体离子拟合得到的衰减时间十分接近,这意味着丙酰离子完全来自于母体离子的解离性电离,反映的是S2→S1内转换过程,τb是内转换所需要的时间.

图3 母体及典型碎片离子的变化曲线 (a)CH3COCH2CH(72 amu);(b)CH3CH2CO+(57 amu);(c)CH3CO+(43 amu).圆圈表示实验数据,不同颜色的实线代表拟合结果Fig.3.Typical transient obtained by monitoring the mass signal of butanone parent ion and fragment ions:(a)CH3COCH2CH3+(72 amu);(b)CH3CH2CO+(57 amu);(c)CH3CO+(43 amu).Circles represent the experimental data,and the colored lines are the fitting results.
不同于丙酰离子,乙酰离子(图3(c))的时间线型展现出更为丰富的动力学特征.除了类似于母体离子的τ1组分,还需要再添加其他三个时间组分才能很好地拟合实验结果.拟合得到四个时间组分分别为τ1=(2.40±0.15)ps,τ2=(1.10±0.25)ps,τ3=(0.08±0.02)ps,τ4=(17.72±0.80)ps,这四个组分的相对比值分别为A1(τ1)=0.46,A2(τ2)=0.01,A3(τ3)=0.01,A4(τ4)=0.05. 由于丁酮对应S2(n,3s)的吸收带具有明显的振动结构[13],这说明S2(n,3s)并非直接解离态,而是存在预解离过程.处于S2里德堡态带源附近的丁酮分子,除了在探测光作用下直接被电离生成母体离子外,也可能通过内转换弛豫到S1态,并快速地随机分配S2与S1态之间能量差对应的振动能.处于S1态高振动态的丁酮分子,可能存在电离、解离性电离和两个α-C-C键的解离反应.我们的研究结果显示(图3),CH3CO-CH2CH3键会发生初次解离生成CH3CO()和CH2CH3,经历的时间为τ2=(1.10±0.25)ps,代表了处于S1态高振动态上的分子发生初步解离生成激发态的CH3CO()基团所需要的时间.
热的乙酰基CH3CO()解离过程多年来一直是研究的热点[22-26].我们根据实验结果(图3(c)),分析认为丁酮S1态初步解离的产物CH3CO(),类似于母体离子的S2→S1内转换过程,通过CCO弯曲振动,迅速内转换为基态的CH3CO(),所需时间为τ3=(0.08±0.02)ps,也就是说τ3代表了激发态的CH3CO()基团内转换至基态CH3CO()基团所需要的时间.随后,基态CH3CO()基团继续发生二次解离生成CO和CH3,所需要的时间为τ4=(17.72±0.80)ps.丁酮被激发到S2态后的弛豫过程示意图如图4所示.丁酮的α-C-C光解离过程受到很多因素的制约,包括探测光的能量、内转换时间、解离势垒以及CCO弯曲运动等.如分子的初步解离和→内转换都是飞秒超快过程,受到缓慢的S2→S1内转换影响,τ2,τ3具有很大的绝对误差.

图4 丁酮分子的弛豫过程示意图Fig.4.Schematic relaxation processes of butanone.
对于丁酮分子的Norrish I型反应,α-C-C键的解离存在分子内振动能量再分配(IVR)与势垒解离两种竞争的解离方式[10,11].我们的实验结果显示,初步解离和二次解离的时间都达到了皮秒量级,尤其是二次解离的时间高达17.72 ps.对于丁酮分子的初步光解离,通过S2→S1内转换获得的大部分振动能量会首先集中于CCO弯曲模式.800 nm的探测光作用于处于S1热振动态的分子时,1.55 eV的探测光子能量无论对CH3CO-CH2CH3键还是CH3-COCH2CH3键,都不能使其发生解离,但却容易被CCO弯曲振动吸收,并进行分子内能振动能量再分配.随着吸收光子的增加,α-C-C键的振动能量在达到3.54 eV时,CH3CO-CH2CH3键的解离反应发生.

丁酮分子光解离的复杂动力学过程可以通过反应通道(1)所示的动力学模型近似地给出,hν为泵浦光子能量.其中二次解离长达17.72 ps的解离时间很可能是分子内振动能量再分配通道发生解离的结果.而且,分子内振动能量再分配也造成了二次解离时间远大于初步解离.初步解离时,各振动模式的振动能量较小,分子内振动能量再分配过程显得缓慢,使得光子能量更容易集中于CCO弯曲振动,解离会在短时间内发生.在二次解离时,由于之前积累了很大的振动能量,分子内振动能量再分配的速度也相应地加快,CH3CO()吸收的探测光子能量容易耗散为其他振动模式,CCO弯曲振动能量达到解离阈值就需要更长的时间.
4 结 论
195.8 nm泵浦光将丁酮分子激发到S2里德堡态后,再吸收3个800 nm探测光子被电离.母体离子的时间线型拟合得到一个约为2.23 ps时间常数,归属为S2→S1内转换的时间.丙酰离子展现出母体离子类似的动力学特征,说明它完全来自于母体离子的解离性电离过程.但乙酰离子的时间线型表现出更丰富的动力学特征,拟合得到四个时间组分,τ1=(2.40±0.15)ps,τ2=(1.10±0.25)ps,τ3=(0.08±0.02)ps,τ4=(17.72±0.80)ps,分别对应S2内转换至S1,S1发生初步解离生成CH3CO(),CH3CO()内转换至CH3CO(),CH3CO()发生二次解离生成CO和CH3的时间.其中S2→S1内转换后,处于S1态高振动态的丁酮分子吸收探测光子后,解离方式上存在分子内振动能量再分配与势垒解离的竞争.由于较小的探测光子能量(约1.55 eV)容易被CCO弯曲振动吸收,两个竞争性的解离通道只有CCO弯曲振动导致的解离发生.而且,键能最低的CH3CO-CH2CH3键具有解离优先权,生成CH3CO()和CH2CH3,所需时间约为1.10 ps.CH3CO()通过CCO弯曲振动,在约0.08 ps的时间内迅速内转换为CH3CO().基态的CH3CO()与S1态的初步解离类似,通过分子内振动能量再分配通道发生解离,生成CO和CH3,解离时间约为17.72 ps.
感谢中国科学院武汉分院物理与数学研究所波谱与原子分子物理国家重点实验室的全体同仁在实验和论文写作上给予的热心帮助.
[1]Vacher J R,Jorand F,Blin-Simiand N,Pasquiers S 2008Int.J.Mass Spectrom.273 117
[2]Mu Y,Mellouki A 2000J.Photochem.Photobiol.A134 31
[3]Haas Y 2004Photochem.Photobiol.Sci.3 6
[4]Noyes W A,Porter G B,Jolley J E 1956Chem.Rev.56 49
[5]Diau E W G,Kötting C,ZewailA H 2001ChemPhysChem2 273
[6]Diau E W G,Kötting C,ZewailA H 2001ChemPhysChem2 294
[7]Diau E W G,Kötting C,Sølling T I,Zewail A H 2002ChemPhysChem3 57
[8]Sølling T I,Diau E W G,Kötting C,Feyter S D,Zewail A H 2002ChemPhysChem3 79
[9]Chen W K,Ho J W,Cheng P Y 2003Chem.Phys.Lett.380 411
[10]Chen W K,Ho J W,Cheng P Y 2005J.Phys.Chem.A109 6805
[11]Chen W K,Cheng P Y 2005J.Phys.Chem.A109 6818
[12]Chen W K,Ho J W,Cheng P Y 2005Chem.Phys.Lett.415 291
[13]O Toole L,Brint P,Kosmidis C,Boulakis G,Tsekeris P 1991J.Chem.Soc.,Faraday Trans.87 3343
[14]Loo R O,Hall G E,Houston P L 1989J.Chem.Phys.90 4222
[15]Zou P,McGivern W S,North S W 2000Phys.Chem.Chem.Phys.2 3785
[16]Wei Z,Zhang F,Wang Y,Zhang B 2007Chin.J.Chem.Phys.20 419
[17]Zhang R R,Qin C C,Long J Y,Yang M H,Zhang B 2012Acta Phys.-Chim.Sin.28 522
[18]Sun C K,Hu Z,Yang X,Jin M X,Hu W C,Ding D J 2011Chem.Res.Chinese Universities27 508
[19]Shen L,Zhang B,Suits A G 2010J.Phys.Chem.A114 3114
[20]Traeger J C 1985Org.Mass Spectrom.20 223
[21]Traeger J C,McLouglin R G,Nicholson A J C 1982J.Am.Chem.Soc.104 5318
[22]Owrutsky J C,Baronavski A P 1998J.Chem.Phys.108 6652
[23]Mordaunt D H,Osborn D L,Neumark D M 1998J.Chem.Phys.108 2448
[24]Shibata T,Li H Y,Katayanagi H,Suzuki T 1998J.Phys.Chem.A102 3643
[25]Deshmukh S,Myers J D,Xantheas S S,Hess W P 1994J.Phys.Chem.98 12535
[26]Kroger P M,Riley S J 1977J.Chem.Phys.67 4483
PACS:33.80.Gj,33.20.Lg,82.80.Ms,82.30.Lp DOI:10.7498/aps.66.023301
Ultrafast photodissociation dynamics of butanone in 3s Rydberg state∗
Luo Jin-Long1)Ling Feng-Zi2)Li Shuai2)Wang Yan-Mei2)Zhang Bing2)†
1)(Department of Physical Science and Technology,Kunming University,Kunming 650214,China)
2)(State Key Laboratory of Spectroscopyand Atomic and Molecular Physics,Wuhan Institute of Physics and Mathematics,Chinese Academy of Sciences,Wuhan 430071,China)
12 September 2016;revised manuscript
1 November 2016)
The initiation and subsequent control or exploration study of chemical transformation in real time by using ultrashort laser pulses aim at femtochemistry.The real-time investigations of ultrafast dynamics of excited molecules in gas and condensed phases have attracted a great deal of attention over the last two decades.As a kind of important organic compound,aliphatic ketone is an area of much interest for many research fields,especially for atmospheric photochemistry.Via photodissociation reaction,it can release carbonyl radical whose chemical character is active and can react with hydroxyl easily.As a typical aliphatic ketone,butanone has been a research focus over the past decades.The ultrafast dissociation dynamics of butanone after excitation to the second electronically excited state(S2)with a 195.8 nm pump pulse is studied by the femtosecond pump-probe technique combined with the time-of-flight mass spectrometry(TOF-MS).Time-resolved mass spectrometry(TRMS)has proven to be a powerful technique to study the ultrafast dynamics of excited states in molecules.In this technique,the MCP detector is capable of recording time-resolved ion yield measurements of different cations by monitoring the current output directly from the anode by using an oscilloscope.This enables a time-of-flight mass spectrum to be recorded at each delay time,which is controlled by a delay stage,and the measured total signal is then integrated,yielding a time-resolved ion yield transient,which is conducted by LABVIEW software.The pump wavelength in this work is set to be 195.8 nm and the probe laser wavelength is centered at 800 nm.The complex ultrafast dynamics in butanone with 3s Rydberg state excitation and its possible decay paths and following dissociation mechanism are given.Experimental results show that the Norrish I type dissociation kinetics of butanone exhibit rich features,for it has a methyl group and an ethyl group atαposition.The decay time constant of the parent transient is approximately 2.23 ps±0.02 ps.There is only one time constant of 2.15 ps±0.02 ps for the fitting of the propionyl transient.The best fit of acetyltransient is obtained with four time constants:τ1=(2.40±0.15)ps,τ2=(1.10±0.25)ps,τ3=(0.08±0.02)ps,andτ4=(17.72±0.80)ps,corresponding to S2→S1internal conversion,the primary dissociation of the S1state generating CH3CO(),→internal conversion and secondary dissociation of CH3CO()respectively.Two competitiveα-CC bond dissociation processes are observed and discussed.They are dissociation channels through intramolecular vibrational energy redistribution(IVR)and/or by getting over the dissociation barrier inα-cleavage of butanone.But hereunder the condition of this experiment,the dissociation is the result of IVR.
time-resolved mass spectrum,ultrafast dynamics,pump-probe,photodissociation
:33.80.Gj,33.20.Lg,82.80.Ms,82.30.Lp
10.7498/aps.66.023301
∗国家重点基础研究发展计划(批准号:2013CB922200)和国家自然科学基金(批准号:21573279,21273274)资助的课题.
†通信作者.E-mail:bzhang@wipm.ac.cn
*Project supported by the National Basic Research Program of China(Grant No.2013CB922200)and the National Natural Science Foundation of China(Grant Nos.21573279,21273274).
†Corresponding author.E-mail:bzhang@wipm.ac.cn

