气雾剂包装材料中多环芳烃的提取及迁移量测定
叶烨
摘 要 目的:建立同时测定气雾剂包装材料中17种多环芳烃的提取及迁移量的GC-MS方法。方法:采用HP-5MS色谱柱,程序升温, 质谱检测器采用电子轰击源(EI),定量方法采用SIM模式。结果:17种多环芳烃在5~200 ng/ml浓度范围内均线性良好,检测限为2 ng/ml,回收率在74%~111%之间。
关键词 气雾剂包装材料 多环芳烃 提取 迁移
中图分类号:R954 文献标识码:A 文章编号:1006-1533(2017)13-0070-04
Extraction of polycyclic aromatic hydrocarbon in metered dose inhaler packaging material and the determination of its migration
YE Ye*
(Shanghai Food and Drug Packaging material Control Center, Shanghai 201203, China)
ABSTRACT Objective: To establish a GC-MS method for simultaneous determination the extraction and migration of 17 PAHs in metered dose inhaler packaging material. Methods: A GC-MS method was established based on a column of HP-5MS with a programmed column temperature rise. The EI ion source was used for MS detector, and SIM model was used in quantification. Result: The standard curves of 17 PAHs were linear over the range of 5~200 ng/ml with detection limit of 2 ng/ml. The average recovery was in the range of 74%~111%.
KEY WORDS metered dose inhaler packaging material; polycyclic aromatic hydrocarbon (PAHs); extraction; migration
多環芳烃(PAHs)是由两个或多个苯环相互键接而形成的碳氢化合物,包括150余种化合物。其中苯并[α]芘为代表的16种PAHs因具有极强的致癌、致畸、致突变性而得到了广泛的关注。欧盟2005年发布的《关于多环芳烃的指令》(2005/69/EC)限制了16种PAHs的使用。德国、美国、中国国标中均有关于PAHs的限量。PAHs在塑料和橡胶制品中的来源可能是加工过程的添加和原材料的残留,如橡胶制品中含硫的硫化剂体系。现在用于多环芳烃的测定方法主要有GC-MS法[1-3],GC-MSMS法[4-6],HPLC法[7-9]等,这些方法主要用于测定饮用水、土壤、食品、气雾剂中的多环芳烃。
FDA在1999年出版的《人用药品和生物制品的包装容器系统》工业指导原则中,吸入气雾剂是给药途径关注度最高和包装制剂间相互作用可能性最高的药品,因此属于关注度最高的药品范畴。FDA又为这类产品提供了两个相关的指导原则。而气雾剂使用的包装材料系统非常复杂,主要包括耐压容器和阀门系统。同时,现有研究文献表明[10-11],气雾剂药品中含有提取性极强的溶剂,如氢氟烷烃(HFA)类抛射剂、乙醇等。尤其对于溶液性的气雾剂,一般使用醇类为潜溶剂,这些溶剂对于气雾剂包装材料中,特别是阀门系统中的多环芳烃物质有良好的溶解性能。因此研究建立了同时测定17种多环芳烃的GC-MS法,方法简单可行,可用于不同气雾剂包装材料中多环芳烃的提取和迁移研究,也可进一步扩展至其他药品包装材料的检测。
1 材料和方法
1.1 材料
阀门1(由A制药企业提供),阀门2(由B制药企业提供),阀门3(由C制药企业提供),苯环喹溴胺定量吸入气雾剂(采用阀门1包装,批号201412001,由A制药企业提供),吸入用布地奈德混悬液(采用阀门2包装,批号141126001,由B制药企业提供),沙美特罗替卡松气雾剂(采用阀门3包装,批号1502001T,由C制药企业提供),丙酸氟替卡松吸入气雾剂(采用阀门3包装,批号1504004T,由C制药企业提供);乙腈(99.9%,批号:JA040230,Merck公司),二氯甲烷(99.8%,批号:#WXBC3464V,Sigma-Aldrich公司);EPA16种多环芳烃混合对照液(2.0 mg/ml,批号214101348,AccuStandard);苯并[e]芘(99.9%,批号40516)、苊-d10(98.2%,批号20525)、菲-d10(98.4%,批号20525)、蒽-d10(98.0%,批号40612)均购自Dr. Ehrenstorfer GmbH公司;苯并[α]芘-d12(101.3 mg/L,批号233834,O2Si公司);纯化水由Milli-Q系统制备。
1.2 仪器
安捷伦GC/MS联用仪7890A/5975C(Agilent公司),电子天平XS205(梅特勒-托利多上海有限公司)。
1.3 溶液配制
1)内标储备溶液的配制 分别取苊-d10 10 mg、菲-d10 10 mg、蒽-d10 10 mg,精密称定,置于100 ml量瓶中,用乙腈稀释至刻度,得到浓度约为100 mg/L的苊-d10、菲-d10、蒽-d10内标对照储备液。
取内标对照储备液1. 00 ml至10 ml容量瓶中,取苯并[α]芘-d12对照品一支,置于同一10 ml量瓶中,用甲醇-乙腈混合溶液(體积为1∶9)稀释至刻度,得到浓度约为10 mg/ L的苊-d10、菲-d10、蒽-d10、苯并[α]芘-d12内标混合标准溶液。
2)对照溶液的配制 取苯并[e]芘10 mg,精密称定,置于100 ml量瓶中,用乙腈稀释至刻度得到浓度为0.1 mg/ml的苯并[e]芘标准溶液;取0.1 mg/ml的苯并[e]芘标准溶液1.0 ml和EPA16种多环芳烃混合溶液(2.0 mg/ml)50 ml至10 ml量瓶中,用乙腈稀释至刻度得到浓度约为10 mg/L的17种多环芳烃混合溶液。分别取10 mg/L的17种多环芳烃混合溶液适量,并精密加入10 mg/L的内标混合标准溶液50 ml,用乙腈稀释得到四种内标浓度约为50 mg/L的17种多环芳烃系列浓度对照溶液。
1.4 GC-MS条件
进样口温度为300 ℃,不分流进样; HP-5MS毛细管色谱柱(0.25 mm×30 m,0.25 mm),载气为氦气,流速为1.0 ml/min;柱温:50 ℃保持1 min,25 ℃/min升至200 ℃,再7 ℃/min升至315 ℃,保持1.5 min。进样量:1 ml。色谱与质谱接口温度:280 ℃,电离方式:电子轰击源(EI),监测方式:SIM模式,离子源温度:230 ℃,四级杆温度:150 ℃,电离能量:70 eV,溶剂延迟:5 min。
1.5 样品液制备
1)提取试验液制备 取阀门10个剪碎,置于索氏提取器中,加二氯甲烷100 ml索氏提取20 h。取10 ml二氯甲烷提取液至烧杯中用氮气吹干,用适宜乙腈少量多次洗涤烧杯至5 ml量瓶中,每瓶分别精密加入10 mg/L的内标混合标准溶液25 ml,用乙腈定容,摇匀。
2)迁移试验试验液制备 取样品1瓶经液氮冷冻后,在定量阀门上凿开一个小口缓慢放气(避免喷出),待抛射剂挥尽后,用切割器切开铝罐,将药液转移至10 ml量瓶中,用乙腈分次清洗铝罐内壁,洗液合并至10 ml量瓶中,每瓶分别精密加入10 mg/L的内标混合标准溶液50 ml,用乙腈稀释至刻度,摇匀。
2 结果
2.1 专属性及系统适用性试验
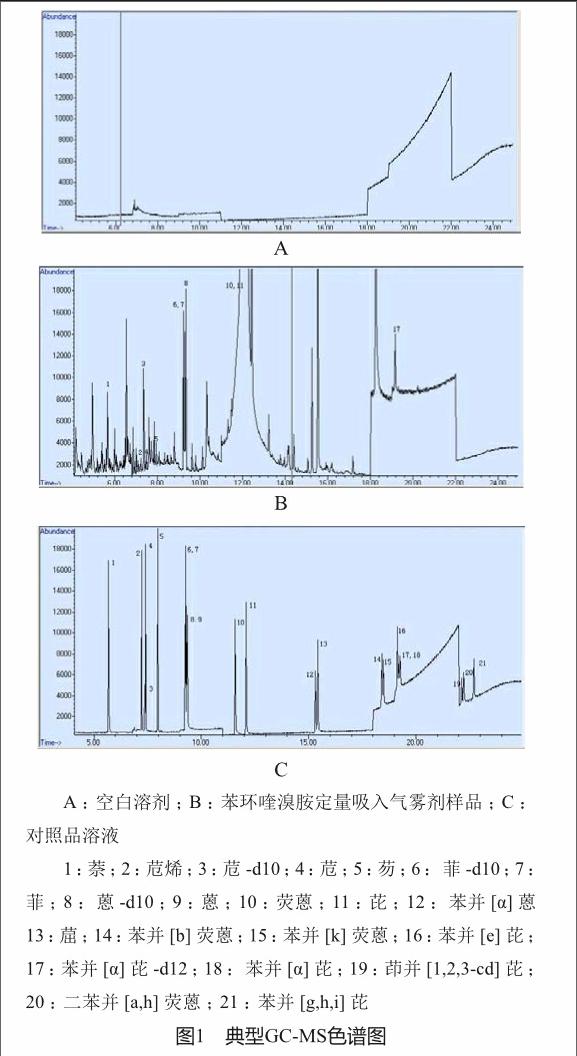
取二氯甲烷及乙腈作为空白溶液、对照品溶液及空白药品溶液,分别进样,记录谱图,结果显示,各对照品分离度良好,空白溶剂及药品无干扰(图1)。
2.2 线性试验
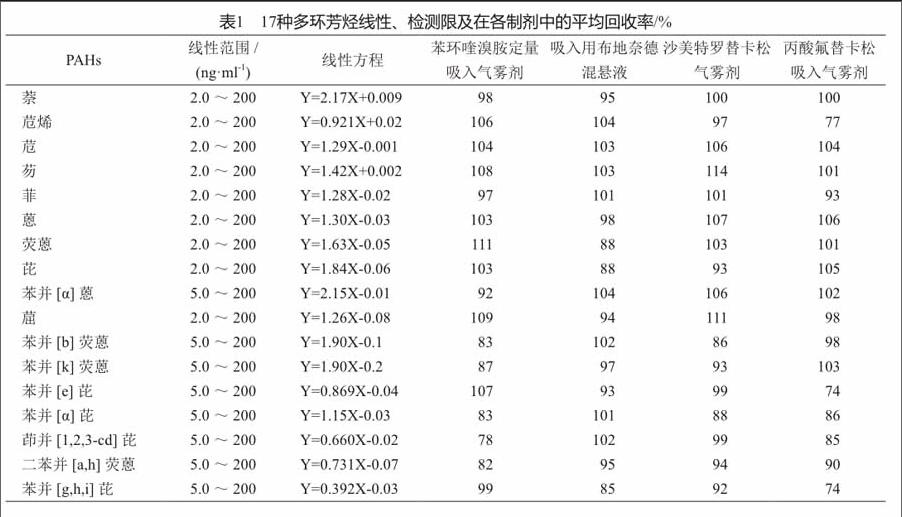
取对照溶液,分别进样,记录谱图。萘、苊、芴以苊-d10为内标计算,苊烯、菲以菲-d10为内标计算,蒽、荧蒽、芘、?、苯并[e]芘、苯并[g,h,i] 芘以蒽-d10为内标计算,苯并[α]蒽、苯并[b]荧蒽、苯并[k]荧蒽、苯并[α]芘、茚并[1,2,3-cd]芘、二苯并[α,h]荧蒽以苯并[α]芘-d12为内标计算。以各组分与内标峰面积的比值(Y轴)对各组分与内标的相对浓度(X轴)进行线性回归,结果见表1。结果显示17种多环芳烃在5~200 ng/ml的范围内,线性良好,相关系数均大于0.99。检测限均不大于2 ng/ml,灵敏度良好。
2.3 回收率试验
取相当于1个药品包装的空白药液各4份,置于10 ml量瓶中,均用微量注射器注入内标工作溶液50 ml,其中3个分别用微量注射器注入17种多环芳烃混合溶液适量,混匀,用乙腈稀释定容,分别作为空白测试溶液、低、中、高浓度回收率测试溶液。各平行制备3份,分别进样,记录谱图。回收率结果见表1,结果表明在苯环喹溴胺定量吸入气雾剂、吸入用布地奈德混悬液、沙美特罗替卡松气雾剂、丙酸氟替卡松吸入气雾剂四种药品中,17种多环芳烃的回收率良好。
2.4 稳定性试验
将浓度为100 ng/ml的混合对照溶液,分别在室温放置0、72 h,分别进样3次,记录谱图,计算各待测物与内标峰面积比值,代入表1标准曲线线性方程计算0、72 h时的浓度,计算各浓度结果的RSD值。结果表明RSD值均小于10%,17种多环芳烃的日间稳定性良好。
2.5 样品测定结果
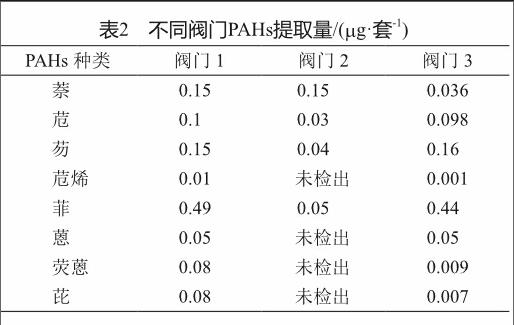
取不同阀门系统的提取液,各平行制备2份,分别进样,记录谱图。结果见表2。
取不同阀门系统包装药液的迁移试验液,平行制备2份,分别进样,记录谱图。结果见表3。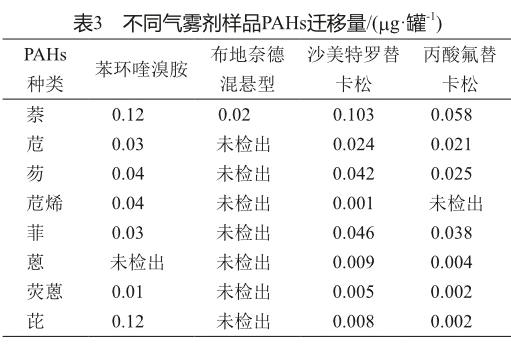
3 讨论
根据表2,表3的数据结果可知,气雾剂阀门提取液中主要存在萘、苊烯、苊、芴、菲、蒽、荧蒽、芘这几种PAHs,不同药品的迁移结果也表明了这几种PAHs的存在。根据德国食品及日用品法规(German Food Stuff and Consumer Goods Law)中规定与食品接触材料苯并[α] 芘不得检出(0.2 mg/kg),16种受关注的PAHs总量不得检出(0.2 mg/kg)。本次试验检出的这8中PAHs虽然不像苯并[α]芘这样有强致癌性,但考虑到是结构类似物,根据ICH M7中可接受标准1.5 mg/天对应于十万分之一的生命时长患癌风险,本次试验检出的PAHs最大迁移量为0.2 mg/罐,按气雾剂每天4揿,每罐标示量为120揿计算[12-13],最大的暴露量为0.007 mg/d,可认为这些药品中的多环芳烃的迁移量是安全的。
本次试验主要对GC-MS条件进行了摸索,通过优化进样口温度和离子源温度,改善了多环芳烃中茚并[1,2,3-cd]芘、二苯并[α,h]荧蒽、苯并[g,h,i] 芘等高沸点组份的灵敏度。通过对于色谱柱的选择及程序升温方法的优化实现了17种多环芳烃的分离以及多环芳烃与药品主峰的分离。根据文献检索结果,GC-MS 法测定多环芳烃多用于水、土壤、食品等基质。本研究首次建立方法用于气雾剂包装材料中多环芳烃的提取试验及多种有代表性的气雾剂药品基质中迁移试验,具有良好的通用性。为进一步进行不同药品包装材料中多环芳烃的提取及迁移研究奠定了良好的基础。
参考文献
[1] 张婕. 固相微萃取与5975T低热容GC-MS联用快速分析水中多环芳烃[J]. 分析仪器, 2011, 6: 17-23.
[2] 毕鸿亮, 张浩原, 孙翠香, 等. 蔬菜中多环芳烃的GC-MS分析[J]. 分析测试学报, 2007, 26(4): 530-532.
[3] 秦玉荣, 余翀天, 梁丽娜. CSR-GC-MS测定环境水体中的18种多环芳烃[J]. 环境化学, 2016, 35(3): 601-603.
[4] Meng Qiao, Weixiao Qi, Huijuan Liu, et al. Simultaneous determination of typical substituted and parent polycyclic aromatic hydrocarbons in water and solid matrix by gas chromatography-mass spectrometry[J]. J Chromatogr A, 2013, 1291: 129-139.
[5] 王海娇, 王娜, 宋丽华, 等. GC-MS-MS法测定土壤中的16种多环芳烃[J]. 分析试验室, 2010, 29(S1): 412-414.
[6] 孙谦, 王立闱, 范军, 等. GC-MS/MS测定生活饮用水中16种多环芳烃[J]. 环境化学, 2016, 35(3): 604-606.
[7] GB/T15439-1995. 环境空气苯并[α]芘的测定高效液相色谱法[EB/OL]. [2017-05-30]. http://www.bzxz.net/bzxz/14279. html.
[8] 馬娟, 叶晓霞, 杨永健, 等. 定量吸入气雾剂中多环芳烃的HPLC-UV-FLD法测定[J]. 中国医药工业杂志, 2014, 45(2): 155-158.
[9] 刘桂明, 邓义敏. 二极管阵列检测器和荧光检测器联合测定应用水中多环芳烃[J]. 中国卫生检验杂志, 2007, 17(11): 1943-1945.
[10] 丁立. 张钧寿, 游一中. 等. 药用气雾剂抛射剂的替代:从CFC到HFA[J]. 药学进展, 2001, 25(2): 93-95.
[11] 廖永红. 曾宪明. 以氢氟烷为抛射剂的定量吸入气雾剂研究进展[J]. 药学学报, 2006, 41(3): 197-202.
[12] 刘元. 甾体激素类鼻喷雾剂容器密闭系统相容性研究[D].上海: 上海医药工业研究院, 2015.
[13] 叶晓霞. 吸入气雾剂容器密闭系统的相容性研究[D]. 上海: 上海医药工业研究院, 2014.

