阿帕替尼单药治疗进展期非小细胞肺癌疗效观察
毕金玲 刘海源 黄勇
阿帕替尼单药治疗进展期非小细胞肺癌疗效观察
毕金玲 刘海源 黄勇
目的 探索阿帕替尼单药治疗进展期非小细胞肺癌(NSCLC)的疗效和安全性。方法 选取进展期NSCLC患者共65例。随机分为对照组(n=30),行多西他赛化疗;治疗组(n=35),行阿帕替尼治疗。对两组患者进行疗效和毒副反应评价。结果 对照组完全缓解0例,部分缓解3例,稳定11例,进展16例,治疗组完全缓解0例,部分缓解6例,稳定17例,进展12例,P<0.05。阿帕替尼毒副反应可控,较对照组毒副反应发生率显著降低。结论 阿帕替尼对进展期NSCLC具有一定疗效和可耐受的毒性。
阿帕替尼;非小细胞肺癌;多西他赛;进展期
肺癌为常见恶性肿瘤,据统计,2015年美国新增肺癌病例221200例,死亡158040例,占肿瘤死亡病例27%[1]。肺癌可分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)两大类,其中非小细胞肺癌又分为腺癌和鳞癌两种亚型。临床实践中,非小细胞肺癌的标准一线治疗方案为铂类药物联用方案[2]。美国批准用于治疗进展期NSCLC二线治疗的靶向药物主要为雷莫芦单抗和厄洛替尼[3-6]。靶向治疗药物的出现,如单克隆抗体,小分子激酶抑制剂等使得抗肿瘤治疗方式更加个体化、特异化[7]。新近开放的治疗药物定位于肿瘤的免疫学机制[8]。阿帕替尼作为分子靶向药物目前已经广泛应用于消化道恶性肿瘤,尤其在胃癌和肝癌的多线治疗中。但是,阿帕替尼对于其它恶性肿瘤的治疗疗效和安全性观察尚不完全明确。本研究通过对非小细胞肺癌患者中应用阿帕替尼单药治疗的疗效评估,初步了解其对于其它肿瘤的作用效应。
资料与方法
一、研究对象
选取2014年1月-2016年3月间,我院收治的65例诊断为复发性非小细胞肺癌患者作为研究对象。患者入选标准为:① 年龄18岁-70岁之间,男女不限;② 经病理组织学和/或细胞学明确诊断为NSCLC;③ EGFR野生型的非小细胞肺癌患者;④ 具有可测量病灶(螺旋CT扫描大于10mm,满足RECIST1.1标准);⑤ 二线治疗失败的晚期非小细胞肺癌患者(注:a.治疗失败的定义:治疗过程中疾病进展或治疗结束后肿瘤复发转移,或出现不可耐受的毒性;b.进展期疾病每一线的治疗包括用药时间≥1个周期或者更长时间的一种或者多种化疗药物);⑥ 患者经评估KPS评分70分以上;⑦ 预计生存期≥3个月。排除标准:① 终末期患者无法耐受治疗;② 既往合并慢性基础性疾病经评估可能对于治疗产生干扰;③ 合并严重肝肾功能损害。评估标准:根据1.1版RECST标准,完全缓解(CR),部分缓解(PR),稳定(SD)和进展(PD),PR+CR为客观缓解效率(0RR),PR+CR+SD为疾病控制率(DCR)。
二、研究方法
65例患者随机分为对照组和治疗组,对照组30例患者接受多西他赛75mg/m2d1化疗,21天为一周期。两个用药周期为一个观察周期,两个观察周期为一个疗效评价周期。治疗组35例患者接受阿帕替尼治疗,剂量500mg/d,连用28天为一个给药和观察周期,两个观察周期为一个疗效评价周期。患者每周行血常规及生化指标的全面检测,评估药物不良反应(AE)。当出现病情进展,严重毒性反应影响远期治疗以及患者主动退出研究时,治疗予以终止。
三、统计学方法
应用SPSS 19.0软件进行数据分析,两组间比较采用χ2检验,P<0.05为差异有统计学意义。
结 果
一、患者疗效评估结果
治疗组中,客观缓解率ORR(17.14%)和疾病控制率DCR(65.71%)均显著高于对照组,P<0.05,(见表1)。
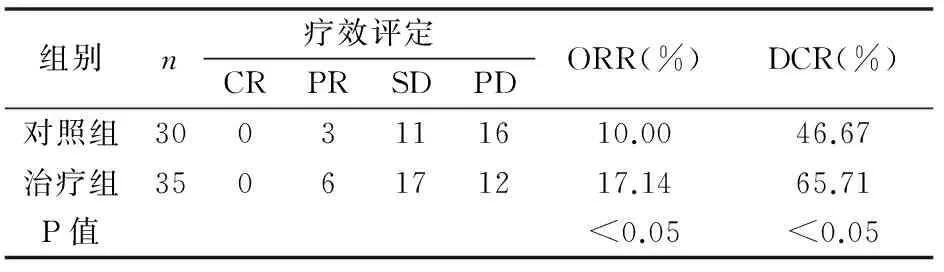
表1 患者疗效评估结果
二、毒性反应评估结果
65例患者均未出现治疗相关性死亡。对照组中血液系毒性、乏力、食欲下降及高胆红素血症反应均显著升高。治疗组毒副反应发生率均较低,且未发生Ⅳ度严重不良反应,所有不良事件都是可耐受和可控制的,P<0.05。(见表2)。
讨 论
近年来,对于肿瘤控制的研究方向主要集中在内皮生长因子(VEGF)通路的阻断。靶向治疗机制在于降低激活的和游离状态的VEGF浓度并切断VEGF与其受体(VEGFR)信号的传导通路。进展期NSCLC的标准化疗方案为以铂类药物为基础的二联疗法。多项研究指出,在既定的铂类方案中增加化疗药物对于NSCLC患者的预后并无显著改善,且可能导致药物毒性增加[9]。抗血管生成的靶向药物对于进展期NSCLC的治疗发挥至关重要的作用,重组人单克隆抗体贝伐单抗与VEGF竞争性结合进而抑制肿瘤血管生成,是目前唯一批准用于NSCLC治疗的抗血管生成药物[10]。
阿帕替尼是中国自主研发的第一代口服靶向药,其主要靶位点为VEGFR-2和酪氨酸激酶受体(RTK)[11]。在多项肿瘤药物的研究中,阿帕替尼通过阻断VEGFR-2从而抑制内皮增殖并最终抑制血管生成[12]。从本研究疗效评估中可见,相比较于传统三线化疗方案,阿帕替尼疗效更为确定。在毒副反应的对比中发现,对照组血液毒性反应显著高于治疗组,这也提示阿帕替尼在用药的安全性方面值得肯定。我们的研究结果与Hu[13]和Qin[14]的报告相一致。阿帕替尼常见毒副反应为高血压和手足综合征。在本研究中,阿帕替尼设定剂量为500g/天,毒性反应呈现出可控性和耐受性。有研究指出,阿帕替尼剂量水平为750mg/天时安全性和耐受性仍然可以保障[15]。

表2 药物毒性反应评估结果
综上所述,本研究通过对NSCLC患者中应用阿帕替尼单药治疗的疗效进行评估,初步明确了阿帕替尼在NSCLC三线治疗中的疗效及其毒副作用。分子靶向药物阿帕替尼能够有效抑制肿瘤血管生成,在NSCLC的治疗中具有一定疗效和可耐受的毒性。
[1] National Cancer Institute. SEER stat fact sheets: Lung and bronchus cancer [M]. Available Accessed October 15, 2015.
[2] Schiller JH,Gandara DR,Goss GD,et al.Non-small-cell lung cancer: then and now[J].J Clin Oncol,2013,31(8):981-983.
[3] Shepherd FA,Dancey J,Ramlau R,et al.Prospective randomized trial of docetaxel versus best supportive care in patients with non-small-cell lung cancer previously treated with platinum-based chemotherapy[J].J Clin Oncol,2000,18(10):2095-2103.
[4] Rizvi NA,Hellmann MD,Snyder A,et al.Mutational landscape determines sensitivity to PD-1 blockade in non-small cell lung cancer[J].Science,2015,348(6230):124-128.
[5] Hanna N,Shepherd FA,Fossella FV,et al.Randomized phase Ⅲ trial of pemetrexed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy[J].J Clin Oncol,2004,22(9):1589-1597.
[6] Shepherd FA,Rodrigues Pereira J,Ciuleanu T,et al.Erlotinib in previously treated non-small-cell lung cancer[J].N Engl J Med,2005,353(2):123-132.
[7] Oxnard GR,Binder A,J?nne PA.New targetable oncogenes in non-small-cell lung cancer[J].J Clin Oncol,2013,31(8):1097-1104.
[8] Davies M.New modalities of cancer treatment for NSCLC: Focus on immunotherapy[J].Cancer Manag Res,2014,6(1):63-75.
[9] Delbaldo C,Michiels S,Syz N,et al.Benefits of adding a drug to a single-agent or a 2-agent chemotherapy regimen in advanced non-small-cell lung cancer: a meta-analysis[J].JAMA,2004,292(4):470-484.
[10] Stinchcombe TE.Targeted therapy of advanced non-small cell lung cancer:the role of bevacizumab[J].Biologics:Target Ther,2007,1(3):185-194.
[11] Tian S,Quan H,Xie C,et al.YN968D1 is a novel and selective inhibitor of vascular endothelial growth factor receptor-2 tyrosine kinase with potent activity in vitro and in vivo[J].Cancer Sci,2011,102(7):1374-1380.
[12] Tanigawa N,Amaya H,Matsumura M,et al.Correlation between expression of vascular endothelial growth factor and tumor vascularity, and patient outcome in human gastric carcinoma[J].J Clin Oncol,1997,15(2):826-832.
[13] Hu X,Zhang J,Xu B,et al.Multicenter phase Ⅱ study of apatinib, a novel VEGFR inhibitor in heavily pretreated patients with metastatic triple-negative breast cancer[J].Int J Cancer,2014,135(8):1961-1969.
[14] Qin S.PhaseⅢ study of apatinib in advanced gastric cancer: a randomized, double-blind, placebo-controlled trial[J].J Clin Oncol,2014,32(15 suppl):4003.
[15] Li J,Zhao X,Chen L,et al.Safety and pharmacokinetics of novel selective vascular endothelial growth factor receptor-2 inhibitor YN968D1 in patients with advanced malignancies[J].BMC Cancer,2010,10(1):529-537.
Effect of apatinib as single agent on advanced non-small cell lung cancer
BI Jin-ling, LIU Hai-yuan, HUANG Yong
Oncology Department, the 2nd People’s Hospital of Hefei, Hefei, Anhui 230000, China
Objective To evaluate the efficacy and safety of apatinib as single-agent in treatment of advanced non-small cell lung cancer (NSCLC). Methods A total of 65 patients with relapse NSCLC were enrolled and divided into two groups. The control group (n=30) was given docetaxel and the treatment group (n=30) was given apatinib. All patients were evaluated for efficacy and safety. Results There was no case of complete response, 3 cases of partial response, 11 stable cases and 16 advanced case in the control group, and no case of complete response, 6 cases of partial response, 17 stable cases and 12 advanced cases in the treatment group (P<0.05). Compared with the control group, the toxicity of single agent was controllable with significant lower incidence of Ⅲ-VI adverse reaction. Conclusion Apatinib has certain curative efficacy and tolerable toxicity in treatment of advanced NSCLC.
apatinib; non-small cell lung cancer; docetaxel; advanced
10.3969/j.issn.1009-6663.2017.08.034
230000 安徽 合肥,合肥市第二人民医院肿瘤科
黄勇,E-mail:hy670716@163.com
2016-12-16]
——评《卵巢恶性肿瘤诊疗手册》

