微孔球状氢氧化镁对水样中刚果红的吸附工艺优化
蒋德敏,陈书鸿,赖庆轲,黄美英,陈明君,陈建钧,何阳
微孔球状氢氧化镁对水样中刚果红的吸附工艺优化
蒋德敏1,陈书鸿1,赖庆轲1,黄美英1,陈明君1,陈建钧2,何阳1
(1重庆三峡学院环境与化学工程学院,重庆404100;2四川大学化学工程学院,四川成都 610065)
为了解决氢氧化镁净化染料废水过程中过滤难的问题,提出了一种球状氢氧化镁的合成方法以及刚果红废水净化处理工艺。采用七水硫酸镁、氢氧化钠和氨水为原料,在晶型控制剂条件下制备球状氢氧化镁,利用X射线衍射仪(XRD)、扫描电子显微镜(SEM)等对产物进行表征。通过振荡实验研究了微孔球状氢氧化镁对水溶液中刚果红的吸附行为,分别考察氢氧化镁加入剂量、时间、溶液pH、振荡转速、温度等因素对吸附效果的影响。研究表明,球状氢氧化镁加入剂量、时间、溶液pH、温度对氢氧化镁吸附刚果红影响较大,振荡转速对其吸附影响较小。同时,在刚果红初始浓度为100mg/L时,得到其最佳吸附工艺条件为:在室温下,微孔球状氢氧化镁的投入量为2g/L,吸附时间为70min,刚果红溶液的pH调节到4~8,吸附振荡转速为220r/min。在此吸附工艺条件,对刚果红初始浓度为100mg/L的吸附率高达93.29%。吸附平衡实验表明,在刚果红废水溶液初始pH为2和吸附温度为40℃时,球状氢氧化镁对刚果红分子的吸附更符合Langmuir模型;刚果红废水溶液初始pH在4~8时,Freundlich吸附模式更适合描述球状氢氧化镁对刚果红的吸附。
微孔球状;氢氧化镁;制备;吸附;刚果红
近年来纺织染料工业迅猛发展,染料废水的产生量也在随之逐年增大。印染废水中的染料多为芳香族、稠环芳香族或杂环化合物[1]。其中,联苯胺偶氮阴离子型染料刚果红是印染废水中具有代表性的污染物之一,有毒且难以被生物降解,可致畸、致癌和致突变[2]。目前,印染废水处理方法主要包括化学氧化法、生物处理法、萃取法、絮凝沉淀法、吸附法、光催化法和电解法等[3-10]。但是化学法处理费用高,难以推广;萃取法仅适用于处理小量的废水,同时容易引入二次污染;生物法受外界因素的影响较大,运行不稳定,适用性差;光催化和电解法等处理方法具有运行成本高、后处理工艺复杂等缺点。吸附法由于具有不用或少用有机溶剂、操作简便、安全、设备简单、生产过程pH变化小、对有毒污染物不敏感及不产生二次污染物等优点,成为目前极具发展潜力的除去废水中难生物降解污染物的一种有效方法。近年来,吸附法净化处理刚果红废水已经成为研究热点。在处理刚果红废水时,报道较多的吸附剂是活性炭、二氧化钛、生物质等。韩秀丽等[11]用木质素基活性炭对刚果红的吸附进行了深入研究,结果表明在25℃时,最大饱和吸附量为62.49mg/g。刘凤艳等[12]用多孔二氧化钛吸附刚果红,研究结果表明在刚果红初始浓度为70mg/L、二氧化钛加入量为0.1g、吸附时间为30min、振荡转速为160r/min时,对刚果红的去除率达98%。吴艳等[13]用十六烷基三甲基溴化铵对木屑进行改性后用于水中刚果红的去除研究,当初始浓度为90mg/L、木屑加入量为0.05g、150r/min转速下室温振荡120min后,废水中的刚果红去除率在90%,同时,改性前后木屑的最大吸附量分别为30.30mg/g、111.36mg/g。活性炭对废水中的刚果红吸附效果很好,由于活性炭价格较贵,再生性能差,导致活性炭在处理刚果红废水时难以推广应用。二氧化钛和生物质等在吸附处理刚果红时吸附速度慢、饱和吸附量低,使其在实际应用中受到限制。探索一种绿色环保对刚果红吸附速度快、饱和吸附量大的废水处理剂具有重要研究意义。
氢氧化镁作为吸附剂,由于其同时具备良好缓冲性、无毒、安全、不腐蚀设备等特性[14],目前,在环保方面,氢氧化镁作为废水净化处理剂已广泛用于各种水质废水处理,如酸性废水处理[15]、印染废水脱色[16-17]、重金属离子去除[18-19]、废水脱磷脱铵[20]等。有关氢氧化镁吸附净化刚果红印染废水的研究报道少见,为了对刚果红印染废水进行无害化处理,本文研究微孔球状氢氧化镁的制备,并采用微孔球状氢氧化镁对废水中刚果红的吸附处理工艺条件进行优化研究,对印染废水中刚果红的净化处理提供参考与借鉴。
1 实验部分
1.1 实验仪器与试剂
试剂:刚果红,上海试剂三厂;柠檬酸三钠,汕头市西陇化工厂有限公司;乙二胺四乙酸二钠,天津市化学试剂一厂;MgSO4·7H2O,西陇化工股份有限公司;无水乙醇、HCl(36%~38%)、NaOH,四川西陇化工有限公司;NH4Cl、NH3·H2O,成都科龙化工试剂厂。所用试剂均为分析纯。
准确称取分析纯的刚果红2000mg,置于干净的烧杯中溶解,转移到1L的容量瓶中,用超纯水定容,配制得到2000mg/L的溶液。取250mL的上述刚果红溶液于5L的容量瓶中,用超纯水稀释定容,配制得到100mg/L的刚果红溶液作为模拟印染废水标准储备液备用。
仪器:JSM-5900LV型扫描电子显微镜,日本电子株式会社(JEOL);X′Pert Pro MPD型X射线衍射仪(XRD),荷兰飞利浦公司;722E型可见光分光光度计,上海光谱仪器有限公司;FA124型电子天平,上海舜宇恒平科学仪器有限公司;KQ-5200E型超声波清洗器,巩义市英峪予华仪器厂;UPC-I-20T优普系列超纯水器,成都超纯科技有限公司;PHS-3C-02型酸度计,上海三信仪表厂;BS-1E智能型振荡培养箱,金坛市正基仪器有限公司。
1.2 微孔球状氢氧化镁的制备及表征
准确称取一定量的七水硫酸镁和氢氧化钠,分别配制成0.5mol/L的硫酸镁和氢氧化钠溶液,量取200mL氢氧化钠溶液滴加到200mL硫酸镁溶液中,滴加完后,将氢氧化镁料浆和100mL浓氨水同置于一个密闭容器中,利用氨水易溶于水的特性,在密闭容器内形成恒定浓度的氨气浴,室温下料浆在晶型控制剂作用下通过慢反应自组装合成微孔球状氢氧化镁颗粒,氨气浴陈化24h。反应完成后过滤,用超纯水洗涤4次,再用无水乙醇洗涤2次,在120℃的恒温干燥箱中干燥6h。得到的产品在外观上为白色粉末,为了确定其微观结构,采用电子扫描电镜和X射线衍射对合成得到的氢氧化镁产品进行表征,SEM图如图1所示,XRD谱图如图2 所示。
从图1可知,氢氧化镁产品在电子显微镜条件下观察呈微孔球形颗粒,颗粒直径主要在8~10μm,颗粒分布较均匀,有少量小球形颗粒聚集物出现。球形氢氧化镁由片层纳米氢氧化镁颗粒堆积而成,在堆积过程中形成许多微孔,这样增加了球状氢氧化镁的比表面积,在印染废水处理时可以提供更多的接触面积,有利于加快吸附速率、增加饱和吸附量。传统纳米氢氧化镁颗粒在水溶液中易形成胶体,在吸附实验后难以过滤分离,而微孔球状氢氧化镁颗粒较大,解决了纳米氢氧化镁在废水处理过程中过滤分离难的问题。
为了进一步确定其球状颗粒产品结构组成,对球状氢氧化镁晶体进行X射线衍射(XRD)检测分析,产品的X射线衍射谱图如图2所示。从图2中将检测所得的球状氢氧化镁衍射谱图与(JCPDF7-239)标准谱图对比分析,衍射峰的值与标准谱一致,可以确定在该条件下制备的球状产品的纯度高,其结构组成为Mg(OH)2。
1.3 吸附实验
1.3.1 吸附实验条件优化
准确称取一定质量的微孔球状氢氧化镁置于100mL的锥形瓶中,用吸量管准确移取15mL的100mg/L刚果红印染废水加入锥形瓶中,将锥形瓶放入恒温振荡床中进行吸附实验。分别对氢氧化镁加入剂量、时间、废水pH、振荡转速、温度等吸附条件进行优化。
氢氧化镁加入剂量影响的实验条件:向每个锥形瓶中加入不同质量的球状氢氧化镁粉末,设定振荡床转速为200r/min,吸附振荡温度为20℃,振荡时间150min。
吸附时间影响的实验条件:向每个锥形瓶中加入20mg的球状氢氧化镁粉末,设定振荡床转速为200r/min,吸附振荡温度为20℃。设定不同的吸附时间,分别为10min、20min、30min、40min、50min、60min、70min、80min、90min、100min、110min。
废水pH影响的实验条件:配制系列不同pH的100mg/L的刚果红模拟印染废水,每个锥形瓶中加入15mL的刚果红废水溶液,向每个锥形瓶中加入20mg的球状氢氧化镁粉末,设定振荡床转速为200r/min,吸附振荡温度为20℃,吸附时间为50min。
振荡转速影响的实验条件:向每个锥形瓶中加入20mg的球状氢氧化镁粉末,吸附振荡温度为20℃,吸附时间为30min,设定不同的振荡床转速,振荡转速分别为100r/min、140r/min、180r/min、200r/min、220r/min、260r/min、300r/min。
吸附温度影响的实验条件:向每个锥形瓶中加入20mg的球状氢氧化镁粉末,设定振荡床转速220r/min,吸附时间为30min,吸附振荡温度分别为10℃、20℃、30℃、40℃、50℃、60℃、70℃、80℃。
1.3.2 吸附等温线测定
配制一系列质量浓度在100~900mg/L的刚果红溶液,将其pH控制在4~8。向每个锥形瓶中加入20mg球状氢氧化镁粉末,15mL上述溶液,振荡转速为220r/min,分别在20℃、30℃、40℃下振荡吸附120min至吸附平衡,吸附时间完成后取出,将混合溶液转移到离心管中离心分液,用分光光度法测定吸附后废液中刚果红的含量,并计算出刚果红平衡浓度和平衡吸附量。采用Langmuir和Freundlich模型[21-22]来拟合染料在球状氢氧化镁上的吸附平衡数据。
Langmuir和Freundlich公式分别如式(1)、 式(2)。
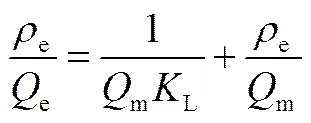
(2)
式中,e为平衡浓度,mg/L;e为平衡吸附量,mg/g;m为最大吸附量,mg/g,L为平衡系数,L/mg;F为平衡常数,代表吸附容量的大小;为Freundlich吸附指数,表征吸附强度的量度。
1.3.3 刚果红的测定方法
吸附实验结束后,将混合液倒入15mL的离心管中离心分离。离心后吸取少量上清液于50mL比色管中,加入15mL无水乙醇、1mL 0.01mol/L的乙二胺四乙酸二钠和柠檬酸三钠金属离子掩蔽剂溶液,再加入5mL氯化铵-氨水缓冲溶液将溶液pH调节到6~11后定容。放入40℃水浴锅中恒温10min后,在500nm测定波长下,以分光光度法测定刚果红的浓度。吸附率和吸附量采用如式(3)、式(4)计算。
吸附率计算公式
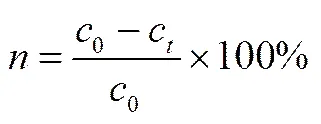
吸附量计算公式
(4)
式中,为吸附率;0为废水中刚果红的初始浓度,mg/L;c为废水中刚果红在吸附实验中时刻的浓度,mg/L;为吸附量,mg/g;为微孔球状氢氧化镁的质量,g;为刚果红模拟废水的体积,mL。
2 结果与讨论
2.1 吸附剂添加量的影响
从图3可知,在微孔球状氢氧化镁粉末添加量小于40mg时,吸附率随微孔球状氢氧化镁添加量的增加而提高,当微孔球状氢氧化镁粉末添加量大于40mg后,添加量增加,吸附率基本保持不变。单位质量氢氧化镁的吸附量随微孔球状氢氧化镁添加量的增加而降低。氢氧化镁加入量增加后,提供吸附刚果红的表面积增加,更有利于废液中刚果红的吸附,从而使吸附率增加,同时使单位微孔球状氢氧化镁的吸附量降低。废液中刚果红初始浓度为100mg/L时,微孔球状氢氧化镁的加入量以2g/L为宜。
2.2 吸附时间的影响
从图4可得,微孔球状氢氧化镁对废液中刚果红的吸附率随吸附时间的延长而提高,吸附速率与氢氧化镁粉末质量有关,氢氧化镁粉末添加量越多,吸附速率越快。当氢氧化镁添加量为20mg时,吸附时间小于70min时,氢氧化镁粉末对刚果红 的吸附率随吸附时间的增加而提高,吸附时间超过70min后基本保持不变。当氢氧化镁添加量为40mg时,吸附平衡时间为50min,同等实验条件下比添加量为20mg时提前20min达到吸附平衡。
2.3 废水pH的影响
从图5可知,当模拟废水pH小于2时,吸附率随pH的升高而增大;当pH在2~7时,吸附率随pH的升高而减小;当溶液呈碱性时,吸附率随pH的增加而略有升高。刚果红溶液初始pH为2时,氢氧化镁对刚果红的吸附率最高。由于氢氧化镁具有调节酸度的作用,使固液混合溶液呈弱酸性。刚果红分子中含有苯磺酸钠结构,刚果红在弱酸性环境中,磺酸钠盐转换成磺酸基团,磺酸基团与球状氢氧化镁表面的羟基发生酸碱中和反应,更有利于对刚果红的吸附。在实验中发现,当pH小于2时微孔球状氢氧化镁有溶解现象;在pH降低到0.8时,所加入的微孔球状氢氧化镁会全部溶解,导致吸附率为0。在pH小于2时,由于溶液酸性过强而使微孔球状氢氧化镁溶解,导致吸附率随pH的减小而降低。虽然刚果红废水pH在2左右,氢氧化镁对刚果红的吸附率最高,考虑到在实际工业应用中对废水pH不易控制,导致操作不稳定。考虑实际生产操作过程与经济成本等因素,在吸附应用实验中,刚果红废液的pH调节到4~8为宜。
2.4 振荡转速的影响
从图6可知,当振荡转速小于220r/min时,吸附率随振荡速率的增加而提高;当振荡转速大于220r/min时,吸附率基本保持不变。在低转速时,氢氧化镁对刚果红的吸附是刚果红分子的传递率为整个吸附过程的控制步骤,增加振荡速率能够加快废液中刚果红分子的传质速率,刚果红分子传递到氢氧化镁颗粒表面所需要的时间缩短,使球状氢氧化镁颗粒对刚果红的吸附速率加快,从而使吸附率增加。当振荡转速增加到一定程度时,由于此时整个吸附速率的控制步骤为氢氧化镁表面对刚果红的物理化学吸附反应,即振荡转速的增加对吸附率再无影响。球状氢氧化镁颗粒对刚果红的吸附实验中,振荡转速选择220r/min为宜。
2.5 吸附温度的影响
从图7可得,温度对氢氧化镁颗粒吸附刚果红的过程有较大的影响,吸附率随温度的升高而增加。当温度低于40℃时,吸附率随温度的升高而增加较快;当温度超过40℃后,吸附率增加变化量不大。在一定温度范围内,增加温度能够加快刚果红分子在溶液中的传质速率;同时氢氧化镁对刚果红的吸附为物理化学吸附过程,温度升高能够加快物理化学吸附速率,即在相同的实验时间条件下,升高温度能够提高氢氧化镁对刚果红的吸附率。虽然升高温度可以提高吸附率,但是在实际生产过程中,对废水加热保温需要消耗更多的能源,导致刚果红废水处理工艺更加复杂。实际应用过程考虑节能与成本因素,吸附过程的温度选择室温为宜。
2.6 吸附等温线
从图8可得,在40℃时,刚果红溶液初始pH对饱和吸附量有影响,初始pH为2的饱和吸附量高于pH在4~8的饱和吸附量,这一实验结果与废水pH的影响一致。在同一温度下,球状氢氧化镁对刚果红的单位吸附量随刚果红平衡浓度的升高而增加。平衡浓度越高,吸附推动力越大,导致平衡时单位吸附量越大;其他条件相同时,温度升高能增大单位吸附量。较高温度溶液中的刚果红分子运动速度加快,有更多的刚果红分子被球状氢氧化镁内表面吸附,从而导致吸附量增加。
等温吸附线的拟合参数及结果如表1所示,刚果红废水溶液初始pH为2和吸附温度为40℃时,Langmuir等温式拟合程度较好,其拟合相关系数为0.9931,而Freundlich等温式拟合程度较差,其拟合相关系数为0.8488。表明在此条件下Langmuir优于Freundlich吸附模式,球状氢氧化镁对刚果红分子主要以单分子层吸附。当刚果红废水溶液初始pH在4~8时,Freundlich吸附模式更适合于球状氢氧化镁对刚果红的吸附,表明球状氢氧化镁对刚果红的吸附出现了不均相吸附行为,其值均大于1,说明球状氢氧化镁对刚果红的吸附是优惠吸附[23]。
a,b,c—刚果红溶液初始pH均在4~8,温度分别为20℃、30℃、40℃;d—刚果红溶液初始pH为2,温度为40℃
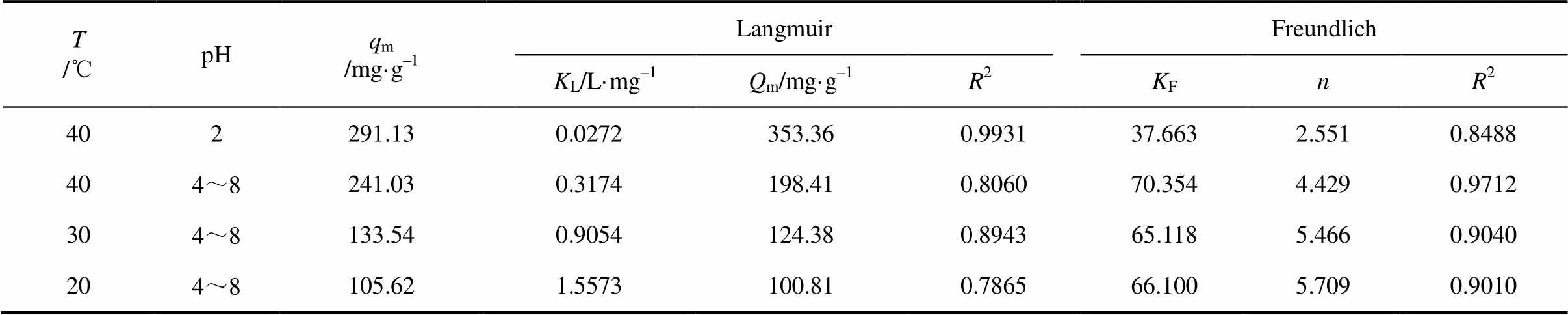
表1 等温吸附参数
3 结论
吸附平衡实验表明,在刚果红废水溶液初始pH为2和吸附温度为40℃时,Langmuir等温式拟合程度较好,球状氢氧化镁对刚果红分子的吸附更符合Langmuir模型,属于单分子层吸附。刚果红废水溶液初始pH在4~8时,Freundlich吸附模式更符合球状氢氧化镁对刚果红的吸附,属于优惠吸附。在刚果红初始浓度为100mg/L时,通过实验研究得到球状氢氧化镁对印染废水中刚果红的吸附最佳工艺条件为:微孔球状氢氧化镁的投入量为2g/L,吸附时间为70min,刚果红溶液的pH调节到4~8,吸附振荡转速为220r/min,振荡吸附温度为室温。在此吸附工艺条件,微孔球状氢氧化镁对刚果红的吸附率高达93.29%。微孔球状氢氧化镁对刚果红的饱和吸附量大,工艺流程简单易行,有利于在刚果红废液净化处理中工业化应用推广。
[1] 詹艳慧,林建伟.羟基磷灰石对水中刚果红的吸附作用研究[J]. 环境科学,2013,34(8):3143-3149.
ZHAN Y H,LIN J W. Adsorption of Congo red from aqueous solution on hydroxyapatite[J]. Environmental Science,2013,34(8):3143-3149.
[2] 赵芳,马亚红,李振林,等. 松香基季铵盐表面活性剂改性沸石对水中刚果红的吸附性能[J]. 环境化学,2015,34(12):2223-2232.
ZHAO F,MA Y H,LI Z L,et al. Adsorption properties of Congo red on natural zeolite modified with cationic surfactant of rosin-based quaternary ammonium[J]. Environmental Chemistry,2015,34(12):2223-2232.
[3] 王敏敏,薛振华,王丽. 羧甲基纤维素/有机蒙脱土纳米复合材料对刚果红的吸附与解吸性能[J]. 环境工程学报,2014,8(3):1001-1006.
WANG M M,XUE Z H,WANG L. Adsorption and desorption capacity of Congo red on CMC/OMMT nanocomposite[J]. Chinese Journal of Environmental Engineering,2014,8(3):1001-1006.
[4] 段小月,刘伟,于艳艳,等. 电吸附法去除水中刚果红的研究[J]. 环境污染与防治,2012,34(1):56-59.
DUAN X Y,LIU W,YU Y Y,et al. Study on the electro-sorption of Conguo red solution[J]. Environmental Pollution and Control,2012,34(1):56-59.
[5] 王元刚,刘诗雨,赵建海,等. 氢氧化镁混凝过程应用于活性黄X-R废水脱色研究[J]. 环境工程,2015(7):61-65.
WANG Y G,LIU S Y,ZHAO J H,et al. Removal of color from reactive yellow X-R wastewater by magnesium hydroxide coagulation process[J]. Environmental Engineering,2015(7):61-65.
[6] 薛如意,鞠剑峰,徐山青. TiO2纳米复合纤维光催化处理印染废水的进展[J]. 印染,2015(21):44-48.
XUE R Y,JU J F,XU S Q. Progress on degradation of dyeing wastewater with TiO2nanofiber photocatalysts[J]. Dyeing and Finishing,2015(21):44-48.
[7] 高永,孔峰,程洁红,等. TiO2光催化-微滤膜分离深度净化亚甲基蓝印染废水[J]. 环境工程学报,2012,6(10):3585-3590.
GAO Y,KONG F,CHENG J H,et al. Advanced treatment of methylene blue dye wastewater by TiO2photocatalysis and microfiltration membrane separation[J]. Chinese Journal of Environmental Engineering,2012,6(10):3585-3590.
[8] 张丽,郭俊旺. 模拟印染废水中酸性紫红-10B的萃取资源化技术研究[J]. 环境科学与管理,2010,35(10):97-99.
ZHANG L,GUO J W. Study on extraction and recovery of acid violet red-10B from simulated printing and dyeing effluent[J]. Environmental Science and Management,2010,35(10):97-99.
[9] 赵菁,张改,马爱洁,等. 高级氧化法处理模拟印染废水的研究[J]. 工业水处理,2015,35(3):37-39.
ZHAO J,ZHANG G,MA A J,et al. Study on the treatment of simulated dyeing wastewater by advanced oxidation technology[J]. Industrial Water Treatment,2015,35(3):37-39.
[10] 方巧,林建伟,詹艳慧,等. 羟基磷灰石-四氧化三铁-沸石复合材料制备及去除水中刚果红研究[J]. 环境科学,2014,35(8):2992-3001.
FANG Q,LIN J W,ZHAN Y H,et al. Synthesis of hydroxyapatite/ magnetite/zeolite composite for Congo red removal from aqueous solution[J]. Environmental Science,2014,35(8):2992-3001.
[11] 韩秀丽,郭晓锋,王铎,等. 木质素基活性炭对刚果红的吸附性能研究[J]. 应用化工,2016,45(10):1903-1907.
HAN X L,GUO X F,WANG D,et al. Study on the adsorption characteristics of Congo red by lignin-based activated carbon[J]. Applied Chemical Industry,2016,45(10):1903-1907.
[12] 刘凤艳,肖丽伟,康志成,等. 多孔二氧化钛吸附刚果红[J]. 化工进展,2014,33(5):1321-1326.
LIU F Y,XIAO L W,KANG Z C,et al. Adsorption of Congo red by porous TiO2[J]. Chemical Industry and Engineering Progress,2014,33(5):1321-1326.
[13] 吴艳,罗汉金,王侯. 改性木屑对水中刚果红的吸附性能研究[J]. 环境科学学报,2014,34(7):1680-1688.
WU Y,LUO H J,WANG H.Adsorption properties of modified sawdust for Conge red removal from wastewater[J]. Acta Scientiae Circumstantiae,2014,34(7):1680-1688.
[14] 霍闪,卿彬菊,邓小川,等. 氢氧化镁作为吸附剂的应用研究进展[J]. 盐湖研究,2014,22(4):57-60.
HUO S,QING B J,DENG X C,et al. Progress in application of magnesium hydroxide as an adsorbent[J]. Journal of Salt Lake Research,2014,22(4):57-60.
[15] 杜娜娜. 氢氧化镁处理酸性含铁废水的研究[J]. 广州化工,2011,39(6):134-138.
DU N N. Study on the removal of acidic iron-containing wastewater with magnesium hydroxide[J]. Guangzhou Chemical Industry,2011,39(6):134-138.
[16] 郭效军,李雨甜,李静. 氢氧化镁改性硅藻土对水中活性红的吸附性能研究[J]. 硅酸盐通报,2014,33(9):2170-2175.
GUO X J,LI Y T,LI J.Performance of magnesium hydroxide-modified diatomite in adsorption of reactive red from aqueous solution[J]. Bulletin of the Chinese Ceramic Society,2014,33(9):2170-2175.
[17] 傅明连,陈彰旭,郑炳云,等. 氢氧化镁/壳聚糖复合絮凝剂处理模拟印染废水的研究[J]. 化工新型材料,2014,42(10):137-139.
FU M L,CHEN Z X,ZHENG B Y,et al. Study on the process of analogue dyeing wastewater using magnesium hydroxide/chitosan complex flocculant[J]. New Chemical Materials,2014,42(10):137-139.
[18] 郭效军,李静,路娟,等. 室温固相法制备氢氧化镁及其对水溶液中Ni(II)的吸附[J]. 硅酸盐通报,2012,31(2):406-410.
GUO X J,LI J,LU J,et al. Preparation of magnesium hydroxide by room temperature solid phase method and adsorption of Ni(Ⅱ)from aqueous solution[J]. Bulletin of the Chinese Ceramic Society,2012,31(2):406-410.
[19] 胡婉玉,袁新松,郝建文,等. 片状纳米氢氧化镁吸附铅离子性能研究[J]. 轻金属,2012(9):60-62.
HU W Y,YUAN X S,HAO J W,et al. Study on treatment of lead ion by adsorption with nanoflake magnesium hydroxide[J]. Light Metals,2012(9):60-62.
[20] 邢坤,王海增. 改性与成型层状氢氧化镁铝对不同水体中PO43-的脱除性能[J]. 环境科学,2013,34(4):1611-1616.
XING K,WANG H Z.Removal of PO43-from solution,wastewater and seawater by modification and granulation magnesium and aluminium layered double hydroxide[J]. Environmental Science,2013,34(4):1611-1616.
[21] 刘小霞,邓浩,王妍媖,等. BSA在不同形貌氧化锌材料上的吸附热力学[J]. 高等学校化学学报,2014,35(10):2156- 2163.
LIU X X,DENG H,WANG Y Y,et al. Thermodynamics studies on the BSA adsorption onto zinc oxide surfaces with different morphologies[J]. Chemical Journal of Chinese Universities,2014,35(10):2156-2163.
[22] 黄凤羽,易发成,王哲. 坡缕石对Sr(ӀӀ)的吸附热力学研究[J]. 原子能科学技术,2016,50(5):782-788.
HUANG F Y,YI F C,WANG Z. Thermodynamic study on adsorption of Sr(Ⅱ) on palygorskit[J]. Atomic Energy Science and Technology,2016,50(5):782-788.
[23] 武占省,王雅言,孙喜房,等. 活性白土对油脂溶液中-胡萝卜素的吸附热力学及动力学研究[J]. 离子交换与吸附,2009,25(6):488-495.
WU Z S,WANG Y Y,SUN X F,et al. Study on adsorption Thermodynamics and kinetics of-carotene in oil solution on acid activated bentonite[J]. Ion Exchange and Adsorption,2009,25(6):488-495.
Adsorption process optimization of Congo red in water samples by micro-porous spherical magnesium hydroxide
JIANG Demin1,CHEN Shuhong1,LAI Qingke1,HUANG Meiying1,CHEN Mingjun1,CHEN Jianjun2,HE Yang1
(1School of Environment and Chemical Engineering,Chongqing Three Gorges University,Chongqing 404100,China;2School of Chemical Engineering,Sichuan University,Chengdu 610065,Sichuan,China)
In order to solve the problem for the difficulty of mixture filtration in the process of dye wastewater purification by magnesium hydroxide,a new synthesis method of spherical magnesium hydroxide and its process for purification of Congo red wastewater were proposed. Using magnesium sulfate heptahydrate,sodium hydroxide and ammonia as raw materials,the spherical magnesium hydroxide was prepared under the condition of crystal formation controlling agent. The spherical product was characterized by X-ray diffraction(XRD)and scanning electron microscopy(SEM).The adsorption behavior of Congo red on micro-porous spherical magnesium hydroxide in aqueous solution was studied by jar test.The effect of magnesium hydroxide dosing,time,solution pH,oscillation speed and temperature on the adsorption was comprehensively investigated. The study showed that the spherical magnesium hydroxide dosing,time,pH and temperature have major influence on the adsorption of Congo red,while the oscillation speed has a minor effect on its adsorption.The optimized adsorptionprocess conditions are as follows. The oscillation adsorption temperature is room temperature. The amount of the micro porous spherical magnesium hydroxide is 2g/L. The adsorption time is 70min. The pH of the Congo red solution is adjusted to 4—8. The adsorption oscillation speed is 220r/min. Under these adsorption process conditions,the adsorption rate is 93.29% with the initial concentration of Congo red of 100mg/L. The adsorption equilibrium experiments showed that at the initial pH of 2 and the temperature of 40℃,the Langmuir model is more suitable for the adsorption of Congo red on spherical magnesium hydroxide. However,when the Congo red wastewater pH is up to between 4 and 8,the Freundlich model is probably more suitable for its adsorption behavior on the spherical magnesium hydroxide.
micro-porous spherical;magnesium hydroxide;preparation;adsorption;Congo red
TQ09
A
1000–6613(2017)07–2707–07
10.16085/j.issn.1000-6613. 2016-2188
2016-11-24;
2017-01-12。
国家自然科学基金(21076131)、四川省科技支撑计划(2014GZ0076)、重庆市教委科技项目(KJ1710245)及重庆三峡学院大学生创新实验项目(2017039)。
蒋德敏(1987—),男,硕士,助教,研究方向为化工新技术新工艺开发。E-mail:dmhuagong@163.com。

