电化学方法研究脱脂乳在金电极表面的吸附
,,,,*,
(1.南昌大学食品科学与技术国家重点实验室,江西南昌 330047; 2.赣州市食品药品检验检测中心,江西赣州 341000)
电化学方法研究脱脂乳在金电极表面的吸附
李昌高1,曾善荣2,赖理智1,黄赣辉1,*,邓丹雯1
(1.南昌大学食品科学与技术国家重点实验室,江西南昌 330047; 2.赣州市食品药品检验检测中心,江西赣州 341000)
本文研究脱脂乳在金电极表面的吸附,并探讨脱脂乳的变化对吸附的影响。以微分电容法研究脱脂乳在金电极表面的吸附,并用循环伏安法和交流阻抗表征电极吸附,采用石英晶体微天平研究不同脱脂乳在金电极表面的界面吸附。结果表明:在一定浓度范围内,脱脂乳在金电极表面吸附是单分子层吸附,符合Langmuir吸附等温方程式;随着脱脂乳浓度的增加,脱脂乳在金晶体表面逐步达到饱和吸附;在不同pH缓冲溶液的吸附量也不同,在pH为5时吸附量最大;在同一稀释浓度及pH条件下,吸附量随着掺杂离子强度的增加呈现先增大后减小的规律。
微分电容,吸附,金电极,石英晶体微天平
牛乳及其产品的检测方法有多种,电化学检测方法正得到重视。电化学检测方法可以应用到乳制品检测方面,可从源头监控,给出乳制品的总体评价,目前已经在奶牛疾病的监控[1]、生乳掺杂掺假[2]、乳制品的分类[3]、乳制品的质量控制[4]等方面都有相关的研究。根据“交互感应-相对选择性”概念[5],可以构建一个基于电化学和化学计量学方法的生乳掺杂快速检测系统,达到对生乳掺杂的综合性识别目的[6-7]。由于目前电化学之于生乳及乳制品的研究工作主要是针对乳制品的品质控制进行研究,而关于电化学检测系统中电极与牛乳界面信息研究较少,对于传感器与牛乳之间的相互作用还不是太清楚。Farcas M[8]等人通过循环伏安法、电化学石英晶体微天平、电化学阻抗谱、微分电容四个实验技术和五个测量变量研究铂电极上纤维蛋白原的吸附,结果表明吸附可逆并伴随电荷转移,使用朗缪尔吸附等温式描述吸附过程,计算了相应的热力学吸附值。Diniz[9]等人采用交流阻抗法研究伴刀豆球蛋白在玻碳电极上吸附,微分电容曲线揭示了蛋白吸附存在电容弥散效应,并指出该蛋白吸附具有平行于表面的偶极矩。本实验采用电化学方法研究脱脂乳在金电极表面的吸附行为,通过改变吸附条件,使用石英晶体微天平研究稀释浓度、pH以及离子强度对脱脂乳在金电极表面吸附的影响,为电化学方法监测乳及其制品技术的发展提供理论依据。
1 材料与方法
1.1材料与仪器
德运脱脂纯牛奶 市售;超纯水 18.25 MΩ·cm-1;γ-Al2O3粉末、镀金晶振片、石英晶体微天平电解池 上海辰华仪器有限公司;无水乙醇 分析纯,天津市大茂化学试剂厂;高纯氮气 99.99%,江西华东特种气体有限公司;磷酸氢二钠、磷酸二氢钠、30%双氧水、氯化钠、氯化钙、氯化镁、高氯酸、铁氰化钾、亚铁氰化钾、浓硫酸、盐酸、氢氧化钠 分析纯,西陇化工股份有限公司;Piranha洗液VH2SO4∶V30% H2O2=3∶1。
金电极Φ2.0 mm、铂片电极0.2 cm2、C001单层五口电解池 武汉高仕睿联有限公司;217型饱和甘汞电极 上海雷磁有限公司;CHI660B电化学工作站、40通道多通道选通器、CHI440C石英晶体微天平 上海辰华仪器有限公司;PHS-3C pH计 上海雷磁有限公司;KQ-2200DB超声波清洗器 昆山市超声清洗仪器有限公司;5810R高速离心机 Eppendorf 艾本德中国公司;DHL-200恒流泵 上海精科实业有限公司。
1.2实验方法
1.2.1 微分电容法研究脱脂乳在金电极表面的吸附
1.2.1.1 金电极预处理 将金电极依次用0.3 μm和0.05 μm的γ-Al2O3抛光粉在润湿麂皮上抛光至镜面,冲洗净电极表面后再使用无水乙醇超声清洗。磨好的电极通过0.01 mol/L Fe(CN)63-/4-+0.15 mol/L NaCl溶液对其进行判定,通过循环伏安法测得电位差在100 mV以下。将磨好的电极再依次用Piranha溶液、无水乙醇和超纯水超声清洗。以0.2 mol/L高氯酸水溶液、0.1 V/s的扫描速度在-0.1~1.5 V之间循环扫描直至CV曲线重合为止,氮气吹干保护待用。
1.2.1.2 测试方法 以金电极为工作电极,铂片电极为辅助电极,217型饱和甘汞电极为参比电极,固接于单层五口电解池中在屏蔽箱内进行测试。样品脱脂纯牛奶4000 r/min离心20 min,去除脂肪。配制pH=7.0的0.01 mol/L PBS缓冲溶液。在配制好的0.01 mol/L PBS(pH=7.0)溶液中加入一定量的离心脱脂乳,分别配制成0、0.05、0.1、0.25、0.5、0.75、1.0、1.5、2.0、3.0 g/L的脱脂乳稀释液。量取不同浓度脱脂乳稀释液70 mL置于组装好的电解池中,测试前通氮除氧。分别使用预处理好的金电极在开路电位下测得平衡电位,随后采用交流阻抗-电位测量方法分别在20 Hz恒定频率下进行测量并做出相应的微分电容曲线。电位范围:-0.2~0.6 V,采样频率:0.05 V,测试温度:(22±2) ℃。
本实验采用交流阻抗单频测量方法,利用以下公式计算微分电容值C:

式(1)
式中,f为实验设定的恒定频率,Z″为交流阻抗虚部值,π为3.14。
1.2.2 石英晶体微天平研究脱脂乳在电极表面的吸附
1.2.2.1 溶液配制 脱脂乳的制备:将纯牛奶在4000 r/min条件下离心20 min,去除脂肪。
不同浓度脱脂乳稀释液:使用0.01 mol/L PBS(pH=7.0)溶液,NaCl浓度为0.15 mol/L。在缓冲溶液中添加脱脂乳,配制成0、0.25、0.5、0.75、1.0、2.0、3.0、4.0 g/L脱脂乳稀释液。
不同pH的脱脂乳稀释液:配制成pH为3、4、5、6、7、8的0.01 mol/L PBS缓冲溶液,NaCl浓度为0.15 mol/L,脱脂乳浓度为1 g/L。
不同NaCl浓度的脱脂乳稀释液:配制NaCl浓度为0.05、0.1、0.15、0.2、0.25、0.3 mol/L的0.01 mol/L PBS(pH=7.0)溶液缓冲溶液,脱脂乳浓度均为1 g/L。
1.2.2.2 测试方法 石英晶体微天平电解池使用两个O型橡胶圈将镀金晶振片密封在电解池中,晶振片一侧接触测试溶液。将晶振片两触角连接到石英晶体微天平振荡器上,待测溶液预先置于进样池中,用干净橡胶管(Φ3.0 mm)通过恒流泵将待测液体送进测试池中,再用另一个橡胶管使用恒流泵把测试池中的样品回流到进样池中,组成回流系统;由于电解池中液体高度对晶体频率有一定的影响,保持两个橡胶管流速一样,调整测试池中橡胶管的高度,保证电解池中液位保持一致,减少由于液位差对测试结果的影响。电解池和振荡器置于屏蔽箱中。
预先用少量Piranha洗液清洗金晶振片表面30 s,重复两次,再分别用无水乙醇、超纯水超声清洗电极,氮气吹干。将进样橡胶管置于放有对应的缓冲溶液的进样池,通过恒流泵输送到电解池中,待晶振片在缓冲溶液中达到动态平衡后,再将配制好的不同浓度、不同pH、不同离子浓度、不同离子强度的脱脂乳稀释液输送到测试池中测试。测试时恒流泵流速为2 mL/min,测试温度为(22±2) ℃,所有溶液测试前通氮除氧。测试结果使用Sigmaplot 12作图。
1.2.3 循环伏安法(CV)和电化学交流阻抗法(EIS)表征电极吸附过程
1.2.3.1 溶液配制 脱脂乳的制备:同1.2.2.1。
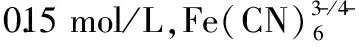
在上述配制好的0.01 mol/L PBS(pH=7.0)溶液中加入一定量的离心脱脂乳,配制成1.0 g/L的脱脂乳稀释液。


表1 不同浓度脱脂乳在金电极上的微分电容值Table 1 The differential capacitance measurements of skimmed milk on the gold interface
本实验测试温度为(22±2) ℃,所有测试溶液待通氮后除去氧气再进行测试。运用Microsoft Excel处理数据,Sigmaplot软件作图。
2 结果与讨论
2.1电极在不同浓度脱脂乳稀释液中的微分电容曲线
2.1.1 微分电容曲线测定 不同浓度脱脂乳在金电极上的微分电容值见表1。随着脱脂乳浓度的增加,金电极在0.3 V左右由初始19.76 μF/cm2到最后在3.0 g/L下降到12.21 μF/cm2,相差7.55 μF/cm2,电极微分电容峰值变化较为明显,峰形由陡峭变得平缓。从脱脂乳的浓度可以看出,金电极在低浓度脱脂乳稀释液后微分电容值下降较为明显,而随着浓度的增加,电容值下降较为缓慢。脱脂乳浓度的增加造成了电极表面的覆盖度增加,微分电容值变化增加,并随着浓度的增加逐渐趋向于饱和,微分电容值的变化减小。
对金电极在PBS(pH7.0)缓冲溶液以及添加0.1、1.0、3.0 g/L脱脂乳稀释液测得微分电容曲线,由图1可以看出,金电极在缓冲溶液以及在0.1、1.0、3.0 g/L脱脂乳稀释液后呈现不同的微分电容曲线。随着电位的变化,微分电容值也发生变化,金电极在0.3 V左右有一个较为突出的峰。

图1 金电极的微分电容曲线Fig.1 Differential capacitance versus potential for the gold electrode
2.1.2 电极表面覆盖度变化及其吸附模型的确定 牛乳蛋白质分子包含有两种功能性基团:疏水基团和亲水基团。当电极与牛乳接触时,乳中蛋白质在电极表面发生重排,其中不带电荷的疏水基团会靠近电极表面一侧,而带有静电荷的亲水基团则与电极排斥,靠近水溶液一侧。这时候由于蛋白质带有电荷以及电极界面结构发生变化,电极溶液界面双电层也发生变化。牛乳在电极表面的吸附可以根据Frumkin-Damaskin理论[]中的公式:
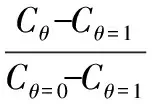
式(2)
其中,Cθ为部分活性粒子覆盖在电极表面时的微分电容值,Cθ=1和Cθ=0表示完全覆盖(θ=1)和未覆盖(θ=0)时的微分电容值。在溶液中添加牛乳后,在零电荷电势附近一小段电势范围内,微分电容值(Cθ)降低,而两侧出现较高电容峰值,随着溶液中牛乳有机活性粒子增加,电极表面覆盖度(θ)加大,Cθ数值跟着减小,直到达到极限值(Cθ=1)。这是因为牛乳有机分子取代了原本吸附在电极表面的水分子,双电层电荷间距变大,同时界面电容值减小。
Langmuir吸附等温线经常被用来研究活性粒子在电极表面的吸附[11-12]。根据吸附等温线的形式,计算吸附平衡常数。假设电极表面均匀,吸附粒子之间没有相互作用,则可以使用Langmuir吸附等温方程式:

式(3)
式中,Γ(mol/cm2)是指电极表面活性粒子吸附量,即表面浓度;c(mol/cm3)是溶液中蛋白质平衡时的浓度;Γmax(mol/cm2)是指电极表面吸附量达到饱和的值;参数BADS(cm3/mol)反映吸附有机活性分子与电极表面吸附位点的结合能力。
根据θ代表电极表面有机分子的覆盖率,则根据Γ=θΓmax可对式(3)进行转换,将Γ进行替换,整理后可获得如下公式[13]:
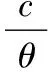
式(4)
从式(4)可以看出,以c/θ对c作图,可获得一条直线。可由此判断吸附是否属于单分子层吸附。

图2 脱脂乳在金电极表面覆盖度的变化 Fig.2 Changes on the gold interface coverage of skimmed milk注:插图表示建模后的Langmuir吸附等温线。
根据表1中数据以及公式(2),以脱脂乳浓度m为横坐标,电极表面覆盖度θ为纵坐标,通过计算可获得图2金电极表面覆盖度图。从图2中可知,在恒定温度条件下,在一定的浓度范围内,随着浓度的增加,脱脂乳稀释液中物质在金电极表面覆盖度增加,在0~1 g/L浓度内两种电极表面已经达到较大覆盖度,说明在很低浓度情况下,覆盖度就可以达到很大值,在1 g/L以后覆盖度趋于缓和,在3 g/L浓度下两种电极覆盖度可认为饱和。根据公式(4),以m对c/θ作图,可以获得牛乳分散液在金电极建模后的吸附等温线,图2中插图可知,实验结果和拟合值相差不大,直线相关系数R2>0.99,表明具有很好的线性关系,也说明了在低浓度下,脱脂乳稀释液在金电极表面的吸附行为可以用Langmuir等温方程描述,即吸附为单分子层吸附。
2.2石英晶体微天平研究脱脂乳在金晶振片表面吸附行为
石英晶体微天平主要包括石英晶体晶振片、振荡器、频率计数器以及数据处理组成,其检测原理是晶体的压电效应[14]。当物质吸附于晶振片表面时会导致晶振片频率发生变化,且吸附量与频率变化成正比,通过测得频率的大小可以获知吸附物质的质量。可根据Sauerbrey[15]提出的公式进行计算:

式(5)
式中,f晶振片基本谐振频率(MHz),Δm晶体表面质量变化(ng),A是晶体表面金盘的面积(cm2),ρq为晶体密度(g/cm3),μq为晶体剪切量(g/cm·s2)。
2.2.1 不同浓度脱脂乳在金晶振片表面吸附行为 图3表示不同浓度脱脂乳稀释液在pH为7的PBS缓冲溶液的吸附行为,当加入脱脂乳后,由于脱脂乳中成分与金晶振片表面相互作用,吸附在金晶振片表面,由于晶振片的压电效应,导致振荡频率的减小。随着脱脂乳浓度的增加,在0到1 g/L浓度范围内Δf开始有一个快速增加的过程,在1到3 g/L范围内Δf增加变缓,在1~4 g/L浓度时,Δf逐步趋向于平缓,此时可认为在4 g/L浓度时乳中酪蛋白、乳清蛋白以及其他小肽有机分子在晶振片表面基本达到饱和覆盖。

图3 脱脂乳浓度与频率变化的关系Fig.3 The relationship between the concentration of skimmed milk and frequency shift
2.2.2 pH对脱脂乳在金晶振片上吸附的影响 图4表示当脱脂乳稀释液浓度为1 g/L,添加氯化钠使各个稀释液离子强度一致,比较金晶振片在不同pH环境的吸附变化,从图4可知,脱脂乳稀释液在pH为5时Δf变化最大,在pH=5左右两侧吸附趋向于减小,呈现抛物线的形状。牛乳中蛋白质主要有酪蛋白、乳清蛋白以及少量脂肪球膜蛋白组成,其中,酪蛋白占总量的80%~82%,等电点为4.6,乳清蛋白占总量18%~20%,等电点为4.1~4.8[16]。由于溶液中pH变化时,脱脂乳中蛋白质的表面电荷也发生变化,电荷的变化影响了蛋白质之间的静电作用及其聚集状态,从而影响了脱脂乳稀释液在晶振片表面的吸附。在pH小于5一侧,随着pH的减小,Δf变化也减小,在酸性条件下,脱脂乳中蛋白质带有正电荷而相互排斥,无法聚集吸附在电极表面,且pH越小,带有的正电荷数越多,排斥作用越明显,吸附量越小。在pH=5附近,由于靠近脱脂乳中大部分蛋白质的等电点,蛋白质分子带有的电荷少,分子间排斥力最小,各个分子容易相互聚集在一起,使得吸附量达到最大。在pH大于5一侧,由于脱脂乳中蛋白质带负电荷,随着pH增大,分子间排斥力增加,从而导致吸附量减小。由于脱脂乳中蛋白质占有比重较大,蛋白质在吸附过程中贡献率较大。蛋白质作为两性电解质,带有可解离的酸性和碱性基团,在不同的pH环境下,蛋白质可带有正、负电荷形成离子形式,蛋白质之间的聚集状态发生改变,进而影响蛋白质在电极表面的吸附。
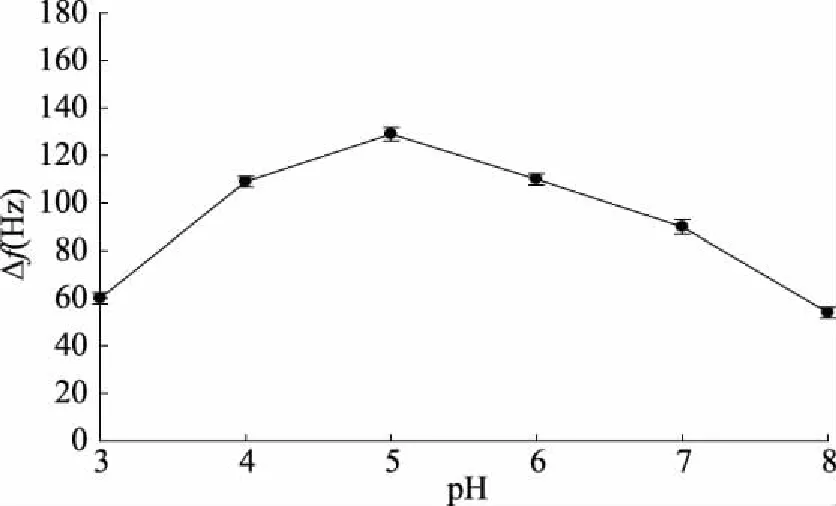
图4 pH与频率变化的关系Fig.4 The relationship between pH and frequency shift
2.2.3 离子浓度对脱脂乳在金晶振片上吸附的影响 图5可看出NaCl浓度改变造成频率变化,在0.05 mol/L到0.2 mol/L浓度范围内,脱脂乳在晶振片表面的吸附量随着NaCl浓度的增加而增大,在0.2~0.3 mol/L浓度范围内,随后NaCl浓度的增加造成吸附量逐渐减小,在浓度为0.2 mol/L时吸附量达到最大。由此可以看出离子浓度对于晶振片上的吸附有很大的影响,另外通过观察实验现象,还发现离子浓度对于金电极晶振片的平衡时间也有很大的影响,在低离子浓度情况下,平衡较快容易达到平衡,随着离子浓度的增加,晶振片体系的平衡时间也增加。当在脱脂乳稀释液中添加氯化钠时,一方面,离子浓度的增加改变了溶液中蛋白质的状态,乳中蛋白吸附离子,减小了乳中蛋白的静电排斥力作用,使蛋白容易聚合在一起,易于吸附在晶振片表面;另一方面,离子浓度的增加也改变了晶振片与溶液之间的界面性质,使得晶振片表面离子吸附增加,改变原有的双电层结构,减小了乳中蛋白在晶振片表面的吸附位能,使得乳中蛋白易于吸附。在较高离子强度下,盐离子强烈地屏蔽蛋白质分子和吸附剂之间的静电引力,使蛋白质分子难以在吸附剂表面上吸附和重排,吸附剂对蛋白质的吸附能力减弱[17]。
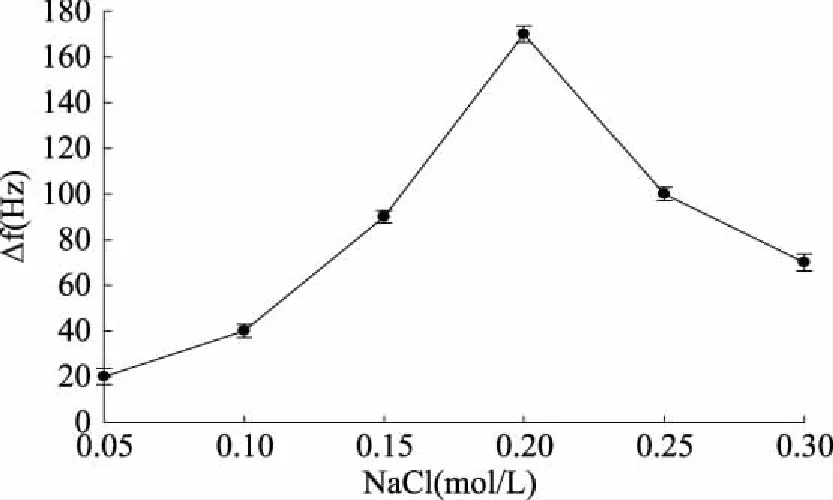
图5 氯化钠浓度与频率变化的关系Fig.5 The relationship between the concentration of sodium chloride and frequency shift
2.3循环伏安法(CV)和电化学交流阻抗法(EIS)表征电极吸附过程


图6 金电极的循环伏安图Fig.6 The cyclic voltammogram of the gold electrode


图7 金电极的交流阻抗图Fig.7 The electrochemical impedance spectra of the gold electrode
3 结论
在低浓度下,脱脂乳稀释液在金电极表面的吸附行为单分子层吸附。脱脂乳稀释液浓度、pH以及离子强度影响脱脂乳在金电极表面的吸附。在酸性条件下脱脂乳在电极表面吸附量较大,低浓度离子对吸附有促进作用。
[1]Scagion V P, Mercante L A, Sakamoto K Y, et al. An electronic tongue based on conducting electrospun nanofibers for detecting tetracycline in milk samples[J]. RSC Advances, 2016, 6(105):103740-103746.
[2]Bueno L, de Araujo W R, Salles M O, et al. Voltammetric Electronic Tongue for Discrimination of Milk Adulterated with Urea, Formaldehyde and Melamine[J]. Chemosensors, 2014, 2(4):251-266.
[3]Bueno L, de Araujo W R, Salles M O, et al. Voltammetric electronic tongue for discrimination of milk adulterated with urea, formaldehyde and melamine[J]. Chemosensors, 2014, 2(4):251-266.
[4]Wei Z, Wang J, Zhang X. Monitoring of quality and storage time of unsealed pasteurized milk by voltammetric electronic tongue[J]. Electrochimica Acta, 2013, 88:231-239.
[5]黄赣辉, 邓少平. 人工智能味觉系统:概念, 结构与方法[J]. 化学进展, 2006, 18(4):494-500.
[6]曾祥盛, 邓丹雯, 黄赣辉, 等. 传感器阵列对生乳及其若干形态的差异性识别[J]. 食品科学, 2013, 34(12):208-212.
[7]黄赣辉, 石磊, 曾祥盛, 等. 综合型传感器阵列对掺杂生乳的识别[J]. 食品工业科技, 2014, 35(6):63-66.
[8]Farcas M, Cosman N P, Ting D K, et al. A comparative study of electrochemical techniques in investigating the adsorption behaviour of fibrinogen on platinum[J]. Journal of Electroanalytical Chemistry, 2010, 649(1):206-218.
[9]Silva D J R, Diniz F B. Electrochemical Impedance Spectroscopy Study of Concanavalin A Adsorption on Glassy Carbon Electrode:An Analysis of Capacitance Dispersion[J]. Electrochimica Acta, 2014, 119:99-105.
[10]Frumkin A N, Damaskin B B, Bockris J O M, et al. Modern Aspects of Electrochemistry[J]. Butterworths,1964:149.
[11]Gettens R T T, Bai Z, Gilbert J L. Quantification of the kinetics and thermodynamics of protein adsorption using atomic force microscopy[J]. Journal of Biomedical Materials Research Part A, 2005, 72(3):246-257.
[12]Bajpai A K, Mishra D D. Adsorption of fibrinogen onto macroporous, biocompatible sponges based on poly(2-hydroxyethyl methacrylate)[J]. Journal of Applied Polymer Science, 2006, 102(2):1341-1355.
[13]Farcas M, Cosman N P, Ting D K, et al. A comparative study of electrochemical techniques in investigating the adsorption behaviour of fibrinogen on platinum[J]. Journal of Electroanalytical Chemistry, 2010, 649(1):206-218.
[14]王秋菊. 浅析石英晶体的压电效应及应用[J]. 职业, 2013 (2):136-136.
[15]Sauerbrey G. Verwendung von Schwingquarzen zur Wägung dünner Schichten und zur Mikrowägung[J]. Zeitschrift für Physik, 1959, 155(2):206-222.
[16]Imamura K, Shimomura M, Nagai S, et al. Adsorption characteristics of various proteins to a titanium surface[J]. Journal of Bioscience and Bioengineering, 2008, 106(3):273-278.
[17]周笑鹏, 白姝, 孙彦. 离子强度和溶质浓度对蛋白质在Q Sepharose FF中吸附动力学的影响[J]. 化工学报, 2005, 56(1):130-134.
TheadsorptionofskimmedmilkatAuelectrodebyelectrochemicalmethod
LIChang-gao1,ZENGShan-rong2,LAILi-zhi1,HUANGGan-hui1,*,DENGDan-wen1
(1.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China; 2.Ganzhou Center For Food and Drug Control,Ganzhou 341000,China)
In the study,the adsorption of skimmed milk at Au electrode was nvestigated. Differential capacitance were used to study skimmed milk of different concentrations dispersion adsorption property on the surface of Au electrode,the adsorption behavior of milk on the Au electrode was characterized by cyclic voltammetry and electrochemical impedance spectroscopy. The adsorption behavior of different skimmed milk dispersion on gold crystal surface were researched by QCM. The results showed that within a certain concentration range,skimmed milk dispersion was monomolecular layer adsorption on the surface of the Au electrodes and in line with the Langmuir adsorption isotherm equation. Skimmed milk on the adsorption of gold crystal surface gradually reached saturation with the increasing skimmed milk concentration. In different pH buffer solutions,the adsorption quantity of milk on gold crystal surface was different,with the maximum adsorption in the pH of 5. At the same concentration and pH,adsorption capacity increased firstly and then decreased with the increase of ionic strength.
differential capacitance;adsorption;Au electrode;QCM
2016-11-04
李昌高(1989-),男,硕士研究生,研究方向:电化学人工智能识别,E-mail:wwwlichanggao@163.com。
*通讯作者:黄赣辉(1967-),男,博士,教授,研究方向:电化学人工智能识别、功能性淀粉、天然产物提取利用,E-mail:huangganhui@163.com。
国家自然科学基金项目(31360387)。
TS252.1
:A
:1002-0306(2017)12-0113-06
10.13386/j.issn1002-0306.2017.12.021

