氮掺杂类金刚石薄膜的制备及生物相容性研究
吾凡别克·巴合提马嘉平米拉·巴合提阿依古丽·吐尔地董棣文祖力卡尔江·阿合买提
氮掺杂类金刚石薄膜的制备及生物相容性研究
吾凡别克·巴合提1马嘉平1米拉·巴合提2阿依古丽·吐尔地1董棣文1祖力卡尔江·阿合买提1
目的 利用等离子体增强化学气相沉积(Plasma Enhanced Chemical Vapor Deposition,PECVD)技术,在钛合金表面制备含氮类金刚石薄膜(DLC∶N),并对其生物相容性进行研究。方法采用扫描电子显微镜、X-射线光电子能谱仪、接触角测量仪、拉曼光谱仪对样品的表面形貌特征、组成元素和表面润湿性进行表征;利用MTT比色法、荧光染色法进行生物学行为的评价。结果成骨细胞在掺氮类金刚石薄膜(DLC∶N)表面不论是增殖黏附状态还是细胞数量都优于其他实验组(P<0.05)。结论在DLC中加入氮元素,能够提升其生物相容性,促进成骨细胞黏附和增殖。
类金刚石薄膜;氮掺杂;黏附;生物相容性
类金刚石薄膜(Diamond-Like Carbon Film,DLC)的产品涉及机械、光学、电子和医学等各个领域,因为其具有出色的耐磨损性、超高硬度、高表面光洁度及生物相容性[1-3]。对于DLC薄膜,研究人员一直尝试用不同方法来改进其性能,在DLC薄膜中掺杂金属离子提高DLC的机械性能就是其中一种[4-10]。但Gutensohn等认为,在人体环境中,无法保证DLC薄膜中的金属离子,如W、Cr、Ni,不发生释放而引起细胞毒性或者过敏反应[11,12]。对于DLC中掺杂非金属元素的研究,Liao发现在类金刚石薄膜中掺杂氮元素能够增强类金刚石薄膜的耐腐蚀性能[13],但对于掺入氮元素是否会影响其生物相容性的研究较少。本实验通过等离子体增强化学气相沉积(Plasma Enhanced Chemical Vapor Deposition,PECVD)技术制备掺氮类金刚石薄膜(DLC∶N)并表征,同时与成骨细胞体外共培养,对其生物相容性和成骨细胞活性进行评价。
1 实验方法
1.1 薄膜制备
将医用钛合金片(双威金属制品有限公司,江苏)通过由粗到细的砂纸逐级打磨抛光至镜面状,超声荡洗20分钟,用氮气吹干备用,记为Ti组。
通过PECVD技术在备用的钛合金片表面分别制备出单纯的DLC薄膜(记为DLC组)以及含有氮元素的DLC薄膜(记为DLC∶N组)。制备参数见表1。
1.2 类金刚石薄膜的表征
采用扫描电子显微镜(SEM)、X-射线光电子能谱仪(XPS)、激光拉曼光谱仪(Raman)、接触角测量仪对Ti组、DLC组以及DLC∶N组的表面形态特征进行观察、对元素含量、拉曼光谱及表面润湿性能进行观察、测量、分析。
1.3 生物学性能研究
将Ti组、DLC组以及DLC∶N组样品同成骨细胞分别共培养1、3、5天(每个时间点每组6个样),采用MTT比色法检测样品吸光度值,并记录结果。
对各组样品表面培养第5天的成骨细胞固定并用荧光染色法染色,通过荧光显微镜(Olympus BX5-1型)对细胞附着形态进行观察。利用Image J软件对三组样品表面细胞进行计数及所占面积进行统计学分析。
2 结果
2.1 扫描电镜、XPS、Raman、接触角
图1为Ti组、DLC组以及DLC∶N组样品在SEM下的表面形貌图。Ti组表面呈现不规则的凹坑及划痕状结构。DLC组和DLC∶N组表面呈平滑的浅凹和波浪状结构,将钛合金基底表面凹坑及划痕状结构覆盖。

图1 Ti、DLC、DLC∶N组扫描电镜图(×100)
图2 所示为Ti组、DLC组以及DLC∶N组样品的XPS测试图。在Ti组表面测出Ti2p(456 ev)峰。而DLC组和DLC∶N组中,未出现Ti2p峰。DLC组中以C1s(285 ev)和O1s(531ev)为主。DLC∶N组以C1s(285 ev)、O1s(531ev)、N1s(398 ev)为主,其中氮元素含量为4.9%,说明含氮元素类金刚石薄膜制备成功。


图2 Ti6Al4V、DLC、DLC∶N的XPS光谱图
图3 为DLC组和DLC∶N组的拉曼光谱图。典型的DLC薄膜具有分布在1520 cm-1处的G峰以及分布于1220 cm-1左右的D峰,两组样品均具有DLC薄膜的典型特征,也说明了DLC薄膜的结构没有受到掺入N元素的影响。

图3DLC、DLC:N薄膜的拉曼光谱图
图4 为三组样品表面接触角测试图,Ti组表面相对亲水,平均接触角为49.82°(图3);DLC∶N组相对于DLC组更加亲水。Xu LC等学者研究发现[14-17]:一般情况下,细胞在接触角低于54°的材料表面不易黏附。而Sen A研究认为细胞最容易在表面接触角为66°的材料表面黏附生长[16],三组材料中DLC∶N组(70.40°)最为接近。

图4 Ti6Al4V、DLC、DLC∶N平均接触角
2.2 生物学性能
图5(彩图见插页)所示为MTT比色法得到的Ti组、DLC组以及DLC∶N组样品细胞增殖率的比较。可见DLC组以及DLC∶N组表面成骨细胞增殖率在第1、第3天均大于Ti组(P<0.05),DLC组增殖率在第5天同Ti组无明显差异(P≥0.05),DLC∶N组在每个测试时间点的增殖率均高于Ti组,在第1天和第5天的增殖率高于DLC组(P<0.05),说明DLC∶N组对于成骨细胞黏附生长有明显促进作用。

图5成骨细胞在Ti6Al4V、DLC、DLC∶N薄膜表面细胞的增殖率
图6 (彩图见插页)为Ti组、DLC组以及DLC∶N组表面成骨细胞第5天的荧光染色图。可以看出,三组材料表面细胞核形态保持正常,无细胞核碎片出现,说明无早期细胞凋亡和坏死现象。细胞以圆球形、长梭形为主,数量以长梭形细胞居多。Ti组和DLC组的表面细胞具有明显伪足,但密度较稀疏;DLC∶N组细密度更高,细胞延伸出长短不同的突起,具有良好的铺展性和团簇生长倾向。利用Image J软件完成细胞计数的统计,标记样品表面细胞数,细胞所占总面积以及平均细胞面积进行比较。统计结果如表2。DLC∶N组表面成骨细胞在细胞数量、所占面积上都明显优于其他实验组(P<0.05),也证实了DLC∶N组能促进表面成骨细胞的增殖。
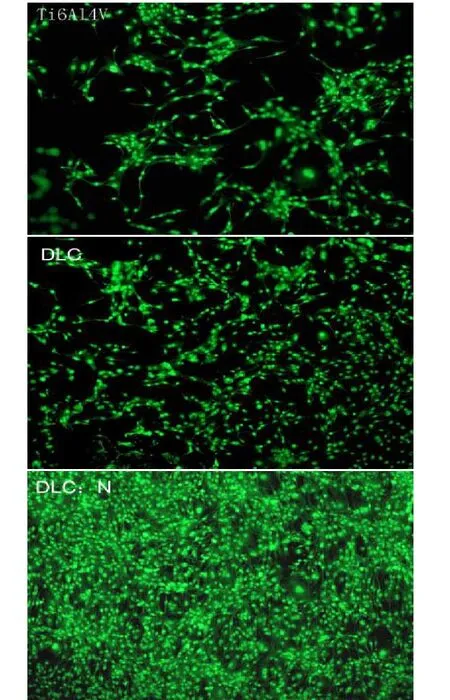
图6 Ti6Al4V、DLC、DLC∶N薄膜表面的成骨细胞的荧光照片(×100)

表2 Ti6Al4V、DLC、DLC∶N表面成骨细胞计数、细胞总面积和平均尺寸
3 讨论
对于骨科植入材料来说,我们需要材料具有良好的机械性能及出色的生物相容性。类金刚石薄膜在问世以来就受到医学界研究人员的广泛关注,这同其自身结构和特性密不可分,类金刚石薄膜是由C原子以Sp2和Sp3杂化轨道组合,兼备金刚石的机械性能以及石墨材料的生物学性能,它的产品涉及机械、光学、电子和医学等各个领域[1],但对于类金刚石薄膜的改性也一直在继续,曾有研究人员通过掺杂金属元素来降低薄膜内部应力,但在生物组织环境中金属元素可能会从薄膜中析出,影响材料生物学性能[11,12]。N元素是蛋白质主要组成元素,不会产生细胞毒性,其次Liao研究发现在类金刚石薄膜中掺杂氮元素能够增强类金刚石薄膜的耐腐蚀性能[13],但对于掺入氮元素是否会影响DLC薄膜生物相容性的研究较少。本实验通过PECVD技术制备掺氮类金刚石薄膜(DLC∶N)并表征,同时与成骨细胞体外共培养,研究其生物学行为,为最终临床应用提供依据。
首先通过XPS及拉曼光谱检测,我们发现采用PECVD技术在一定参数下可以成功制备掺杂氮元素的类金刚石薄膜(图2),而且在钛合金表面的DLC和DLC∶N可以完全覆盖薄膜,这对于植入性材料来说,隔绝了基底金属材料同组织之间的接触,防止周围体炎的发生。其次电镜下我们发现钛合金材料虽然经过打磨抛光至镜面状,但在电镜下仍具有许多凹坑状结构,经过严格清洗消毒后仍会有少量金属碎屑掺杂其中,这必将影响植入体在体内的长期使用,但经过薄膜表面处理后,表面呈致密浅凹状,通过简单清洗就能将表面清洗干净,基本不会残留碎屑。而通过表面亲水性测试可以发现,类金刚石薄膜相对于钛合金表面来说相对疏水,但通过掺氮处理可以使其更加亲水,Sen研究认为细胞最容易在表面接触角为66°的材料表面黏附生长[16],三组材料中DLC∶N组(70.40°)最为接近。
最后,我们通过MTT实验对于三组材料表面成骨细胞生长情况进行测试,并通过荧光显微镜观察发现,DLC∶N组表面成骨细胞生长状况明显好于DLC组以及Ti组,N元素的掺入对于促进DLC薄膜表面成骨细胞黏附生长的原因可能为以下几点:和Ti组相比,DLC∶N可以把基底材料完全覆盖,防止钛合金基底(Ti6Al4V)中Al元素的释放而产生细胞毒性,而且致密光滑的表面,也可以防止影响细胞增殖的碎屑材料残留于基底凹坑结构中。相比于DLC组,N元素的加入使得DLC薄膜亲水角更接近最适于细胞初期黏附的接触角度。N元素是我们人类必不可少的营养物质—蛋白质的组成部分,不但没有细胞毒性,而且还有可能同表面细胞形成某种化学键结构,促进细胞黏附增殖。综上所述,对于DLC薄膜来说,掺氮是一种切实有效的改性方法,DLC∶N不但可以大大提升材料表面耐磨损能力,硬度以及光洁度,还增加了材料的生物相容性能,展示了作为植入性材料应用于实际临床中的潜力。
4 结论
本文采用PECVD技术,在钛合金表面成功制备了DCL∶N薄膜。在材料表面接种培养成骨细胞,通过MTT、荧光染色法对成骨细胞的生物学性能进行评价,结果表明钛合金表面的DCL∶N薄膜具有良好的生物相容性。
[1]Bewilogua K,Hofmann D.History of diamond-like carbon films-From first experiments to worldwide applications[J].Surface& Coatings Technology,2014,242(4):214-225.
[2]Miksovsky J,Voss A,Kozarova R,et al.Cell adhesion and growth on ultrananocrystalline diamond and diamond-like carbon films after different surface modifications[J].Applied Surface Science, 2014,297(2):95-102.
[3]Roy R K,Lee K R.Biomedical applications of diamond-like carbon coatings:a review.[J].Journal of Biomedical Materials Research Part B Applied Biomaterials,2007,83(1):72-84.
[4]Allen M,Law F,Rushton N.The effects of diamond-like carbon coatings on macrophages,fibroblasts and osteoblast-like cells in vitro[J].Clinical Materials,1994,17(1):1-10.
[5]Yang WJ,Sekino T,Shim KB,etal.Deposition and microstructure of Ti-containing diamond-like carbon nanocomposite films[J]. Thin Solid Films,2005,473(2):252-258.
[6]Chiu MC,Hsieh WP,Ho WY,et al.Thermal stability of Cr-doped diamond-like carbon films synthesized by cathodic arc evaporation[J].Thin Solid Films,2005,476:258-263.
[7]Wang A Y,Lee K R,Ahn J P,et al.Structure and mechanical properties of W incorporated diamond-like carbon films prepared by a hybrid ion beam deposition technique[J].Carbon,2006,44(9): 1826-1832.
[8]Ji L,Li H,Zhao F,et al.Microstructure and mechanical properties of Mo/DLC nanocomposite films[J].Diamond&Related Materials,2008,17(11):1949-1954.
[9]Khun N W,Liu E,Yang G C.Structure,scratch resistance and corrosion performance of nickel doped diamond-like carbon thin films[J].Surface&Coatings Technology,2010,204(20):3125-3130.
[10]Dai W,Wang A.Deposition and properties of Al-containing diamond-like carbon films by a hybrid ion beam sources[J].Journal of Alloys&Compounds,2011,509(13):4626-4631.
[11]Gutensohn K,Beythien C,Bau J,et al.In vitro analyses of diamond-like carbon coated stents.Reduction of metal ion release, platelet activation,and thrombogenicity[J].Thrombosis Research, 2000,99(6):577-585.
[12]Gillespie W J,Frampton C M,Henderson R J,et al.The incidence of cancer following total hip replacement[J].Bone&Joint Journal,1988,70(4):539-542.
[13]Liao W H,Lin C R,Wei D H,et al.Concurrent improvement in biocompatibility and bioinertness of diamond-like carbon films with nitrogen doping[J].Journal of Biomedical Materials Research Part A,2012,100(11):3151
[14]Webster T J,Ergun C,Doremus R H,et al.Enhanced osteoclastlike cell functions on nanophase ceramics[J].Biomaterials,2001, 22(11):1327-1333.
[15]Hallab N J,Bundy K J,O'Connor K,et al.Evaluation of metallic and polymeric biomaterial surface energy and surface roughness characteristics for directed cell adhesion[J].Tissue Engineering, 2001,7(1):55-71.
[16]Sen A,Barizuddin S,Hossain M,et al.Preferential cell attachment to nitrogen-doped diamond-like carbon(DLC:N)for the measurementofquantalexocytosis[J].Biomaterials,2009,30(8):1604-1612.
[17]Xu L C,Siedlecki C A.Effects of surface wettability and contact time on protein adhesion to biomaterial surfaces[J].Biomaterials, 2007,28(22):3273-3283.
The research of preparation and biocompatibility of nitrogen-doped diamond-like carbon films
Wufanbieke·Baheti1,Ma Jiaping1,Mira·Baheti2,et al.1 Department of Stomatology,People's Hospital of Xinjiang Uygur Autonomous Region;2 Xinjiang Medical University,Xinjiang Urumqi,830000,China
Objective The nitrogen-doped diamond-like carbon film(DLC∶N)was made on Ti6Al4V alloy by means of plasma enhanced chemical vapor deposition(PECVD)technique,and its biocompatibility researched.Methods The surface morphology,chemicalcomposition and contact angle were characterized by means ofSEM,XPS,Raman Spectrometer and contact angle measuring device.The biological behavior was evaluated by MTT and fluorescent staining. Results The proliferation of osteoblastscell on the surface of nitrogen-doped diamond like carbon films(DLC∶N)were higher than those of other experimental groups(P<0.05).Conclusion The addition of nitrogen in DLC can enhance its biocompatibility,improve adhesion and proliferation of osteoblast.
Diamond-like carbon;N-doped;Biocompatibility
R318
A
10.3969/j.issn.1672-5972.2017.03.003
swgk2016-12-00292
2016-12-19)
1新疆维吾尔自治区人民医院口腔科;2新疆医科大学口腔医学院,新疆乌鲁木齐830000
吾凡别克·巴合提(1988-)男,硕士,住院医师。研究方向:口腔医学。

