废无汞碱性电池极性材料制备锰锌铁氧体磁性纳米颗粒
郝 旗,余 静,袁 率,朱顺利,王 博,邱海浪
(成都信息工程大学 资源环境学院,四川 成都 610225)
综合利用
废无汞碱性电池极性材料制备锰锌铁氧体磁性纳米颗粒
郝 旗,余 静,袁 率,朱顺利,王 博,邱海浪
(成都信息工程大学 资源环境学院,四川 成都 610225)
以硝酸浸取废无汞碱性电池极性材料,再加入硝酸铁及蔗糖生成前驱体,最后通过焙烧制得锰锌铁氧体磁性纳米颗粒。优化了酸浸和焙烧条件,采用FTIR和DTA-TG技术研究了前驱体的形成和热解过程,采用XRD、FTIR、TEM技术和振动样品磁强计对锰锌铁氧体进行了表征。结果表明:废无汞碱性电池极性材料酸浸的最佳条件为H2O2加入量3%(w)、液固比10 mL/g、稀硝酸浓度4 mol/L、浸取温度40 ℃,该条件下浸取10 min锰和锌的浸出率均可达100%;所得前驱体为葡萄糖酸盐,其最佳焙烧条件为焙烧温度450 ℃、焙烧时间2 h;最佳条件下所得锰锌铁氧体为尖晶石型Mn0.5Zn0.5Fe2O4,其颗粒为球形、大小均匀,且磁性能优良。
废碱性电池;蔗糖;硝酸盐;锰锌铁氧体;磁性纳米颗粒
铁氧体材料分为软磁、硬磁、旋磁、矩磁和亚磁五类[1-2],其中,被广泛应用的锰锌铁氧体[3-5]是软磁铁氧体的代表之一。近年来,具有尖晶石结构的锰锌铁氧体(Mn1-xZnxFe2O4)磁性纳米颗粒逐渐被应用于废水处理领域中,可作为磁性载体、吸附剂、催化剂等[6-9]。如姜德彬等[10-11]制备了锰锌铁氧体表面包裹SiO2的核壳型磁性纳米复合物吸附剂,对亚甲基蓝表现出良好的吸附性能,且可快速实现固液分离。
锰锌铁氧体的制备分为干法工艺和湿法工艺。其中,湿法工艺因制备的锰锌铁氧体成分均匀,粉体烧结活性高而得到广泛应用。湿法工艺主要有共沉淀法、水热法、溶胶-凝胶法等[12-13]。其中,柠檬酸溶胶-凝胶法工艺简单、产品均匀性较高,但原料成本高、反应时间长、产率低等缺点使其难以工业化应用。因此,高效、低成本的锰锌铁氧体制备方法成为研究的焦点。
随着科技进步和社会发展,无汞碱性电池在一次电池中占据主导地位,在生活中被广泛使用。无汞碱性电池的极性材料的主要成分为锰和锌的氧化物,正是制备锰锌铁氧体所需的原料。
本工作以硝酸浸取废无汞碱性电池极性材料,再加入硝酸铁及蔗糖生成前驱体,最后通过焙烧制得锰锌铁氧体。优化了酸浸和焙烧条件,并对前驱体和锰锌铁氧体进行了表征。该制备方法工艺简单、成本低廉,为废无汞碱性电池资源化提供了可行性,对保护不可再生资源亦具有重要意义。
1 实验部分
1.1 试剂、材料和仪器
85%(w)硝酸、30%(w)H2O2溶液、硝酸锰、硝酸锌、硝酸铁、蔗糖:成都科龙化工试剂厂,分析纯。
废无汞碱性电池(以下简称废电池):废弃的市售5号南孚无汞废碱性锌锰电池。
GGX-6型赛曼火焰原子吸收分光光度计:北京海光仪器公司;DX-2700型X射线衍射仪:辽宁丹东方圆仪器厂;XRF-1800型X射线荧光分析仪:日本岛津公司;FTIR-8400S型傅里叶变换红外光谱仪:日本岛津公司;HCT-2型差热分析仪:北京恒久科学仪器厂;JEM-2100F型透射电子显微镜:日本电子株式会社;CFM-5型振动样品磁强计:Crygenic公司。
1.2 实验方法
1.2.1 废电池的人工拆解
人工拆解废电池(见图1)。将所得废电池的极性材料(图1的4和5)研磨、水洗、烘干,得到预处理后的极性材料,其成分(X射线荧光分析仪测定)见表1。
1.2.2 极性材料的酸浸
称取5 g预处理后的极性材料置于250 mL烧杯中,加入已预热的一定浓度的稀硝酸(浓硝酸稀释而成),再加入一定量的H2O2溶液。将烧杯置于40℃水浴中,玻璃棒搅拌下反应10 min。将反应液过滤,即得含有硝酸锌和硝酸锰的酸浸液。将H2O2有效质量与混合后所有物质总质量的百分比定义为H2O2加入量,将稀硝酸的体积与预处理后的极性材料的质量之比定义为液固比。

图1 废电池的拆解

表1 预处理后极性材料的成分 w,%
1.2.3 锰锌铁氧体的制备
根据目标产物化学式,按照化学计量比向电池酸浸液中加入所需的金属硝酸盐,得到溶液A;取适量蔗糖(金属离子与蔗糖的摩尔比为1∶1),加少量水溶解,得到溶液B;分别将溶液A和B预热后混合,磁力搅拌条件下于110 ℃油浴中加热3 h,得到前驱体。
将前驱体在105 ℃下干燥90 min,得到干燥后前驱体。然后置于马弗炉中在空气气氛下焙烧,即得到锰锌铁氧体粉末。
1.3 分析方法
采用火焰原子吸收分光光度计测定酸浸液中锰离子与锌离子的浓度,分别计算锰和锌的浸出率(酸浸液中锰或锌的质量占酸浸前极性材料中锰或锌质量的百分比)。
采用FTIR,DTA-TG,XRD,TEM技术对试样进行表征分析。采用振动样品磁强计对试样进行磁性能分析。
2 结果与讨论
2.1 酸浸条件对酸浸效果的影响
2.1.1 H2O2加入量
在液固比10 mL/g、稀硝酸浓度4 mol/L、浸取温度40 ℃的条件下,H2O2加入量对浸出率的影响见图2。由图2可见:锰浸出率随H2O2加入量的增加而增大,当H2O2加入量为3%时,锰浸出率最大;但H2O2加入量对锌浸出率影响较小,锌浸出率均保持在较高水平。根据体系中各氧化还原电对的标准电极电势值[14]可推测存在如式(1)的反应,根据反应前后各物质的标准摩尔生成吉布斯自由能[14],可得该反应的标准吉布斯自由能变为-117.19 kJ/ mol,数值小于0表明该反应具有热力学可能性。因此,加入H2O2可提高锰的浸出率。也有其他文献表明,MnO2难溶于稀酸中,如稀盐酸、稀硫酸,但可溶于加入一定量H2O2的稀酸中[15-16],这与本实验的研究结果相符。

图2 H2O2加入量对浸出率的影响
由图2还可见,当H2O2加入量超过3%时,锰浸出率出现下降。这可能是由于MnO2完全反应后,反应生成的Mn2+与过量的H2O2存在如式(2)的反应所致。综合考虑,选择H2O2加入量为3%。

2.1.2 液固比
在H2O2加入量3%、稀硝酸浓度4 mol/L、浸取温度40 ℃的条件下,液固比对浸出率的影响见图3。由图3可见,锰和锌的浸出率均随液固比的增大而增大,并分别在液固比为10 mL/g和15 mL/g时达到最大值。综合考虑两种离子的浸出效果,选择液固比为10 mL/g。
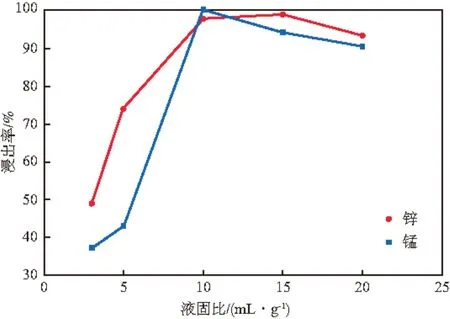
图3 液固比对浸出率的影响
2.1.3 稀硝酸浓度
在H2O2加入量3%、液固比10 mL/g、浸取温度40 ℃的条件下,稀硝酸浓度对浸出率的影响见图4。由图4可见:锰和锌的浸出率均在稀硝酸浓度为0.1~2.0 mol/L的范围内呈线性增加趋势;当稀硝酸浓度超过2 mol/L后,锰和锌的浸出率增加缓慢,在稀硝酸浓度为5 mol/L时浸出率达最大值;此后,锰和锌的浸出率均有所下降。综合考虑药剂成本和浸出效果,选择稀硝酸浓度为4 mol/L。

图4 稀硝酸浓度对浸出率的影响
2.1.4 浸取温度
在H2O2加入量3%、液固比10 mL/g、稀硝酸浓度4 mol/L的条件下,浸取温度对浸出率的影响见图5。由图5可见,随着温度的升高,锰和锌的浸出率的变化越来越小。这是因为,由Arrhenius方程可推导出,对同一反应,温度升幅一定时低温条件下反应速率的增速更快[16]。综合考虑浸出效果和操作成本,选择浸取温度为40 ℃。
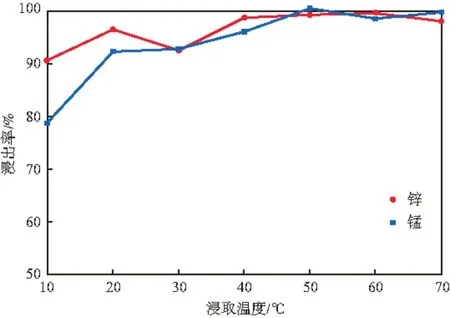
图5 浸取温度对浸出率的影响
在上述最佳条件下,锰和锌的浸出率均可达100%。
2.2 前驱体的表征结果
干燥后前驱体的FTIR谱图见图6。由图6可见:1 630 cm-1为羟基伸缩振动特征峰,1 364 cm-1为羧酸根的伸缩振动吸收峰,1 321 cm-1为C—O—H的面内弯曲振动峰,820 cm-1为—OH弯曲振动吸收峰;729 cm-1和495 cm-1可归属于金属与氧成键的特征吸收峰;在前驱体的谱图中,并未发现硝酸根的特征吸收峰(1 384 cm-1)。这是由于:蔗糖在酸性条件下可以水解生成葡萄糖和果糖,葡萄糖为多羟基醛类化合物,其分子中的醛基是还原性基团,在氧化剂Fe3+和NO3-存在时醛基被氧化成羧基,生成葡萄糖酸;而葡萄糖酸可解离形成羧酸根,羧酸根及羟基与锰、锌及铁络合,形成金属离子均匀分布的葡萄糖酸盐。
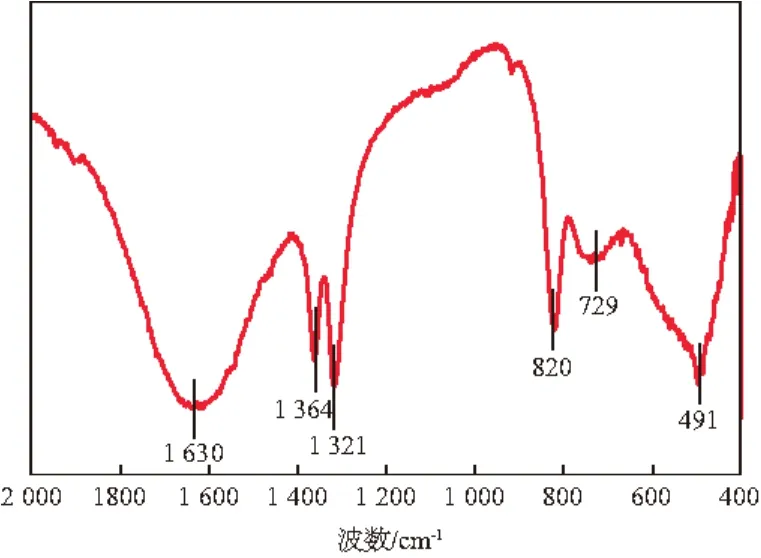
图6 干燥后前驱体的FTIR谱图
干燥后前驱体的DTA-TG曲线见图7。由图7可见:DTA曲线在164 ℃前存在一个较弱的放热峰,对应的TG曲线处有较小的失重,应为前驱体脱水所致;DTA曲线在164~390 ℃之间出现了一个宽而强的放热峰,对应的TG曲线处有较大的失重,应为前驱体中有机物燃烧而放出大量热所致,由于燃烧过程中某些元素以气体释放,故有较大失重;DTA曲线在390~562 ℃之间无放热峰存在,此时应为锰锌铁氧体的形成阶段,故适宜的焙烧温度应在此温度区间。
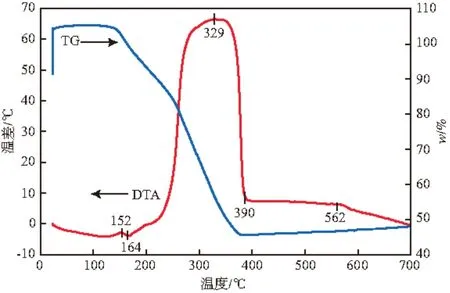
图7 干燥后前驱体的DTA-TG曲线
2.3 焙烧条件对锰锌铁氧体晶体结构的影响
前驱体经高温焙烧发生固相反应得到锰锌铁氧体粉末,其固相反应的机理很复杂,不同焙烧温度以及时间将直接影响锰锌铁氧体的晶体结构。
不同焙烧条件制备的锰锌铁氧体的XRD谱图见图8。由图8a可见:当焙烧温度为350 ℃时产物已经开始晶化,出现立方尖晶石型的特征衍射峰,衍射峰强度较弱,峰型较宽,表明产物晶化不完整,结晶度低,故需进一步提高焙烧温度;当焙烧温度为450 ℃时,谱图上仅有尖晶石锰锌铁氧体的特征衍射峰[17],衍射峰逐渐尖锐,峰宽变窄,这说明提高焙烧温度有利于铁氧体的晶化过程,该温度下固相反应完全,产物为单一尖晶石型;焙烧温度进一步升至550 ℃时,谱图上除尖晶石型的特征峰外,还有Fe2O3杂相的衍射峰存在;继续升高焙烧温度,Fe2O3杂相的衍射峰逐渐减弱。综上,适宜的焙烧温度为450 ℃,此时固相反应最完全,产物为单一尖晶石型。
由图8b可见:450 ℃下,焙烧时间超过1 h后,不同焙烧时间条件下所得产物的谱图基本相同,均无Fe2O3杂相衍射峰,粉体均为单一尖晶石型。但焙烧时间延长会导致锰锌铁氧体致密化、粒径变大,增加能耗及经济成本,故选择焙烧时间为2 h。
2.4 锰锌铁氧体的表征结果
锰锌铁氧体的FTIR谱图见图9。由图9可见,1 630 cm-1处为羟基伸缩振动特征峰,在567 cm-1处出现尖晶石铁氧体结构中次晶格A位的特征吸收峰,在443 cm-1处出现尖晶石铁氧体结构中次晶格B位的特征吸收峰[18]。
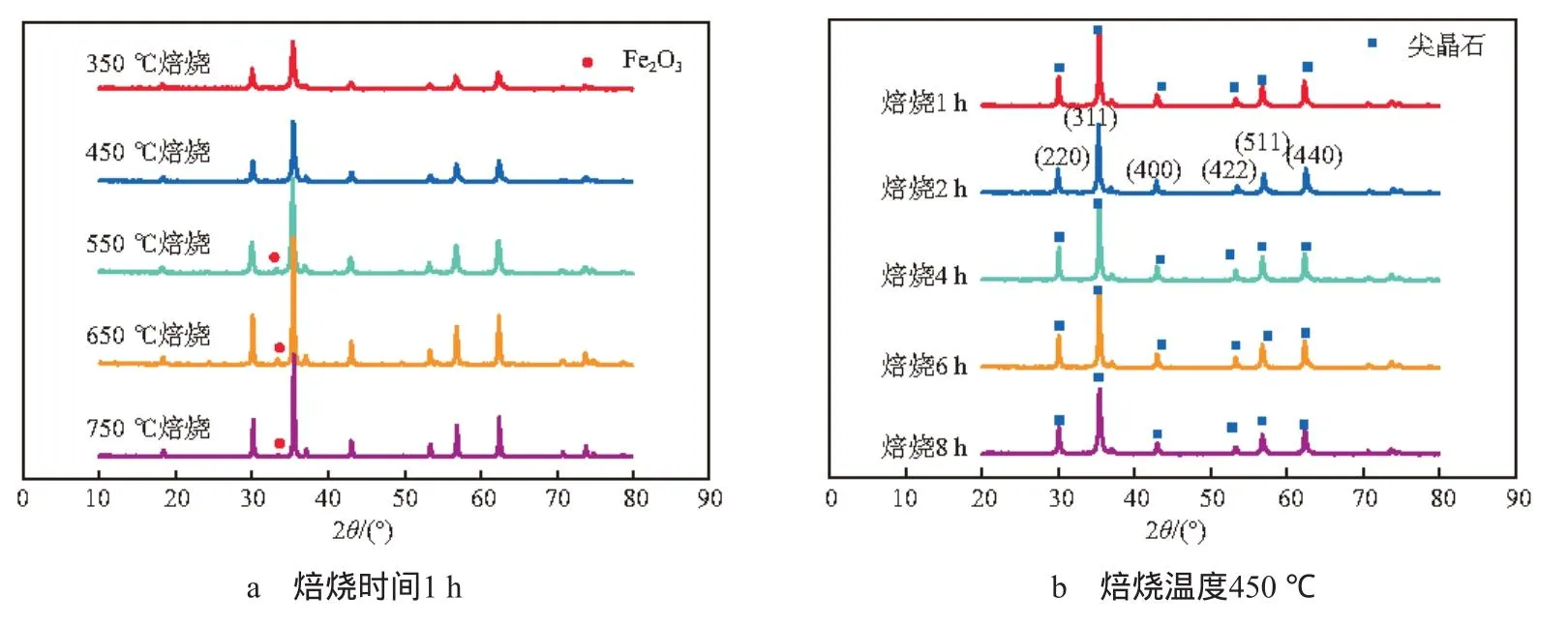
图8 不同焙烧条件制备的锰锌铁氧体的XRD谱图
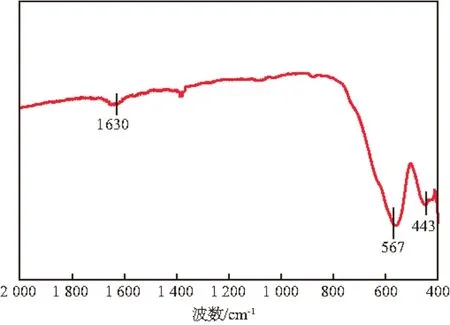
图9 锰锌铁氧体的FTIR谱图
将图8中优化条件下所得产物的谱图与Mn0.5Zn0.5Fe2O4标 准 谱 图[17]对 比 可 见 , 试样 在2θ=30.1°,35.4°,43.1°,53.0°,56.9°,62.4°分别出现特征衍射峰,各衍射峰的位置和相对强度与标准谱图基本吻合,说明所得产物为尖晶石结构的Mn0.5Zn0.5Fe2O4。根据Scherrer公式估算可得,锰锌铁氧体的晶粒尺寸为14.49 nm,晶格常数为0.820 7 nm。
锰锌铁氧体的TEM照片见图10。由图10可见,锰锌铁氧体颗粒为球形,大小均匀。这说明在优化条件下制备的锰锌铁氧体的结晶情况较好,晶化比较完整。此外,由于所制备的锰锌铁氧体具有磁性,故分散制样时易发生团聚现象。

图10 锰锌铁氧体的TEM照片
经测定,锰锌铁氧体的饱和磁化强度为10.3 A·m2/kg,剩余磁化强度磁为3.5 A·m2/kg,矫顽力为2 000 A/m,磁性能优良。
3 结论
a)废无汞碱性电池极性材料酸浸的最佳条件为:H2O2加入量3%,液固比10 mL/g,稀硝酸浓度4 mol/L,浸取温度40 ℃。该条件下浸取10 min后,锰和锌的浸出率均可达100%。
b)所得前驱体为葡萄糖酸盐,其最佳焙烧条件为:焙烧温度450 ℃,焙烧时间2 h。该条件下所得锰锌铁氧体为尖晶石型Mn0.5Zn0.5Fe2O4,其颗粒为球形、大小均匀,且磁性能优良。
[1] 曲远方. 功能陶瓷及应用[M]. 北京:化学工业出版社,2003:535 - 536.
[2] 关振铎,张中太,焦金生. 无机材料物理性能[M].北京:清华大学出版社,1992:391 - 398.
[3] Nagamatsu Jun,Nakagawa Norimasa,Muranaka Takahiro,et al. Superconductivity at 39 K in magnesiumdiboride[J]. Nature,2001,410(6824):63 - 64.
[4] Yang Cao,Jie Ren,Li Jianbo,et al. Preparation and characterization of Mn-Zn ferrite/poly(N,N′-isopropyl acrylamide)core/shell nanocomposites via in-situ polymerization[J]. Mater Lett,2010,64(14):1570 - 1573.
[5] Mathur P,Thakur A,Singh M. Low temperature synthesis of Mn0.4Zn0.6In0.5Al0.1Fe1.4O4nano-ferrite and characterization for high frequency applications[J]. Eur Phys J Appl Phys,2008,41(2):133 - 138.
[6] Harikishore Kumar Reddy D,Yun Yeoung-Sang. Spinel ferrite magnetic adsorbents:Alternative future materials for water purification?[J]. Coord Chem Rev,2016,315:90 - 111.
[7] 陈金媛,彭图治. 磁性纳米TiO2/Fe3O4光催化复合材料的制备及性能[J]. 化学学报,2004,62(20):2093 -2097.
[8] Wang Lixia,Li Jianchen,Wang Yingqi,et al. Adsorption capability for Congo red on nanocrystalline MFe2O4(M = Mn,Fe,Co,Ni)spinel ferrites[J]. Chem Eng J,2012,181/182:72 - 79.
[9] 张亚菲,刘晓茜,董清,等. 磁性多孔尖晶石铁氧体制备及催化臭氧性能[J]. 材料科学与工艺,2012,20(6):13 - 17.
[10] 姜德彬,余静,程庆峰,等. 锰锌铁氧体/SiO2复合磁性材料的制备和表征[J]. 化工环保,2015,35(5):536 - 541.
[11] 姜德彬,余静,叶芝祥,等. 磁性纳米复合物对水中亚甲基蓝的吸附及其机理研究[J]. 中国环境科学,2016,36(6):1763 - 1772.
[12] 席国喜,路迈西. 锰锌铁氧体材料的制备研究新进展[J]. 人工晶体学报,2005,34(1):164 - 168.
[13] 李伯刚,尹光福,查忠勇,等. 软磁MnZn铁氧体粉料可连续化生产新工艺[J]. 有色金属,1999,51(3):87 - 89,92.
[14] 大连理工大学无机化学教研室. 无机化学[M]. 5版.北京:高等教育出版社,2006:92 - 97.
[15] Khan M H,Gulshan F,Kurny A S W. Recovery of metal values from spent zinc-carbon dry cell batteries[J]. J Inst Eng:Ser D,2013,94(1):51 - 56.
[16] Shin Shun-Myung,Kang Jin-Gu,Yang Dong-Hyo,et al. Development of metal recovery process from alkaline manganese batteries in sulfuric acid solutions[J]. Mater Trans,2007,48(2):244 - 248.
[17] Arulmurugan R,Vaidyanathan G,Sendhilnathan S,et al. Mn-Zn ferrite nanoparticles for ferrofluid preparation:Study on thermal-magnetic properties[J]. J Magn Magn Mater,2006,298(2):83 - 94.
[18] Freitas M B J G,Garcia E M,Celante V G. Electrochemical and structural characterization of cobalt recycled from cathodes of spent Li-ion batteries[J]. J Appl Electrochem,2009,39(5):601 - 607.
(编辑 魏京华)
“连云港2017年挥发性有机物污染治理技术交流会”召开
2017年3月17日,由连云港市环境保护局主办、中国化工环保协会提供技术支持的“连云港2017年挥发性有机物污染治理技术交流会”在江苏省连云港市成功举办。90余家挥发性有机物治理技术供方单位以及全市600余家企业负责人参会。本次技术交流会不仅通过展台展示等形式为供需双方搭建交流平台,还同期安排了8场专题技术宣讲。上海安居乐、山东天利和、淄博宝泉、聚光科技、南京霍普斯、德睿测量、江苏天瑞、赛默飞世尔等公司分别就挥发性有机物污染治理、监测新技术、新方法等做了详细的技术宣讲,现场反应热烈。
本次交流会在中国化工环保协会和连云港市环保局的共同合作下,以政府搭台、企业唱戏、协会提供技术支持的形式,保障了交流会的成功举办,也全面助力了江苏省连云港市2017年挥发性有机物的污染治理工作。
2017年,中国化工环保协会还将从不同的污染物治理出发,联合各级单位不定期举办具有行业针对性和引领性的环保专项会议,向环保技术需方企业提供丰富的技术和设备资源,向环保技术供方单位提供广阔的市场平台,向化工行业参与者提供第一手的环保政策解读,为绿水青山贡献环保人的力量。
以上摘自《化工环保通讯》
Preparation of manganese-zinc ferrite magnetic nano-particles using spent polar material in mercury-free alkaline battery
Hao Qi,Yu Jing,Yuan Shuai,Zhu Shunli,Wang Bo,Qiu Hailang
(College of Resources and Environment,Chengdu University of Information Technology,Chengdu Sichuan 610225,China)
The spent polar material in mercury-free alkaline batteriy was leached in nitric acid and added ferric nitrates and sugar to form the precursor,and then manganese-zinc ferrite magnetic nano-particle was prepared by roasting. The conditions for acid leaching and roasting were optimized. The formation and thermal decomposition processes of the precursor were investigated by FTIR and DTA-TG methods. The manganese-zinc ferrite was characterized by XRD,FTIR,TEM methods and vibrating sample magnetometer. The results showed that:Under the optimum leaching conditions of H2O2amount 3%(w),ratio of liquid to solid 10 mL/g,nitric acid concentration 4 mol/L,leaching temperature 40 ℃and leaching time 10 min,the leaching rate of manganese and zinc both reached 100%;The precursor was gluconate,and the optimum roasting conditions were roasting temperature 450 ℃ and roasting time 2 h;The manganese-zinc ferrite prepared under these conditions was spinel Mn0.5Zn0.5Fe2O4with spherical particle shape,uniform size and good magnetic performance.
spent alkaline batteriy;sugar;nitrate;manganese-zinc ferrite;magnetic nano-particle
X705
A
1006-1878(2017)03-0340-06
10.3969/j.issn.1006-1878.2017.03.016
2016 - 09- 18;
2017 - 03 - 05。
郝旗(1990—),男,河南省周口市人,硕士生,电话13228203119,电邮 haoqicuit@163.com。联系人:余静,电话18615798673,电邮 yujing@cuit.edu.cn。
国家自然科学基金项目(51408076);四川省教育厅科研项目(15ZA0189);成都信息工程大学大学生创新创业训练计划项目(CX2015050)。

