创新高校基础有机化学教学的探索
武晓霞 李青 谢明胜


摘 要: 介绍一种通过红黑笔来判断电环化产物立体构型的方法,该方法具有红色、黑色区分明显,轨道翻转和旋转灵活,立体感强,道具简单易得等特点,且能解放双手,特别适合课堂教学,取得了很好的教学效果。最后,还列举了一些该方法应用的实例。
关键词:红黑笔;电环化反应;构型
中图分类号:G642 文献标志码:A 文章编号:2096-000X(2017)16-0126-03
Abstract: This paper introduced a method to determine the configuration of electrocyclic products via red-black gel pens. This method exhibited several features, including obviously distinguishingthe red and black, flexibly flip and rotatingthe orbital, strong tri-dimensional sense, and easily available materials. Especially, it could release our hands, which was suitable for classroom teaching. This method has acquired good teaching effect. Finally, several examples were listed employing the red-black gel pens method.
Keywords: red-black gel pens; electrocyclic reactions; configuration
在基础有机化学教学中,协同反应包括电环化反应、环加成反应和σ迁移反应三部分内容,这一章的内容比较抽象,对于初学者,尤其是立体感较弱的学生来说,学习起来相对困难。教材中[1,2]一般先介绍电环化反应,因此,如果能发展一种简单易学的判断电环化产物构型的方法,帮助同學们掌握电环化反应的规律,就有利于进一步学习其他协同反应,从而达到事半功倍的教学效果。
一、 问题的提出
在光照或加热的作用下,共轭多烯烃末端两个碳原子的π电子环合成一个σ键,从而形成比原来分子少一个双键的环状烯烃或者环状烯烃开环变成共轭多烯烃的反应统称为电环化反应。根据Woodward-Hoffmann规则,电环化反应时反应物按照顺旋或对旋的方式开环或关环。在开环或关环的过程中,两端碳原子上的取代基团,也会进行立体化学的转化,生成具有一定立体构型的电环化产物。
从图1我们可以看到(Z,E)-2,4-己二烯(1,3-丁二烯型化合物)在加热条件下环合,只得到顺-3,4-二甲基环丁烯,在光照时却得到反式异构体。(Z,Z,E)-2,4,6-辛三烯(1,3,5-己三烯型化合物)加热时得到反-5,6-二甲基-1,3-环己二烯,光照则得到顺式异构体。同学们一看,比较困惑,难以理解,怎么有的生成顺式?有的生成反式?这该如何判断?
二、红黑笔表示法
课堂教学工具:两只红笔、两只黑笔和两个燕尾夹。取两只黑笔,一头戴上黑笔帽,另一头戴上红笔帽,然后将两个燕尾夹分别夹在两只笔的中间(如图2)。我们用中性笔表示p轨道,黑笔帽表示p轨道的正相部分,红笔帽表示p轨道的负相部分(如图2左),燕尾夹代表烯烃端位上较大取代基,如果燕尾夹代表较小取代基如氢原子,也可以。σ键是轨道经轴向重叠形成的,因此在发生电环化反应时,末端碳原子的键必须旋转,发生同相位的重叠即红碰红或黑碰黑。如图2所示,端位上两个大取代基(甲基)均指向左边,只有顺旋才能使位相相同的轨道瓣相互交盖生成σ键,顺时针顺旋(黑碰黑)后两个燕尾尖方向均为朝上的,表示顺旋后这两个取代基(甲基)均为朝上的。逆时针顺旋(红碰红)后两个燕尾尖方向均为朝下的,表示顺旋后这两个取代基均为朝下的。
此红黑笔法具有以下特点:
1. 红色黑色区别明显,适用于课堂教学。
2. 立体感较强,能更直观的表示原料/产物的立体构型。
3. 学生无需死记硬背电环化反应的规则,只需记住红碰红、黑碰黑即可,便可轻松判断出加热或光照条件下是顺旋还是对旋。
4. 教学道具简单易得。
5. 红黑笔旋转和翻转灵活,使双手得以解放,可以同时进行板书和使用教鞭。
三、共轭链烯的分子轨道及其对称性规律
我们为什么只采用两只笔来研究电环化反应的立体化学过程呢?学习过前线轨道理论和分子轨道对称守恒原理以后,我们便可以很轻松地理解这个问题。
1,3-丁二烯(4n体系)和1,3,5-己三烯(4n+2体系)的分子轨道见图3。
从图3我们可以看出,链状共轭多烯的分子轨道是按照镜面对称-反对称-镜面对称交替分布的,能量最低的轨道为镜面对称,且共轭多烯两端碳原子的对称性与整个分子轨道的对称性是一致的,也是按照镜面对称-反对称-镜面对称交替分布的。
在判断电环化产物的立体构型时,仅涉及共轭多烯两端碳原子的P轨道,与中间碳原子的P轨道无关。因此,我们只需考虑共轭多烯两端碳原子的对称性规律或者只考虑HOMO与LUMO两端的对称性即可(无论是4n体系还是4n+2体系,只要是热反应一定是HOMO参与反应,只要是光照,一定是LUMO即新的HOMO参与反应),这样问题便大为简化。若用两只笔(一头戴黑笔帽一头戴红笔帽的黑笔)来表示1,3-丁二烯两端碳原子的HOMO和LUMO轨道,就是固定左手中的笔黑笔帽朝上不变,右手中的笔红笔帽朝上为HOMO轨道,再将右手中的笔翻转180°黑笔帽朝上即为LUMO轨道。
加热反应时,按照分子轨道对称性交替分布規律,同学们很容易判断出4n体系中HOMO为偶数,轨道为反对称,顺旋成键;4n+2体系中HOMO为奇数,轨道为对称,对旋成键。光照反应时,4n体系中LUMO为奇数,轨道为对称,对旋成键;4n+2体系中LUMO为偶数,轨道为反对称,顺旋成键。
四、红黑笔法举例
我们以(Z,E)-2,4-己二烯和(Z,Z,E)-2,4,6-辛三烯进行热环化和光照电环化反应为例,介绍电环化产物立体构型的判断办法。
1,3-丁二烯型化合物(4n体系)
具体做法:将两只笔中间的夹子均朝左摆放,夹子代表两个甲基(或两个氢原子),根据顺旋或对旋的要求,两只笔同时旋转90°,由夹子的朝向,判断产物的立体构型。
1,3,5-己三烯型化合物(4n+2体系)
具体做法:将两只笔中间的夹子均朝左摆放,夹子代表两个甲基(或两个氢原子),根据顺旋或对旋的要求,两只笔同时旋转90°,由夹子的朝向,判断产物的立体构型。
五、课堂练习
解题思路
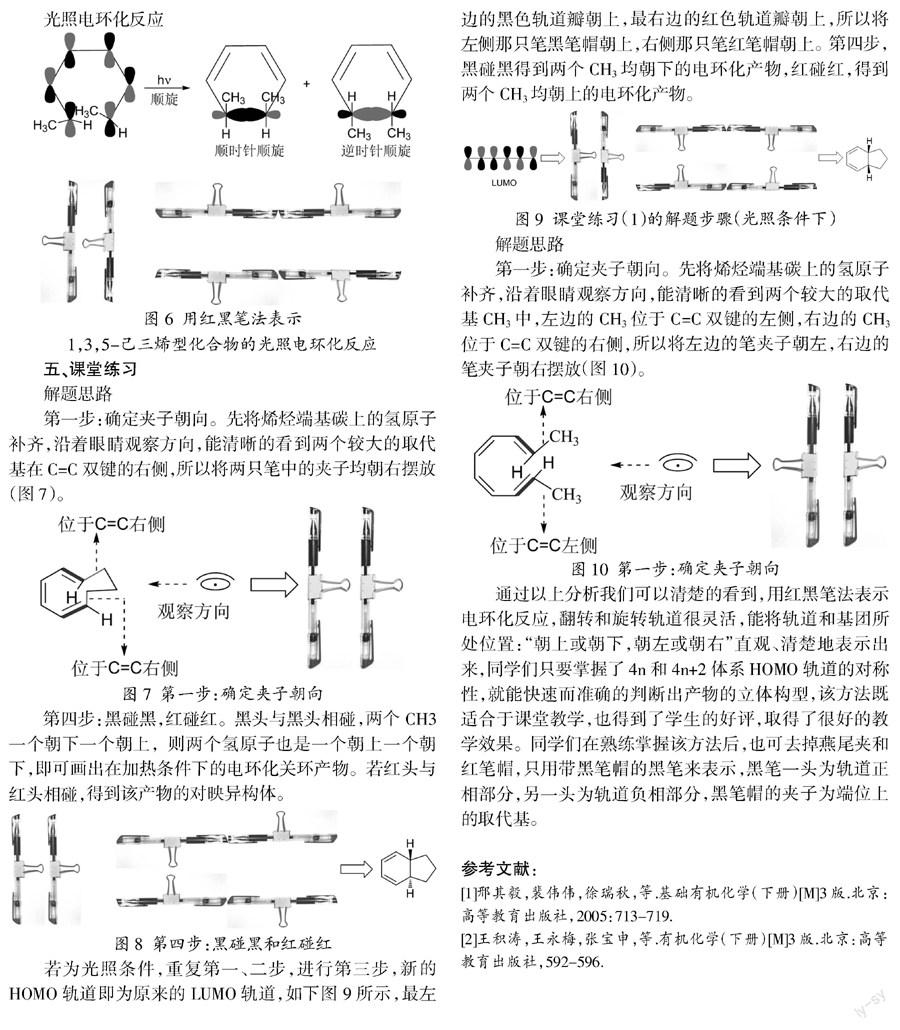
第一步:确定夹子朝向。先将烯烃端基碳上的氢原子补齐,沿着眼睛观察方向,能清晰的看到两个较大的取代基在C=C双键的右侧,所以将两只笔中的夹子均朝右摆放(图7)。
第四步:黑碰黑,红碰红。黑头与黑头相碰,两个CH3一个朝下一个朝上,则两个氢原子也是一个朝上一个朝下,即可画出在加热条件下的电环化关环产物。若红头与红头相碰,得到该产物的对映异构体。
若为光照条件,重复第一、二步,进行第三步,新的HOMO轨道即为原来的LUMO轨道,如下图9所示,最左边的黑色轨道瓣朝上,最右边的红色轨道瓣朝上,所以将左侧那只笔黑笔帽朝上,右侧那只笔红笔帽朝上。第四步,黑碰黑得到两个CH3均朝下的电环化产物,红碰红,得到两个CH3均朝上的电环化产物。
解题思路
第一步:确定夹子朝向。先将烯烃端基碳上的氢原子补齐,沿着眼睛观察方向,能清晰的看到两个较大的取代基CH3中,左边的CH3位于C=C双键的左侧,右边的CH3位于C=C双键的右侧,所以将左边的笔夹子朝左,右边的笔夹子朝右摆放(图10)。
通过以上分析我们可以清楚的看到,用红黑笔法表示电环化反应,翻转和旋转轨道很灵活,能将轨道和基团所处位置:“朝上或朝下,朝左或朝右”直观、清楚地表示出来,同学们只要掌握了4n和4n+2体系HOMO轨道的对称性,就能快速而准确的判断出产物的立体构型,该方法既适合于课堂教学,也得到了学生的好评,取得了很好的教学效果。同学们在熟练掌握该方法后,也可去掉燕尾夹和红笔帽,只用带黑笔帽的黑笔来表示,黑笔一头为轨道正相部分,另一头为轨道负相部分,黑笔帽的夹子为端位上的取代基。
参考文献:
[1]邢其毅,裴伟伟,徐瑞秋,等.基础有机化学(下册)[M]3版.北京:高等教育出版社,2005:713-719.
[2]王积涛,王永梅,张宝申,等.有机化学(下册)[M]3版.北京:高等教育出版社,592-596.

