药用植物双参正丁醇部位化学成分研究
陈雅凤,张祖珍,王福生
(大理大学药学与化学学院,云南大理 671000)
药用植物双参正丁醇部位化学成分研究
陈雅凤,张祖珍,王福生*
(大理大学药学与化学学院,云南大理 671000)
目的:对药用植物双参正丁醇部位的化学成分进行研究,以期寻找活性成分。方法:运用硅胶、AB-8、ODS以及凝胶等分离材料分离双参正丁醇部位,利用NMR技术鉴定化合物结构。结果:从双参正丁醇部位分离得到5个化合物,分别鉴定为(3S,4R,4a S,6S,7R,7a S)-Methyl3,6-dihydroxy-7-methyloctahydrocyclopenta〔c〕pyran-4-carboxylate(1)、咖啡酸甲酯(2)、(+)-Lariciresinol(3)、蔗糖(4)和Alyxialactone(5)。结论:这5个化合物首次从该植物中分离得到,其中,化合物1首次从天然产物中分离得到。
川续断科;双参;化学成分
双参(Triplostegia glandulifera)为川续断科双参属植物,又称萝卜参,对对参,童子参,肚拉,土洋参和一支蒿等,主要产于云南、西藏、四川等地〔1-2〕。双参因有补肾,健脾益气,活血调经的功能,常用于久病体虚、补血补气等〔2〕。
本课题组前期研究发现,云南民间药用植物双参的粗提物具有明显的降血糖功能和显著的抗氧化应激作用〔3-4〕。目前未见文献报道其化学成分,为了解药用植物双参的活性成分,本文对该植物地下部分的正丁醇部位进行了研究,从中分离鉴定了5个化合物,分别为(3S,4R,4a S,6S,7R,7a S)-Methyl 3,6-dihydroxy-7-methyloctahydrocyclopenta〔c〕pyran-4-carboxylate(1)、咖啡酸甲酯(2)、(+)-Lariciresinol(3)、蔗糖(4)和Alyxialactone(5)。化合物结构见图1。
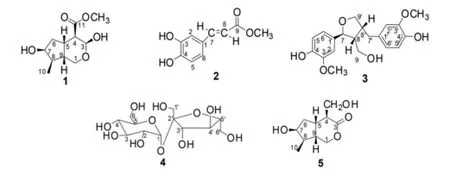
图1 化合物1~5的结构
1 仪器与材料
1.1实验材料双参采于云南省大理白族自治州云龙县五宝山,经大理大学段宝忠副教授鉴定为川续断科双参属植物双参(Triplostegia glandulifera Wall.ex D C.)的地下部分,植物标本(编号:WFS-20141128)存放于大理大学药学与化学学院王福生教授研究组。
1.2仪器与试剂NMR用Bruker AM-400型核磁共振仪测定;旋转蒸发仪RE-2000A(上海亚荣生化仪器厂);柱色谱硅胶与薄层色谱硅胶GF254(青岛海洋化工厂);Sephadex LH-20(Pharmacia);ODS(日本YMC公司);石油醚、氯仿、丙酮、乙酸乙酯、甲醇和乙醇等为工业级试剂,均需重蒸后使用。
2 提取与分离
取双参干燥地下部分3 kg,粉碎后用95%乙醇水冷浸反复提取5次浓缩得到浸膏,滤渣用50%乙醇水冷浸反复提取5次浓缩得到浸膏,将总浸膏分散于水中,依次用石油醚、乙酸乙酯和正丁醇萃取。将正丁醇部分浓缩得到的612 g浸膏经大孔吸附树脂(AB-8)分离,用水-甲醇(1:0,9:1,7:3,5:5,3:7,0:1)梯度洗脱,得到6个组分A~F。Fr.A经ODS柱层析和凝胶柱层析分离得化合物4(13 mg)。Fr.F反复经硅胶柱层析(氯仿-丙酮和氯仿-甲醇)、凝胶柱层析得化合物1(19 mg)、化合物2(10 mg)、化合物3(17 mg)和化合物5(11 mg)。
3 实验结果
化合物1:黄色糖浆状液体。1H NMR(400 MHz,CDCl3)δ:3.89(dd,J=12.2,3.9 Hz,1H,H-1α),3.85(dd,J=12.2,4.0 Hz,1H,H-1β),4.83(d,J= 8.6 Hz,1H,H-3α),2.20(dd,J=11.9,8.6 Hz,1H,H-4α),2.49(ddt,J=11.9,7.7,3.9 Hz,1H,H-5β),1.93~1.87(m,1H,H-6a),1.85~1.80(m,1H,H-6b),4.24(td,J=5.4,2.5 Hz,1H,H-7α),1.97~1.93(m,1H,H-8α),1.81~1.77(m,1H,H-9β),1.00(d,J=6.9 Hz,3H,H-10),3.71(s,1H,OCH3)。13CNMR(100 MHz,CDCl3)δ:64.31(C-1),95.93(C-3),52.72(C-4),38.17(C-5),39.72(C-6),74.64(C-7),38.86(C-8),41.84(C-9),11.77(C-10),173.76(C-11),52.21(OCH3)。以上数据与文献〔5〕报道的波谱数据基本一致,故确定化合物1为(3S,4R,4a S,6S,7R,7a S)-Methyl3,6-dihydroxy-7-methyloctahy⁃drocyclopenta〔c〕pyran-4-carboxylate。
化合物2:淡黄色粉末。1H NMR(400 MHz,CD3OD)δ:6.97(d,J=2.2 Hz,1H,H-2),6.71(d,J=8.1 Hz,1H,H-5),6.87(dd,J=8.1,2.2 Hz,1H,H-6),7.48(d,J=15.9 Hz,1H,H-7),6.19(d,J= 15.9 Hz,1H,H-8),3.69(s,3H,OCH3)。13C NMR(100 MHz,CD3OD)δ:127.64(C-1),115.07(C-2),149.54(C-3),146.77(C-4),116.45(C-5),122.92(C-6),146.92(C-7),114.77(C-8),169.73(C-9),51.98(OCH3)。以上数据与文献〔6〕报道的波谱数据一致,故确定化合物2为咖啡酸甲酯。
化合物3:黄色粉末。1HNMR(400 MHz,CDCl3)δ:6.90~6.66(m,6H,H-2,2′,5,5′,6,6′),4.79(d,J=6.6 Hz,1H,H-7α),2.91(dd,J=13.6,5.0 Hz,1H,H-7′a),2.54(dd,J=13.6,10.7 Hz,1H,H-7′b),2.47~2.34(m,1H,H-8β),2.80~2.64(m,1H,H-8′β),3.98~3.90(m,1H,H-9a),3.80~3.75(m,1H,H-9b),4.02~4.07(m,1H,H-9′a),3.75~3.70(m,1H,H-9′b),3.87(s,3H,OCH3),3.88(s,3H,OCH3′)。13C NMR(100 MHz,CDCl3)δ:134.89(C-1),132.40(C-1′),108.41(C-2),111.32(C-2′),149.49(C-3),148.13(C-3′),146.65(C-4),146.76(C-4′),114.54(C-5),114.31(C-5′),121.32(C-6),118.88(C-6′),82.94(C-7),33.46(C-7′),52.74(C-8),42.54(C-8′),61.02(C-9),73.03(C-9′),56.07(OCH3),56.05(OCH3′)。以上数据与文献〔7〕报道的波谱数据基本一致,故确定化合物3为(+)-Lariciresinol。
化合物4:白色晶体(甲醇)。1H NMR(400 MHz,D2O)δ:5.39(d,J=3.9 Hz,1H,H-1),3.54(dd,J= 10.0,3.9 Hz,1H,H-2),3.80(dd,J=10.0,9.6 Hz,1H,H-3),3.74(dd,J=9.6,9.4 Hz,1H,H-4),3.45(t,J=9.4 Hz,1H,H-5),3.80~3.75(m,4H,H-6,H-1′),4.20(d,J=8.8 Hz,1H,H-3′),4.03(t,J=8.8 Hz,1H,H-4′),3.87(m,1H,H-5′),3.65(d,J=3.1 Hz,2H,H-6′)。13C NMR(100 MHz,D2O)δ:92.11(C-1),71.01(C-2),72.51(C-3),72.34(C-4),69.16(C-5),62.30(C-6),61.28(C-6′),81.31(C-5′),73.93(C-4′),76.34(C-3′),103.62(C-2′),60.05(C-1′)。以上数据与文献〔8〕报道的波谱数据基本一致,故确定化合物4为蔗糖。
化合物5:白色粉末。1HNMR(400 MHz,Acetoned6)δ:3.77~3.70(m,1H,H-1a),3.70~3.64(m,1H,H-1b),2.56(q,J=2.9,2.0 Hz,1H,H-4α),2.54~2.48(m,1H,H-5β),2.17~2.10(m,1H,H-6a),1.63~1.57(m,1H,H-6b),2.54~2.48(m,1H,H-7α),1.79~1.73(m,1H,H-8α),2.26~2.17(m,1H,H-9β),1.05(d,J=6.8 Hz,3H,H-10),4.36(dd,J=11.2,6.2 Hz,2H,CH2OH)。13CNMR(100 MHz,Acetoned6)δ:61.02(C-1),175.71(C-3),47.24(C-4),36.51(C-5),42.24(C-6),76.50(C-7),43.15(C-8),43.68(C-9),13.64(C-10),70.11(CH2OH)。以上数据与文献〔9〕报道的波谱数据基本一致,故确定化合物5为Alyxialactone。
[参考文献]
〔1〕何银堂,胡作亮.本草名释与传说〔M〕.北京:中国中医药出版社,1998.
〔2〕大理白族自治州人民政府.大理中药资源志〔M〕.昆明:云南民族出版社,1991.
〔3〕刘晓波,郭美仙,李龙星,等.双参降血糖作用的研究〔J〕.云南中医中药杂志,2008,29(5):49-50.
〔4〕刘晓波,郭美仙,施贵荣.鸡肉参对小鼠抗应激作用的实验研究〔J〕.中国药事,2008,22(8):659-660.
〔5〕KOCSISÁ,SZABÓL F,PODÁNYI B.New Bis-Iridoids from Dipsacus laciniatus〔J〕.Journal of Natural Products,1993,56(9):1486-1499.
〔6〕任慧,徐巧林,董丽梅,等.南美蟛蜞菊中的酚酸类化学成分〔J〕.热带亚热带植物学报,2015,23(4):469-473.
〔7〕QIN WANG L,XING ZHAO Y,ZHOU L,et al.Lignans from Gnetum montanum Markgr.f.megalocarpua〔J〕. Chemistry of Natural Compounds,2009,45(3):424-426.
〔8〕周乐,王宁,杨维霞,等.秦岭龙胆的化学成分研究〔J〕.西北农林科技大学学报(自然科学版),2004,32(1):89-92.
〔9〕FENG T,CAI X H,DU Z Z,et al.Iridoids from the Bark of Alstonia scholaris〔J〕.Helvetica Chimica Acta,2008,91(12):2247-2251.
Study on Chemical Components from n-butanolFraction of MedicinalPlants Triplostegia glandulifera
Chen Yafeng,Zhang Zuzhen,Wang Fusheng*
(College of Pharmacy and Chemistry,Dali University,Dali,Yunnan 671000,China)
Objective:To study the chemical constituents of n-butanol fraction of Triplostegia glandulifera,aiming at searching for active components.Methods:The n-butanol fraction of T.glandulifera was separated by a combination of various chromatographied including silica gel,AB-8,ODS and LH-20 gel column chromatography methods,and the structure were identified based on spectroscopic analysis(1H NMR and13C NMR).Results:Five compounds were isolated from T.glandulifera and characterized as(3S, 4R,4a S,6S,7R,7a S)-Methyl 3,6-dihydroxy-7-methyloctahydrocyclopenta〔c〕pyran-4-carboxylate(1),Methyl caffeate(2),(+)-Lariciresinol(3),Sucrose(4)and Alyxialactone(5).Conclusion:The five constituents were isolated from this genus for the first time,and the compound 1 was isolated from naturalproducts for the firsttime.
Dipsacaceae;Triplostegia glandulifera;chemicalconstituents
R932
A
2096-2266(2017)04-0009-03
10.3969/j.issn.2096-2266.2017.04.003
(责任编辑 李 杨)
国家自然科学基金资助项目(31360082)
2016-09-06
2017-01-04
陈雅凤,硕士研究生,主要从事天然药物化学研究.
*通信作者:王福生,教授,博士.

