黄连颗粒剂与水煎剂的主要成分和抑菌效果对比研究
王 爽,何生虎,孙 鹏,郭亚男,曹思婷,张 鑫
(宁夏大学农学院,宁夏银川 750021)
黄连颗粒剂与水煎剂的主要成分和抑菌效果对比研究
王 爽,何生虎*,孙 鹏,郭亚男,曹思婷,张 鑫
(宁夏大学农学院,宁夏银川 750021)
为了对比黄连颗粒剂与水煎剂主要成分和抑菌效果,采用高效液相色谱法(HPLC)和薄层色谱法(TLC)对黄连对照药材、黄连饮片水煎剂与黄连颗粒剂中盐酸小檗碱等主要成分进行含量测定并比较,并进行了体外抑菌试验比较。结果表明,黄连颗粒剂与水煎剂所含有效成分基本一致,特征图谱在相同时间出现相似的峰,属于盐酸小檗碱特征峰;黄连煎剂和黄连颗粒剂的抑菌圈大小相似。说明在临床治疗中黄连颗粒剂可以代替黄连饮片应用。
黄连颗粒剂;盐酸小檗碱;黄连水煎剂;高效液相色谱法;薄层色谱法
黄连(味连RhizomaCoptischinensisFranch)为常用中药,具有清热燥湿、泻火解毒之功效[1],其主要活性成分为原小檗碱型生物碱。黄连的药用方法自古至今多为生用,亦有根据中医临床辨证用药的需要,将其炮制后入药的记载。其中,生黄连苦寒之性偏胜,善清心火;经反制即以热制寒,药性偏温;经从制即寒者益寒,可去肝胆之火[2]。为探讨黄连颗粒剂和黄连饮片之间的区别,从薄层色谱(TLC)、高效液相色谱(HPLC)和体外抑菌试验等进行研究,旨在为黄连颗粒剂的临床使用提供研究基础资料。
1 材料与方法
1.1 材料
1.1.1 试验药物 黄连对照药材(三角叶黄连)(批号:120913-201310)、盐酸小檗碱对照品(批号:110713-201212),中国食品药品检定研究院;黄连颗粒剂(批号:6031892,0.5 g包装相当于饮片3 g),广东一方制药有限公司;黄连饮片(批号:150501),毫州金勺堂中药饮片有限公司。
1.1.2 主要试剂 乙醇,甲醇,环己烷,乙酸乙酯,异丙醇,三乙胺,浓氨水,乙腈,磷酸二氢钾,十二烷基硫酸钠,盐酸等。
1.1.3 菌种与培养基 菌种:金黄色葡萄球菌、大肠埃希菌、沙门菌和链球菌,均由宁夏大学农学院兽医微生物实验室分离、鉴定并保存。
培养基:MH琼脂(批号:HB6231),青岛高科园海博生物技术有限公司。
1.1.4 仪器、耗材与软件 1200高效液相色谱仪,透明短螺纹广口进样瓶(容量:2 mL),美国Agilent公司;KQ-300VDB型数控超声波清洗器,昆山市超声仪器有限公司;BS210型电子天平,深圳市深美仪器有限公司;CAMAG薄层成像系统,瑞士卡玛公司;硅胶G(100 mm×200 mm,批号:112926-00-8),青岛海洋化工特种硅胶有限公司;毛细管(4 μL),北京先驱威锋技术开发公司;Cat#65-1001涂布器,BIOLGIX Cell Spreader ;中药色谱指纹图谱相似度评价系统2008版,中国软件与技术服务股份有限公司研发。
1.2 方法
1.2.1 样品制备
1.2.1.1 水提法 取50 g黄连饮片,粉碎至40目,将粉碎后的黄连放入药材重量10倍量的水中煎煮1.5 h,然后将所有提取溶液混合之后4 000 r/min的条件下离心6 min,取上清液单层滤纸真空抽滤,抽滤后的液体留下备用,将离心后剩下的药渣再次煎煮,第2次、第3次时间缩短为1 h,过程与第1次相同,最后将3次滤过的药液合并,提取液进行旋转蒸发仪浓缩,最后制成1∶1的中药流浸膏[3],所得流浸膏每1 mL相当于1 g原药材,放入4℃冰箱保存。
1.2.1.2 颗粒剂的制备 取黄连颗粒剂1包(0.5 g包装),溶于3 mL超纯水中,即得相对于黄连饮片浓度1 g/mL的溶液。
1.2.2 TLC法
1.2.2.1 供试品溶液的制备 取黄连饮片水煎剂和黄连颗粒剂0.25 g,加甲醇25 mL,超声处理30 min,滤过,取续滤液作为供试品溶液。
1.2.2.2 对照品溶液的制备 取黄连对照药材0.25 g,同供试品溶液的制备方法制成对照药材溶液。取小檗碱对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。
1.2.2.3 TLC检查 吸取已制备的黄连颗粒剂供试品溶液、对照药材溶液和小檗碱对照品溶液各1 μL,分别点于同一高效硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3∶3.5∶1∶1.5∶0.5∶1)为展开剂,置用浓氨试液预饱和20 min的展开缸内,展开,取出,晾干,置365 nm紫外光灯下检视。
1.2.3 HPLC法
1.2.3.1 色谱条件 按高效液相色谱法[4],色谱柱:Agilent Extend-C18柱(4.6 mm×250 mm,5 μm),柱温:35℃,以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.05 mol/L磷酸二氢钾溶液(50∶50)(每100 mL中加十二烷基硫酸钠0.4 g,再以磷酸调节pH4.0)为流动相,流速:1.0 mL/min,检测波长:345 nm,进样量:10 μL。
1.2.3.2 供试品溶液的制备 取黄连饮片水煎剂和黄连颗粒剂粉末0.2 g,精密称定,置锥形瓶中,精密加入甲醇-盐酸(100∶1)的混合液50 mL,密塞后称定重量,超声(250 W,40 kHz)处理30 min,放冷,再称定重量,用甲醇补足减失的重量。摇匀,用0.22 μm微孔滤膜滤过,取续滤液2 mL,置10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得供试品溶液。
1.2.3.3 对照药材溶液的制备 取黄连对照药材1 g,同1.2.3.2中的方法制成对照药材溶液。
1.2.3.4 对照品溶液的制备 取盐酸小檗碱对照品,加甲醇制成每1 mL含90.5 μg的溶液,作为对照品溶液。
1.2.3.5 方法学考察 ①标准曲线的制备:精密量取适量的小檗碱标准品溶液置于容量瓶中,用甲醇配成系列标准溶液,使浓度分别为0.001、0.010、0.020、0.050、0.100、1.000 mg/mL,按1.2.3.1项色谱条件分别进样10 μL测定。②稳定性考察:在避光条件下,精密吸取黄连颗粒剂、煎剂供试品溶液各6份,进样量10 μL,分别于0 h、2 h、4 h、8 h、12 h、24 h进样。③精密度考察:精密吸取小檗碱对照品溶液10 μL,连续进样6次,测峰面积。④重复性考察:精密吸取黄连颗粒剂、水煎剂,同供试品溶液的制备方法平行制备6份供试品溶液,按1.2.3.1色谱条件分别进样检测分析。
1.2.3.6 HPLC特征图谱 同上法制备黄连颗粒剂、水煎剂和对照药材溶液,按1.2.3.1色谱条件测定特征图谱。
1.2.3.7 小檗碱含量测定 同上法制备黄连颗粒剂、水煎剂和对照药材各3份,按1.2.3.1色谱条件测定。
1.2.3.8 指纹图谱相似度匹配 采用《中药色谱指纹图谱相似度评价系统2008版》进行相似度检测。打开软件,将黄连颗粒剂、水煎剂和对照药材溶液HPLC特征图谱导入其中,把对照药材溶液HPLC特征图谱设定为参照图谱后,与黄连颗粒剂、水煎剂HPLC特征图谱进行自动匹配,利用相似度计算功能对颗粒剂和水煎剂进行相似度评价。
1.2.4 体外抑菌试验
1.2.4.1 菌液制备 将菌种接种于营养肉汤中,37℃培养24 h后,采用平板倾注法进行活菌计数并将菌液浓度稀释为105CFU/mL的含菌量。
1.2.4.2 MH琼脂培养基制备 将培养基装在三角瓶中,121℃高压灭菌15 min。无菌条件下,温度控制在45℃时倒入平皿中。链球菌使用加50 mL/L绵羊血的MH琼脂。
1.2.4.3 黄连颗粒剂及煎剂体外抑菌试验 取稀释好的菌液100 μL,用涂布器均匀涂在MH琼脂板上,在室温下干燥3 min~5 min。采用牛津杯法,进行抑菌试验[5]。将培养基平均分为5个区域,用无菌镊子将无菌牛津杯放在固定位置,并轻轻加压,使不锈钢小管和培养基表面接触时不产生空隙。最后在牛津杯中加入100 μL(1 g/mL)药液,将培养皿小心移入培养箱中,37℃培养24 h,测量抑菌环直径。设3个平行试验组,并设阳性、空白对照。
1.2.4.4 结果判定 抑菌效果判定标准:抑菌直径d≥20 mm为极敏,20 mm>d≥15 mm高敏;15 mm>d≥10 mm为中敏,10 mm>d>8 mm为低敏,d≤8 mm无抑菌效果。
2 结果
2.1 TLC法
黄连颗粒剂在与对照药材色谱相应的位置上,显4个以上相同颜色的荧光斑点,对照品色谱相应的位置上,显相同颜色的荧光斑点(图1)。
2.2 HPLC法
2.2.1 方法学考察
2.2.1.1 标准曲线 以标准品溶液的质量浓度(x)为横坐标,峰面积积分值(y)为纵坐标,制备小檗碱的标准曲线,回归方程为y=2.056×105x+16.63,r=0.999 8(n=6)。结果表明,小檗碱的质量浓度在0.001 mg/mL~1.000 mg/mL范围内与峰面积积分值呈良好的线性关系(保留时间)。
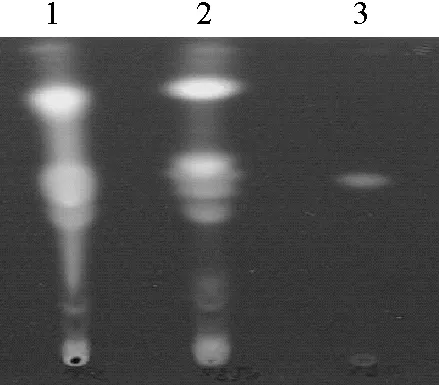
1.黄连颗粒剂; 2.黄连对照药材; 3.小檗碱
2.2.1.2 稳定性考察 取同一供试品溶液,分别于0、2、4、8、12、24 h时进样10 μL。小檗碱的峰面积RSD(n=6)均<0.15%,表明供试品溶液中小檗碱在24 h内稳定。
2.2.1.3 精密度考察 精度吸取对照品溶液10 μL,连续进样6次小檗碱的峰面积RSD(n=6)为0.95%,表明本方法精密度良好。
2.2.1.4 重复性考察 取同一批号样品,按供试品溶液制备方法制备6份,分别进样测定,小檗碱的峰面积RSD(n=6)均<0.18%,说明本方法重复性良好。
2.2.2 HPLC特征图谱

S1.黄连颗粒剂HPLC总离子流图; S2.黄连煎剂HPLC总离子流图; S3.黄连对照药材HPLC总离子流图
2.2.3 盐酸小檗碱含量 由表1可知:黄连颗粒剂和煎剂与盐酸小檗碱对照药材中盐酸小檗碱的平均值含量差距较大,其中颗粒剂的盐酸小檗碱含量与煎剂差不多。颗粒剂中的盐酸小檗碱标准差最小,说明颗粒剂这组数据的差异性不显著,其次是黄连水煎剂,数据差异性最显著的是对照药材。
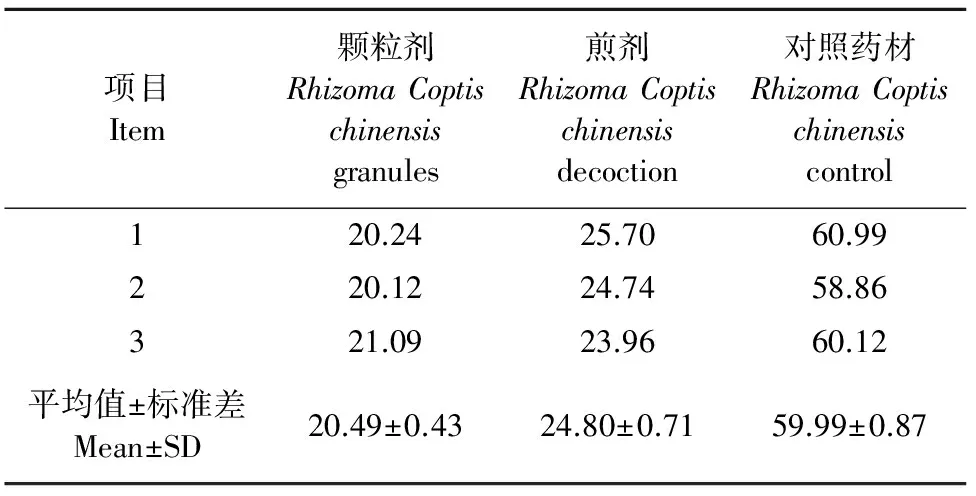
表1 盐酸小檗碱含量
2.2.4 相似度比较 黄连颗粒剂、黄连煎剂与对照药材的相似度分别为 99.4%和99.5%,相似性较好。
2.2.5 体外抑菌结果 观察抑菌圈大小并记录结果(表2)。由表2可知,黄连颗粒剂、黄连水煎剂和黄连对照药材对金黄色葡萄球菌和大肠埃希菌的抑菌效果是极敏,黄连颗粒剂和黄连水煎剂对沙门菌、链球菌的抑菌效果是中敏,黄连对照药材对沙门菌的抑菌效果是高敏,对链球菌的抑菌效果是中敏。
3 讨论
从TLC的结果中可以看出黄连颗粒剂和黄连饮片拥有几个相同的斑点,而且与盐酸小檗碱对照品有相同的光斑,说明黄连颗粒剂和黄连饮片中所含物质大部分相同,且均含有盐酸小檗碱。对主要有效物质盐酸小檗碱进行了比较,3种黄连待测品和盐酸小檗碱对照品的特征图谱都在15 min~16 min之间出现了明显的峰,对盐酸小檗碱的含量进行计算,说明黄连颗粒剂和黄连饮片中盐酸小檗碱所占比例也相差不大,虽然与黄连标准品有一些差距,可能是由于黄连标志品纯度比较高。通过相似度软件的比较,可以看出颗粒剂与黄连饮片煎剂的相似度也很高。

图3 小檗碱对照品HPLC总离子流图

表2 黄连颗粒剂和煎剂体外抑菌结果
常见细菌对黄连颗粒剂、黄连饮片和黄连对照药材体外抑菌试验结果表明,黄连颗粒剂和黄连饮片的抑菌圈大小一致,略差于黄连对照品。本试验中黄连饮片采用了简单的水煎法提取,可能对有效成分造成一些损失,煎剂提取时过滤次数相对较少,“杂质”相对较多,而中药的抗菌作用除与所含特异性成分有关外,“杂质”等非特异性成分还往往影响病原微生物的生长[6]。
总之,黄连颗粒剂和黄连饮片煎剂化学组成接近,主要成分盐酸小檗碱的含量也相似,均可用于临床,而且中药颗粒剂有方便携带,便于储存和服用,中药颗粒剂的质量也较稳定[7],可应用于动物临床疾病的治疗。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2005:213.
[2] 高晓山.中药药性论[M].北京:人民卫生出版社,1992:179.
[3] 王志华,陈 碧,陈新玉.黄连提取方法的试验研究[J].使用药物与临床,2008,11(3):191-192.
[4] 周国莉,林晓莲,程 聪.HPLC法测定复方黄连液中盐酸小檗碱的含量[J].中医药导报,2010,16(8):80-81.
[5] 张学沛,朱盛山,刘 静,等.评价中药体外抑菌法的研究进展[J].药物评价研究,2014,37(2):189.
[6] 任 非,王育红,丁 力,等.中药免煎颗粒剂与煎剂体外抗菌活性的对比研究[J].河北中医,2010,32(12):1869-1871.
[7] 张 惠,胡 敏.中药配方颗粒剂的临床应用评价[J].西部医学,2011,23(7):129-131.
Comparison of Main Components and Antibacterial Effects ofRhizomaCoptischinensisand Decoction
WANG Shuang,HE Sheng-hu,SUN Peng,GUO Ya-nan,CAO Si-ting,ZHANG Xin
(CollegeofAgriculture,NingxiaUniversity,Yinchuan,Ningxia,750021,China)
In order to compare the main components and bacteriostatic effects of Rhizoma Coptidis granules and decoction, the HPLC and TLC method were used to measure and compare theCoptischinensisgranules and elixation, the main components of berberine hydrochloridemCoptis, decoction ofCoptisand other granules were determined and compared, antibacterial effectsinvitrowere also compared. The results showed thatRhizomaCoptidisgranules and decoction of effective ingredients contained in the basic agreement, the characteristic spectrum of similar peak at the same time, berberine hydrochloride belongs to the characteristic peak; similar inhibitory circle ofCoptisdecoction andRhizomaCoptidisgranules. The results showed thatCoptischinensisgranules could be used instead of coptis chinensis elixation in clinical treatment.
RhizomaCoptidisgranule;berberine hydrochloride;RhizomaCoptidisdecoction;HPLC;TLC
2016-09-29
王 爽(1993- ),女,宁夏银川人,硕士研究生,主要从事兽药临床诊断和中兽药医药研究。*通讯作者
S853.7
A
1007-5038(2017)05-0069-05

