XELOX方案与FOLFOX4方案在原发性肝癌化疗中的比较观察
柳家荣
(平煤神马医疗集团总医院肿瘤科,河南 平顶山 467000)
XELOX方案与FOLFOX4方案在原发性肝癌化疗中的比较观察
柳家荣
(平煤神马医疗集团总医院肿瘤科,河南 平顶山 467000)
目的 比较分析XELOX方案与FOLFOX4方案在原发性肝癌化疗中的应用价值。方法 52例原发性肝癌患者按照随机数表法分为2组,每组26例。研究组采用XELOX化疗方案,对照组采用FOLFOX4化疗方案。比较观察2组的临床疗效、治疗前后甲胎蛋白(AFP)及癌胚抗原(CEA)水平变化情况、不良反应发生情况及1 a生存率。结果 2组治疗有效率、疾病控制率比较差异均无统计学意义(P均>0.05);治疗后研究组AFP及CEA水平低于对照组,差异有统计学意义(P<0.05);研究组不良反应情况优于对照组,差异有统计学意义(P<0.05)。结论 采用XELOX方案与FOLFOX4方案治疗原发性肝癌均可取得显著疗效,提高生存率,但XELOX方案可有效降低AFP及CEA水平,且不良反应更轻。
奥沙利铂;卡培他滨;亚叶酸钙;氟尿嘧啶;原发性肝癌
原发性肝癌为临床高发的恶性肿瘤,在我国东南沿海地区具有较高发病率,好发于40~50岁群体。临床多认为与病毒性肝炎、肝硬化、环境及黄曲霉素等多种化学致癌物质具有密切相关性[1]。原发性肝癌患者首发症状主要为肝区疼痛,表现为持续性胀痛、刺痛等,其主要原因可能是肿瘤快速增长,导致肝包膜张力增大所致。外科手术为原发性肝癌首选治疗措施,但针对无法切除的肝癌患者,则需通过化疗对其实施救治。近年来,随着卡培他滨、奥沙利铂等多种新型化疗药物的研发应用,系统性化疗方案逐渐成为原发性肝癌常用姑息性治疗措施,可有效杀伤肿瘤细胞,缩小肿瘤体积,改善患者临床症状。本研究选取我院52例原发性肝癌患者,通过分组分析,探究XELOX方案与FOLFOX4方案在原发性肝癌化疗中的应用效果。
1 资料与方法
1.1 一般资料 选取2012年1月至2015年4月我院收治的52例原发性肝癌患者,按照随机数表法分为研究组和对照组,每组26例。2组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
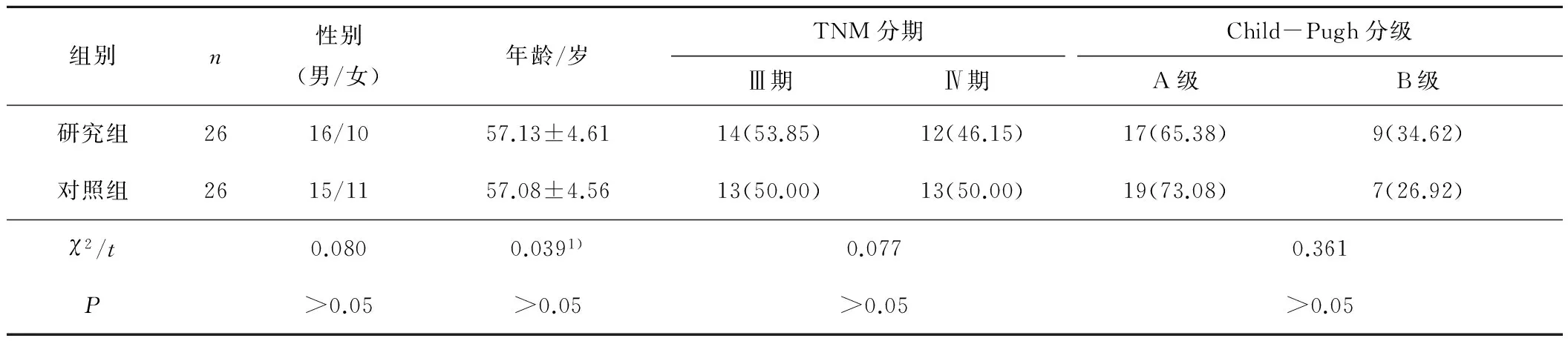
表1 2组患者一般资料对比 n(%)
注:1)为t值
1.2 纳入及排除标准 纳入标准:符合中华医学会制定的原发性肝癌相关临床诊断标准[2];预计生存期≥3个月;血红蛋白>100 g·L-1,血清肌酐≤110 μmol·L-1。排除标准:合并充血性心力衰竭、不稳定心绞痛、心肌梗死者;伴有凝血功能障碍及活动性胃肠出血者;并发其他恶性肿瘤者;既往行肝移植手术者。
1.3 治疗方法 研究组:采用XELOX化疗方案,第1~14天早晚餐后分2次服用卡培他滨1 000 mg·m-2;第1天静脉滴注奥沙利铂130 mg·m-2,间隔3周重复1次,3周为1周期。对照组:采用FOLFOX4 化疗方案,第1天静脉滴注奥沙利铂85 mg·m-2,滴注2 h;第1~2天静脉滴注亚叶酸钙200 mg·m-2;第1~2天静脉滴注氟尿嘧啶400 mg·m-2,随后持续静脉滴注600 mg·m-2氟尿嘧啶22 h,2周为1周期。2组均持续治疗4周期。1 a后随访。
1.4 观察指标 1)依照RECIST实体瘤疗效评定标准评估2组近期疗效,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),以CR+PR计算有效率,以CR+PR+SD计算疾病控制率[3];2)以酶联免疫吸附法(ELISA)测定治疗前后2组甲胎蛋白(AFP)、癌胚抗原(CEA)水平变化情况;3)比较观察2组不良反应发生情况,根据NCI毒性分度标准分为0~Ⅳ度[4];4)比较观察2组1 a生存率。

2 结果
2.1 临床疗效 2组治疗有效率、疾病控制率比较差异均无统计学意义(P均>0.05)。见表2。
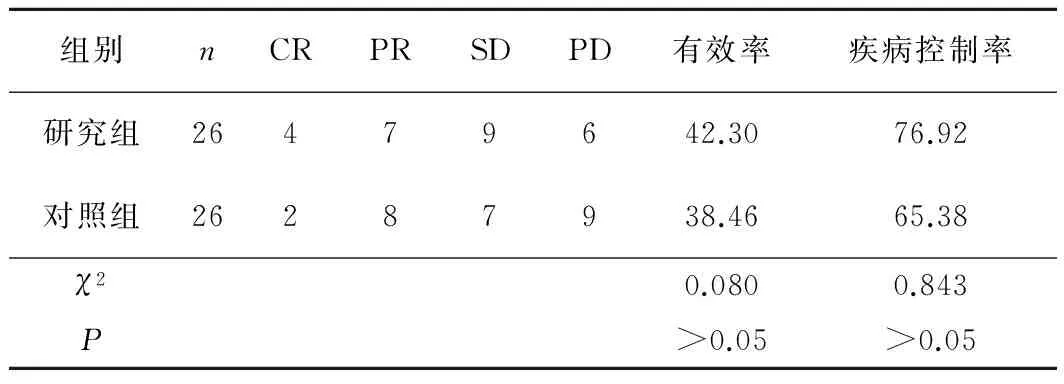
表2 2组临床疗效比较
2.2 AFP及CEA水平变化情况 治疗前2组AFP及CEA水平比较差异均无统计学意义(P均>0.05)。经治疗,2组各指标均较治疗前降低,且研究组AFP及CEA水平低于对照组,差异均有统计学意义(P均<0.05)。见表3。
2.3 2组不良反应发生情况比较 研究组不良反应情况优于对照组,差异有统计学意义(P<0.05)。见表4。
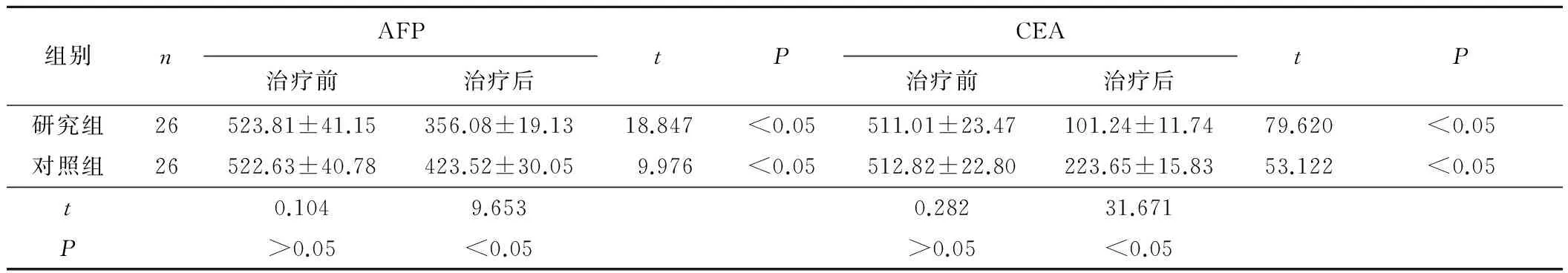
表3 2组AFP及CEA水平变化情况比较 μg·L-1
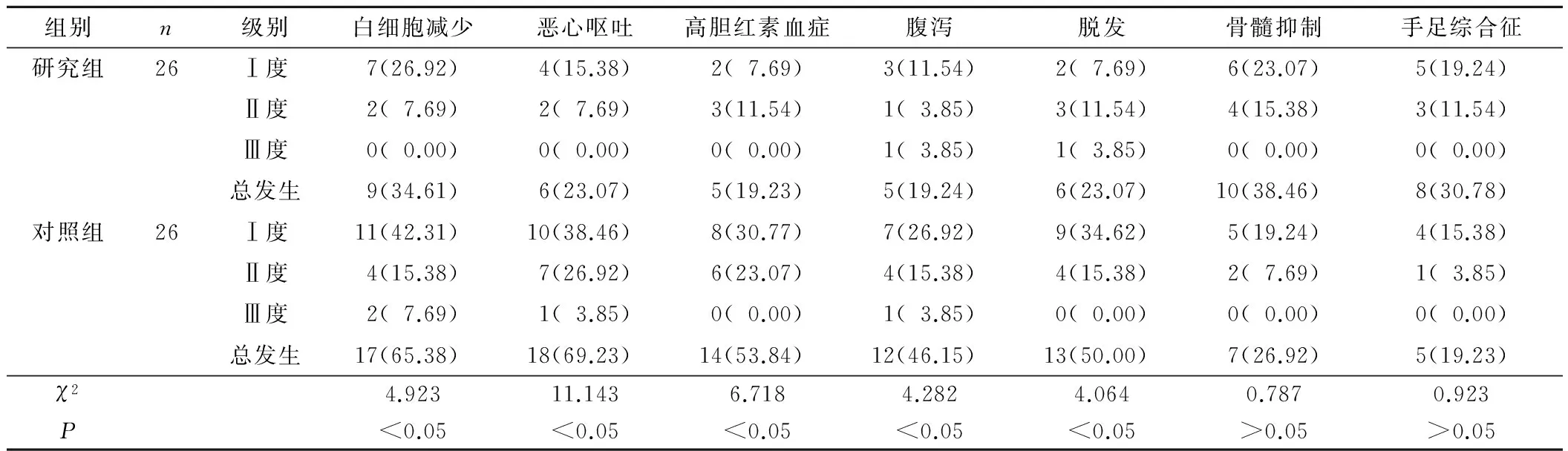
表4 2组不良反应发生情况比较 n(%)
2.4 1 a生存率 研究组1a存活20例,1 a生存率为76.92%(20/26),对照组存活18例,存活率为69.23%(18/26),比较差异无统计学意义(χ2=0.391,P>0.05)。
3 讨论
原发性肝癌对传统化疗药物敏感性较低,其主要原因是肝癌细胞自身存在天然多药耐药性,并且原发性肝癌多与肝硬化、乙肝、丙肝等多种基础肝病并存,致使肝功能受损,且肝细胞对药物代谢解毒作用较弱,明显降低了化疗给药的剂量密度及强度,导致临床疗效难以满足临床预期[5]。随着替吉奥、吉西他滨、卡培他滨及奥沙利铂等新一代细胞毒性药物的应用,明显提高了肠、胃、胰腺癌等疾病的临床治疗效果,且推动了原发性肝癌系统性化疗研究进展。国外有研究[6]分别采用单药阿霉素与FOLFOX4方案对无法手术的原发性肝癌患者进行治疗,结果发现FOLFOX4方案组中位总生存期可达6.47个月,中位无进展生存期为2.97个月,有效率为8.7%,疾病控制率为54.26%。有力佐证系统性化疗,尤其是含奥沙利铂方案可使晚期原发性肝癌患者生存及病情局部控制获益。同时,2013年3月12日国家食品药品监督管理总局已批准奥沙利铂可用于“不适合手术切除或局部治疗的局部晚期或转移的原发性肝癌的治疗”,也是全球第1个获批的用于原发性肝癌系统化疗的药物。
奥沙利铂为第3代铂类化合物,与其他铂类药物相同,其药理作用也是以DNA作靶点,使DNA链间与链内构成交联,对其复制、转录予以抑制,以此发挥抗肿瘤功效。相较于卡铂、顺铂,该药物抗肿瘤功效更强,且肝、肾毒性较小,同时无交叉耐药性。此外,奥沙利铂可迅速与DNA结合,最长仅需15 min便可完成所有DNA的结合。陈海石等[7]的研究表明,XELOX方案治疗有效率及血清肿瘤标志物水平优于FOLFOX4,提示XELOX方案在原发性肝癌化疗治疗中效果更佳。而本研究中,虽2组治疗有效率及疾病控制率、1 a生存率较接近(P>0.05),但研究组AFP及CEA水平低于对照组(P<0.05),与上述结果一致。卡培他滨药物对肿瘤组织选择性较高,可有效减少氟尿嘧啶对机体正常组织造成的损伤。王荦楠等[8]研究发现,晚期肝癌患者经XELOX联合化疗方案治疗后,不良反应主要为Ⅰ度,患者均可耐受。而本研究结果显示,研究组整体不良反应发生情况低于对照组,且多为Ⅰ、Ⅱ度,与前述研究结果基本一致,提示XELOX方案不仅疗效确切,且不良反应较轻。
综上所述,采用XELOX方案与FOLFOX4方案治疗原发性肝癌均可取得显著疗效,提高生存率,但XELOX方案可有效降低AFP及CEA水平,且不良反应发生率较低。
[1] 杨柳青,秦叔逵,华海清,等.XELOX方案治疗中晚期原发性肝癌的临床观察[J].临床肿瘤学杂志,2013,18(8):704-708.
[2] ZHANG M,ZHANG H,SUN C,et al.Targeted constitutive activation of signal transducer and activator of transcription 3 in human hepatocellular carcinoma cells by cucurbitacin B[J].Cancer Chemother Pharmacol,2009,63(4):635-642.
[3] 丁德权,曹齐生,何昌霞,等.中晚期原发性肝癌的TACE治疗和FOLFOX4方案化疗疗效分析[J].安徽医药,2013,17(8):1388-1391.
[4] 钟俊勇,郭予武,刘锦新,等.含奥沙利铂的化疗及介入化疗方案治疗晚期原发性肝癌的临床研究[J].海南医学,2013,24(13):1887-1889.
[5] 郑婷,寇晓霞,吴孟超,等.含奥沙利铂化疗方案联合DC-CIK细胞治疗中晚期原发性肝癌的临床疗效[J].中国肿瘤生物治疗杂志,2015,22(6):760-764.
[6] TAWADA K,ISHIHARA T,KOBAYASHI A,et al.Quantitative analysis of vascular endothelial growth factor in liver metastases from pancreatic carcinoma as a predictor of chemotherapeutic effect and prognosis[J].Clin Cancer Res,2008,14(22):7438-7443.
[7] 陈海石,陈勇.奥沙利铂联合卡培他滨治疗晚期原发性肝癌临床疗效分析[J].现代诊断与治疗,2014,25(5):1024-1025.
[8] 王荦楠,杨萌,崔艳慧,等.奥沙利铂联合卡培他滨治疗晚期肝细胞癌的疗效及安全性[J].新乡医学院学报,2012,29(10):787-789.
柳家荣(1975-),女,硕士,主治医师,主要从事肿瘤相关临床研究。E-mail:liujiarong006@163.com
10.3969/j.issn.1673-5412.2017.02.013
R735.7;R730.53
B
1673-5412(2017)02-0132-03
2016-07-13)

