北京地区种植不同种源的柴胡药材质量分析
薛文峰 刘长利,2 陈 炎
(1 首都医科大学中医药学院,北京,100069; 2 首都医科大学中医络病研究北京市重点实验室,北京,100069)
北京地区种植不同种源的柴胡药材质量分析
薛文峰1刘长利1,2陈 炎1
(1 首都医科大学中医药学院,北京,100069; 2 首都医科大学中医络病研究北京市重点实验室,北京,100069)
目的:通过田间种植试验,分析不同种源的柴胡药材质量,为确定适宜北京地区种植柴胡的种源提供技术依据。方法:在北京市顺义区设置田间试验,种植从河北安国药材市场、安徽亳州药材市场、中国医学科学院药用植物研究所购买的3个种源的柴胡,采用紫外-可见分光光度法及高效液相色谱(HPLC)法,测定药材样品中的柴胡总皂苷、柴胡皂苷a、柴胡皂苷c和柴胡皂苷d的含量,以甘肃、山西种植柴胡药材为对照,评价北京地区3个不同种源的柴胡药材质量。结果:3种不同种源的柴胡药材,在柴胡总皂苷、柴胡皂苷a、柴胡皂苷c、柴胡皂苷d含量等化学成分指标与甘肃、山西种植柴胡药材的差异无统计学意义,且符合中华人民共和国药典的标准,其中河北安国药材市场、中国医学科学院药用植物研究所种源的药材质量更优。结论:北京地区是种植柴胡的适宜产区,种源可从河北安国药材市场或中国医学科学院药用植物研究所购买。
柴胡;种植;药材质量;北京地区
柴胡性辛、苦、微寒,入肝、胆、肺经,具有疏散退热,疏肝解郁,举阳气的功效,用于感冒发寒热往来、胸胁胀痛、月经不调、子宫脱垂脱等证[1]。始载于《神农本草经》,在我国已有两千多年的使用历史。2015版《中华人民共和国药典》收录其来源为伞形科植物柴胡BupleurumchineseDC.或狭叶柴胡Bupleurumscorzonerifoliumwilld.的干燥根。
柴胡药材以野生品种应用为主,随着对柴胡药材的使用量的增加,野生柴胡不足以提供市场的需求。我国北方一些省区已开始进行柴胡的人工种植,而且柴胡的栽培技术发展迅速。但是由于柴胡的种植品种混乱[2],以及不同的种植品种、环境、地域、年限以及种植方法使得不同地区的柴胡质量参差不齐[3]。历史上北京沿燕山山脉一带山区是北柴胡的主要产区之一。早在1992年在北京密云怀柔就有种植三岛柴胡的文献[4],后来李勇等[5]在延庆种植北柴胡,并且对种植北柴胡根腐病的病原菌鉴定,杨成民等[6]研究了平谷区种植北柴胡皂苷含量动态变化,建议柴胡在10月底果实成熟期适于采收。顺义区位于北京市东北部,地处燕山南麓,年平均气温为11.5 ℃,年均相对湿度50%,年均降雨量约625 mm。安徽亳州药材市场、河北安国药材市场等主要中药药材市场,市场主流商品种植北柴胡产地以甘肃和山西产地为主。
在北京市顺义区设置田间试验,种植从河北安国药材市场、安徽亳州药材市场、中国医学科学院药用植物研究所购买的3个种源的柴胡,采用紫外-可见分光光度法及高效液相色谱(HPLC)法,测定药材样品中的柴胡总皂苷、柴胡皂苷a、柴胡皂苷c和柴胡皂苷d的含量,以甘肃、山西种植柴胡药材为对照,评价北京地区3个不同种源的柴胡药材质量,为确定京郊山区人工种植北柴胡的种源类型提供技术依据。
1 仪器与试药
1.1 仪器 高效液相色谱仪(Agilent Technologies 1260 Infinity);紫外分光光度计(UV-6100S);电子天平(SOP);超声清洗仪(KQ5200DV)。
1.2 试药 柴胡皂苷d对照品购自中国食品药品检定研究院(批号110778-201409);柴胡皂苷a对照品购自中国食品药品检定研究院(批号110777-201409);柴胡皂苷c对照品购自中国科学院成都生物研究所(批号20736-08-7);乙腈(AS1122-001)TEDIA,对二甲氨基苯甲醛(L1410064)购自阿拉丁公司,甲醇、磷酸购自北京化工厂,娃哈哈纯净水。
1.3 分析样品 试验田位于北京顺义区河南村,2015年4月播种,人工撒播,播深1 cm,行距25 cm,亩播量1.5 kg[7],出苗后不间苗。生长期间干旱时喷灌浇水,人工除草,不施肥,种子来源为3种,分别来源于河北安国药材市场、安徽亳州药材市场、中国医学科学院药用植物研究所。于2016年5月,选择出苗均匀,生长正常地块,按S行取样,取同一种源柴胡为3份,试验田柴胡共为9份。收集甘肃4个地区、山西3个地区种植2年生北柴胡,每个地区柴胡平行3份,共21份。所有柴胡药材及种子,经首都医科大学刘长利副教授鉴定为北柴胡BupleurumchineseDC.。见表1。
2 方法与结果
2.1 色谱条件 以甲醇配制一定浓度的柴胡皂苷a溶液,精密吸取0.80 mL,100 ℃水浴挥干,加入0.1%对二甲氨基苯甲醛乙醇溶液0.1 mL,继续100 ℃水浴挥干,加入磷酸4.0 mL,70 ℃反应30 min,按照紫外-可见分光光度法(参照《中华人民共和国药典》)于200~800 nm范围内进行波长扫描,发现全波长扫描结果在528 nm处,有最大吸收峰,故确定检测波长为528 nm。分析柱为Eclipse Plus C18柱(4.6 mm×250 mm,5 μm);流动相为乙腈(B)-水(A);流速为1.0 mL/min,进样量为20 μL,柱温25 ℃,紫外检测波长为210 nm,采用梯度洗脱方式测定,(0~5 min,35%B→40%B;5~15 min,40%B→45%B;15~25 min,45%B→55%B;25~30 min,55%B→90%B;30~45 min,90%B→35%B)。

表1 柴胡样本收集表
注:1号样本种源来自河北安国药材市场;2号样本种源来自安徽亳州药材市场;3号样本种源来自中国医学科学院药用植物研究所。
2.2 对照品溶液的制备 将精密称取柴胡皂苷a标准品适量,加甲醇制成每1 mL含1 mg的溶液(精称量1.74 mg标准品,溶于2 mL甲醇中,超声溶解),摇匀,即得浓度为0.868 8 mg/mL的标准品液。称取柴胡皂苷a、c、d标准品4.37 mg、3.35 mg、4.55 mg,溶于2 mL甲醇中逐级稀释,用作柴胡皂苷a、c、d的测定。
2.3 供试品溶液的制备 精密称定柴胡样品粉末(过四号筛)0.20 g,加入5%浓氨水试液的甲醇溶液25 mL,30 ℃水温超声处理30 min,过滤,洗液与滤液合并,回收溶剂至干。残渣加少量水溶解,再用水饱和正丁醇萃取,回收正丁醇至干,甲醇溶解,并定容至5 mL,摇匀,0.45 μm微孔滤膜滤过,作为测定总皂苷的供试品溶液。
取柴胡粉末(过四号筛)精密称定0.50 g,加入含5%浓氨试液的甲醇溶液25 mL,密闭,30 ℃水温超声处理(功率200 W,频率40 kHz)30 min,过滤,洗液与滤液合并,回收溶剂至干。残渣加甲醇溶解,转移至5 mL容量瓶中,加甲醇至刻度,摇匀,0.45 μm微孔滤膜滤过,即得作为测定柴胡皂苷a、c、d的供试品溶液。
2.4 线性关系考察 将柴胡皂苷a标准品液逐级稀释,即得不同浓度(0.00543、0.01086、0.02172、0.04344、0.08688、0.15204 mg/mL)的对照品稀释液,以空白溶媒作为空白校正,在528 nm处测定各稀释液吸光度,用于柴胡总皂苷的测定。回归曲线方程Y=6.786X+0.017,r=0.9997,线性范围0.00543~0.15204。
称取柴胡皂苷a、c、d标准品4.37 mg、3.35 mg、4.55 mg,溶于2 mL甲醇中逐级稀释,按方法进样20 μL测定,以峰面积为纵坐标(Y),浓度(mg/mL)为横坐标(X),对各对照品进行回归分析,用于SSa、SSc、SSd的测定。见表2。

表2 柴胡中有效成分线性回归方程
2.5 精密度试验 吸取柴胡皂苷a稀释液0.80 mL,按“2.1”方法测定吸光度,重复上述步骤测定6次,柴胡皂苷a标准品的RSD值为1.881%,证明此仪器精密度良好。柴胡SSa、SSc、SSd标准品为供试液,连续进样6次,柴胡皂苷a、柴胡皂苷c、柴胡皂苷d的RSD分别为0.2864%、0.9026%、0.1337%,证明该仪器的精密度良好。
2.6 供试品溶液稳定性试验 取柴胡粉末0.20 g,精密称定。按“2.3”中供试液的制备方法操作,吸取供试液0.80 mL,按“2.4”方法分别于0、5、10、15、20、25、30、45、60 min测定吸光度,样品总皂苷吸光度值的SRD为0.492%,证明总皂苷含量在0~60 min内稳定性良好。取1号柴胡,按照提取方法平行制备6份供试品溶液,照色谱条件,分别在0,2,4,6,8,24 h进样分析,记录峰面积,计算其相对标准偏差,SSa、SSc、SSd的RSD分别为4.219%、1.319%、3.509%,证明SSa、SSc、SSd的稳定性良好。
2.7 重复性试验 取柴胡粉末0.20 g,精密称定,共6份。按“2.3”供试液的制备方法操作,吸取供试液0.80 mL,按“2.4”方法测定总皂苷吸光度,样品总皂苷含量的RSD值为2.822%,证明此方法重现性良好。同1号柴胡6份,测定SSa、SSc、SSd含量,SSa、SSc、SSd的RSD分别为3.576%、2.503%、2.982%,证明该方法的重现性良好。
2.8 回收率试验 取柴胡粉末0.20 g,精密称定6份。加入柴胡皂苷a标准品适量。按“2.3”供试液的制备方法操作,吸取供试液0.80 mL,按“2.4”方法测定,结果表明:总皂苷的平均加样回收率为98.870%,RSD值为1.699%,符合实验要求。取1号柴胡6份,分别加入一定含量的对照品,按照“2.3”方法制备供试液,进样20 μL,记录目标峰峰面积,计算回收率,SSa、SSc、SSd的平均加样回收率分别为100.26%、101.64%、100.62%,RSD值分别为4.5884%、2.1983%、3.4808%,符合实验要求。
2.9 样品测定结果
2.9.1 各成分的测定结果 按供试品溶液制备方法制备,测定各成分含量。根据回归曲线方程计算柴胡总皂苷及SSa、SSc、SSd的含量见表3。
2.9.2 各成分比较分析 北京种植3种源北柴胡与甘肃、山西总皂苷含量各不相同。见图1,其中以甘肃武山县北柴胡总皂苷的含量为最高,山西运城县种植北柴胡总皂苷含量则最低,北京种植3种源种植柴胡皂苷含量差异较小;在SSa+SSd含量方面,除山西运城县种植柴胡未达到药典标准,其他所测北柴胡SSa+SSd含量均能达到2015版《中华人民共和国药典》规定的不小于0.30%的要求,其中以甘肃武山县种植柴胡SSa+SSd含量最高,山西运城县最低。见表3;所测柴胡中SSa、SSc、SSd含量各不相同,以甘肃武山县种植北柴胡SSa、SSd含量最高,山西运城县最低;甘肃漳县三岔镇SSc含量最高,北京种植安徽亳州药材市场种源最低。见图2。

表3 不同产地柴胡总皂苷含量结果±s)
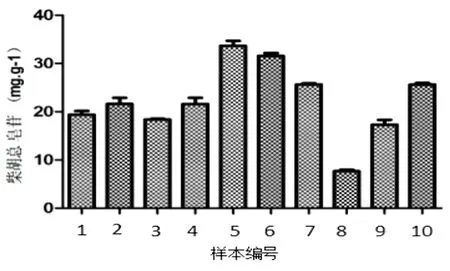
图1 不同柴胡样本总皂苷含量差异

图2 不同柴胡样本SSa、SSc、SSd含量差异
为了进一步比较北京种植北柴胡与主流商品产地甘肃、山西种植柴胡的质量,以甘肃、山西种植为一个样本,分别与北京种植不同种源柴胡实验数据进行分析,差异无统计学意义(P>0.05)。可以看出北京种植不同种源柴胡与山西、甘肃种植北柴胡差异无统计学意义,在化学成分上来说,北京种植柴胡与主流产地商品差异无统计学意义,北京种植3个种源的北柴胡可以作为药材使用。
2.9.3 聚类结果分析 将10份样本进行系统聚类,结果见图3,结果表明10份样本分为2类:第Ⅰ类为样本1,9,2,4,7,3,10,8;第Ⅱ类为样本5,6。表明北京种植北柴胡能够与全部山西种植北柴胡、大部分甘肃种植北柴胡完全聚为一支,说明北京种植3种源北柴胡与甘肃、山西差异不大。
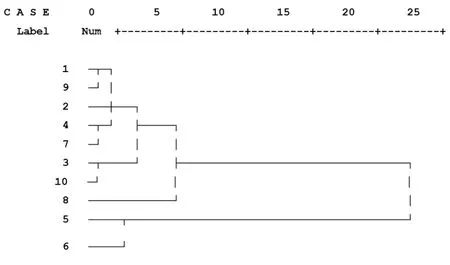
图3 10份样本聚类分析树状图
3 讨论
现在我国野生中药资源日趋减少,全国各地正大力发展中药栽培产业[8],中药柴胡现已在甘肃、山西、四川、河北等[9]地形成了规模化种植。但是由于野生柴胡来源混杂,存在引种非国家药典种柴胡的现象,导致栽培柴胡的种质也出现了混乱问题,栽培柴胡还存在品质、产量待提高等问题[10]所以提高柴胡种植技术非常重要,而其中种质筛选又是非常重要的一个环节,本实验就为确定适宜京郊山区人工种植柴胡的种质类型提供技术依据。
本实验结果初步说明北京地区栽培柴胡可达到现今市场主流商品柴胡(山西、甘肃)的质量标准,且SSa+SSd含量符合《中华人民共和国药典》要求,初步认为北京种植柴胡可作为商品流通。而在种质筛选方面,发现安国、药植所种源所含柴胡皂苷a、c、d含量相对于亳州种源含量更高,更值得进一步研究。聚类结果表明北京种植北柴胡能够与全部山西种植北柴胡、大部分甘肃种植北柴胡完全聚为一支,说明北京各种植种源与主流商品柴胡具有较近的关系,在实验所测的各指标上差异不大,推测是由于同为北柴胡所致。
对于发展北京地区种植柴胡,应当进一步扩大试验田种植面积以及种植区域,还需要对北京地区种植柴胡的病虫害及产量等问题进一步研究。同时为了中药柴胡资源的可持续发展,应当加强野生中药柴胡资源保护。
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:105,158-159.
[2]潘胜利.中药柴胡的药源调查及商品鉴定[J].中药材,1996,19(5):231-234.
[3]袁伯川,李文东,马永生,等.柴胡属药用植物的分子鉴定及市售柴胡药材的质量调查[J].药学学报,2017,52(1):162-171.
[4]索建政,宋清华.三岛柴胡在北京地区的生长动态观察[J].中药材,1992,15(7):10-13.
[5]李勇,刘时轮,杨成民,等.北京地区柴胡根腐病的病原菌鉴定[J].植物病理学报,2009,39(3):314-317.
[6]杨成民,魏建和,程惠珍,等.北柴胡皂苷含量动态变化[J].中药材,2006,29(4):316-318.
[7]李竞,高英,李海龙,等.太行山区柴胡中总皂苷及柴胡皂苷a、d的含量测定[J].中国医药导报,2013,10(8):124-126,129.
[8]段琼辉,李永.中药资源现状与可持续发展[J].西部中医药,2013,26(10):142-144.
[9]秦雪梅,王玉庆,岳建英.栽培柴胡资源状况分析[J].中药研究与信息,2005,7(8):30-32.
[10]孟祥才,马礴,杨兴旺,等.柴胡基源及栽培柴胡种质问题的探讨[J].现代中药研究与实践,2011,25(2):29-31.
(2016-08-26收稿 责任编辑:王明)
Medicinal Materials Quality Analysis of Different Provenances of Radix Bupleuri Planted in Beijing
Xue Wenfeng1,Liu Changli1,2,Chen Yan1
(1SchoolofTraditionalChineseMedicine,CapitalMedicineUniversity,Beijing100069,China;2BeijingKeyLabofTCMCollateralDiseaseTeoryReaserch,Beijing100069,China)
Objective:To analysis of different provenances of radix bupleuri medicinal materials quality using field planting test, and to determine the provenance of suitable cultivation of radix bupleuri in Beijing. Methods:Field experiment was set in Shunyi district of Beijing, growing 3 provenances of radix bupleuri bought from Hebei Anguo medicine market, Anhui Bozhou medicine market and Chinese academy of medical sciences institute of medicinal plant. By ultraviolet-visible spectrophotometry and high performance liquid chromatography (HPLC) method, total saponins in radix bupleuri, radix bupleuri saponins (a,b and c) were measured. Compared with those cultivated in Gansu and Shanxi, those three different provenance of radix bupleuri medicinal materials′ quality were evaluated. Results:Three different provenance of radix bupleuri had few difference comparing with those cultivated in Gansu and Shanxi in total saponins in radix bupleuri,and radix bupleuri saponins (a,b and c), besides, it met with Chinese pharmacopoeia standards, in which product of Hebei Anguo medicine market and Chinese academy of medical sciences institute of medicinal plant shared better quality.Conclusion:Beijing is suitable for planting of radix bupleuri, and provenance from hebei anguo medicine market or the Chinese academy of medical sciences institute of medicinal plant can be purchased.
Radix bupleuri; Planting; Medicinal materials′ quality; Beijing
北京市自然科学基金面上项目(编号:6142002)
薛文峰(1988.12—),男,首都医科大学中医药学院在读硕士研究生,研究方向:中药资源,E-mail:xuewenfeng.boy@163.com
刘长利(1974.11—),男,博士,副教授,研究方向:中药材规范化生产及其药材质量调控研究,E-mail:lcl74@126.com
R282.2
A
10.3969/j.issn.1673-7202.2017.03.043

