逍遥散调节慢性应激肝郁脾虚模型大鼠下丘脑弓状核ob-R、α-MSH变化机制
旷湘楠 王少贤 方朝义 王杰鹏 陈家旭 刘玥芸
(1 河北中医学院,石家庄,050200; 2 北京中医药大学基础医学院,北京,100029)
逍遥散调节慢性应激肝郁脾虚模型大鼠下丘脑弓状核ob-R、α-MSH变化机制
旷湘楠1王少贤1方朝义1王杰鹏1陈家旭2刘玥芸2
(1 河北中医学院,石家庄,050200; 2 北京中医药大学基础医学院,北京,100029)
目的:研究中药复方逍遥散(《太平惠民和剂局方》)疏肝解郁、健脾以调节食欲的作用机制。方法:以每天持续3 h慢性束缚应激方法制备动物模型。SD健康雄性大鼠随机分为正常组、7 d模型组、21 d模型组和逍遥散组4组,正常组予常规饲养,模型组和逍遥散组每天选择随机时间点进行束缚应激,7 d模型组束缚应激7 d,21 d模型组束缚应激21 d,逍遥散组在连续束缚应激21 d同时予逍遥散灌胃。观测各组大鼠体重、摄食量、行为学、血清D-木糖含量变化;免疫荧光双染、RT-qPCR方法观测下丘脑ARC中瘦素受体(Leptin Receptor,ob-R)、α-促黑素细胞激素(α-melanocyte Stimulating Hormone,α-MSH)基因与蛋白表达水平。结果:与正常组比较,束缚应激21 d模型大鼠体重、摄食量和血清D-木糖含量明显降低,行为学实验表明模型大鼠自主活动能力下降、对新异环境探究行为明显减少,而逍遥散则具有相应的调节作用。综合表明,每天3 h连续21 d捆绑束缚可制备慢性应激肝郁脾虚样动物模型,慢性束缚应激大鼠下丘脑弓状核(Arcuate Nucleus,ARC)中ob-R、α-MSH表达水平增加,逍遥散可下调其表达。结论:逍遥散调节下丘脑ARC中ob-R和α-MSH表达变化,可作为其疏肝健脾,调节机体食欲和能量代谢影响脾胃功能的作用靶点之一。
慢性应激;逍遥散;肝郁脾虚;瘦素受体;α-促黑素细胞激素
慢性、持久的应激可诱发躯体或心理疾病。由工作问题、家庭问题、经济问题、人际关系问题等各种生活事件引发的心理应激(心理压力),常常引发情绪障碍和以腹胀、食欲减退、大便失调为主要表现的脾胃功能失调,严重影响着我们的生活质量。中医中药在调治慢性应激方面疗效显著,逍遥散是中医经典心身同治复方,为国内学者抗应激的首选方剂。
本课题组一直从事中药复方逍遥散(《太平惠民和剂局方》)防治慢性心理应激研究工作[1-5],尤其对其调理脾胃运化,调节食欲的效应进行了重点研究。本研究以束缚捆绑方式制备慢性应激动物模型,结合动物摄食量、体重、行为学变化,运用免疫荧光双染、实时荧光定量(Real-time Fluorescent Quantitative PCR,RT-qPCR)技术与方法,从基因与蛋白水平,检测下丘脑(Arcuate Nucleus,ARC)中瘦素受体(Leptin Receptor,ob-R)、α-促黑素细胞激素(α-melanocyte Stimulating Hormone,α-MSH)表达,探讨逍遥散疏肝解郁、助脾胃运化功能与调食欲的作用机制。
1 材料与方法
1.1 材料
1.1.1 动物与分组 SD健康雄性大鼠,体质量180~200 g,购自北京维通利华实验动物有限公司[动物许可证号:SCXK(京)2012-0001]。清洁级动物房饲养:室温(21±1)℃,相对湿度40%~60%,光照明暗各12 h(明7:00—19:00,暗19:00—7:00),自由饮用纯净水,予常规饲养。大鼠适应喂养1周,按体重编号,查随机数字表,随机分为4组:正常组、7 d模型组、21 d模型组、逍遥散组各24只,每4只大鼠饲养于1笼,每组6笼。
1.1.2 药物 逍遥散制备:逍遥散,出自《太平惠民和剂局方》,按照原书组方,由当归、白芍、柴胡、白术、茯苓、甘草、煨生姜、薄荷8种中药按3∶3∶3∶3∶3∶1.5∶1∶1比例,由河北中医学院中药药理室进行鉴定和提取,最终制成干粉备用。所有生药均购自北京同仁堂健康药业股份有限公司(石家庄店)。提取方法同文献[4],最终提取率为18.8%。以去离子水混悬给药。
1.2 方法
1.2.1 慢性束缚应激模型制备 大鼠束缚于特制的T型束缚架上,束缚架由导师课题组设计:上端束缚台有两条可调节松紧的粘带,用于固定动物胸、腹部;下面是支架,高15 cm。束缚应激方法同文献[4]。束缚时间点随机,每天连续3 h束缚制备应激大鼠模型。实验前和开始实验后每周称量1次大鼠体质量、摄食量。于束缚前30 min进行灌胃,正常组每天灌服0.9%生理盐水;7 d模型组大鼠每天束缚应激3 h连续7 d,同时灌服0.9%生理盐水;21天模型组大鼠每天束缚应激3 h连续21 d,同时灌服0.9%生理盐水;逍遥散组大鼠每天束缚应激3 h连续21 d,同时灌服逍遥散[3.854 g/(kg·d)]。
1.2.2 行为学实验 于实验前1 d和实验开始后第7、21天观测各组大鼠行为学。
1.2.2.1 旷场实验 长×宽×高为100 cm×100 cm×40 cm旷场箱,底面平分为20 cm×20 cm小正方格的25格。动物运动轨迹由上海欣软信息科技有限公司提供的行为学记录分析软件(Version 2.0)分析:大鼠5 min内活动总路程。
1.2.2.2 高架十字实验 高架十字迷宫由两条相对的开放臂、两条相对的封闭臂、一个联结四条臂的中央平台组成。行为学记录分析软件分析5 min内大鼠进入开放臂、封闭臂的次数和停留时间。
1.2.3 ELISA方法检测大鼠血清D-木糖 每组12只大鼠取血2 mL(2管),离心,分离血清,-20 ℃下保存待测。按照试剂盒说明书步骤操作测定血清D-木糖含量(间苯三酚法),试剂盒购自南京建成生物工程研究所。
1.2.4 免疫荧光双染观测 各组大鼠下丘脑ARC中α-MSH、ob-R蛋白表达水平
1.2.4.1 取材与染色步骤 7 d组于7 d取材,21 d组于实验第22天取材。各组随机取6只大鼠予10%水合氯醛腹腔麻醉(0.35~0.40 mL/100 g体质量),行左心室升主动脉心脏灌注固定,20%、30%蔗糖溶液梯度脱水。Leica CM1950恒温冷冻切片机切片,片厚25 μm。
免疫染色具体步骤:1)切片用0.01M PBS漂洗后,加入含0.5%TritonX-100的0.01M PBS液,37 ℃,温箱孵育1 h;2)0.01M PBS漂洗,加入封闭液,室温孵育,摇床轻摇1 h;3)吸出封闭液,加入1∶100的Rabbit anti-α-MSH polyclonal antibody,4 ℃冰箱孵育,过2夜;4)从冰箱取出室温平衡30 min,配制漂洗液漂洗;5)加入1∶200的Alexa Fluor@ 594 donkey anti-rabbit IgG,避光,室温孵育4 h;6)0.01M PBS漂洗,加入封闭液,室温孵育,轻摇1 h;7)吸出封闭液,加入1∶50的Goat anti-ob-R polyclonal antibody,入4 ℃冰箱孵育,过2夜;8)从冰箱取出,室温平衡30 min,漂洗液漂洗;9)加入1∶200的Alexa Fluor@ 488 donkey anti-goat IgG,室温孵育4 h;10)0.01M PBS漂洗,防荧光淬灭封片剂封片。染色过程中涉及到用0.01M PBS漂洗过程,均为每次5 min,漂洗3次;封闭液为含10% donkey serum和0.5%TritonX-100的0.01M PBS;漂洗液为含2% donkey serum和0.5%TritonX-100的0.01M PBS,均每次漂洗5 min,漂洗3次;Ⅰ抗Ⅱ抗稀释液为含2% donkey serum和0.5%TritonX-100的0.01MPBS。
Donkey serum,购自Millipore Corporation,USA;Goat anti-ob-R polyclonal antibody购自Santa Cruz Biotechnology,Inc.,USA;Rabbit anti-α-MSH antibody购自Phoenix Pharmaceuticals,Inc.,USA;Alexa Fluor@ 594 donkey anti-rabbit IgG和Alexa Fluor@ 488 donkey anti-goat IgG均购自Thermo Fisher,USA。
1.2.4.2 图像处理 使用Leica SP8激光共聚焦显微镜扫描成像,经Image-Pro Plus 6.0图像分析系统进行图像分析。每组10张切片,下丘脑ARC部位选取150 μm×150 μm面积,统计α-MSH、ob-R阳性表达面积(area,μm2)、积分光密度(Intergral optical density,IOD)、阳性细胞表达数(SUM),及ob-R和α-MSH共染程度(Pearson′s correlation coefficient)。数据处理:Area=area测量值/测量总面积,IOD=IOD测量值/测量总面积。
1.2.5 RT-qPCR方法检测各组大鼠下丘脑ob-R mRNA、α-MSH mRNA表达
1.2.5.1 取材、总RNA提取、反转录和PCR扩增 每组6只大鼠,予10%水合氯醛腹腔麻醉,断头,剥取全脑,液氮速冻,干冰环境下切取ARC组织。每个样本取约50 μg匀浆,采用TRIzol(购自Invitrogen Corporation,Carlsbad,USA)常规操作提取总RNA,1%琼脂糖凝胶电泳测定RNA纯度(OD260/OD280比值在1.8~2.0之间),表明提取的RNA纯度较高,污染很少,可后续反转录反应。
根据a M-MLV反转录试剂盒(购自Promega Corporation,Madison,USA)说明,将1 μg总RNA转录生成cDNAs。然后根据SYBR Green I荧光定量PCR试剂盒(Fermentas Inc.,Canada)采用ABI 7300 Real-time PCR System进行扩增。扩增引物:GAPDH,Forward:5′-TGAACGGGAAGCTCACTG-3′,Reverse:5′-GCTTCACCACCTTCTTGATG-3′,NM_017008,120bp;Ob-R,Forward:5′-GCCAAAGTCAACTACGCTCTT-3′,Reverse:5′-CTTCCATACGCAAACCCA-3′,NM_012596.1,133bp;a-MSH,Forward:5′-CAAGTTCCGCCAGAAACAG-3′,Reverse:5′-TTGCCTTAGCCCTTCGGT-3′,NM_012982.3,116bp。PCR热循环参数:95 ℃ 5 min,然后40个循环反应:94 ℃ 30 s,58 ℃ 30 s,72 ℃ 30 s,于每个循环的第3个步骤,即:72 ℃ 30 s收集荧光信号。
1.2.5.2 结果分析 扩增完毕后,进入SDS V1.3软件结果分析界面,设置基线为第3~15个循环,GAPDH为内参照基因,设置对照组的第1号样品为标准1,得到各样本各目的基因的Ct值。按照公式RQ=2-△△Ct计算各目的基因表达的相对定量值(RQ值),将RQ值用于统计分析。
1.3 统计学方法 以SPSS 21.0的一般线性模型(general linear model,GLM)的重复测量过程实现对重复测量资料体重、摄食量、行为学数据的单变量方差分析,并用多因素方差分析过程实现每个时间点上组间的两两比较(LSD法),其他数据采用单因素方差分析(One-way ANOVA)进行统计处理,采用LSD法进行组间比较。以P<0.05为差异有统计学意义。
2 结果
2.1 各组大鼠体质量和摄食量变化 见表1、表2。

表1 各组大鼠体质量变化比较
注:与正常组比较,*P<0.05,**P<0.01;与21 d模型组比较,△P<0.05,△△P<0.01。

表2 各组大鼠摄食量变化比较
注:与正常组比较,*P<0.05,**P<0.01。
束缚应激前,3组大鼠体质量、摄食量无统计学差异。束缚第7、14、21天,在相同时间点内21 d模型组大鼠体重明显低于正常大鼠(P<0.01);束缚第7、21天,在相同时间点内逍遥散组大鼠体重明显高于21 d模型组(P<0.05)。束缚第7、14、21天,在相同时间点内21 d模型组大鼠摄食量少于正常组,第7、21天最明显(P<0.01);实验第7、14、21天逍遥散组大鼠摄食量均多于21 d模型组,但组间比较差异均无统计学意义。
2.2 各组大鼠行为学变化
2.2.1 旷场实验结果 见表3。从表3可以看出,束缚应激前,各组大鼠5 min内活动总路程无统计差异,束缚造模第7天、21天,模型大鼠活动总路程较正常大鼠减少,虽然逍遥散组大鼠5 min内活动总路程较模型大鼠有所增加,但组间比较差异均无统计学意义。

表3 各组大鼠旷场实验移动总路程
2.2.2 高架十字实验结果 见表4~表7。在实验第7、21天,模型大鼠5 min内进入高架十字迷宫开放臂次数和停留时间均较正常大鼠减少,尤其束缚应激21 d大鼠进入开放臂次数减少明显(P<0.01);模型大鼠5 min内进入封闭臂次数、停留时间均有所增加,但组间比较无统计学意义。
实验第21天,5 min内逍遥散组大鼠较单纯应激大鼠进入开放臂次数、停留时间有所增多,尤其逍遥散组大鼠在开放臂停留时间增加明显(P<0.01);逍遥散大鼠进入封闭臂次数、停留时间均较模型大鼠下降,尤其第7天逍遥散大鼠进入封闭臂次数下降明显(P<0.01)。

表4 各组大鼠5 min进入开放臂次数比较(n=20,次,
注:与正常组比较,*P<0.05,**P<0.01。

表5 各组大鼠5 min开放臂停留时间比较
注:与正常组比较,*P<0.05,**P<0.01;与21 d模型组比较,△P<0.05,△△P<0.01。

表6 各组大鼠5 min进入封闭臂次数比较(n=20,次,
注:与正常组比较,*P<0.05,**P<0.01;与21 d模型组比较,△P<0.05,△△P<0.01。
2.3 血清D-木糖含量 21 d模型组(0.16±0.01 mmol/L)和逍遥散组(0.66±0.01 mmol/L)大鼠血清D-木糖水平较正常组(0.73±0.12 mmol/L)明显下降,P<0.05;但逍遥散组大鼠血清D-木糖水平较21 d模型大鼠明显升高,差异有统计学意义(P<0.01)。
2.4 免疫荧光双染观测各组下丘脑ARC中ob-R、α-MSH蛋白水平变化 见表8~表10、图1。

表7 各组大鼠5 min封闭臂停留时间比较
注:与正常组比较,*P<0.05,**P<0.01;与21天模型组比较,△P<0.05,△△P<0.01。

图1 各组大鼠下丘脑ARC中а-MSH和ob-R表达
21 d模型组和逍遥散组大鼠下丘脑ARC中ob-R的阳性表达面积、积分光密度和阳性细胞数明显高于正常组(P<0.01);逍遥散组大鼠下丘脑ARC中ob-R的阳性表达面积、阳性细胞数较21 d模型组明显下降(P<0.01)。
7 d模型组、21 d模型组、逍遥散组大鼠下丘脑ARC中α-MSH的阳性表达面积、平均光密度、积分光密度、阳性细胞数均较正常组升高,尤其21 d模型组大鼠α-MSH的阳性表达面积和逍遥散组α-MSH的积分光密度增加明显(P<0.01)。逍遥散组α-MSH虽然较模型组有所下降,但差异无统计学意义。
21 d模型组大鼠ob-R与α-MSH共表达系数较正常大鼠明显增加(P<0.01),逍遥散组的共染程度低于21 d模型组,但组间比较差异无统计学意义。
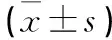
表8 各组大鼠下丘脑ARC中ob-R表达情况
注:与正常组比较,*P<0.05,**P<0.01;与21 d模型组比较,△P<0.05,△△P<0.01。
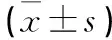
表9 各组大鼠下丘脑ARC中α-MSH表达情况
注:与正常组比较,*P<0.05,**P<0.01。
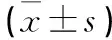
表10 各组大鼠下丘脑ARC中α-MSH、ob-R共表达情况
注:与正常组比较,*P<0.05,**P<0.01。
2.5 RT-qPCR法观测各组大鼠下丘脑ARC ob-R mRNA和α-MSH mRNA表达变化
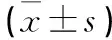
表11 各组大鼠下丘脑ARC ob-R mRNA和α-MSH mRNA表达比较
注:与正常组比较,*P<0.05,**P<0.01;与21天模型组比较,△P<0.05,△△P<0.01。
从表11可以看出,与正常组比较,7 d模型组大鼠下丘脑ARC中ob-R mRNA与α-MSH mRNA表达均增加,其中ob-R mRNA表达变化更为明显(P<0.01);21 d模型组和逍遥散组大鼠下丘脑ob-R mRNA和α-MSH mRNA表达均较正常大鼠明显增加(P<0.05或P<0.01);与21 d模型组比较,逍遥散组大鼠下丘脑ARC中ob-R mRNA表达明显下降(P<0.01),α-MSH mRNA表达虽然也较21 d模型大鼠下降,但组间比较差异无统计学意义。
3 讨论
由于束缚制动可模拟人被长期限制在狭小空间,与人类心身疾病过程相似,属于纯粹的心理挫折应激[6]。本研究采用束缚制动方式制备心理应激动物模型,以逍遥散为干预用药,以旷场实验和高架十字实验客观观测大鼠的自主活动能力、对新奇环境的探究行为,分析应激动物出现的心理状态,结合大鼠摄食、体重和外观皮毛色泽等的变化,首先观测了慢性束缚应激21 d大鼠相关变化及灌服逍遥散后的反应。
本研究中,随着束缚应激时间的延长,21 d模型组大鼠体重增长缓慢,摄食量较正常组大鼠下降;行为学表现在旷场实验中5 min大鼠活动总路程减少,高架十字实验中大鼠进入开放臂的次数和停留时间减少,进入封闭臂次数和时间增加,说明大鼠自主活动能力下降,探究性行为减少,对新异环境产生了恐惧、郁闷心理;伴随应激因素的持续施加,模型大鼠由最初的强烈挣扎反抗,到后期的倦怠懒动、反应迟钝、毛色枯涩、大便溏结不调的表现;结合模型大鼠血清D-木糖含量明显下降,说明胃肠消化吸收功能亦下降。综合表明,心理应激因素的施加首先刺激大鼠出现狂躁、焦虑的情绪反应,但随着应激因素的持续施加,逐渐出现了郁闷、挫折心理反应和胃肠功能失调的内在变化。采用中药复方逍遥散干预的应激大鼠,其体重、摄食量、皮毛色泽、行为学均得到一定的改善,与课题组之前报道[3-4,7]一致。方药反证,也说明每天3 h连续21 d捆绑束缚方式可制备慢性应激肝郁脾虚样大鼠模型。
ob-R是瘦素(Leptin)的高亲和力受体,属I类细胞因子超家族。功能性ob-R广泛表达于下丘脑弓状核、腹内侧核、背内侧核、室旁核、室周核及下丘脑外侧区的神经元[8-9],这些区域是调节摄食和体重的重要区域。其中ARC在能量代谢调节过程中发挥主要作用[10]。
ARC内的Neuropeptide Y(NPY)/Agout-related peptide(AgRP)神经元和Proopiomelanocortin(POMC)/Cocain and amphetamine-regulated transcript(CART)神经元,前者能增强食欲、抑制能量消耗;后者所分泌的POMC的降解产物α-MSH可起到抑制食欲和促进能量消耗的作用。功能性ob-R与NPY/AgRP和POMC/CART神经元共存[11],下丘脑ARC中的ob-R被Leptin激活,作用于这两类神经元,可抑制NPY/AgRP神经元产生和释放NPY、AgRP,另一方面则可促进POMC神经元产生和释放α-MSH,从而调节机体的能量代谢、摄食行为和体质量平衡等[12-13]。α-MSH是一种具有强烈的中枢性抑制摄食、促进能量消耗作用的神经肽[14-15]。
本课题组前期研究表明,慢性束缚应激可导致进入下丘脑的Leptin水平增高,刺激功能性ob-R表达增加,Leptin和ob-R特异性地结合,破坏了下丘脑“食欲调节网络”的平衡[4]。在前期基础上,本研究重点观测了ARC中ob-R和α-MSH蛋白与基因表达情况,进一步研究慢性应激影响脾胃功能的中枢神经内分泌机制及逍遥散疏肝健脾调节食欲的作用靶点。
本研究通过RT-qPCR法、免疫荧光双染方法检测了模型大鼠下丘脑ARC中ob-R和α-MSH表达变化,结果表明随着束缚应激因素的持续施加,21 d模型组大鼠下丘脑ARC中ob-R和α-MSH蛋白和基因表达,及ob-R和α-MSH共表达均高于正常组,逍遥散则具有相应的下调其表达作用。说明,外周进入下丘脑的Leptin与ob-R结合后引起大鼠体重和摄食量下降机制与通过调节下丘脑弓状核α-MSH通路有关,这也可能为慢性应激状态下逍遥散疏肝健脾,调节机体食欲和能量代谢影响脾胃功能的作用靶点之一。
[1]Jiang YM,Li XJ,Meng ZZ,et al.Effects of Xiaoyaosan on Stress-Induced Anxiety-Like Behavior in Rats:Involvement of CRF1 Receptor[J].Evid Based Complement Alternat Med,2016:1238426.doi:10.1155/2016/1238426.
[2]Meng ZZ,Chen JX,Jiang YM,et al.Effect of xiaoyaosan decoction on learning and memory deficit in rats induced by chronic immobilization stress[J].Evid Based Complement Alternat Med,2013:297154.doi:10.1155/2013/297154.
[3]Liang Y,Guo XL,Chen JX,et al.Effects of the chinese traditional prescription xiaoyaosan decoction on chronic immobilization stress-induced changes in behavior and ultrastructure in rat hippocampus[J].Evid Based Complement Alternat Med,2013:984797.doi:10.1155/2013/984797.
[4]Wang SX,Chen JX,Yue GX,et al.Xiaoyaosan decoction regulates changes in neuropeptide y and leptin receptor in the rat arcuate nucleus after chronic immobilization stress[J].Evid Based Complement Alternat Med,2012:381278.doi:10.1155/2012/381278.
[5]李晓娟,白晓晖,陈家旭,等.逍遥散对慢性束缚应激抑郁模型大鼠JAK/STAT信号通路的影响[J].中华中医药杂志,2016,31(5):1700-1704.
[6]谢兴振,迟晓丽,周文霞,等.应激动物模型研究进展[J].中国新药杂志,2008,17(16):1375-1380.
[7]王杰鹏,旷湘楠,张成浩,等.慢性应激肝郁脾虚模型大鼠行为学变化及逍遥散调节作用[J].河北中医药学报,2016,31(4):7-10,21.
[8]王红星,雷治海,丁菲,等.用原位杂交法研究猪下丘脑内瘦素长形受体mRNA的分布定位[J].南京农业大学学报,2002,25(1):80-84.
[9]吴坚,邹大进.瘦素受体的研究进展[J].生理科学进展,2000,31(2):143-146.
[10]Spiegelman BM,Flie JS r.Obesity and the regulation of energy balance[J].Cell,vol.2001,104(4):531-543.
[11]Millington GW.The role of proopiomelanocortin(POMC)neurones in feeding behaviour[J].Nutr Metab(Lond).2007,4(18):1-16.
[12]Elias CF,Aschkenasi C,Lee C,et al.Leptin differentially regulates NPY and POMC neurons projecting to the lateral hypothalamic area[J].Neuron,1999,23(4):775-786.
[13]王斌,章卫平.瘦素调节下丘脑神经肽Agouti相关蛋白表达的研究进展[J].第二军医大学学报,2009,30(5):569-572.
[14]Mountjoy KG,Wong J.Obesity,diabetes and functions for proopiomelanocortin-derived peptides[J].Mol Cell Endocrinol,1997,128:171-177.
[15]Vergoni AV,Bertolini A.Role of melanocortins in the central control of feeding[J].Eur J Pharmacol,2000,405:25-32.
(2017-02-20收稿 责任编辑:洪志强)
Mechanism of Xiaoyaosan Decoction on ob-R and α-MSH in arcuate nucleus of hypothalamus of chronic restraint stress modeling rats with liver depression and spleen deficiency
Kuang Xiangnan1, Wang Shaoxian1, Fang Chaoyi1, Wang Jiepeng1, Chen Jiaxu2, Liu Yueyun2
(1HebeiCollegeoftraditionalChinesemedicine,Shijiazhuang050200,China; 2BeijingUniversityofChineseMedicine,SchoolofBasicMedicalSciences,Beijing100029,China)
Objective:To study the mechanism of Xiaoyaosan Decoction in regulating appetite by soothing liver to relieve depression, and invigorating spleen. Methods:SD male rats were randomly divided into four groups; the control group (A), the 7-day model group (B), the 21-day model group (C) and the Xiaoyaosan (XYS) group (D). Except for the control group, models of the other three groups were established by chronic restraint stress method 3 h a day persistently for 7 days, 21 days and 21 days respectively, while Xiaoyaosan Decoction was given in the XYS group at the same time. Body weight, food intake, animal behavior, and the level of D-xylose in the serum were detected in all four groups; the mRNA and protein levels of leptin receptor(ob-R) and-melanocyte stimulating hormone(-MSH) were measured by RT-qPCR and immunofluorescence double staining method. Results:Compared with the control group, the body weight, food intake and the level of D-xylose in the serum were significantly decreased in group C, with decreased autonomous activity and new environment exploratory behavior; while the result of group D showed that Xiaoyaosan Decoction could regulate all of those mentioned above. All together indicated that chronic restraint animal model with liver depression and spleen deficiency can be established by restraining 3 h a day, for 21 days continually; the expression of ob-R and-MSH increased in arcuate nucleus (ARC) of chronic restraint stress rats and Xiaoyaosan Decoction could reduce the expression. Conclusion:The expression of ob-R and-MSH can be regulated by Xiaoyaosan Decoction, indicating that ob-R and-MSH may be the targets of Xiaoyaosan Decoction in regulating the function of spleen and stomach through soothing the liver and invigorating the spleen so as to regulate appetite and energy metabolism.
Chronic Stress; Xiaoyaosan Decoction; Liver depression and spleen deficiency; Leptin Receptor (ob-R);-melanocyte Stimulating Hormone (-MSH)
国家自然科学基金项目(编号:81202644;81673881;81630104);河北省自然科学基金项目(编号:H2016423049);高等学校博士学科点专项科研基金资助课题(编号:20121323120016);河北省教育厅高等学校科学研究项目(编号:QN2014118)
王少贤,女,副教授,医学博士,硕士研究生导师,E-mail:muhudie@163.com
R228
A
10.3969/j.issn.1673-7202.2017.03.003

