经皮左心室重建术对心尖部室壁瘤形成的缺血性心肌病患者术后即刻心排量的影响
王建 赖可可 张哲义 苏茂龙 王焱
经皮左心室重建术对心尖部室壁瘤形成的缺血性心肌病患者术后即刻心排量的影响
王建 赖可可 张哲义 苏茂龙 王焱
目的 评价经皮左心室重建术对心尖部室壁瘤形成的缺血性心肌病患者术后即刻心排量的影响。方法 纳入2015年1月至2016年12月于厦门大学附属心血管病医院行经皮左心室重建术的心尖部室壁瘤形成的缺血性心肌病患者25例。监测患者在经皮左心室重建术前、后的心功能指标变化情况。结果 25例患者中男23例(92.0%),平均年龄(65.4±11.9)岁,体重指数(23.2±4.0)kg/m2。共24例(96.0%)患者成功进行经皮左心室重建术,1例因装置无法达到最佳位置而终止手术。PARACHUTE装置植入后,患者心排量[(4.85±0.93)L/min比(3.83±0.72)L/min,P<0.01]、心排量指数[(2.90±0.82)L/(min·m2)比(2.32±0.74)L/(min·m2),P<0.01]均显著高于开伞前,差异均有统计学意义。复苏后患者的心功能仍保持稳定,心排量[(5.01±0.92)L/min比(3.83±0.72)L/min,P<0.01]、心排量指数[(3.01±0.87)L/(min·m2)比(2.32±0.74)L/(min·m2),P<0.01]均较术前显著增加,差异均有统计学意义。结论 经皮左心室重建术后即刻明显提高心尖部室壁瘤形成的缺血性心肌病患者的心排量和心排量指数,这可能与植入物即刻改善心尖部室壁瘤的矛盾运动相关。
经皮左心室重建术; 缺血性心肌病; 心尖部室壁瘤
近三十年来,抑制心脏内分泌系统的药物在治疗慢性心肌病方面似乎已难有突破性的进展[1],而血运重建对于已经发生心肌梗死并出现左心室严重重构的缺血性心肌病患者的作用甚微[2]。外科手术进行左心室重建及植入性器械治疗逐渐进入了缺血性心肌病的治疗领域,成为近年来心肌病治疗领域的热点。左心室室壁瘤通常发生在急性心肌梗死后,是由于坏死心肌处收缩力下降或丧失,在心腔内压力的作用下向外膨出而形成,是急性心肌梗死后的常见并发症之一[3]。室壁瘤所导致的左心室矛盾运动、收缩顺序改变,严重影响心肌梗死后重塑的左心室功能[4]。此外,室壁瘤内血栓栓塞的风险也是导致心肌梗死患者再次发生心脑血管事件的重要因素[5]。本中心前期临床研究初步结果已显示,使用PARACHUTE装置行经皮左心室重建术的短期安全性较好且手术成功率较高[6-7]。但目前该术式的有效性主要通过临床功能学评估[例如6 min步行试验、明尼苏达心力衰竭问卷调查及美国纽约心脏病协会(NYHA)心功能分级],超声心动图也仅仅显示左心室收缩末期和舒张末期容积的减少。尚无证据表明该装置改善左心室矛盾运动后所带来的心排量的增加。本研究通过监测接受经皮左心室重建术术中全程的心排量,研究该术式对即刻心排量的影响。
1 对象与方法
1.1 研究对象
纳入2015年1月至2016年12月在厦门大学附属心血管病医院行经皮左心室重建术的心尖部室壁瘤形成的缺血性心肌病患者25例,其中男23例(92.0%),平均年龄(65.4±11.9)岁。25例患者中吸烟18例(72.0%),高血压病14例(56.0%),糖尿病9例(36.0%),脂质代谢紊乱10例(40.0%),心房颤动3例(12.0%),室性心动过速或心室颤动1例(4.0%)。
入选标准:(1)年龄≥18岁;(2)前壁心肌梗死后60 d以上、已接受优化抗心力衰竭药物治疗、NYHA心功能分级Ⅱ~Ⅳ级的心力衰竭患者;(3)超声心动图标准:15%≤左心室射血分数(left ventricular ejection fraction,LVEF)≤40%;(4)左心室前壁存在结构异常或者运动异常;(5)超声心动图显示心尖部形态及大小符合PARACHUTE大小要求[8];(6)CT血管造影(computed tomographic angiography,CTA)再次证实左心室心尖部的形态及大小符合PARACHUTE大小要求。
排除标准:(1)仍有冠状动脉需再血管化;(2)存在左心室前壁以外的室壁运动异常;(3)6个月内发生过脑血管事件;(4)存在常规心导管手术或抗凝禁忌证;(5)具有人工机械二尖瓣或主动脉瓣;(6)患者存在中度以上二尖瓣或主动脉瓣反流或狭窄。本研究已通过厦门大学附属心血管病医院伦理委员会批准,所有患者术前均签署手术知情同意书。
1.2 手术过程及有创心排量监测
患者平卧于手术台,喉罩通气全麻后常规消毒铺巾,建立股动脉入径后,送入6 F猪尾导管行左心室心尖造影。沿猪尾导管置入2.6 m Amplatz Extra Stiff 导丝,保留导丝,撤出猪尾导管。沿保留导丝将14 F或16 F输送鞘管(内有扩张鞘和6 F JR4导管)送至左心室心尖部并调整输送鞘位置和指向,使之头端位于左心室心尖部且输送鞘管走向与预计封堵区域的长轴一致。将装载PARACHUTE装置的输送系统,在左心室造影及经胸超声心动图指引下送入心尖部,复查左心室造影及经胸超声心动图确认PARACHUTE装置的脚已经位于心尖部室壁瘤理想位置后,后撤输送鞘管并充盈球囊打开PARACHUTE装置,使锚定装置锚定于正常心肌与梗死瘢痕交界处,隔离心尖部室壁瘤区域。复查左心室造影和经胸超声心动图评估PARACHUTE装置的分区效果后,释放该装置。术中全程采用Edwards Life sciences Vigileo系统进行心排量监测。全麻后根据患者的每搏量变异度(stroke volume variation, SVV)适当地扩容,保证患者的心脏前负荷足够。术中测量患者在全麻后扩容前、后,PARACHUTE开伞前、后,以及复苏时的心排量和心排量指数。
1.3 统计学分析
所有数据采用SPSS 13.0进行处理。符合正态分布的计量资料以均数±标准差表示,组间比较采用配对t检验;非正态分布的计量资料用中位数(四分位间距)表示;计数资料以例数(率)表示。以P<0.05为差异有统计学意义。
2 结果
2.1 患者临床基本情况
共入选25例心尖部室壁瘤形成的缺血性心肌病患者,体重指数(23.2±4.0)kg/m2。18例(72.0%)患者行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI),5例(20.0%)行急诊PCI,1例(4.0%)行冠状动脉旁路移植术,1例(4.0%)患者因心肌梗死后出现心室颤动植入植入式心律转复除颤器(implantable cardioverter defibrillator,ICD)。1例(4.0%)男性患者因装置未能到达理想位置未释放,最终24例(96.0%)患者成功植入PARACHUTE装置。患者术后口服阿司匹林、P2Y12受体拮抗药、血管紧张素转化酶抑制药/血管紧张素Ⅱ受体拮抗药、β阻滞药等治疗(表1)。

表1 25例患者的临床资料情况
注:BMI,体重指数;ICD,植入式心律转复除颤器;PCI,经皮冠状动脉介入治疗;CABG,冠状动脉旁路移植术;ACEI,血管紧张素转化酶抑制药;ARB,血管紧张素Ⅱ受体拮抗药;NYHA,纽约心脏病协会
患者植入PARACHUTE的时间距心肌梗死的平均时间为(14.3±8.1)个月。植入的PARACHUTE型号见表2。
2.2 术中血流动力学监测(图1)
24例成功植入PARACHUTE的患者。根据SVV对患者进行适当扩容,并没有明显增加患者的心排量[(3.90±1.11)L/min比(4.13±0.93)L/min,P=0.0502]或心排量指数[(2.41±1.16)L/(min·m2)比(2.52±0.99)L/(min·m2),P=0.08]。PARACHUTE装置置入后,心排量[(4.85±0.93)L/min比(3.83±0.72)L/min,P<0.01]、心排量指数[(2.90±0.82)L/(min·m2)比(2.32±0.74)L/(min·m2),P<0.01]均显著高于开伞前,差异均有统计学意义。复苏后患者的心功能仍保持稳定,心排量[(5.01±0.92)L/min比(3.83±0.72)L/min,P<0.01]、心排量指数[(3.01±0.87)L/(min·m2)比(2.32±0.74)L/(min·m2),P<0.01]均较术前显著增加,差异均有统计学意义;而与患者术后即刻心排量、心排量指数比较差异均无统计学意义(均P>0.05)。

表2 24例成功植入PARACHUTE患者的装置型号[例(%)]
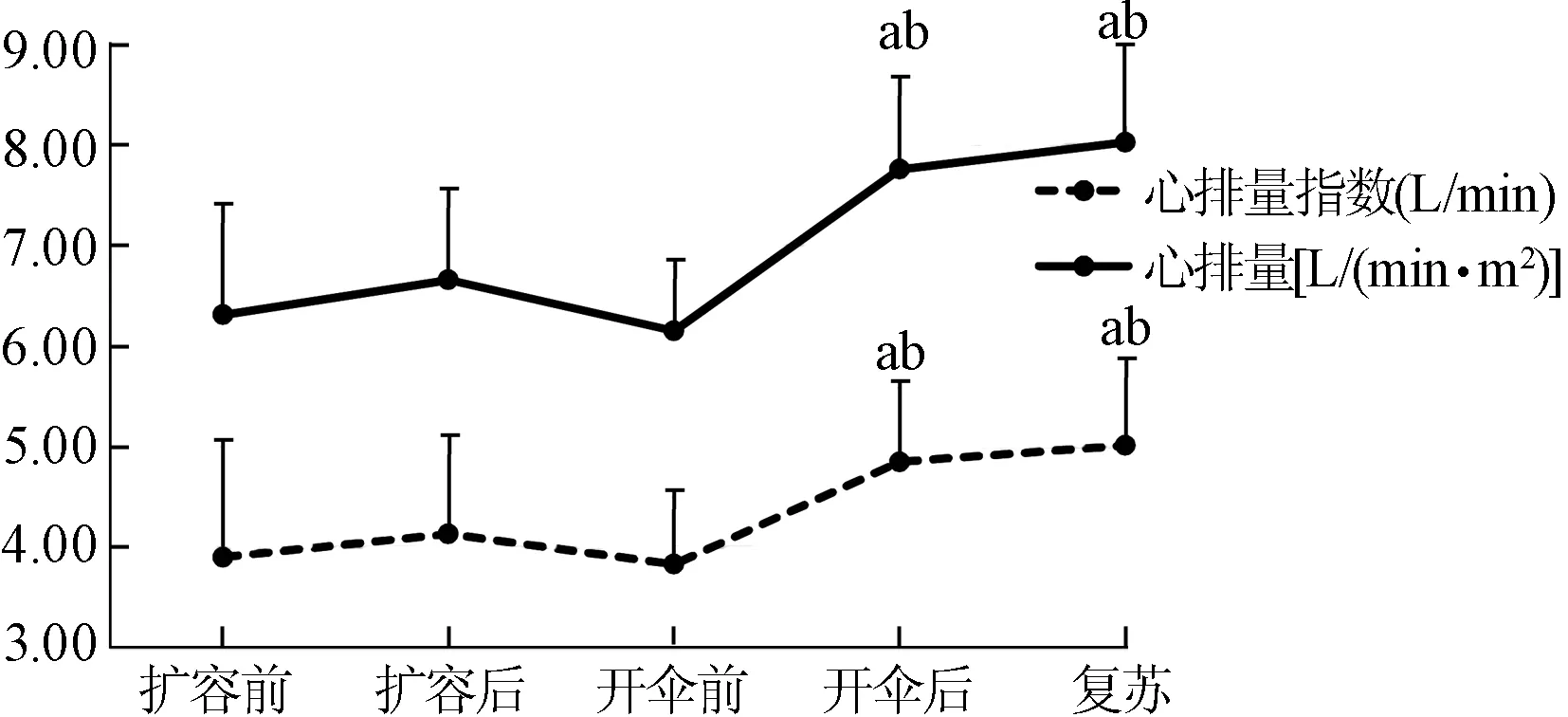
a,与扩容前相比较,P<0.01;b,与开伞前相比较,P<0.01图1 24例患者术中心排量和心排量指数
3 讨论
心肌梗死后由于坏死心肌处收缩力下降或丧失,室壁瘤在心腔内压力的作用下向外膨出而形成,是急性心肌梗死后期常见的并发症之一,发生率为10%~30%;左心室室壁瘤5年的存活率为10%~24%[3]。有研究报道显示,心肌梗死后室壁瘤形成患者5年的死亡率为64%,对照组为有心肌梗死而无室壁瘤的患者,5年存活率为29%[9]。心肌梗死后室壁瘤形成的缺血性心肌病患者伴有恶性心律失常、心功能不全或功能性的二尖瓣反流时,是ICD、CRT(-D)或MitraClip的植入适应证。但是,由于梗死瘢痕区域的存在,上述治疗方式无法改善左心室功能或对治疗低应答;而接受冠状动脉旁路移植术时的左心室重建也未能降低缺血性心肌病患者的总体死亡率[10]。我国目前急性心肌梗死的急诊救治网络尚不健全,胸痛中心网络正处于建设中[11],有相当多的患者在心肌梗死后形成室壁瘤,而且LVEF降低的缺血性心肌病患者ICD的植入率很低[12],这部分患者预后极差。目前,能够改善左心室室壁瘤患者室壁活动异常的,除了创伤性较大的外科左心室重建,还有处于临床研究阶段的左心室分区装置PARACHUTE[13]。本中心既往研究证实,使用PARACHUTE装置进行经皮左心室重建术的短期安全性和较高的手术成功率[3-4]。目前,临床试验主要通过临床功能学评估(例如6 min步行试验、明尼苏达心力衰竭问卷调查和NYHA分级)[14-15],而CTA、磁共振成像和超声心动图也仅仅显示左心室容积的减少。本研究通过术中监测PARACHUTE装置植入前后患者的有创心排量,结果显示植入后即刻增加患者的心排量及心排量指数。
室壁瘤形成以后最初是梗死区域扩张,整个心室壁张力增高,进而使健康心肌也受累扩张,使心腔扩大,室壁张力进一步增高,从而形成恶性循环,导致整个左心室功能衰竭,并引起继发性二尖瓣关闭不全、肺动脉高压和右心功能衰竭,最终导致全心衰竭,表现为胸闷、呼吸困难、不能平卧、肢体水肿、胸水和腹水,危及生命;有的还会在心腔内形成血栓,并发脑部等重要脏器栓塞而致残甚至致死[16-17]。外科左心室重建术未能改善部分心肌梗死后室壁瘤形成患者的心功能和预后,且外科手术风险仍较高[7,18]。经皮左心室重建术为心尖部室壁瘤患者提供了一个侵入性更小的治疗方式。根据现有的数据,其安全性似乎优于外科手术,其有效性将在未来的临床研究中得到进一步的证实[8]。由于目前受植入器械对于室壁瘤的部位及大小形态要求的局限,并非所有患者都可以接受这一治疗。术前较为完善的病史回顾、抗心力衰竭治疗及超声影像学筛选极为重要,评估患者的外科手术风险及生存预期也是必要的。
本研究证实了使用PARACHUTE装置进行经皮左心室重建术,术后即刻心排量和心排量指数显著增加,这可能与消除心尖部室壁瘤的矛盾运动相关。但由于本研究入选例数有限,且未对患者的长期心功能进行随访,无法明确PARACHUTE植入后心排量的升高与患者预后之间的关系,这是本研究的缺点。左心室分区所带来的心室容积、心室壁应力减小,即刻增加了缺血性心肌病患者的心功能储备,但对此类患者的长期心功能及预后的影响还有待中长期的随访结果。
[1] Krum H, Teerlink JR. Medical therapy for chronic heart failure. Lancet,2011,378(9792):713-721.
[2] Schinkel AF, Poldermans D, Rizzello V, et al. Why do patients with ischemic cardiomyopathy and a substantial amount of viable myocardium not always recover in function after revascularization? J Thorac Cardiovasc Surg,2004,127(2):385-390.
[3] Mills NL, Everson CT, Hockmuth DR. Technical advances in the treatment of left ventricular aneurysm. Ann Thorac Surg, 1993, 55 (3):792-800.
[4] Høst NB, Hansen PR. Infarction expansion and ventricular remodelling after acute myocardial infarction. Ugeskr Laeger,1993,155(43):3463-3467.
[5] Asinger RW, Herzog CA, Dick CD. Echocardiography in the evaluation of cardiac sources of emboli: the role of transthoracic echocardiography. Echocardiography,1993,10(4):373-396.
[6] 王建, 王斌, 肖国胜, 等. 经皮左心室分隔术对心尖部室壁瘤形成的缺血性心力衰竭患者的安全性及疗效评估. 中国循环杂志,2016,31(8):775-779.
[7] 李桂阳,王建,苏茂龙,等.左室室壁瘤分区术治疗缺血性心力衰竭并室壁瘤.中国分子心脏病学杂志,2016,17(3):1718-1720.
[8] Thomas M, Nienaber CA, Ince H, et al. Percutaneous ventricular restoration (PVR) therapy using the Parachute device in 100 subjects with ischaemic dilated heart failure: one-year primary endpoint results of PARACHUTE III, a European trial. EuroIntervention,2015,11(6):710-717.
[9] Bruschke AV, Proudfit WL, Sones FM Jr. Progress study of 590 consecutive nonsurgical cases of coronary disease followed 5-9 years. II. Ventriculographic and other correlations. Circulation, 1973,47(6):1154-1163.
[10] Jones RH, Velazquez EJ, Michler RE, et al. Coronary bypass surgery with or without surgical ventricular reconstruction. N Engl J Med,2009,360(17):1705-1717.
[11] 王焱,王斌,常贺,等.厦门市心血管病医院构建区域协同胸痛急救网络探索.中华医院管理杂志,2016,32(6):453-455.
[12] Dai SM, Zhang S, Chen KP, et al. Prognostic factors affecting the all-cause death and sudden cardiac death rates of post myocardial infarction patients with low left ventricular ejection fraction. Chin Med J (Engl), 2009,122(7):802-806.
[13] Silva G, Melica B, Pires de Morais G,et al. Percutaneous implantation of a ventricular partitioning device for treatment of ischemic heart failure: initial experience of a center. Rev Port Cardiol, 2012,31(12):795-801.
[14] Costa MA, Mazzaferri EL Jr, Sievert H,et al. Percutaneous ventricular restoration using the parachute device in patients with ischemic heart failure: three-year outcomes of the PARACHUTE first-in-human study. Circ Heart Fail,2014,7(5):752-758.
[15] Costa MA, Pencina M, Nikolic S, et al. The PARACHUTE Ⅳ trial design and rationale: percutaneous ventricular restoration using the parachute device in patients with ischemic heart failure and dilated left ventricles. Am Heart J, 2013,165 (4) 531-536.
[16] Baxley WA, Jones WB, Dodge HT. Left ventricular anatomical and functional abnormalities in chronic post infarction heart failure. Ann Intern Med, 1971,74(4):499-508.
[17] 吕昀,曾亚莉,郭晔炳,等.不同血运重建方法对陈旧前壁心肌梗死合并左心室室壁瘤患者预后的影响.中国介入心脏病学杂志,2015,23(4):203-207.
[18] 申磊磊,汪成,王嵘,等.左心室室壁瘤患者行左室成形术与单纯冠脉旁路移植术的中远期疗效对比.南方医科大学学报,2016,35(5):681-687.
Immediate effect of percutaneous ventricular restoration on cardiac output of ischemic cardiomyopathy patients with apical aneurysm
WANGJian,LAIKe-ke,ZHANGZhe-yi,SUMao-long,WANGYan.
DepartmentofCardiology,XiamenCardiovascularHospital,XiamenUniversity,Xiamen361000,China
WANGYan,Email:wy@medmail.com.cn
Objective To evaluate the immediate effect of percutaneous ventricular restoration (PVR) using the PARACHUTE system in ischemic cardiomyopathy patients with apical aneurysm. Methods The study included 25 patients who received PARACHUTE partitioning device (PVD) implantation in the Xiamen Cardiovascular Hospital between January 2015 to December 2016. Invasive left ventricular hemodynamic assessments as well as cardiac output and cardiac output index were analyzed. Results Twenty-five patients [mean age (65.4±11.9) years] suffered from left ventricular aneurysm and heart failure patients after anterior myocardial infarction were enrolled. Ventricular partitioning device implantation was successful in 24/25 (96.0%) patients. PVR was failed in 1 patient due to unable to land the PVD in a satisfactory location. After implantation, a significant increase in cardiac output [(3.83±0.72) L/minvs. (4.85±0.93) L/min,P<0.01] and cardiac index [(2.32±0.74) L/(min·m2)vs. (2.90±0.82) L/(min·m2),P<0.01] was found. Conclusions Our preliminary experience on percutaneous ventricular restoration using PARACHUTE system demonstrates its feasibility and safety with increase in cardiac output and cardiac index immediately following the device implantation.
Percutaneous ventricular partitioning; Ischemic cardiomyopathy; Apical aneurysm
10.3969/j.issn.1004-8812.2017.03.003
361000 福建厦门,厦门大学附属心血管病医院心内科(王建、赖可可、苏茂龙、王焱);厦门大学附属中山医院放射科(张哲义)
王焱,Email:wy@medmail.com.cn
R541.6
2016-11-21)
王建、赖可可为本文共同第一作者

