蜗牛酶辅助提取马勃多糖的工艺研究
王 华, 王 莹,詹长娟,王 翼, 徐 伟
(1.南京理工大学泰州科技学院 环境与制药工程学院,江苏泰州 225300;2.江苏农牧科技职业学院 动物药学院,江苏泰州225300)
蜗牛酶辅助提取马勃多糖的工艺研究
王 华1*, 王 莹2,詹长娟1,王 翼1, 徐 伟1
(1.南京理工大学泰州科技学院 环境与制药工程学院,江苏泰州 225300;2.江苏农牧科技职业学院 动物药学院,江苏泰州225300)
本试验以马勃多糖得率为评价指标,通过研究提取温度、时间、酶用量、pH对多糖提取率的影响,以单因素试验和正交试验设计优选最佳提取工艺条件。结果表明:蜗牛酶辅助提取马勃多糖的最佳提取工艺条件为提取温度35℃、提取时间120 min、酶用量5.0%、pH 6.0。在此条件下,马勃多糖得率为0.908%。与传统水提法相比,多糖得率提高了158.01%。由此可见,蜗牛酶辅助提取具有得率高、提取时间短、条件温和等优点。
马勃;多糖;蜗牛酶;提取
马勃,俗称马蹄包、马粪包、药包子等,是一种担子菌门真菌类中草药(郭晶,2013)。据中国药典(2015年版)记载,马勃具有清肺利咽、止血等功能。近年来,国内外大量科技工作者对马勃的化学成分进行了深入研究,发现马勃成分具有抑菌(郭晶,2013)、抗炎 (苏方华等,2010;左文英等,2004)、抗肿瘤细胞(崔磊等,2006)等药理作用,并从马勃中分离鉴定出了氨基酸盐类、三萜类、甾醇类化合物以及蛋白质、多肽、多糖、微量元素等成分(郭晶,2013;王晨英等,2002)。姜明华等(2014)和赵友生等 (2012)在马勃多糖抗肿瘤试验中发现,多糖组分对宫颈癌细胞、乳腺癌细胞及小鼠艾氏腹水瘤等具有较好的抑制作用。
本研究在传统水提法的基础上 (黄凯等,2008),通过蜗牛酶辅助提取马勃多糖 (马丽雅,2010),以马勃多糖得率为评价指标,比较温度、时间、酶用量、pH四个因素对提取情况的影响,再经正交试验优化提取条件,以确定最佳的提取工艺参数。
1 试验材料与方法
1.1 原料处理 将产自河北的马勃,经除杂,粉碎,烘干后,密封贮藏,备用。
1.2 试验仪器与试剂 HK-02A多功能粉碎机,上海烨昌食品机械有限公司;AL104电子天平,梅特勒-托利多;SHA-B双功能水浴恒温振荡器,金坛市杰瑞尔电器有限公司;UV754N紫外-可见分光光度计,上海精科仪器有限公司。
D-无水葡萄糖对照品 (110833-201506),中国食品药品检定研究院;蜗牛酶及生化试剂,上海金穗生物科技有限公司;其余试剂为市售分析纯。
1.3 试验方法与步骤
1.3.1 马勃多糖的提取 称取5.0 g马勃粉及一定量的柠檬酸-柠檬酸钠缓冲溶液加入到锥形瓶中,将锥形瓶置于水浴恒温振荡器中,待体系温度稳定后,加入蜗牛酶溶液,经酶处理一段时间后,加入2 mL 30%三氯乙酸终止反应 (莫祺晖等,2015),抽滤,收集滤液,蒸发浓缩,冷却。将量为浓缩液的1.5倍,无水乙醇慢慢加入到浓缩液中并不断搅拌,静置40 min,抽滤,所得滤饼即为马勃粗多糖。将马勃粗多糖用蒸馏水溶解并定容至250 mL,得马勃粗多糖溶液。
1.3.2 马勃多糖的测定 本文采用苯酚硫酸法测定多糖的含量。根据池源等(2014)的方法,以吸光度(A486)为纵坐标,葡萄糖的浓度(C)为横坐标,绘制曲线。标准曲线方程:A=0.0055C+0.0045,R2=0.9996。结果表明,以该法测定葡萄糖的浓度,在60~140 μg/mL范围内具有良好的线性关系(见图1)。

图1 苯酚-硫酸法葡萄糖标准曲线
取马勃多糖样品溶液1 mL于10 mL的具塞比色管中,加入5%苯酚溶液1 mL,摇匀,加入硫酸5 mL,加蒸馏水至10 mL,摇匀,放置10 min,置40℃水浴锅中保温18 min,取出后冷却至室温,以相应的试剂为空白,在486 nm波长处测定其吸光度。

式中:C为根据标准曲线计算得到的多糖的浓度,μg/mL;V为马勃多糖溶液的体积,mL;n为稀释倍数;m为马勃粉质量,g。
2 试验结果与分析
2.1 单因素试验结果
2.1.1 提取温度对马勃多糖得率的影响 称取马勃粉5.0 g,共5份,每份中加入pH 5.5的柠檬酸-柠檬酸钠缓冲液及1.5%酶液(共80 mL),分别在30、35、40、45、50℃下水浴提取60 min,结果见图2。
从图2中可看出,30~40℃,随着提取温度的不断升高,马勃多糖得率逐渐增大,35℃后尤为明显,当温度达到40℃时,多糖得率达到最大值,40℃之后,多糖得率明显降低,45℃后趋于平缓。温度升高,有助于蜗牛酶酶解效率的提高,使得马勃细胞壁的破坏速度加快,利于马勃细胞内多糖分子等扩散,但是温度过高,会使得大部分蜗牛酶结构,发生不可逆变性(肖冬光,2004);此外,较高的温度亦会加快多糖糖苷键的裂解,从而降低马勃多糖的得率。

图2 提取温度对马勃多糖得率的影响
2.1.2 提取时间对马勃多糖得率的影响 称取马勃粉5.0 g,共5份,每份中加入pH值为5.5缓冲液及1.5%酶液(共80 mL),在40℃下分别水浴提取60、75、90、105、120 min,结果见图3。

图3 提取时间对马勃多糖得率的影响
从图3中可看出,随着提取时间的增加,多糖得率不断提高,当提取时间超过90 min后,多糖得率趋于稳定。这是因为提取时间延长,马勃细胞的破坏程度加剧,胞内多糖能更多的扩散至提取液中。
2.1.3 酶用量对马勃多糖得率的影响 称取马勃粉5.0 g,共5份,每份中加入pH值为5.5缓冲液及分别加入 1.5%、3%、3.5%、4.0%、4.5%、5.0%、5.5%、6.0%酶液(共80 mL),在40℃下水浴提取60 min,结果见图4。
从图4中可看出,随着酶用量的不断增加,多糖得率也逐渐增大,当酶用量为1.5%~4.5%时,多糖得率增大的速度较快;再增加酶用量多糖提取率趋于平缓。蜗牛酶是纤维素酶、甘露糖酶、半乳聚糖酶、蛋白水解酶、氨基酸转移酶等混合酶(袁久刚,2014),可分解真菌细胞壁中的葡聚糖、甘露聚糖和蛋白质等物质。酶量增加,可迅速破坏细胞壁结构,有助于多糖的提取。

图4 酶用量对马勃多糖得率的影响
2.1.4 提取pH值对马勃多糖得率的影响 称取马勃粉5.0 g,共5份,每份中分别加入pH值为4.0、4.5、5.0、5.5、6.0的缓冲液以及1.5%酶液 (共80 mL),在40℃下水浴提取60 min,结果见图5。
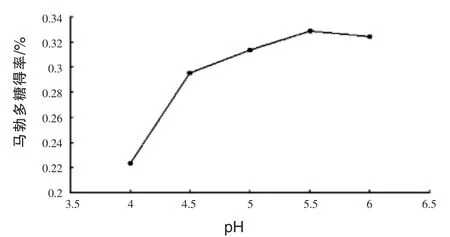
图5 提取pH值对马勃多糖得率的影响
从图5中可看出,缓冲液pH值为5.5时,多糖得率较高,pH过高或过低,多糖得率都会下降,可能与蜗牛酶生物活性受到一定程度的影响有关。此外,pH过低会破坏多糖分子中的糖苷键(宋晓凯,2010),将多糖分子裂解为小分子寡糖甚至单糖,进一步降低多糖的得率。
2.2 正交试验优化马勃多糖的提取工艺 根据单因素试验结果选定因素水平,以提取温度(A)、时间(B)、酶用量(C)以及提取pH(D)作为研究对象,采用L9(34)表,设计正交提取试验,通过对正交试验结果进行分析,优化最佳提取工艺。
2.2.1 因素与水平 根据单因素试验的结果,设计正交试验,四因素与水平见表1。

表1 正交试验因素与水平
2.2.2 试验结果的分析与讨论 正交试验结果与分析见表2。

表2 正交试验设计及结果
由表2中各因素极差可知,四个因素对于试验结果的影响强弱依次为:D>B>A>C(pH>时间>温度>酶用量);最佳提取工艺条件为:提取温度35℃、提取时间120 min、酶用量5.0%、pH 6.0(A2B3C1D3)。
2.2.3 最佳提取工艺条件的验证 由表3可知,在优化工艺条件下,马勃多糖的平均得率达到0.908%,试验结果进一步说明该提取工艺条件能够达到预期目的。
2.3 最佳工艺不加酶对照试验 按最佳工艺条件,即提取温度35℃、提取时间120 min、pH 6.0,在此条件下,直接进行马勃多糖的提取(蜗牛酶添加量为0),马勃多糖得率为0.352%。

表3 验证试验结果
3 结论
本文研究了蜗牛酶辅助提取马勃多糖的最佳提取工艺。在单因素试验的基础上,应用正交试验优化了蜗牛酶辅助提取马勃多糖的提取条件,最终确定最佳的提取工艺条件为:提取温度35℃、提取时间120 min、酶用量5.0%、pH 6.0,在此条件下马勃多糖的得率为0.908%;最佳工艺不加酶的对照试验中多糖得率仅为0.352%,多糖得率提高了158.01%。试验结果表明,蜗牛酶破壁能力很强,能够有效地提高马勃真菌类多糖的提取效率,缩短提取时间,并且提取条件温和,能耗低,故此法可为马勃的综合利用提供参考。
[1]崔磊,宋淑亮,孙隆儒.脱皮马勃化学成分研究及抗肿瘤活性的初筛[J].中药材,2006,29(7):703~705.
[2]池源,王丽波.苯酚 ~硫酸法测定南瓜籽多糖含量的条件优化[J].食品与机械,2014,1:89~92.
[3]郭晶.马勃化学成分及药理作用研究进展 [J].现代医药卫生,2013,29(3):386~389.
[4]国家药典委员会.中华人民共和国药典:2015年版.一部[M].北京:中国医药科技出版社,2015:50.
[5]黄凯,李志孝,邓永康,等.药用真菌马勃多糖的分离纯化及结构分析[J].华西药学杂志,2008,23(5):516~518.
[6]姜明华,田易玲,徐凌川.马勃多糖对荷瘤模型小鼠抑瘤作用及生命延长率的影响[J].山东中医药大学学报,2014,2:157~158.
[7]马丽雅.生物酶法制备真菌菌丝体多糖的工艺优化及生物活性研究:[硕士学位论文][D].哈尔滨:哈尔滨工业大学,2010.
[8]莫祺晖,韦星明,李槐,等.三氯乙酸终止液对木瓜蛋白酶酶活测定的影响研究[J].饮料工业,2015,1:23~25.
[9]苏方华,潘日兴.马勃的抗炎镇痛实验研究[J].齐鲁药事,2010,29(10):586~588.
[10]宋晓凯.天然药物化学(第二版)[M].北京:化学工业出版社,2010.47.
[11]王晨英,高锦明,杨雪,等.黄硬皮马勃的化学成分[J].中草药,2002,33(9):778~780.
[12]肖冬光,刘青,李静,等.酿酒酵母单倍体制备方法的优化[J].酿酒科技,2004,4:21~22.
[13]袁久刚,王强,范雪荣,等.一种利用蜗牛酶对棉机织物进行生物前处理的方法[P].中国,发明专利,103669006.2014-03-26.
[14]左文英,尚孟坤,揣辛桂.脱皮马勃的抗炎、止咳作用观察[J].河南大学学报:医学科学版,2004,23(3):65~65.
[15]赵友生,王进平,宋爱荣,等.马勃多糖提取及体外抗肿瘤研究[J].中国现代应用药学,2012,7:574~578.■
To optimize the snailase-assisted extraction process of polysaccharides from puffball,the optimum extraction conditions were established by single-factor experiment and orthogonal analysis with polysaccharides yield as an index.The optimum extraction conditions were as follows,snailase addition was 5.0%,and pH 5.0 for 120 min extraction at 35℃,the average yield of polysaccharides was 0.908%.The yeild of polysaccharides was 158.01%higher than water extraction method.The snailase-assisted extraction method has the advantages of high yield,short extraction time and mild condition.
puffball;polysaccharide;snailase;extraction
S816.11
A
1004-3314(2017)05-0024-03
10.15906/j.cnki.cn11-2975/s.20170505
*通讯作者

