大体积搅拌棒吸附萃取技术与热脱附-气相色谱-质谱法测定地表水中多环芳烃
冯 利, 张胜军, 朱国华, 李沐霏, 刘劲松,*
(1. 浙江工业大学化学工程学院, 浙江 杭州 310014; 2. 浙江省环境监测中心, 浙江 杭州 310015)
技术与应用
大体积搅拌棒吸附萃取技术与热脱附-气相色谱-质谱法测定地表水中多环芳烃
冯 利1, 张胜军2, 朱国华2, 李沐霏2, 刘劲松1,2*
(1. 浙江工业大学化学工程学院, 浙江 杭州 310014; 2. 浙江省环境监测中心, 浙江 杭州 310015)
基于搅拌棒吸附萃取(SBSE)技术建立了气相色谱-质谱测定地表水中16种多环芳烃(PAHs)的分析方法。该法采用多搅拌吸附棒同时富集,依次热脱附冷聚焦后进样的方式有效解决了搅拌棒吸附时间长、富集水样体积小等问题。优化后的结果表明,在0.2~10 ng/L范围内(萘为0.5~10 ng/L范围),16种PAHs的线性关系良好,相关系数(r)均>0.99,方法检出限(MDL)为0.03~0.20 ng/L(萘为0.50 ng/L)。用该方法对钱塘江流域地表水进行测定,共检测出11种PAHs,含量为0.13~1.57 ng/L,不同添加水平下的加标回收率为75.6%~108.9%。该法可应用于地表水样品中该类物质的超痕量检测。
气相色谱-质谱;热脱附;搅拌棒吸附萃取;多环芳烃;地表水
多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是煤等有机物不完全燃烧时产生的半挥发性碳氢化合物,广泛存在于水体、土壤、沉积物等环境介质中,具有较强的环境内分泌干扰作用,会对人体健康产生危害。近年来受到国内外的广泛关注,在我国地表水环境质量标准及环境风险评价中均对该类物质的含量进行了严格限定。
目前,地表水中多环芳烃的前处理方法主要有液液萃取法(LLE)[1]和固相萃取法(SPE)[2,3]等。这些传统的前处理方法操作复杂、萃取时间长、溶剂消耗量大。因此,研究人员开发了更简单便捷、环境友好的样品前处理技术,如液相微萃取(LPME)、分散液液萃取(DLLME)、固相微萃取(SPME)和搅拌棒吸附萃取(stir bar sorptive extraction, SBSE)等技术[4]。
SBSE技术是一种集萃取、净化、富集为一体,用于痕量有机物分离和浓缩的样品前处理技术[5-7]。该技术萃取涂层体积大,是SPME技术最大涂敷量(0.5 μL)的50~250倍,理论吸附容量也远大于SPME技术的吸附容量,具有灵敏度高、检出限低、不使用有机溶剂等优点,适用于较为清洁的环境样品中挥发性及半挥发性有机物的痕量分析[8-10]。目前商品化的搅拌吸附萃取棒有聚二甲基硅氧烷(PDMS)和聚乙烯-乙二醇改良硅烷化(EG Silicon)两种涂层,后者主要用于极性物质的萃取[11]。
应用搅拌棒吸附萃取技术检测水样中PAHs的文献[10,12-16]报道很多。如León等[10]应用SBSE-热脱附(thermal desorption, TD)-GC-MS法对地表水、地下水和自来水中6种五环或六环多环芳烃的检出限、重复性、方法不确定度等进行了验证,结果显示该方法具有良好的重复性和回收率,但吸附萃取时间较长(14 h); Kolahgar等[12]应用SBSE-TD-GC-MS法测定水中的16种PAHs,并对萃取时间、脱附后残留量参数等进行了优化,实验结果表明,方法具有良好的线性和检出限,但3.5 h的萃取时间仍较长;Guart等[16]应用SBSE-GC-MS/MS法对来自全球27个国家的77个代表性瓶装水中的69种有机污染物进行了测定,其中包含了13种PAHs。虽然SBSE技术具有高灵敏度的特点,但现有报道的方法均存在萃取时间长、萃取量小等缺点,限制了其在实际中的应用。
本文采用SBSE技术,并以多个搅拌棒同时萃取吸附的方式,建立了TD-GC-MS检测地表水中16种PAHs的分析方法。该方法灵敏、高效,适用于超痕量PAHs的快速测定。
1 实验部分
1.1 仪器和试剂
Agilent 6890气相色谱-质谱仪(美国Waters公司),配有热脱附模块(thermal desorption unit, TDU)和冷进样系统(cooled injection system, CIS)(德国Gerstel公司);固相萃取搅拌棒(10 mm×0.5 mm, 20 mm×0.5 mm, PDMS吸附涂层,德国Gerstel公司); HJ-6A多头磁力搅拌器(江苏科析仪器公司); Milli-Q超纯水系统(美国Millipore公司)。

1.2 样品前处理
准确量取500 mL水样于1 L锥形瓶中,将2个10 mm×0.5 mm和1个20 mm×0.5 mm PDMS涂层的固相萃取搅拌棒同时吸附于清洗后的磁力搅拌子上,放入水样密封后,置于磁力搅拌器上,以600 r/min常温搅拌60 min。固相萃取搅拌棒使用前,于TDU中以280 ℃老化60 min。
萃取完成后,使用干净的镊子取出搅拌棒,用少许蒸馏水冲洗搅拌棒上的附加物质(如悬浮物、可溶性盐和其他附着物等),按规格分别放入2个热脱附管中,待仪器分析。
1.3 仪器分析
TDU条件:初始温度50 ℃,以200 ℃/min升温至290 ℃,保持5 min;不分流模式。CIS条件:初始温度-20 ℃(冷聚集温度),以12 ℃/s升温至300 ℃,保持1 min;溶剂放空模式。
GC-MS条件:色谱柱为DB-5MS毛细管柱(30 m×0.25 mm, 0.25 μm);载气为氦气;流速为1 mL/min;程序升温条件为初始温度50 ℃,保持1 min,以10 ℃/min升温至260 ℃,再以15 ℃/min升温至310 ℃,保持3 min。离子源为EI源;离子源温度为200 ℃;接口温度为250 ℃;电离能量为70 eV;扫描方式为全扫描;扫描范围为m/z45~550。
2 结果与讨论
2.1 方法原理
用涂覆有PDMS吸附涂层的固相萃取搅拌棒对水中的PAHs进行搅拌吸附,然后通过热脱附装置对搅拌棒上吸附的目标物进行脱附。脱附后的物质经CIS重新冷聚焦富集后,再快速升温进入气相色谱柱进行分离,最后进入质谱检测器分析。
2.2 分析条件的优化
2.2.1 TDU热脱附时间的考察
热脱附时间会影响PAHs的脱附情况,一般来说,固相萃取搅拌棒的吸附涂层越厚,脱附越困难。本实验考察了热脱附时间对脱附量的影响(见图1a)。结果显示,16种PAHs中大部分物质随着热脱附时间的增加,峰面积先增大后减小,但最佳脱附时间不尽相同,这可能是因为过度的热脱附会导致目标物流失。综合考虑图1a中曲线的变化情况,最终将热脱附时间设为5.0 min。

图 1 (a)热脱附时间、(b)冷聚焦温度、(c)冷阱脱附时间和(d)萃取时间对16种PAHs色谱峰峰面积的影响Fig. 1 Effect of (a) thermal desorption time, (b) cryofocusing temperature, (c) cold trap desorption time and (d) extraction time on the chromatographic peak areas of the 16 PAHs Conditions: a. -20 ℃ cryofocusing temperature, 1 min cold trap desorption time, 1 h stir bar sorptive extraction (SBSE) time, 10 ng/L polycyclic aromatic hydrocarbons (PAHs) spiked in 500 mL blank water sample; b. 5 min thermal desorption time, 1 min cold trap desorption time, 10 μg/L standard test solution, direct injection; c. 5 min thermal desorption time, -20 ℃ cryofocusing temperature, 10 μg/L standard test solution, direct injection; d. 5 min thermal desorption time, -20 ℃ cryofocusing temperature, 1 min cold trap desorption time, 10 ng/L PAHs spiked in 500 mL blank water sample. Nap: naphthalene; Acy: acenaphthylene; Ace: acenaphthene; Fle: fluorene; Phe: phenanthrene; An: anthracene; Flu: fluoranthene; Pyr: pyrene; BaA: 1,2-benzanthracene; Chr: chrysene; BbF: benzo[b]fluoranthene; BkF: benzo[k]fluoranthene; BaP: benzo[a]pyrene; Ind: indeno[1,2,3-cd]pyrene; DahA: dibenz[a,h]anthracene; BghiP: benzo[g,h,i]perylene.
2.2.2 CIS冷聚焦温度的考察
本实验分别考察了不同冷聚焦温度(20、0、-20、-40和-80 ℃)对PAHs色谱峰峰面积的影响(见图1b)。结果显示,当冷聚焦温度为-20 ℃时,绝大部分PAHs的峰面积相对较高,因此最终将冷聚焦温度设为-20 ℃。
2.2.3 CIS冷阱脱附时间的考察
本实验考察了不同冷阱脱附时间(1.0、2.0、4.0、6.0和8.0 min)对目标分析物峰面积的影响(见图1c)。结果表明,脱附时间在1.0~8.0 min之间,PAHs的峰面积变化不大。因此,从提高分析效率、节约分析时间的角度考虑,最终将冷阱脱附时间设为1.0 min。
2.2.4 搅拌棒吸附萃取时间的考察
本文考察了分析500 mL水样时,不同的搅拌棒吸附萃取时间(10、30、60、120和150 min)对PAHs色谱峰峰面积的影响(见图1d)。结果显示,随着萃取时间的增加,PAHs的峰面积不断增加。由Kolahgar等[12]的研究结果可知,10 mL的水样用一个PDMS搅拌棒于室温下以500 r/min搅拌,达到吸附平衡需3~4 h。而本实验的样品量为500 mL,则需更长的时间才能达到吸附平衡。为提高分析效率,达到快速测定的目的,在保证灵敏度的情况下,本实验将搅拌棒吸附萃取时间设为60 min。
2.3 大体积搅拌棒吸附萃取问题的解决
搅拌棒的长度只有10 mm和20 mm两种型号,受到接触面积和萃取容量的限制,文献[10-13]中记载的萃取水样的体积一般为10~100 mL。本实验为了提高分析效率,同时获得较高的灵敏度,将水样体积提高至500 mL。但是增大水样的体积,受吸附棒体积过小、在大体积水样中扰动程度不高的影响,会带来吸附效果变差的问题。为解决该矛盾,本方法将固相萃取搅拌棒的数量增加至3个,并添加一个大号的聚四氟乙烯磁搅拌子,将搅拌棒吸附在搅拌子上,并在高转速(600 r/min)下进行搅拌,水样的扰动速度明显加快,样品中污染物的迁移速率和搅拌棒的吸附速率也相应地加快。在保证吸附效果的同时缩短样品富集时间、提高分析效率,获得较高的灵敏度。
样品萃取完成后,需要将搅拌棒转移至热脱附设备中进行高温热脱附,并进入CIS冷阱中进行冷聚焦富集。由于热脱附管体积较小,每次只能脱附1~2个10 mm或1个20 mm的搅拌棒。本方法使用热脱附装置将两个热脱附管中的被吸附物质先后脱附下来,由CIS冷阱进行冷聚焦合并后,经热脱附进入气相色谱分离,如此可以有效解决多个搅拌棒无法在一根热脱附管中同时脱附的问题。而且理论上可以使用多根搅拌棒同时进行吸附,再将搅拌棒顺次经热脱附进入同一个冷阱中进行冷聚焦合并,扩大了搅拌棒的吸附容量。
2.4 方法学验证
2.4.1 线性关系
分别量取10、25、50、250、500 μL 10 μg/L的PAHs标准工作液,配制500 mL质量浓度为0.2、0.5、1、5、10 ng/L的加标空白水样,并按优化后的实验条件和方法进行测定。在0.2~10 ng/L的线性范围内,以色谱峰面积为纵坐标(y)、对应的质量浓度为横坐标(x, ng/L),绘制标准曲线,得到线性方程和相关系数(r)(见表1)。结果表明,各目标物的线性关系良好,除萘以外的r均>0.994。萘在0.5 ng/L以下时,标准曲线出现弯曲,水样中0.2 ng/L的萘的峰面积与水样中0.5 ng/L的萘的峰面积接近。利用超纯水代替地表水进行空白试验,发现500 mL空白水样中存在一定含量的萘,且含量较为稳定。虽然使用了超纯水制备工艺及其他净化手段,但依然很难完全消除萘的干扰,这可能和萘在环境中大量存在及挥发性高有关。但萘在0.5~10 ng/L范围内线性关系良好,r为0.999 0。
2.4.2 方法检出限与精密度
对含有16种PAHs(1.0 ng/L)的500 mL空白加标水样按优化后的方法连续测定5次,计算16种PAHs的含量,其含量的相对标准偏差为4.69%~17.92%(见表1)。以3倍标准偏差确定方法检出限(MDL),为0.03~0.20 ng/L(n=7),其中萘以线性较好的0.50 ng/L为方法检出限。本实验获得的方法检出限明显优于Guart等[16]测得的MDL(13种PAHs,5~11 ng/L)和Kolahgar等[12]测得的MDL(0.1~2.0 ng/L),且检测时间更短、操作更简单;完全满足GB 3838-2002地表水环境质量标准(苯并芘限值2.8 ng/L)、GB 5749-2006生活饮用水卫生标准(多环芳烃总含量限值2 000 ng/L)以及美国环保局(16种PAHs总含量,0.2 μg/L)[4,17]等规范要求。
2.4.3 加标回收率
采集钱塘江流域的地表水样品,按优化后的方法进行实际样品测定和不同添加水平的回收率试验,结果见表2。由此可知,地表水样中三环或四环PAHs多有检出,大环PAHs除苯并[a]芘外,其余均未检出,平均检出含量为0.13~1.57 ng/L,RSD为3.5%~19.0%(n=3)。在该水样中分别加入0.2 ng/L和1.0 ng/L的16种PAHs标准工作液进行加标回收率试验,其加标回收率分别为79.6%~108.9%和75.6%~95.4%,RSD为2.4%~10.3%和0.2%~9.4%(n=3)。此外,考虑到废水中基质复杂、干扰物多,竞争性吸附可能导致超痕量的PAHs无法有效吸附。因此,该方法目前仅适用于地表水等洁净水样的分析。

表 1 16种PAHs的线性方程、相关系数(r)、相对标准偏差(RSD)及方法检出限(MDL)
Ref.: reference;y: peak area;x: mass concentration, ng/L; * naphthalene with a good linearity of 0.5 ng/L as its MDL; /: not included.
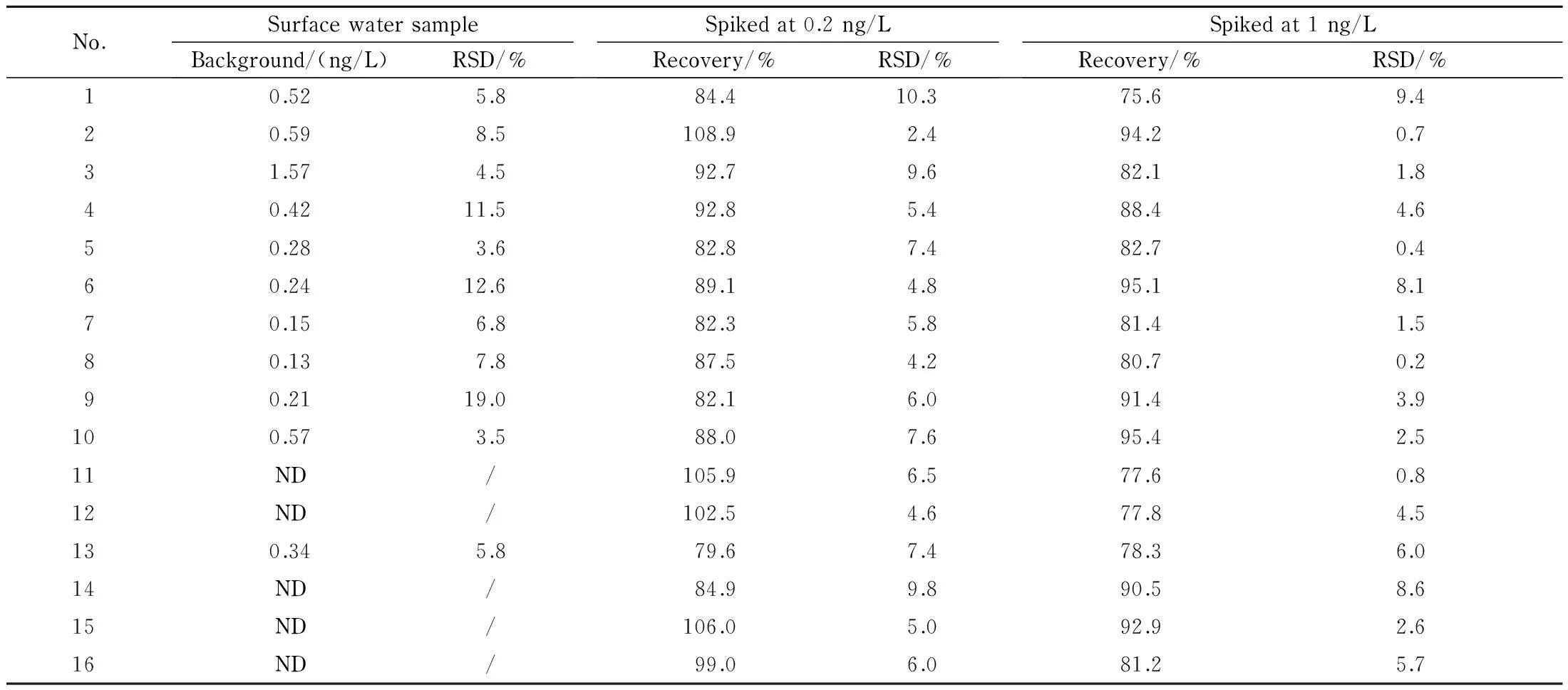
表 2 16种PAHs在地表水样中的含量及加标回收率(n=3)
Nos. 1-16 are the same as in Table 1; ND: less than MDL; /: no data.
3 结论
本文应用SBSE技术,建立了TD-GC-MS检测地表水中16种PAHs的分析方法,并对热脱附时间、冷聚焦温度、CIS冷阱热脱附时间、萃取时间等条件进行了优化。本文采用多个搅拌棒同时富集、依次热脱附冷聚焦后合并的方式有效解决了搅拌棒吸附时间长、富集水样体积小等问题。应用此方法可对地表水中的PAHs进行快速简便的测定。
[1] An H J, Zheng C J, Liu Q H, et al. Modern Scientific Instruments, 2007(3): 92
安华娟, 郑存江, 刘清辉, 等. 现代科学仪器, 2007(3): 92
[2] Chen J, Dai Z Y, Xu Q, et al. Chinese Journal of Analytical Chemistry, 2014, 42(12): 1785
陈静, 戴振宇, 许群, 等. 分析化学, 2014, 42(12): 1785
[3] Mollahosseini A, Rokue M, Mojtahedi M M, et al. Microchem J, 2016, 126: 431
[4] Li Y, Liu Y, Sun X W, et al. Environmental Chemistry, 2015, 34(8): 1460
李荫, 柳叶, 孙晓伟, 等. 环境化学, 2015, 34(8): 1460
[5] Baltussen E, Sandra P, David F, et al. J Microcolumn Sep, 1999, 11(10): 737
[6] Chen L L, Huang X J, Yuan D X. Chinese Journal of Chromatography, 2011, 29(5): 375
陈林利, 黄晓佳, 袁东星. 色谱, 2011, 29(5): 375
[7] Nogueira J M F. TrAC-Trends Anal Chem, 2015, 71: 214
[8] Lin F H, Qiu N N, Huang X J, et al. Chinese Journal of Analytical Chemistry, 2010, 38(1): 67
林福华, 邱宁宁, 黄晓佳, 等. 分析化学, 2010, 38(1): 67
[9] Li X M, Zhang Q H, Wang P, et al. Chinese Journal of Analytical Chemistry, 2011, 39(11): 1641
李晓敏, 张庆华, 王璞, 等. 分析化学, 2011, 39(11): 1641
[10] León V M, Alvarez B, Cobollo M A, et al. J Chromatogr A, 2003, 999(1/2): 91
[11] Cacho J I, Campillo N, Vinas P, et al. J Pharmaceut Biomed, 2013, 78/79: 255
[12] Kolahgar B, Hoffmann A, Heiden A C. J Chromatogr A, 2002, 963(1/2): 225
[13] Yang L, Wang B X, Hou Y, et al. Chinese Journal of Chromatography, 2007, 25(5): 747
杨蕾, 王保兴, 侯英, 等. 色谱, 2007, 25(5): 747
[14] Xu Y, Liu W M, Zhao J H, et al. Chinese Journal of Analytical Chemistry, 2005, 33(10): 1401
徐媛, 刘文民, 赵景红, 等. 分析化学, 2005, 33(10): 1401
[15] Ochiai N, Sasamoto K, Kanda H, et al. J Chromatogr A, 2008, 1200(1): 72
[16] Guart A, Calabuig I, Lacorte S, et al. Environ Sci Pollut R, 2014, 21(4): 2846
[17] Qin Y R, Yu C T, Liang L N. Environmental Chemistry, 2016, 35(3): 601
秦玉荣, 余翀天, 梁立娜. 环境化学, 2016, 35(3): 601
Determination of polycyclic aromatic hydrocarbons in surface water using large volume stir bar sorptive extraction coupled with thermal desorption-gas chromatography-mass spectrometry
FENG Li1, ZHANG Shengjun2, ZHU Guohua2, LI Mufei2, LIU Jinsong1,2*
(1.CollegeofChemicalEngineering,ZhejiangUniversityofTechnology,Hangzhou310014,China;2.ZhejiangEnvironmentalMonitoringCenter,Hangzhou310015,China)
A fast and sensitive analytical method for the ultra trace determination of 16 kinds of polycyclic aromatic hydrocarbons (PAHs) in surface water based on stir bar sorptive extraction (SBSE) coupled with gas chromatography-mass spectrometry was established. Multiple stir bars simultaneous enrichment with sequential cryofocusing and merged injection technique was used to effectively solve the problem of long adsorption time and small sample volume with SBSE. The conditions of thermal desorption time, cryofocusing temperature of cooled injection system (CIS), CIS desorption time and extraction time were investigated. Under the optimized conditions, the results showed that the linear range was between 0.2 ng/L and 10 ng/L (naphthalene, 0.5-10 ng/L), and the method detection limits (MDLs) of the 16 PAHs ranged from 0.03 ng/L to 0.20 ng/L (naphthalene, 0.50 ng/L). The 11 PAHs were determined in the Qiantang River surface water samples, and the contents were between 0.13 ng/L and 1.57 ng/L. The recoveries of the 16 PAHs spiked in surface water samples at different levels were between 75.6% and 108.9%. The method can be efficiently applied to the determination of PAHs.
gas chromatography-mass spectrometry (GC-MS); thermal desorption (TD); stir bar sorptive extraction (SBSE); polycyclic aromatic hydrocarbons (PAHs); surface water
10.3724/SP.J.1123.2016.11013
2016-11-14
浙江省重大科技专项(2014C03026);浙江省环保科技项目(2014A011).
Foundation item: Zhejiang Major Program of Science and Technology (No. 2014C03026); Zhejiang Environmental Protection Program of Science and Technology (No. 2014A011).
O658
A
1000-8713(2017)04-0466-06
* 通讯联系人.E-mail:liu70923@163.com.

