奥氮平自制片处方工艺与溶出度研究
徐小明,张中华,袁 慧,史 琼,潘 凤,程铁
1. 河南大学 药学院,河南 开封 475000;2. 河南大学 校医院,河南 开封 475000
奥氮平自制片处方工艺与溶出度研究
1. 河南大学 药学院,河南 开封 475000;2. 河南大学 校医院,河南 开封 475000
〔目的〕研究奥氮平片剂的处方工艺,比较自制片剂与原研药片剂的溶出度,为奥氮平临床应用提供依据。〔方法〕采用紫外分光光度法,根据辅料相容性结果,将辅料的用量作为考察因素,分别考察稀释剂、崩解剂、黏合剂及包衣对奥氮平片溶出度的影响,计算累积溶出百分率,筛选出奥氮平片处方中辅料的最佳配比。〔结果〕以质量分数为51%的乳糖为稀释剂、质量分数为40%的微晶纤维素为干黏合剂、质量分数为6%的聚乙烯吡咯烷酮水溶液为黏合剂、质量分数为5%的低取代羟丙基纤维素为崩解剂、质量分数为0.5%的硬脂酸镁为润滑剂,以欧伦包衣预混液为包衣材料,自制的奥氮平片溶出度符合《中国药典》(2015版)的规定,其溶出曲线与原研药片剂基本相同。〔结论〕自制的奥氮平片外观优良、硬度适中,溶出性能与原研药相似,且工艺简单,达到了设计要求。
奥氮平;片剂;溶出度;紫外分光光度法;处方工艺
奥氮平(Olanzapine),商品名为再普乐[1],化学名为2-甲基-4-(4-甲基-1-哌嗪基 ) -10H-噻吩并[2,3-b ] [1,5]苯并二嗪,是美国Lilly公司研制开发的非经典抗精神病药[2]。奥氮平为 5-羟色胺 / 多巴胺( 5-HT /DA) 拮抗剂,对大脑边缘和中脑皮质有选择性作用,可快速缓解精神急性症状,对其阴性症状及阳性症状均有显著性疗效,并可改善患者的社会功能和认知功能,能有效治疗器质性精神障碍、酒精所致精神障碍及精神分裂症[3]。
奥氮平于1996年获准在美国上市。目前我国仅有三家药厂生产奥氮平,不能满足临床研究需要,对奥氮平溶出度的相关研究也较少。本研究通过处方筛选,对研制的奥氮平片进行溶出度实验研究,制备与原研药溶出性能相似、质量优良的奥氮平片剂。
1 仪器与试药
1.1 仪器
TU-1801紫外可见分光光度计(北京通用设备仪器厂),ZRC-8D智能溶出试验仪(天津创兴电子设备制定有限公司),Mettler AE100电子分析天平(上海梅特勒公司),ZYD-8型压片机(上海远东制药机械厂),DHG-9140A电热恒温鼓风干燥箱(上海一恒科技有限公司),以及超声波清洗器等。
1.2 试药
奥氮平片(自制片,规格:5 mg/片),奥氮平片(美国Lilly del Caribe 公司,规格:5 mg/片),奥氮平对照品(中国食品药品检定研究院,编号:100948),乳糖,微晶纤维素,低取代羟丙基纤维素(L-HPC),聚乙烯吡咯烷酮(PVPK30),硬脂酸镁等辅料(购自湖州展望药业有限公司),双蒸水。
2 奥氮平片剂的处方工艺
2.1 处方研究
将自制奥氮平片与原研药片剂的溶出度作为主要考察指标,对组成奥氮平片的稀释剂、崩解剂、黏合剂用量筛选比较,优选出较为理想的处方。
初步筛选出以下处方配比,见表1。

表1 处方配比(质量分数/%)
2.2 处方制备
按以上3种处方配比分别称取原料、辅料,过60目筛。将主药、稀释剂及崩解剂按等量递加稀释法混合均匀,加黏合剂制软材,用40目筛制湿颗粒;将湿颗粒置干燥箱内,60℃干燥至含水量约为2%;过40目筛,用欧伦包衣预混液进行包衣,使增重在2%左右;干燥后,做溶出度的考察。
3 奥氮平片剂的质量检查
3.1 标准储备液的制备
精密称取奥氮平对照品2.5 mg,置25.0 mL容量瓶中,用0.1 mol/L的盐酸溶液溶解并稀释至刻度,摇匀,过滤;收集滤液,即得奥氮平标准储备液。
3.2 对照品、供试品及空白辅料溶液的制备
精密吸取标准储备液1.0 mL,置10.0 mL容量瓶中,加入0.1 mol/L的盐酸溶液振摇并稀释至刻度,摇匀,过滤;收集滤液,即得奥氮平对照品溶液。
取奥氮平自制片10片,精密称定,研细;精密称取细粉适量(相当于奥氮平5 mg),置10 mL容量瓶中,加入0.1 mol/L的盐酸溶液,超声5 min使溶解并稀释至刻度,过滤;精确量取续滤液1 mL,置50 mL容量瓶中,加入0.1 mol/L的盐酸溶液振摇并稀释至刻度,摇匀,即得奥氮平供试品溶液。
称取空白辅料适量,同法配制成空白辅料溶液。
3.3 波长的选择
对制备的3种溶液进行紫外全波长扫描,结果见图1。在259.0 nm处主药有最大吸收,并且在259.0 nm处辅料对主药没有紫外干扰。所以,用紫外波长测定含量数据可靠、准确。
3.4 标准曲线的绘制
精密吸取奥氮平标准储备液,用0.1 mol/L盐酸溶液稀释成2.0、3.0、4.0、5.0、6.0、7.0、8.0 μg/mL的奥氮平标准系列溶液。摇匀,用紫外分光光度法在259.0 nm波长处进行测定。以吸光度A为纵坐标、浓度C为横坐标绘制标准曲线,进行回归分析,得:
表明与吸光度呈良好的线性关系。
3.5 自制片与原研药溶出度比较
按《中国药典》(2015 版)[4]采用浆法测定:取自制片和原研药奥氮平片剂各6片,取0.1mol/L的盐酸溶液900mL作为溶出介质;在转速为50r/min、温度为(37±0.5) ℃条件下,分别在5、10、15、30、45、60min时吸取溶出液各10mL(同时补充同温度、同体积的溶出介质),用0.45μm微孔滤膜过滤,测定其含量。计算其平均累积溶出百分率,结果见图2。
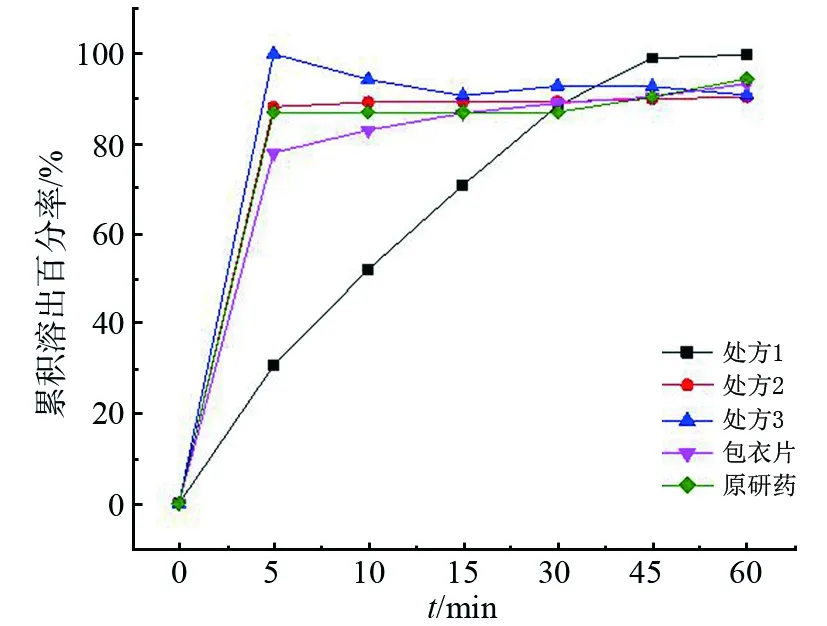
图2 片剂的累计溶出曲线
对比4种片剂的溶出曲线,处方1与其他3种处方差异较大,处方2溶出曲线与原研药提供的接近一致,所以确定处方2为最优处方。
3.6 自制片含量均匀度检测
取自制奥氮平片,研碎,置容量瓶中,用溶出介质溶解,检测含量。经检测,供试品的含量均匀度符合规定。
4 讨论
紫外扫描结果显示,奥氮平仅在259.0nm处有一单一的最大吸收峰,远离短波长末端,峰形较平坦。在259.0nm处标准品和供试品图形一致,且辅料几乎没有吸收,故选用259.0nm作为测定波长进行溶出度测定。奥氮平不溶于水,而在酸性溶液中溶解较好,故选用0.1mol/L的盐酸溶液作为溶出介质。
3种处方相比,处方1中乳糖比重较大,处方3中微晶纤维素的含量较大。累计溶出曲线显示,与原研药相比,处方1在15min内的溶出较慢,处方3在15min内的溶出效果较快,处方2与原研药在溶出度方面相近。所以,在本实验中乳糖和微晶纤维素的用量是关键因素,采用处方2制备的奥氮平片,符合《中国药典》(2015版)的规定,溶出曲线与原研药基本相同。本研究采用紫外分光光度法直接测定奥氮平片的含量,方法简便,准确度较高,稳定性良好。自制的奥氮平片外观优良,硬度适中,溶出性能与原研药相似,工艺简单,达到了设计要求。
[1] 崔道平.奥氮平制备工艺及质量控制研究[D].大连:大连理工大学,2011.
[2] 杨莲华,潘耀,张友婷.紫外分光光度法测定奥氮平片的溶出度[J].光谱实验室,2013,30(6):302-305.
[3] 康明秀.奥氮平的精神科临床应用及其不良反应[J].精神医学杂志,2010,23(3):235-237.
[4] 国家药典委员会编.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2015.
[责任编辑 李麦产]
Study of the Formulation and Dissolution of Self Made Olanzapine Tablets
1. Pharmaceutical College of Henan University, Kaifeng 475000, China; 2. Hospital of Henan University, Kaifeng 475000, China
〔Objective〕To study the formulation and preparation process of olanzapine tablets and compare the dissolution curves of self-made and market available olanzapine tablets. 〔Methods〕According to the results of material compatibility. The effects of diluents, disintegrants, bonding agents and coating processed on the dissolution profile in vitro of the olanzapine tablets were studied by UV spectrophotometry. 〔Results〕Based on the study above, the optimal formulation was determined: 51% lactose, 40% cellulose microcrystalline, 5% hydroxypropyl methyl cellulose. The dissolution profile of the olanzapine tablet prepared was basically similar to those market available.〔Conclusion〕The formulation and dissolution of olanzapine tablets approached to the demands of design.
olanzapine; tablets; formulation; dissolution; UV spectrophotometry
1672-7606(2017)01-0035-03
2016-11-17
河南省高等学校重点科研项目(15A360012)
徐小明(1989-),女,河南漯河人,硕士研究生,从事药物制剂专业研究工作。
程铁峰(1972-),男,河南兰考人,硕士生导师,副教授,从事药物分析测试研究工作。
TQ460.6
A

