用“化学实验研究模型”考查化学实验问题
■浙江省杭州市基础教育研究室 陈进前(特级教师)
用“化学实验研究模型”考查化学实验问题
■浙江省杭州市基础教育研究室 陈进前(特级教师)
化学实验问题大多是综合性问题,解答化学实验题必须抓住这一特征。北京师范大学王磊教授提出如图1所示的一种化学实验研究模型,其中指出化学实验内容包括问题要素、方法和技能要素、知识要素、本体要素、态度要素5个维度的内容,在高中化学中依照该模型来梳理化学实验内容、考查化学实验问题,有助于全面深入理解化学实验内容,是解决化学实验问题的有效途径。

图1
一、梳理知识要素、本体要素、方法技能要素,夯实化学实验基础
本体要素指实验仪器、实验步骤、实验条件和实验用品等;知识要素是指跟某一化学实验相关的物质性质和反应原理等;方法技能要素是相关的实验方法和操作技能等。解决化学实验问题,首先要从这三个方面进行梳理,这是理解实验原理、选取实验仪器、设计实验方案、确定实验条件、解释实验现象、处理实验数据的必备基础。
(杭州市高三抽测试题)高氯酸铵是一种无色晶体,可用作火箭推进剂、高氯酸铵炸药的配合剂,也可用于制造烟火、人工防冰雹的药剂,还可作为分析试剂等。高氯酸铵的部分性质如下:①密度为1.9 5g·c m-3,溶于水、丙酮,微溶于醇;②属于强氧化剂,受热或猛烈撞击能引起爆炸,与有机物或可燃物研磨也会发生爆炸。
有同学在资料上查到如下两种制取高氯酸铵晶体的方案:
方案A:
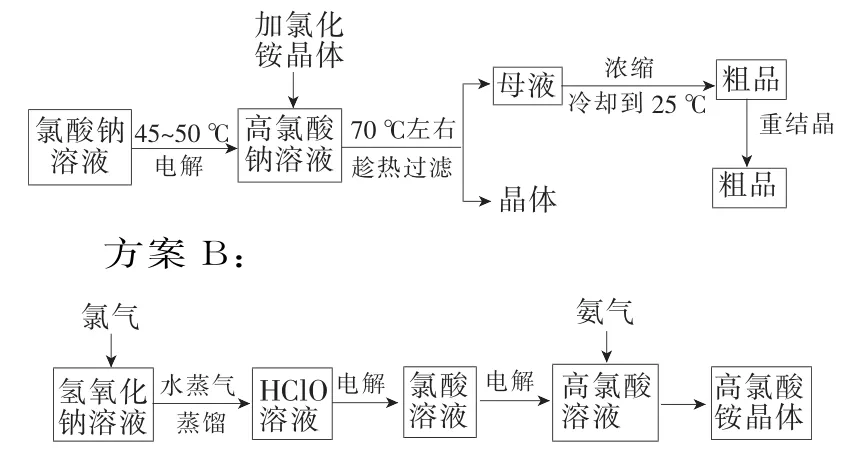
请回答下列问题:
(1)方案B中氯气通入氢氧化钠溶液时发生反应的总化学方程式为____。
(2)方案A、B中共有三处用到电解,这三处电解时阴极的电极反应式为____。
(3)方案A的第一步“趁热过滤”得到的晶体主要成分是____,这一步骤中控制结晶时温度很重要,你认为若高氯酸钠溶液加入氯化铵晶体不采用趁热过滤会造成的后果是____。
(4)两种制取高氯酸铵的方案相比较,方案B的主要优点是____。
解析:正确解答此题的前提是对氯元素及其化合物的性质、电解、化学平衡等知识有深入的理解。
第(1)问中有“陷阱”,有同学会写成C l2+ 2 N a OH══N a C l O+N a C l+H2O,这样就中圈套了。请特别注意观察方案B所给出的信息,氯气通入氢氧化钠溶液中后经水蒸气蒸馏得到HC l O,即产物不是N a C l O,由此研究就会想到总反应式是C l2(过量)+N a OH══HC l O+N a C l。
第(2)问中考查了电解原理,两种方案有三处涉及电解,分别是电解氯酸钠溶液、电解次氯酸溶液、电解氯酸溶液,要注意这三个电解过程中阳极电极反应不相同,但阴极的电极反应完全相同:
2 OH-。
第(3)问中,当用氯化铵、高氯酸钠溶液混合制取高氯酸铵时,须分离除去氯化钠,趁热过滤的目的就是除去氯化钠。由于温度较高时高氯酸铵的溶解度大,不易结晶出来(若此时高氯酸铵也结晶出来就会被当作氯化钠晶体过滤掉),所以“趁热过滤”与“常温下过滤”相比较,前者可以减少高氯酸铵的损耗量。
对于第(4)问,方案A中所得产物的纯度依赖于分离的效果,方案B所得高氯酸铵晶体的纯度要高。所以方案B的优点是:既减少了复杂的分离提纯操作,又提高了产品纯度。
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
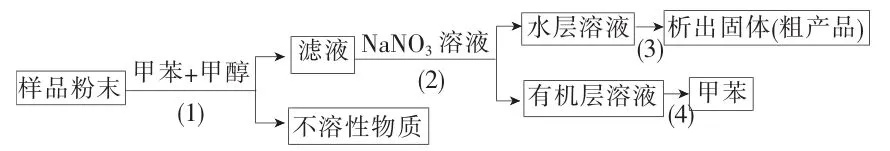
下列说法错误的是( )。
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚
D.步骤(4)需要蒸馏装置
解析:快而准地获得答案的基础是要熟悉过滤、萃取、分液、蒸发浓缩、蒸馏等化学实验基本操作方法。将题给操作流程与各种物质分离操作方法的特点联系起来可判断,操作(1)是过滤(从“滤液”判断出),操作(2)是萃取(从“水层”和“有机层”判断出),必定要用到分液漏斗。步骤(3)是从水溶液中分离出固体粗产品,应该浓缩结晶,一般是用蒸发皿,不会用到坩埚。步骤(4)是从有机层中分离出甲苯,应该用蒸馏方法。答案为C。
二、梳理态度要素和问题要素,提升科学探究能力,强化化学观念
通过化学实验试题考查科学探究能力、测试化学基本观念是一种命题方向,在化学实验学习中要通过梳理态度要素和问题要素来提升科学探究能力,强化化学观念。试剂选择、尾气处理、操作流程、方案选择等,都会涉及绿色化学观念。化学实验的目的就是解决一定的问题,突出并明确化学实验的问题性,实验探究性是围绕着问题展开的,所以要在化学实验中培养科学态度和提高问题意识。
(杭州市高三抽测试题)聚合硫酸铁(P F S)是一种新型高效的无机高分子絮凝剂,现用铁的氧化物为原料来制取聚合硫酸铁的过程如下。
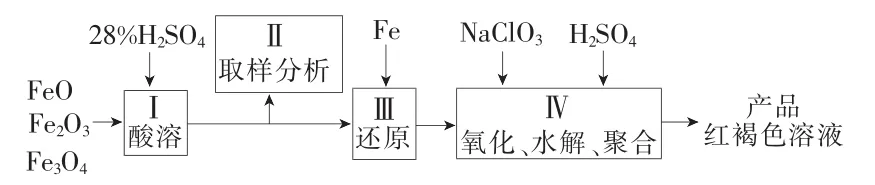
聚合硫酸铁溶液中S O24-与F e3+物质的量之比____3∶2(填“大于”“等于”或“小于”)。设计一个实验方案测定聚合硫酸铁中S O24-与F e3+物质的量之比(写出试剂、操作方法)。
解析:审题时要善于提出问题,如“上述生产流程中涉及哪些化学反应”“产品P F S属于哪类物质,其中除含有S O24-和F e3+外还可能含有哪些离子”“定量测定S O24-、F e3+可选用哪些方法?定量测定P F S中S O24-、F e3+应排除哪些干扰因素”。提出并思考上述问题后,可发现“聚合硫酸铁实际就是碱式硫酸铁,其中n(S O24-)∶n(F e3+)<3∶2。若要测定其比值,必须定量测定S O24-、F e3+的量。
(杭州市高三抽测试题)高锰酸钾是常用的氧化剂。工业上以软锰矿(主要成分是M n O2)为原料制备高锰酸钾晶体。实验室制备高锰酸钾晶体的操作流程如下。
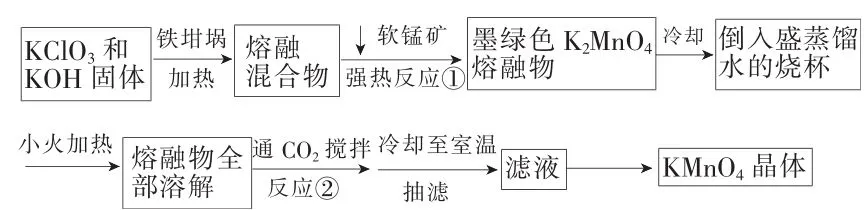
上述反应②的化学方程式:3 K2M n O4+ 2 C O2══2 KM n O4+M n O2+2 K2C O3。
已知:
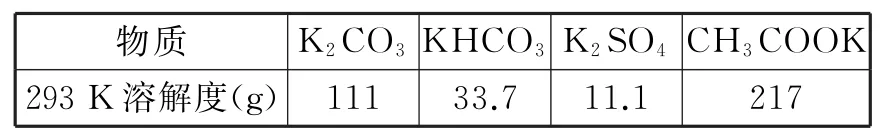
_____物质__________ K2C O3KHC O_ ______ __________3K2SO4CH3C_OOK 2 9 3K溶解度(g) 1 1 1_ ____3 3.7 ___1 1.1_ ________217
(1)加热软锰矿、K C l O3和KOH固体时所采用的操作方法是____,不采用瓷坩埚而选用铁坩埚的理由是____;反应①的化学方程式为____。
(2)从滤液中得到KM n O4晶体的实验操作依次是____(选填字母代号,下同)。
a.蒸馏 b.蒸发 c.灼烧
d.抽滤 e.冷却结晶
(3)制备过程中需要用到纯净的C O2气体。制取纯净C O2最好选择下列试剂中的____。
a.石灰石 b.浓盐酸
c.稀硫酸 d.纯碱
(4)实验时,若C O2过量会生成K H C O3,导致得到的KM n O4产品的纯度降低。原因是____。
(5)由于C O2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通入C O2改为加其他的酸。从理论上分析,选用下列酸中的____,得到的产品纯度更高。
a.醋酸 b.浓盐酸 c.稀硫酸
解析:第(1)和(4)问中要求解题者直接对相关实验操作作出评价,第(2)(3)(5)三个问题看起来是选择题,但其实质还是评价问题,因为必须要对相关实验操作和原理作出评价后才能选出正确选项。
从题给实验流程可知,第一步、第二步操作的目的是将氯酸钾、氢氧化钾和二氧化锰三种固体混合加强热制取锰酸钾,应该选用的操作方法是“灼烧”。由于氢氧化钾具有强碱性,高温下会腐蚀瓷坩埚,应该选用铁坩埚。反应的化学方程式为3 M n O2+K C l O3
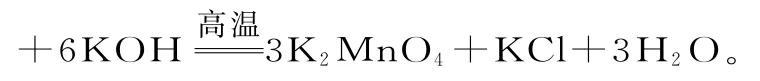
流程中后续操作的目的是:将K2M n O4、K C l等混合物溶解,通入C O2调节p H,使K2M n O4在适宜条件下发生歧化反应转化为KM n O4(根据题给反应式可知同时生成了M n O2、K2C O3),直接抽滤可除去其中的M n O2,所得滤液中有KM n O4、K2C O3等,经过结晶分离得到KM n O4晶体。由于K2C O3在常温下溶解度较大,所以滤液要经过蒸发(提高KM n O4的浓度)、冷却结晶(使KM n O4结晶出来)、抽滤等操作,即第(2)问应选b、e、d。
考虑到用碳酸钙、盐酸制取C O2气体会混入少量HC l,所以最好选用碳酸钠和硫酸,即第(3)问应选c、d。从题给信息可知, KHC O3的溶解度比K2C O3的小很多,滤液蒸发浓缩时KHC O3会随KM n O4一起结晶析出。因为盐酸有还原性,醋酸钾的溶解度比硫酸钾的大很多,蒸发浓缩时基本上都会留在母液里,所以第(5)问选a。
(责任编辑 谢启刚)

