原发灶激素受体阴性腋淋巴结转移灶激素受体阳性乳腺癌患者的内分泌治疗
郑向欣,吴骥,顾书成,江小玲,侍孝红,袁牧,陆柏林,邱兴,张旭旭,柏建印,管小青
(南京鼓楼医院集团宿迁市人民医院 1. 乳腺外科 2. 病理科,江苏 宿迁 223800)
乳腺癌是女性常见的恶性肿瘤,严重影响患者的身心健康及生活质量[1-2]。国内外指南指出乳腺癌的治疗方案主要有手术、放化疗、内分泌治疗及分子靶向治疗等,通过有效的治疗可以提高患者的生存时间及生活质量[3-5]。近年来随着乳腺癌分子分型的广泛应用,乳腺癌的治疗更趋于规范化、个体化,使得患者获益更大[6-10]。对于初发的乳腺癌的治疗主要依据患者原发灶的免疫组化结果,对于出现局部复发、转移的患者,同时需要检测复发转移病灶的免疫组化结果,综合考虑患者的病理特征制定优化的个体化方案。临床上发现部分初发的乳腺癌患者原发灶与同期腋窝淋巴结转移灶免疫组化结果存在不一致,对于这类患者的治疗同样需要综合考虑原发灶与腋淋巴结转移灶的分子分型[11-14]。笔者对原发灶激素受体(HR)阴性,同期淋巴结转移灶HR阳性的患者给予内分泌治疗,观察患者的1、3、5年生存率及复发转移情况,结果令人满意,现报告如下。
1 资料与方法
1.1 一般资料
本组选取2011年1月—2016年1月我院收治的67例原发灶HR(-),腋淋巴结转移灶HR(+)乳腺癌患者,67例患者术前穿刺均为乳腺癌,年龄25~71岁,平均48.4岁。术前未行新辅助化疗、放疗,术后病理证实为乳腺癌,其中浸润性导管癌46例,浸润性小叶癌16例,髓样癌3,黏液腺癌2例。免疫组化结果提示原发灶HR(-),腋淋巴结转移灶HR(+)。肿瘤分期II期55例,III期12例,均伴有同侧腋窝淋巴结转移。手术方式保乳根治术10例,乳腺癌改良根治术52例,乳腺癌根治术5例,术后切除标本均行免疫组化检测。
1.2 分组与治疗
随机分为观察组(33例)和对照组(34例),两组患者术后均行静脉化疗,方案为AC×4序贯T×4(环磷酰胺500 mg/m2,吡柔比星50 mg/m2,多西他赛75 mg/m2或紫杉醇135 mg/m2),21 d为1周期,共8个周期(原发灶分子分型为HER-2过表达型者在蒽环类药物治疗后加用赫赛汀,治疗共1年 );化疗结束后予以放疗,共50 Gy(5周,25次)剂量。观察组33例患者化疗结束后,绝经前患者口服三苯氧胺,10 mg,2次/d,绝经后患者口服来曲唑,2.5 mg/d,1次/d,定期复查子宫附件彩超、血糖血脂及骨密度等,随访中部分患者关节痛,血脂升高,月经失调及肝功能异常等,但均未出现药物引发的子宫内膜癌等严重并发症。对照组34例患者放化疗后定期来院复查。所有患者随访12~60个月,化疗结束后2年内建议每3个月复查1次,3~5年内建议每6个月复查1次,通过复查乳腺肿瘤指标、胸部CT、腹部彩超,骨扫描(建议1年复查1次)等 ,观察患者生存时间及复发转移情况。
1.3 统计学处理
数据统计采用SPSS 13.0统计学软件,计量资料比较采t检验,计数资料比较采用χ2检验,两组患者的生存率采用Log-rank法比较,P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者一般情况及随访情况的比较
两组患者年龄、月经情况、病理类型、手术方式及术后放化疗等基本相同,差异无统计学意义(均P>0.05)(表1)。所有患者均接受随访,随访时间12~60个月,中位随访时间43.5个月,其中观察组局部复发3例,骨转移3例,肺转移2例,肝转移3例,锁骨上淋巴结转移2例,因复发转移死亡者7例;对照组局部复发4例,骨转移4例,肺转移4例,肝转移5例,锁骨上淋巴结转移2例,因复发转移死亡者15例,两组复发、转移例数间比较(13/33vs. 19/34),差异无统计学意义(P>0.05),两组复发、转移、死亡例数间比较(7/33vs. 15/34),差异有统计学意义(P<0.05)。
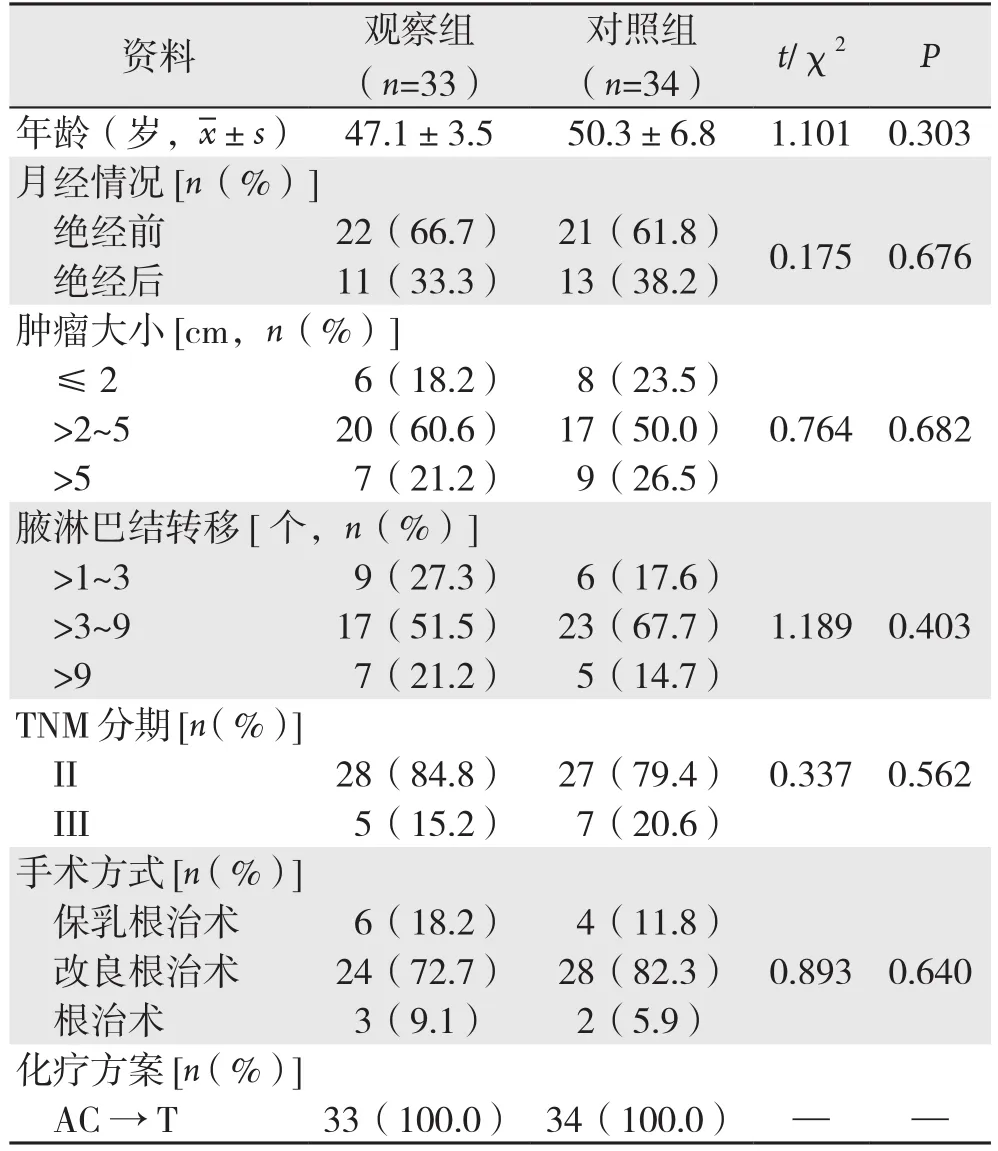
表1 两组患者一般资料比较Table 1 Comparison of the general data between the two groups of patients
2.2 两组患者生存率的比较
观察组患者1、3、5年无病生存率(DFS)分别为100%、81.8%、72.7%;1、3、5年总生存率(OS)分别为100%、90.9%、81.8%。对照组患者1、3、5年DFS分别为100%、58.8%、47.1%;1、3、5年OS分别为100%、70.6%、58.8%,观察组1年DFS及OS与对照组比较,差异无统计学意义(P>0.05),观察组3、5年DFS与OS均明显高于对照组(均P<0.05)(表2)。观察组与对照组生存曲线见图1。
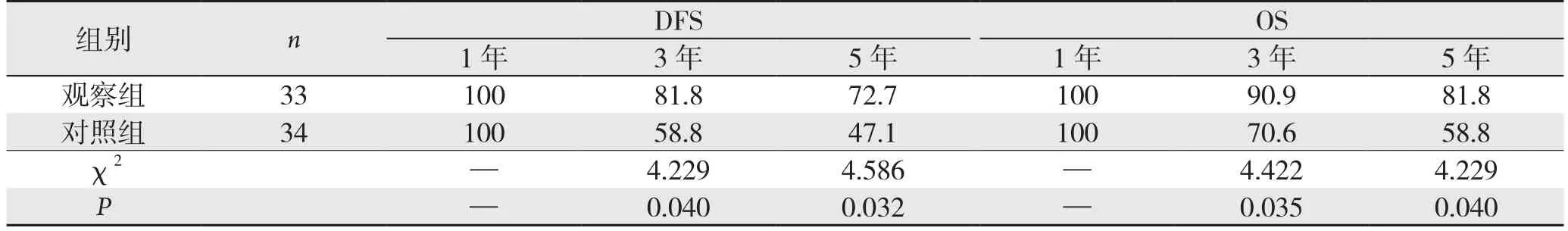
表2 两组患者1、3、5年生存率的比较(%)Table 2 Comparison of the 1-, and 3- and 5-year survival rates between the two groups of patients (%)

图1 两组患者生存曲线 A:DFS曲线;B:OS曲线Figure 1 Survival curves of the two groups of patients A: DFS curves; B: OS curves
3 讨 论
乳腺癌是激素依赖性恶性肿瘤,其肿瘤细胞的生长、增殖受体内性激素水平的影响[15-16]。内分泌治疗在激素依赖性乳腺癌的治疗中起到较为重要的角色,与患者的ER、PR的表达情况密切相关[17-18],其可与通过抗雌激素药物与体内雌、孕激素竞争与激素受体的结合,从而抑制肿瘤细胞的生长。临床上把HR(+)定义为内分泌治疗的适应证[19],然而由于肿瘤的异质性,其细胞生物学或基因会发生改变[20-22],近年来研究[23-27]发现乳腺癌患者原发灶与腋窝淋巴结转移灶的分子分型不一致。针对这一现象,笔者对原发灶HR(-),同期腋淋巴结转移灶HR(+)的患者给予内分泌治疗来观察患者的生存时间及复发转移情况,观察治疗效果,或许能给今后治疗提供新的思路。
本研究对乳腺癌同期伴有同侧腋窝淋巴结转移的患者,原发灶及转移灶均行免疫组化检测,结果发现有部分患者原发灶HR(-),转移灶HR(+)。本研究对这类患者分为观察组和对照组,比较两组患者的生存率及复发转移情况,结果发现:观察组1年无病生存率及总生存率与对照组比较差异无统计学意义(P>0.05),而3、5年无病生存率及总生存率均较对照组明显提高,差异有统计学意义(P<0.05)。两组复发、转移例数间比较差异无统计学意义(P>0.05),但因复发转移死亡例数间比较差异有统计学意义(P<0.05)。说明内分泌治疗虽然没有降低患者复发转移风险,但是它减低了死亡风险,并在患者远期生存率方面发挥了较好的作用。这一结果提示,对于乳腺癌原发灶HR(-),转移灶HR(+)患者,术后行内分泌治疗患者获益。
乳腺癌患者原发灶和同期转移灶免疫组化的检测对于指导患者的治疗起着重要的作用,尤其是转移灶免疫组化的检测,可以发现部分患者原发灶及转移灶存在不一致[13],对于这类患者,特别是转移灶HR(+)患者,加用内分泌治疗,患者生存率得到提高,使得患者从中获益。因此,综合考虑原发灶及转移灶激素受体等差异,能更好的指导乳腺癌个体化治疗。由于本研究样本例数偏少,需要后期增高样本量来证实研究结论。
[1]Coleman MP, Forman D, Bryant H, et a1. Cancer survival in Australia, Canada, Denmark, Norway, Sweden, and the UK, 1995–2007 (the International Cancer Benchmarking Partnership): an analysis of population-based cancer registry data[J]. Lancet, 2011,377(9760):127–138. doi: 10.1016/S0140–6736(10)62231–3.
[2]徐兵河. 要重视乳腺癌的规范化治疗[J]. 临床外科杂志, 2016,24(9):649–652. doi:10.3969/j.issn.1005–6483.2016.09.001.Xu BH. Paying attention to standardized treatment of breast cancer[J]. Journal of Clinical Surgery, 2016, 24(9):649–652.doi:10.3969/j.issn.1005–6483.2016.09.001.
[3]DeSantis C, Ma J, Bryan L, et al. Breast cancer statistics,2013[J].CA Cancer J Clin, 2014, 64(1):52–62. doi: 10.3322/caac.21203.
[4]Gradishar WJ, Anderson BO, Balassanian R, et al. Breast cancer Version 2.2015[J]. J Natl Compr Canc Netw, 2015, 13(4):448–475.
[5]中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2017版)[J].中国癌症杂志, 2017, 27(9):695–760.Committee of Breast Cancer of Chinese Anti-Cancer Association.Guidelines and standardization for diagnosis and treatment of breast cancer of Chinese Anti-Cancer Association (2017 edition)[J]. China Oncology, 2017, 27(9):695–760.
[6]李惠平. 不同分子类型乳腺癌的治疗策略和治疗后管理[J]. 癌症进展, 2016, 14(12):1166–1166.Li HP. Treatment strategies and post-treatment management of breast cancers of different molecular types[J]. Oncology Progress,2016, 14(12):1166–1166.
[7]曹璐, 陈佳艺, 许赪, 等. 分子分型指导下的乳腺癌个体化放疗[J].中华放射肿瘤学杂志, 2016, 25(11):1272–1276. doi:10.3760/cma.j.issn.1004–4221.2016.11.028.Cao L, Chen JY, Xu C, et al. Impact of molecular subtype classification on personalized radiotherapy for breast cancer[J].Chinese Journal of Radiation Oncology, 2016, 25(11):1272–1276.doi:10.3760/cma.j.issn.1004–4221.2016.11.028.
[8]梁越洋, 唐鹏, 王姝姝, 等. 乳腺癌新辅助化疗疗效与分子分型的关系[J]. 中国普外基础与临床杂志, 2014, 21(5):562–566.Liang YY, Tang P, Wang SS, et al. Relation Between Molecular Subtypes and Neoadjuvant Chemotherapy Efficacy in Breast Cancer[J]. Chinese Journal of Bases and Clinics In General Surgery,2014, 21(5):562–566.
[9]王雅杰, 应明真, 陈天然. 三阴性乳腺癌分子分型与个体化治疗[J]. 医学研究杂志, 2016, 45(6):1–5. doi:10.11969/j.issn.1673–548X.2016.06.001.Wang YJ, Ying MZ, Chen TR. Molecular typing and individualized treatment for triple-negative breast cancer[J]. Journal of Medical Research, 2016, 45(6):1–5. doi:10.11969/j.issn.1673–548X.2016.06.001.
[10]刘钟芬, 陈创, 姚晓莉, 等. 乳腺癌不同分子分型的临床病理特点及预后分析[J]. 中华医学杂志, 2016, 96(22):1733–1737.doi:10.3760/cma.j.issn.0376–2491.2016.22.004.Liu ZF, Chen C, Yao XL, et al. Clinicopathological characteristics and prognosis of different molecular types of breast cancer[J].National Medical Journal of China, 2016, 96(22):1733–1737.doi:10.3760/cma.j.issn.0376–2491.2016.22.004.
[11]田枫, 张建国, 仲雷. 乳腺浸润性导管癌病灶与腋窝转移淋巴结中ER和HER-2表达的关系[J]. 中国普通外科杂志, 2012,21(11):1405–1409.Tian F, Zhang JG, Zhong L. Relationship of ER and HER-2 expression in primary tumor and axillary lymph node metastases of invasive ductal breast cancer[J]. Chinese Journal of General Surgery, 2012, 21(11):1405–1409.
[12]刘琪, 左文述, 王新昭, 等. 乳腺癌原发灶和淋巴结转移灶激素受体及HER-2与Ki-67表达相关性分析[J]. 中华肿瘤防治杂志,2013, 20(15):1153–1157.Liu Q, Zuo WS, Wang XZ, et al. Correlation analysis of hormone receptor and HER-2 and Ki-67 expression between primary lesions and lymph node metastases in breast cancer tissues[J]. Chinese Journal of Cancer Prevention and Treatment, 2013, 20(15):1153–1157.
[13]郑向欣, 管小青, 吴骥, 等. 乳腺癌原发灶与腋淋巴结转移灶激素受体与人类表皮生长因子受体2表达情况研究[J]. 中国综合临床, 2017, 33(9):778–781. doi:10.3760/cma.j.issn.1008–6315.2017.09.002.Zheng XX, Guan XQ, Wu J, et al. Study on the expression of hormone receptor and human epidermal growth factor receptor 2 in breast cancer primary tumor and axillary lymph node metastasis[J].Clinical Medicine of China, 2017, 33(9):778–781. doi:10.3760/cma.j.issn.1008?6315.2017.09.002.
[14]姚自翔, 金梁斌, 孔令泉, 等. 乳腺癌原发灶与同期腋淋巴结转移灶雌、孕激素受体和人类表皮生长因子受体2的表达差异研究进展[J]. 中华内分泌外科杂志, 2014, 8(2):134–136. doi:10.3760/cma.j.issn.1674–6090.2014.02.013.Yao ZX, Jin LB, Kong LQ, et al. Research progress of breast cancer with different expressions in estrogen receptor, progestrone receptor and human epidermal growth factor receptor between primary lesion and axillary lymph nodes metastasis[J]. Journal of Endocrine Surgery, 2014, 8(2):134–136. doi:10.3760/cma.j.issn.1674–6090.2014.02.013.
[15]张厚云, 赵凌云.乳腺癌内分泌治疗研究进展[J]. 中国普通外科杂志, 2014, 23(5):680–684. doi:10.7659/j.issn.1005–6947.2014.05.024.Zhang HY, Zhao LZ. Recent advances in endocrine therapy for breast cancer J]. Chinese Journal of General Surgery, 2014,23(5):680–684. doi:10.7659/j.issn.1005–6947.2014.05.024.
[16]Davies C, Pan H, Godwin J, et al. Long-term effects of continuing adjauvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of estrogen receptor-positive breast cancer: ATLAS, a randomized trial[J]. Lancet, 2013, 381(9869):805–816.
[17]Hammond ME, Hayes DF, Dowser M, et a1. American Society of Clinical immunohistochemical testing of estrogen and progesterone receptors in breast cancer(unabridged version)[J]. Arch Pathol Lab Med, 2010, 134(7):e48–72. doi: 10.1043/1543–2165–134.7.e48.
[18]吴世凯, 宋三泰. 对乳腺癌雌孕激素受体检测的认识[J]. 中华乳腺病杂志:电子版, 2012, 6(3):304–308. doi:10.3877/cma.j.issn.1674–0807.2012.03.011.Wu SK, Song ST. Understanding of estrogen receptor detection in breast cancer[J]. Chinese Journal of Breast Disease:Electronic Version, 2012, 6(3):304–308. doi:10.3877/cma.j.issn.1674–0807.2012.03.011.
[19]江泽飞, 徐兵河, 邵志敏, 等. 乳腺癌内分泌治疗专家共识与争议[J]. 中国癌症杂志, 2013, 23(9):772–776. doi:10.3969/j.issn.1007–3969.2013.09.013.Jiang ZF, Xu BH, Shao ZM, et al. Expert consensus and controversy in endocrinotherapy of breast cancer[J]. China Oncology, 2013,23(9):772–776. doi:10.3969/j.issn.1007–3969.2013.09.013.
[20]张敏, 张瑾. 三阴性乳腺癌分子分型与异质性的研究进展[J]. 中国肿瘤临床, 2016, 43(7):306–309. doi:10.3969/j.issn.1000–8179.2016.07.105.Zhang M, Zhang J. Research progress on molecular classi fi cation and heterogeneity of triple-negative breast cancer[J]. Chinese Journal of Clinical Oncology, 2016, 43(7):306–309. doi:10.3969/j.issn.1000–8179.2016.07.105.
[21]邓淼, 刘江波, 张婷, 等. 乳腺癌腋窝淋巴结状态与分子病理特征的关系及临床意义[J]. 实用医学杂志, 2016, 32(12):1962–1965.doi:10.3969/j.issn.1006–5725.2016.12.020.Deng M, Liu JB, Zhang T, et al. Relation of axillary lymph node status and molecular indexes in breast cancer and its signi fi cance[J].The Journal of Practical Medicine, 2016, 32(12):1962–1965.doi:10.3969/j.issn.1006–5725.2016.12.020.
[22]王红鲜, 李呈英, 王开昕, 等. 乳腺浸润性导管癌分子亚型与腋窝淋巴结转移的关系[J]. 中国普通外科杂志, 2016, 25(5):699–704.doi:10.3978/j.issn.1005–6947.2016.05.013.Wang HX, Li CY, Wang KX, et al. Relationship between molecular subtypes of breast invasive ductal carcinoma and axillary lymph node metastasis[J]. Chinese Journal of Clinical Oncology, 2016,25(5):699–704. doi:10.3978/j.issn.1005–6947.2016.05.013.
[23]Curtit E, Nerich V, Mansi L, et a1. Discordances in estrogen receptor status,progesterone receptor status,and HER-2 status between primary breast cancer and metastasis[J]. Oneologist, 2013,18(6):667–674. doi: 10.1634/theoncologist.2012–0350.
[24]Joensuu K, Leidenius M, Kero M, et a1. ER, PR, HER-2, Ki-67 and CK5 in early and late relapsing breast cancer reduced CK5 expression in metastases[J]. Breast Cancer(Auckl), 2013, 7:23–34.doi: 10.4137/BCBCR.S10701.
[25]Sun L, Yu D H, Sun s Y, et a1. Expressions of ER,PR,HER-2,COX-2,and VEGF in primary and relapsed/metastatic breast cancers[J]. Cell Biochem Biophys, 2014, 68(3):511–516. doi:10.1007/s12013–013–9729-y.
[26]Yang YF, Liao YY, Yang M, et a1. Discordances in ER, PR and HER2 receptors between primary and recurrent/metastatic lesions and their impact on survival in breast cancer patients[J]. Med Oncol, 2014, 31(10):214.
[27]Amir E, Clemons M, Purdie CA, et al. Tissue confirmation of disease recurrence in breast cancer patients: pooled analysis of multi-centre, multi-disciplinary prospective studies[J]. Cancer Treat Rev, 2012, 38(6):708–714. doi: 10.1016/j.ctrv.2011.11.006.

