真菌变应原制剂免疫治疗过敏性哮喘的疗效与安全性
高 翔尹 佳
[中国医学科学院北京协和医学院北京协和医院变态 (过敏)反应科过敏性疾病精准诊疗研究北京市重点实验室中国医学科学院临床免疫研究中心,北京100730]
真菌是诱发过敏性哮喘的重要原因,国外研究显示约66%的严重哮喘患者可能对真菌致敏,这已成为全球关注的重大问题[1-2]。真菌与尘螨混合致敏在成人及儿童中也较常见。世界卫生组织指出,变应原特异性免疫治疗 (specific immunotherapy,SIT)是唯一可改变过敏性疾病自然进程的病因治疗方法[3]。目前国际上对于真菌变应原免疫治疗的临床研究较少,且疗效尚不确定。在我国,北京协和医院变态反应科最早开展了真菌变应原SIT。笔者回顾性分析2010年1月至2017年5月使用协和真菌变应原制剂进行免疫治疗的过敏性哮喘患者,评价真菌免疫治疗的疗效与安全性,同时评价真菌与尘螨联合免疫治疗的疗效与安全性。
对象与方法
对象
病例选择标准:(1)2010年1月至2017年5月就诊于北京协和医院变态反应科门诊的男性或女性患者,年龄6~75岁 (含6岁和75岁);(2)符合中华医学会呼吸病学分会哮喘学组2016年版 《支气管哮喘防治指南》与2017年全球哮喘防治创议 (Global Initiative for Asthma,GINA)对于支气管哮喘的诊断标准[4-5],免疫治疗前病程≥1年; (3)有在真菌滋生的环境与季节引起哮喘发作的病史;(4)变应原皮内试验与特异性IgE(sIgE)结果显示:真菌 [枝状枝孢和 (或)链格孢]变应原阳性,或真菌与尘螨变应原均阳性;(5)应用北京协和医院真菌变应原制剂免疫治疗≥1年,目前仍继续治疗;或者曾应用协和真菌变应原制剂免疫治疗≥2年,目前已中断治疗;(6)无免疫治疗禁忌证[6];(7)病历资料完整,免疫治疗前及治疗后每3~6个月有肺功能监测数据;(8)患者本人或其监护人能够配合医师完成调查问卷;(9)患者知晓研究目的,并签署书面知情同意书。
皮内试验
使用北京协和医院变应原制剂室提供的变应原制剂,包括枝状枝孢、链格孢、真菌Ⅰ组 (链格孢、毛壳菌、芽枝霉、镰刀菌)、真菌Ⅲ组 (阿姆斯特丹曲霉、烟曲霉、黑曲霉和土曲霉)、粉尘螨、混合树木花粉、牧草花粉、大籽蒿、葎草、圆柏、美洲大蠊、猫毛等。阳性对照液为0.1 mg/ml磷酸组胺,阴性对照液为变应原溶媒,由山西太原制药厂生产。皮内试验方法与结果判读详见文献 [7],结果评定标准分为 -、 +、 ++、 +++、 ++++,共 5级。 其中+、 ++、+++、 ++++为阳性结果。
血清sIgE检测
所用试剂由Phadia公司提供,采用Phadia公司Immuno CAP系统 (荧光酶联免疫法)检测。血清sIgE检测值分为7级,即0级 (<0.35 kUA/L),1级(≥0.35 kUA/L且<0.7 kUA/L),2级 (≥0.7 kUA/L且<3.5 kUA/L),3级 (≥3.5 kUA/L且<17.5 kUA/L),4级 (≥17.5 kUA/L且<50 kUA/L),5级 (≥50 kUA/L且<100 kUA/L),6级 (≥100 kUA/L)。0级为阴性,1级以上为阳性。
肺通气功能检查
使用瑞士NDD公司EasyOne肺功能仪测定肺功能,通气功能指标主要为第一秒用力呼气容积(forced expiratory volume in first second,FEV1)和呼气流量峰值 (peak expiratory flow,PEF)。初诊肺通气功能异常者行支气管舒张试验,阳性标准为吸入支气管舒张剂后,FEV1增加>12%,且FEV1绝对值增加>200 ml,提示有可变气流受限。
SIT治疗方案
采用北京协和医院变应原制剂室生产的链格孢变应原注射液 [原液浓度1∶20(w/v),总蛋白含量每瓶0.50mg/5 ml,京药制字S20120006]、枝状枝孢变应原制剂 [原液浓度1∶20(w/v),总蛋白含量每瓶0.50 mg/5 ml,京药制字S20120001]。SIT采用皮下注射真菌变应原制剂 (按真菌皮试及sIgE阳性结果配制),注射位置选择上臂外侧部位,双臂交替注射。SIT分起始治疗 (递增量)和维持治疗两个阶段。起始治疗阶段患者接受的变应原制剂浓度从1∶108逐渐递增至1∶100原液浓度,每个浓度的剂量从0.1ml开始注射,每次递增0.1 ml逐渐递增至1.0 ml,每周注射2次,直到维持治疗阶段。维持治疗阶段以1∶100浓度维持 (或以患者最高耐受浓度维持),每周1.0ml[1∶2000(w/v)],分为1或2次注射。注射后密切观察30min。
不良反应
与SIT相关的不良反应指由免疫治疗注射所致的局部和全身不良反应。局部反应包括局部瘙痒、红晕、肿胀、硬结、坏死等。全身不良反应分为5级[8-9]。0级:无症状或症状与免疫治疗无关;Ⅰ级(轻度全身反应):局部荨麻疹、鼻炎或轻度哮喘(PEF较基线下降<20%);Ⅱ级 (中度全身反应):发生缓慢 (>15 min),出现全身荨麻疹和 (或)中度哮喘 (PEF较基线下降<40%);Ⅲ级 (严重全身反应):发生迅速 (<15 min),出现全身荨麻疹、血管性水肿或严重哮喘 (PEF较基线下降>40%);Ⅳ级 (过敏性休克):迅速出现全身瘙痒、潮红、红斑、全身性荨麻疹、喘鸣 (血管性水肿)、哮喘发作、低血压休克等。
观察方法
采集研究对象一般信息、变应原皮肤试验和血清sIgE结果、治疗前后肺功能结果,通过调查问卷方式,了解所有患者在基线前期 (初诊或哮喘未控制或部分控制)、基线期 (SIT起始治疗前)、SIT治疗6、12、24个月后的哮喘控制情况[5]、哮喘控制测试(asthma control test,ACT)[10-11]、 哮喘控制问卷(asthma control test,ACQ)[12-14]、合并哮喘用药情况以及免疫治疗不良反应,并分析比较所得结果。
哮喘控制情况:评价患者过去4周是否出现:(1)日间哮喘症状超过2次/周?(2)因哮喘导致的夜间憋醒?(3)急救药物使用超过2次/周?(4)因哮喘导致活动受限?如果全部为否,为哮喘症状良好控制 (或临床完全控制);1~2项为是,即哮喘症状部分控制;3~4项为是,即哮喘症状未控制。
ACT:为GINA推荐的评估哮喘控制水平问卷[10]。调查患者既往4周内:(1)哮喘妨碍进行日常活动的时间;(2)出现呼吸困难的次数;(3)因哮喘症状造成夜间觉醒或比平时早醒的次数;(4)使用急救药物 (如沙丁胺醇)的次数;(5)如何评估自己哮喘控制情况。每题得分按由重到轻分为1~5分,得分相加,20~25分为哮喘控制良好,16~19分为哮喘控制不佳,5~15分为哮喘控制很差。
ACQ:为常用评估症状控制水平问卷,ACQ-5为5个基本的症状相关问题[13],ACQ-6包括药物使用,ACQ-7还包括使用支气管扩张剂前FEV1水平[14]。本研究选择ACQ-5,调查患者既往1周内:(1)因哮喘而夜间觉醒的次数;(2)晨起时哮喘症状的严重程度;(3)日常活动因哮喘而受限程度;(4)因哮喘而呼吸困难的严重程度;(5)出现喘息的频率。每题得分按由轻到重为0~6分,总分为每题得分的平均值。0~0.75为哮喘控制理想,>0.75且≤1.50为控制一般,>1.50为控制不理想。
哮喘药物评分:按以下标准对患者治疗过敏性哮喘的不同类别药物进行评分[15-16]。口服抗白三烯药物,每日剂量为2分,每日最高为2分;口服缓释茶碱每100μg为0.5分,每天最高为2分;吸入短效 β2-受体激动剂 (short-acting beta 2-agonists,SABA),如沙丁胺醇每100μg为1分,每天最高为8分;吸入性糖皮质激素 (inhaled corticosteroids,ICS):氟替卡松每125μg为 1分,布地奈德每200μg为1分,每天最高为8分;ICS联合长效β2-受体激动剂 (long-acting beta 2-agonists,LABA)按ICS计分后加倍,每天最高为8分;口服激素换算为等效泼尼松,每5 mg为2分,每天最高16分。合计每天用药总分,计算出治疗前后每个评价时点的日均药物评分。
统计学处理
全部数据用SPSS 24.0、Graghpad 7.0统计软件进行分析。计量资料先用Shapiro-wilk法进行正态性检验,正态分布的计量资料以均数±标准差 (±s)表示,治疗前后比较采用方差分析;非正态分布的计量资料使用中位数及四分位数间距 [M(Q25,Q75)]描述,治疗前后比较采用非参数秩和检验。计数资料以构成比 (相对比或率)表示,治疗前后比较采用McNemar检验。以P<0.01为差异有统计学意义。
结 果
一般情况
24例患者符合病例选择标准被纳入研究。其中18例接受真菌与尘螨变应原制剂联合SIT,为联合SIT亚组;6例接受真菌变应原制剂单一SIT,为单一SIT亚组。
24例患者中男性17例,女性7例;平均年龄15(13,16)岁;SIT治疗前过敏性哮喘平均病程5(3,9)年。所有患者枝状枝孢和 (或)链格孢变应原皮内试验均阳性。枝状枝孢sIgE结果为2级6例,3级5例;链格孢sIgE结果为2级2例,3级10例,4级9例,5级2例。全部病例皮试和sIgE检查结果均与病史相符。
联合SIT亚组,男性13例,女性5例;患者开始接受SIT时最小年龄7岁,最大年龄25岁,平均年龄11.5(10.0,13.5)岁,平均疗程 38.5(24.75,48)个月。联合SIT治疗满1、2、3、4年的患者分别为18、16、10和7例。
单一SIT亚组,男性4例,女性2例;患者开始接受SIT时最小年龄6岁,最大年龄15岁,平均年龄10.50(8.25,12.75)岁,平均疗程 40.0(12.0,66.5)个月。SIT治疗满1、2、3、4年的患者分别为6、4、3和3例。
哮喘控制情况
24例患者基线前期哮喘良好控制率为8.33%,经药物规范治疗后,至基线期提高至33.33%,差异无统计学意义 (P>0.01)。SIT治疗1年后哮喘良好控制率为62.50%,治疗2年后哮喘良好控制率提高至80.00%,高于基线期且差异有统计学意义 (P<0.01)。SIT治疗4年哮喘良好控制率达100%(表1)。
联合SIT亚组患者,基线前期与基线期哮喘良好控制率为11.11%和33.33%,治疗1~4年后提升至61.11%~100%;单一SIT亚组患者,基线期哮喘均未控制,治疗1~4年后哮喘良好控制率分别提高至66.67%~100%(表1)。
ACT评分
所有患者SIT治疗6个月、1年、2年的ACT评分均高于基线期,差异有统计学意义 (P<0.001)(表2,图1)。13例患者SIT治疗3年、4年的ACT评分均明显高于基线期,差异有统计学意义 (P<0.001)(表2,图2)。
联合SIT亚组患者SIT治疗1年、2年的ACT评分高于基线期,单一SIT亚组患者,在SIT治疗2年期间ACT评分与基线期相比无统计学差异 (P>0.01)(表2)。各组治疗前后ACT评分呈逐渐递增趋势 (图3)。
ACQ评分
24例患者SIT治疗半年的ACQ评分低于基线期,差异有统计学意义 (P<0.01);SIT治疗1年、2年的ACQ评分低于基线期,差异有统计学意义 (P<0.001)(表3,图1)。13例患者SIT治疗3年、4年的ACQ评分均明显低于基线期,差异有统计学意义(P<0.001)(表 3,图 2)。
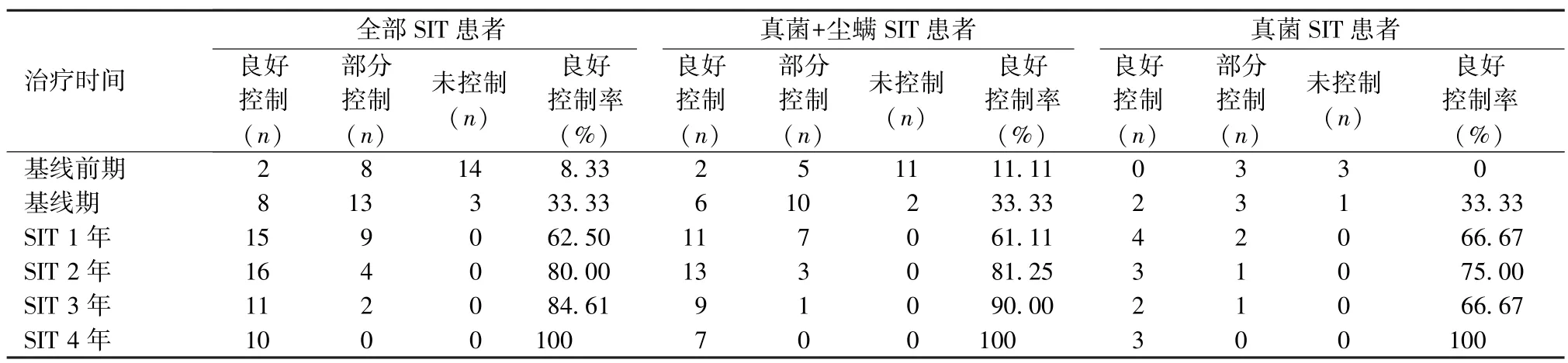
表1 SIT治疗前后过敏性哮喘控制情况比较Table 1 Comparison of level of asthma symptom control before and after SIT
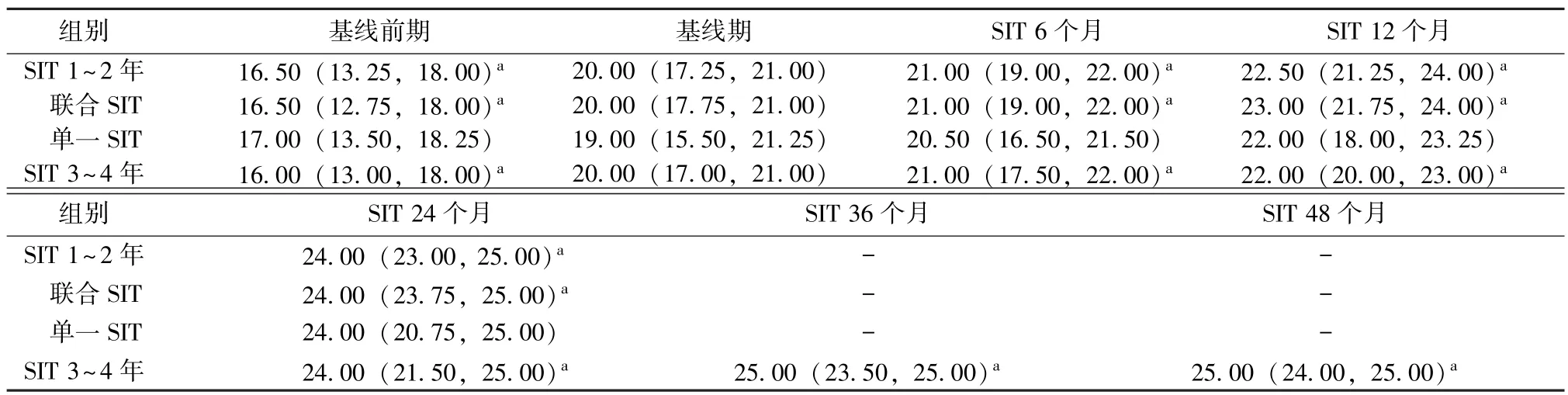
表2 SIT治疗前后过敏性哮喘ACT评分比较Table 2 Comparison of ACT scores of allergic asthma before and after SIT[M(Q25,Q75)]

图1 SIT 1~2年患者 (24例)治疗前后ACT评分、ACQ评分、FEV1%与哮喘药物评分比较Fig 1 Comparison of ACT scores,ACQ scores,FEV1%values,and medicine scores before and after 1-2 years of SIT
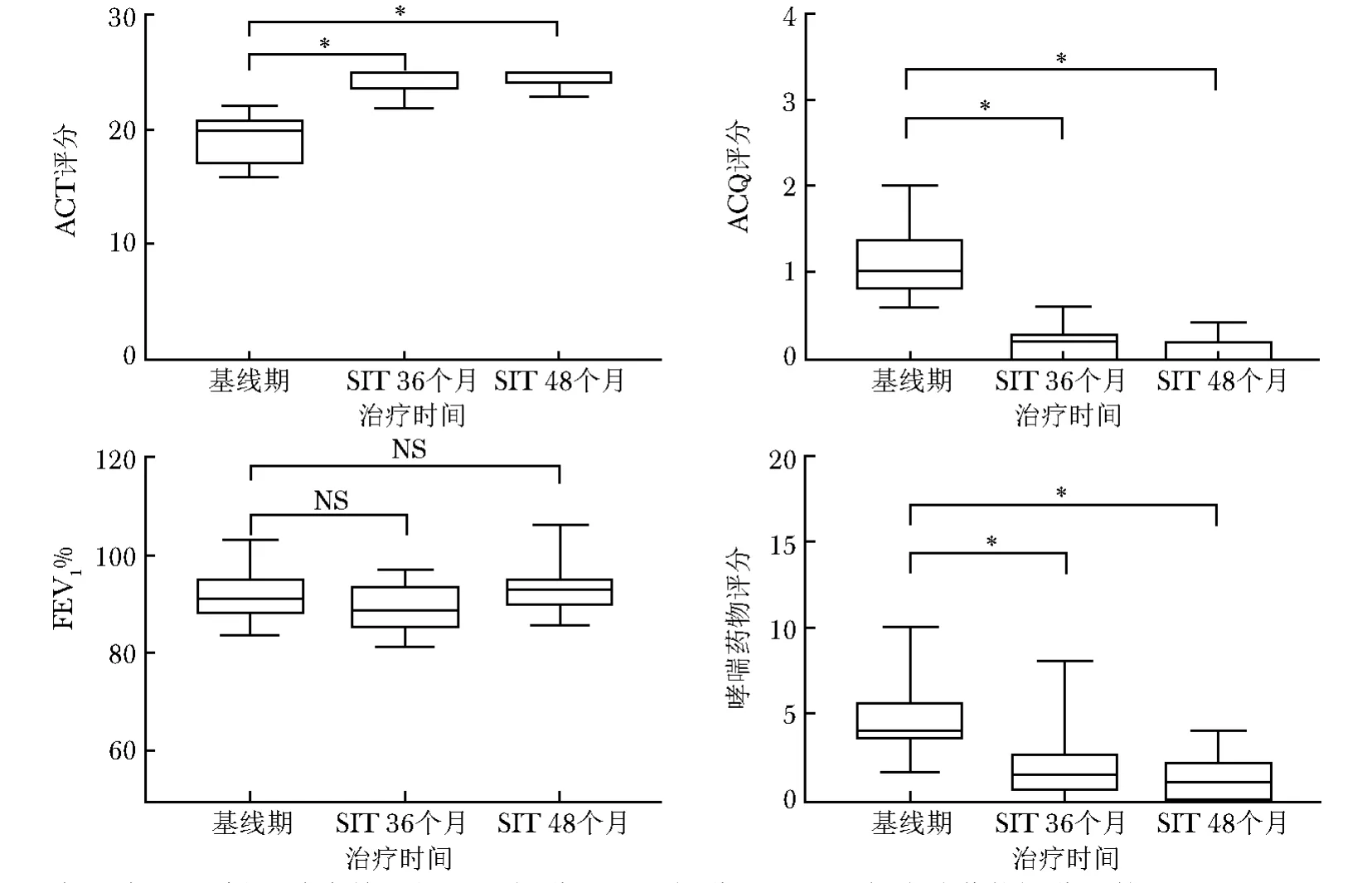
图2 SIT 3~4年患者 (13例)治疗前后的ACT评分、ACQ评分、FEV1%与哮喘药物评分比较Fig 2 Comparison of ACT scores,ACQ scores,FEV1%values,and medicine scores before and after 3-4 years of SIT

图3 24例及各亚组患者治疗前后ACT评分、ACQ评分、FEV1%与哮喘药物评分变化Fig 3 Changes of ACT scores,ACQ scores,FEV1%values,and medicine scores before and after SIT
联合SIT亚组患者SIT治疗1年、2年的ACQ评分低于基线期,单一SIT亚组患者SIT治疗2年期间ACQ评分与基线期相比无统计学差异 (P>0.01)(表3)。各组治疗前后ACQ评分呈逐渐递减趋势(图 3)。
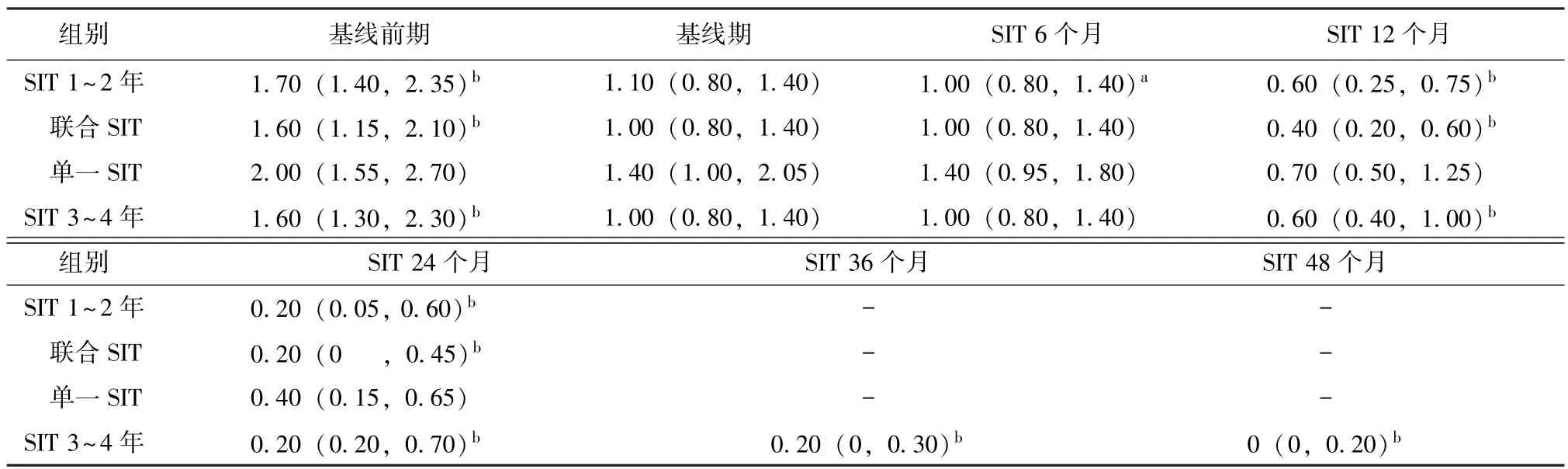
表3 SIT治疗前后过敏性哮喘ACQ评分比较Table 3 Comparison of ACQ scores of allergic asthma before and after SIT[M(Q25,Q75)]
肺通气功能检查
24例患者FEV1%水平在基线前期最低,基线期显著上升,并在SIT治疗期间维持稳定 (图4~6)。患者基线前期FEV1%为 (72.04±11.90)%,经药物规范治疗后基线期FEV1%为 (90.79±5.73)%,与基线前期相比有显著提高,差异有统计学意义 (P<0.001);SIT治疗后半年、1年、2年的FEV1%并无明显变化,与基线期相比差异无统计学意义 (P>0.01)(表4,图1)。13例患者SIT治疗3年、4年时的FEV1%与基线期FEV1%相比无明显变化,差异无统计学意义 (P>0.01)(表4,图2)。
联合SIT亚组和单一SIT亚组患者,基线期FEV1%与基线前期相比明显提高,差异有统计学意义 (P<0.001);但SIT治疗2年期间的FEV1%与基线期相比无明显变化,差异无统计学意义 (P>0.01)(表4)。
表4 SIT治疗前后FEV1%比较Table 4 Comparison of FEV1%values before and after SIT(±s)
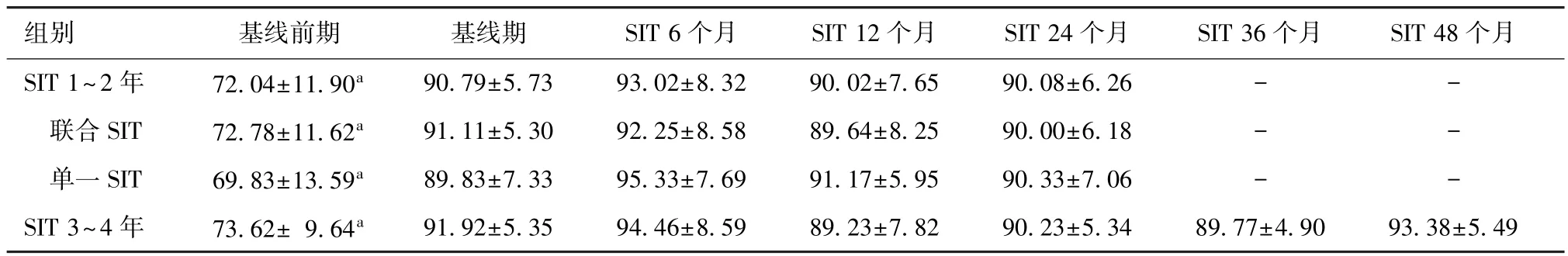
表4 SIT治疗前后FEV1%比较Table 4 Comparison of FEV1%values before and after SIT(±s)
SIT:特异性免疫治疗;FEV1%:第一秒用力呼气容积占预计值的百分比;与基线期相比,a P<0.001
哮喘药物评分
全体患者日均哮喘药物评分在基线前期最高,并随SIT治疗时间而逐渐递减 (图4~6)。患者SIT治疗6个月、1年的哮喘药物评分与基线期相比无统计学差异 (P>0.01),治疗2年时药物评分低于基线期,差异有统计学意义 (P<0.001) (表5,图1)。SIT治疗3~4年的13例患者,治疗2年时药物评分开始低于基线期,差异有统计学意义 (P<0.01),且治疗3、4年后药物评分继续下降 (表5,图2)。

图4 SIT患者 (24例)治疗4年期间FEV1%与哮喘药物评分变化Fig 4 Changes of FEV1%values and medicine scores of all the 24 allergic asthma patients during 4 years of SIT
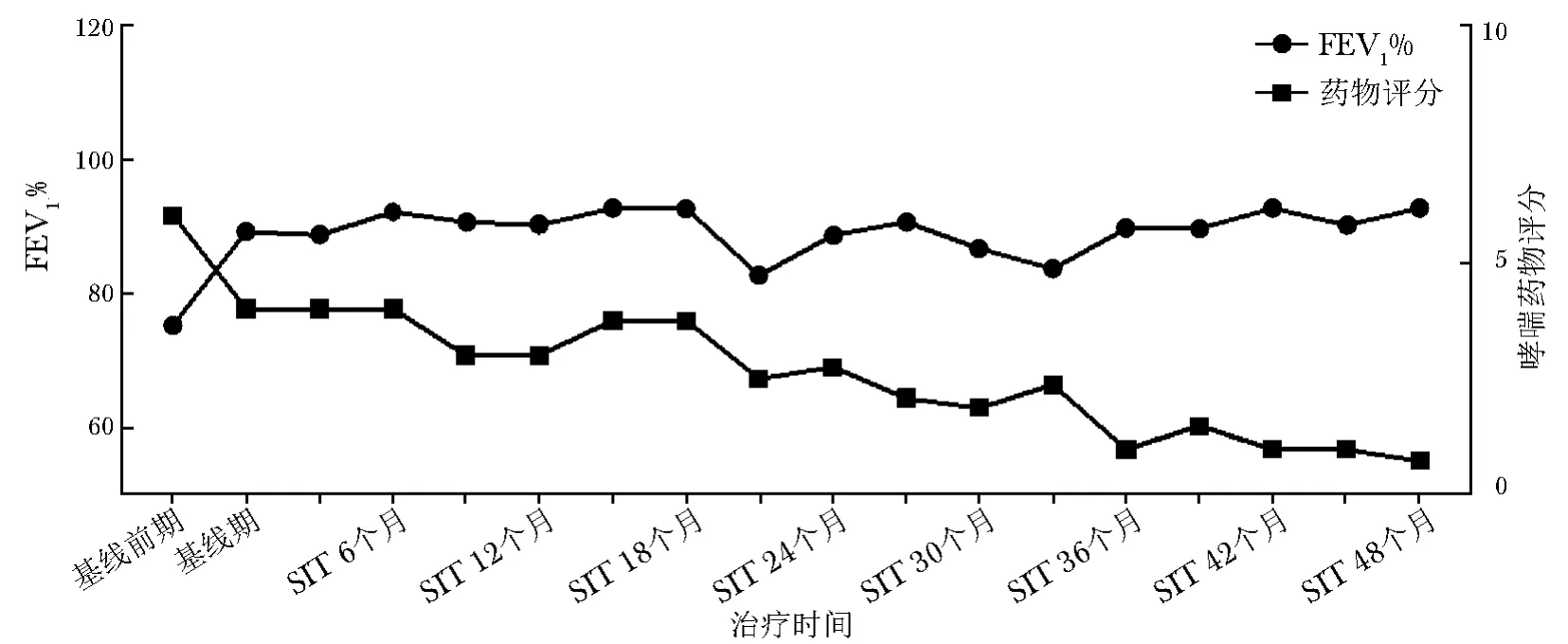
图5 真菌+尘螨SIT患者 (18例)治疗4年期间FEV1%与哮喘药物评分变化Fig 5 Changes of FEV1%values andmedicine scores of18 allergic asthma patients during 4 years of SITwith fungal and dustmite allergen extracts
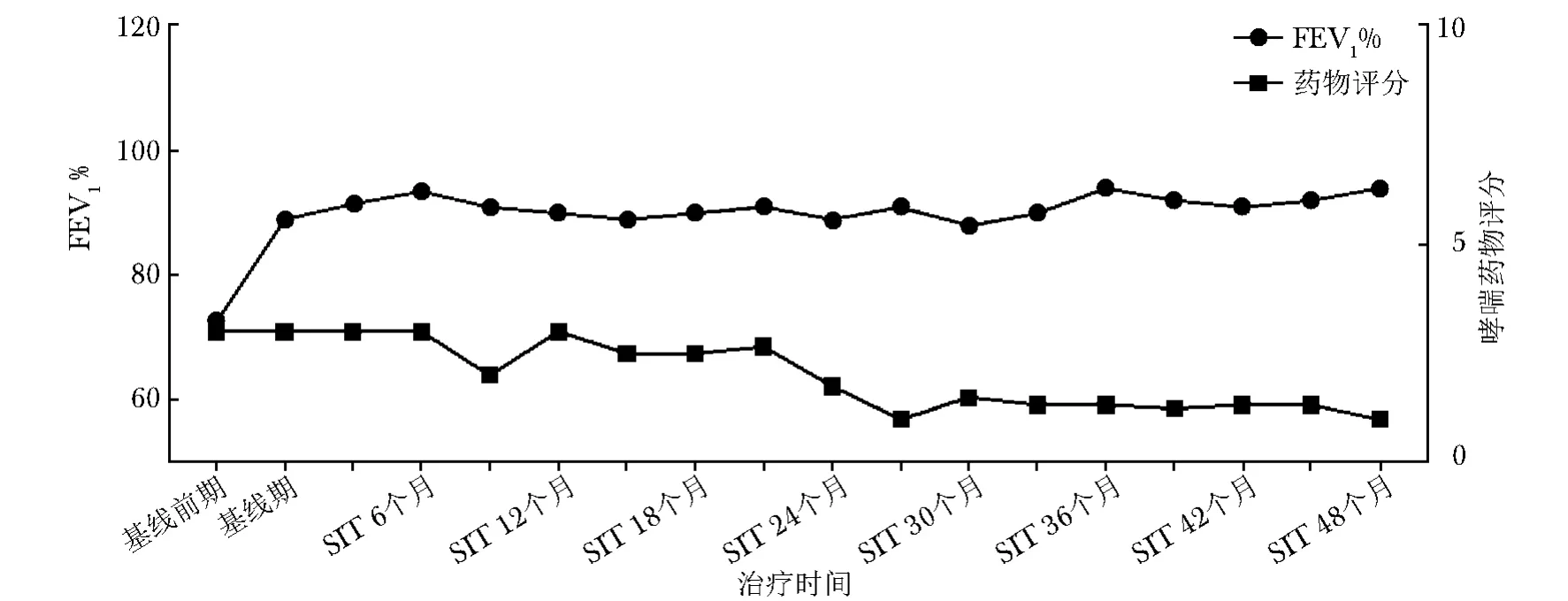
图6 单一真菌SIT患者 (6例)治疗4年期间FEV1%与哮喘药物评分变化Fig 6 Changes of FEV1%values andmedicine scores of6 allergic asthma patients during 4-year of SITwith single fungal allergen extracts
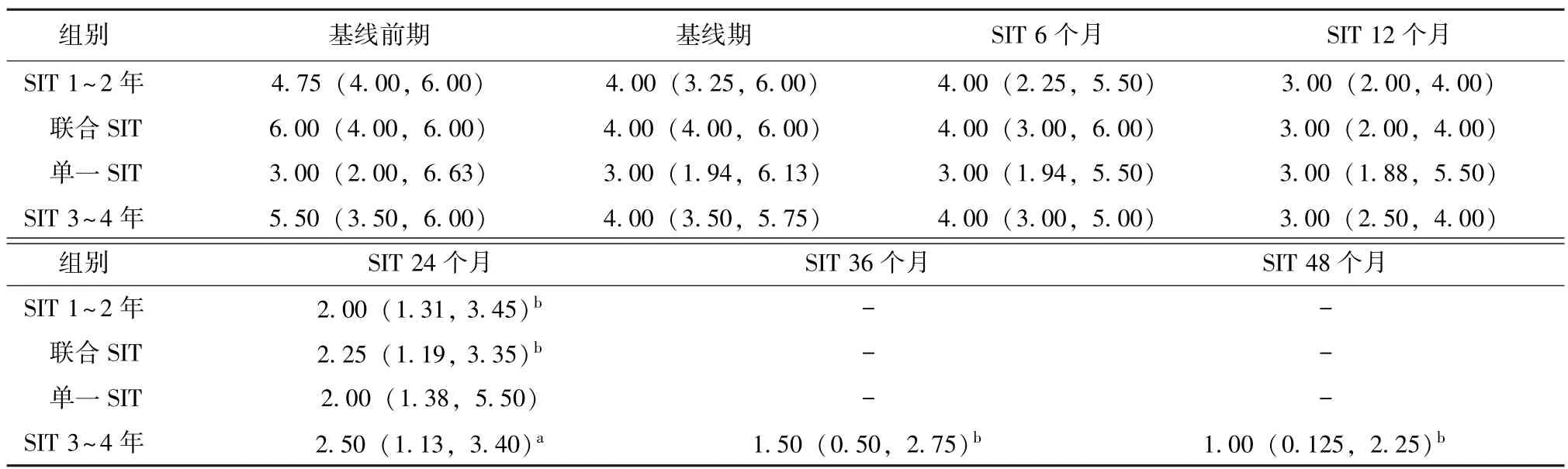
表5 SIT治疗前后过敏性哮喘药物评分比较Table 5 Comparison ofmedicine scores of allergic asthma before and after SIT[M(Q25,Q75)]
联合SIT亚组患者,SIT治疗2年的哮喘药物评分2.25(1.19,3.35),与基线期药物评分 4.00(4.00,6.00)相比,差异有统计学意义 (P<0.001);单一SIT亚组患者,在SIT治疗2年期间未见哮喘药物评分有明显变化 (表5)。
安全性评价
24例患者共进行了6 203例次真菌变应原皮下注射,局部不良反应发生率为1.4%。主要表现为局部红肿、硬结、瘙痒,冷敷或无需处理即可自行缓解。4例患者出现全身不良反应5例次,其中4例次发生于联合SIT亚组,均为Ⅰ级,且均发生在起始治疗(剂量递增)阶段,大部分发生于注射后30 min内。通过降低SIT剂量至无不良反应后,再逐渐递增剂量,患者未再出现全身不良反应。无严重过敏反应发生,无患者因不良反应而中途退出治疗。
讨 论
过敏性哮喘的SIT治疗开始于1949年[17],临床研究证实SIT不仅可以减轻哮喘症状,还能减少过敏性鼻炎发展到哮喘的风险以及减少新的过敏原出现,这是药物治疗无法替代的[18-19]。随着全球哮喘发病率的逐年增高,SIT的作用也越来越重要。2006年GINA将SIT纳入哮喘治疗方案。虽然真菌是诱发哮喘最常见的过敏原之一,但与尘螨、花粉变应原相比,真菌SIT的研究较少。主要原因是真菌变应原致敏蛋白组分的影响因素非常复杂,因此获取标准化变应原提取物的难度较高,目前只有互隔交链孢霉(Alternaria alternate)提取物的标准化取得了一定进展[20]。
交链孢霉 (Alternaria)与芽枝菌 (Cladosporium)是临床研究较多的真菌。在早期研究中,Horst等[21]发现应用标准化交链孢霉提取物免疫治疗1年,治疗组哮喘与鼻炎症状-用药评分明显降低,患者自评改善,特异性IgG显著增加;Cantani等[22]应用交链孢霉提取物免疫治疗过敏性哮喘和 (或)鼻炎患儿3年,发现临床症状改善与剂量相关,当治疗剂量累积超过80 000 PNU时,临床治疗有效率达80%。Helbling等[23]荟萃分析表明,免疫治疗对于交链孢霉过敏的患者具有临床疗效。近年来,真菌SIT研究多采用标准化互隔交链孢霉提取物。Tabar等[24]与Kuna等[25]分别对互隔交链孢霉诱发的过敏性鼻炎和 (或)哮喘患者应用免疫治疗,进行1年和3年的前瞻性、随机、安慰剂对照研究,结果表明SIT能够有效改善症状-用药评分,提高生活质量,提高PEF,且无严重不良反应。上述研究均有一定局限性,如开放式设计[22]、随访期较短[21,24]、病例数较少等。芽枝菌的临床研究证据则更少。Malling等[26]等研究表明,成年哮喘患者经过5~7个月免疫治疗,芽枝菌治疗组临床有效率达81%,安慰剂组为27%;治疗组患者均在剂量增加阶段出现哮喘发作,并有较多局部不良反应。Dreborg等[27]研究表明,哮喘和 (或)鼻炎儿童免疫治疗6个月后,多主枝孢霉治疗组的药物评分明显下降,但症状评分和PEF与安慰剂组相比无统计学差异,且全身不良反应发生率高。由于缺少足够的前瞻性随机对照研究,真菌SIT的有效性和安全性仍然存在争议。
北京协和医院变态反应科在我国最早开展了变应原SIT,临床应用50余年,积累了丰富的经验[28-29]。本研究使用北京协和医院自主研发的真菌变应原制剂,评价了其免疫治疗过敏性哮喘的疗效与安全性,同时评价了真菌与尘螨变应原联合免疫治疗的疗效与安全性。
本研究中,SIT治疗1年后患者ACT评分增高,ACQ评分降低,且与基线期相比均有显著性差异(P<0.001),治疗1年哮喘良好控制率为62.50%,治疗2年为80.00%,明显高于基线期,提示在规律药物治疗的基础上,真菌变应原免疫治疗能够有效控制哮喘发作,改善临床症状。通常认为SIT的起效时间在半年左右,也有研究提出SIT能在治疗后2~4个月显效[6]。本研究发现,免疫治疗半年时,患者的ACT、ACQ评分与基线期相比有改善 (P<0.01),且在治疗1~4年时评分改善更加显著 (P<0.001),这与2008年Tabar等[24]研究结果相符,该研究发现治疗组在SIT 6个月后呼吸道症状明显改善,哮喘严重程度降低。本研究还表明SIT的疗效随治疗时间和剂量累积而不断增强,在治疗4年时观察到了最佳的改善。2011年Kuna等[25]发现症状-药物联合评分在SIT第1年无显著变化,但在第2、3年显著下降。Cantani等[22]的研究也强调了临床疗效与免疫治疗的剂量相关,接受累积剂量最高的患者对SIT有较好的反应。更加长期及脱敏后的远期疗效则需要进一步研究。
肺功能监测对于指导免疫治疗具有重要意义。哮喘治疗后FEV1<70%预计值或哮喘症状未得到控制的患者禁用SIT,应先进行充分的药物治疗[6,30]。本研究中,患者在基线前期的 FEV1%为 (72.04±11.90)%,经规范治疗后显著提升,符合免疫治疗要求。在SIT治疗1~4年中FEV1%维持稳定,与基线期相比无统计学差异。可见,哮喘患者基础肺功能的改善主要取决于基线期的药物规范治疗,SIT治疗后肺功能维持稳定,未观察到进一步改善。但SIT治疗后药物评分逐渐下降,表明SIT可使哮喘患者逐渐减少药物用量,即发挥 “节省药物”(尤其是激素)的效应[31]。SIT长期维持治疗能否提高肺功能,尚需更长时间的观察。临床上建议每次注射前都应监测肺功能,评估最高呼气峰流速,若患者肺功能下降低于本人最佳值的80%,应推迟注射[30]。
本研究证实SIT起效后,药物用量可逐渐减少,在达到临床控制哮喘的同时,避免了持续大量用药的不良反应。药物减量方案通常先减少激素用量 (口服或吸入),然后减少每日使用次数,再减少与激素合用的控制药物 (如LABA),以最低剂量ICS维持治疗直到可以停药。国外荟萃分析显示,每3个月减少ICS剂量25%~50%是安全可行的[32]。但需注意,药物减量过快可能增加哮喘急性发作的风险,必须始终以控制哮喘症状为根本目标,根据病情变化和肺功能进行微调,以巩固和维持SIT的临床疗效[31]。
与过敏性鼻炎相比,哮喘患者在SIT时发生严重气道反应或全身不良反应的风险更大。本研究中,24例患者共进行了6 203例次皮下注射,不良反应以局部反应为主,发生率1.4%,全身不良反应仅有5例次,发生率极低,且均为1级,未见1例严重过敏反应。在早期Tabar等[33]的研究中,交链孢霉免疫治疗不良反应发生率为1.95%,多为全身性、轻度不良反应。随着标准化真菌变应原提取物的发展,Kuna等[25]研究发现互隔交链孢霉疫苗免疫治疗的不良反应发生率为1.1%,最常见为注射后出现局部水肿。其他研究同样显示标准化互隔交链孢霉疫苗有很好的耐受性,不良反应发生率低于1%,主要为局部反应与极少全身反应,如呼吸困难、咳嗽与鼻炎[34-35]。本研究的结果与上述标准化疫苗的研究结果相似,表明国产变应原制剂具有良好的安全性。在临床上应严格掌握适应证,规范操作,严格遵守注射后30 min留观制度,确保免疫治疗的安全进行。
本研究24例患者中,18例为真菌与尘螨联合免疫治疗。既往研究多为单一真菌过敏的免疫治疗,也有研究评价了多种过敏原 (真菌、尘螨、花粉等)混合免疫治疗的疗效及安全性[36],尚无专门对真菌与尘螨联合SIT的评价。本研究首次探讨了真菌与尘螨联合SIT的疗效与安全性。结果显示,联合免疫治疗2年,该亚组的ACT、ACQ评分比基线期显著改善,肺功能维持稳定,药物评分明显下降,无严重不良反应发生,具有良好的疗效与安全性。而单一免疫治疗亚组治疗2年的评价指标与基线期相比无统计学差异,可能的原因是病例数较少,导致统计效力不佳。
真菌变应原疫苗的质量与疗效和安全性密切相关,但目前大部分真菌变应原提取物的 “标准化”程度欠佳,限制了临床免疫治疗的开展。本研究使用的是协和医院变态反应科自主研发的真菌变应原制剂[37]。曹乃清和张宏誉[38]用双向电泳技术分析了链格孢霉的致敏蛋白组分,为变应原的纯化与标准化奠定了基础。北京协和医院变应原制剂室用多年时间对链格孢、枝状枝孢等9种过敏原制剂进行工艺革新、检测方法改进及质量标准升级,通过临床研究评估了其安全性和有效性[28,39-40],获得了北京市食品药品监督管理局的医疗机构制剂注册批件,能够安全用于临床SIT治疗。
本研究对北京协和医院真菌变应原制剂免疫治疗过敏性哮喘进行了回顾性分析,结果表明,真菌变应原免疫治疗能够有效控制哮喘发作,改善临床症状,减少哮喘药物用量,维持稳定的肺功能,且不良反应发生率低,为安全、有效的病因治疗方法。本研究尚存在一些不足:(1)研究病例数较少;(2)用于真菌免疫治疗的并非标准化真菌变应原制剂;(3)大部分患者SIT治疗时间为1~2年,不能评价长期维持治疗的疗效;(4)研究未设置安慰剂对照组。未来拟进一步扩大病例数,设计前瞻性随机对照研究,以更加科学地评估真菌变应原免疫治疗的疗效与安全性。
[1]Rick EM,Woolnough K,Pashley CH,et al.Allergic Fungal airway disease[J].J Investig Allergol Clin Immunol,2016,26:344-354.
[2]Dziadzio L,Bush RK.Assessment and control of fungal allergens[J].Curr Allergy Asthma Rep,2001,1:455-460.
[3]WHO position paper.“Allergen immunotherapy:therapeutic vaccines for allergic diseases” [J].Arerugi,1998,47:698-704.
[4]中华医学会呼吸病学分会哮喘学组.支气管哮喘防治指南 (2016年版) [J].中华结核和呼吸杂志,2016,9:675-697.
[5]Global Initiative for Asthma.Global strategy for asthma management and prevention,2017[EB/OL].[2017-08-01].http://www.ginasthma.org.
[6]Zuberbier T,Bachert C,Bousquet PJ,et al.GA(2)LEN/EAACI pocket guide for allergen-specific immunotherapy for allergic rhinitis and asthma[J].Allergy,2010,65:1525-1530.
[7]叶世泰.变态反应学 [M].北京:科学出版社,1998.
[8]Alvarez-Cuesta E,Bousquet J,Canonica GW,et al.Standards for practical allergen-specific immunotherapy[J].Allergy,2006,61 Suppl 82:1-20.
[9]Cox L,Nelson H,Lockey R,et al.Allergen immunotherapy:a practice parameter third update[J].J Allergy Clin Immunol,2011,127:S1-55.
[10]Nathan RA,Sorkness CA,Kosinski M,et al.Development of the asthma control test:a survey for assessing asthma control[J].J Allergy Clin Immunol,2004,113:59-65.
[11]Zhou X,Ding FM,Lin JT,et al.Validity of asthma control test for asthma control assessment in Chinese primary care settings[J].Chest,2009,135:904-910.
[12]Juniper EF,O'Byrne PM,Guyatt GH,et al.Development and validation of a questionnaire to measure asthma control[J].Eur Respir J,1999,14:902-907.
[13]Nadif R,Siroux V,Oryszczyn MP,et al.Heterogeneity of asthma according to blood inflammatory patterns[J].Thorax,2009,64:374-380.
[14]Laforest L,Van Ganse E,Devouassoux G,et al.Quality of asthma care:results from a community pharmacy based survey[J].Allergy,2005,60:1505-1510.
[15]Dahl R,Stender A,Rak S.Specific immunotherapywith SQ standardized grass allergen tablets in asthmatics with rhinoconjunctivitis[J].Allergy,2006,61:185-190.
[16]Jutel M,Jaeger L,Suck R,et al.Allergen-specific immunotherapy with recombinant grass pollen allergens[J].JAllergy Clin Immunol,2005,116:608-613.
[17]Bruun E.Control examination of the specificity of specific desensitization in asthma[J].Acta Allergol,1949,2:122-128.
[18]Rodriguez Del Rio P,Vidal C,Just J,et al.The European Survey on Adverse Systemic Reactions in Allergen Immunotherapy(EASSI):A paediatric assessment[J].Pediatr Allergy Immunol,2017,28:60-70.
[19]Cox L,Compalati E,Kundig T,etal.New directions in immunotherapy[J].Curr Allergy Asthma Rep,2013,13:178-195.
[20]Aden E,Weber B,Bossert J,et al.Standardization of Alternaria alternata:extraction and quantification of alta 1 by using an mAb-based 2-site binding assay[J].J Allergy Clin Immunol,1999;104:128-135.
[21]Horst M,Hejjaoui A,Horst V,et al.Double-blind,placebo-controlled rush immunotherapy with a standardized Alternaria extract[J].JAllergy Clin Immunol,1990,85:460-472.
[22]Cantani A,Businco E,Maglio A.Alternaria allergy:a three-year controlled study in children treated with immunotherapy[J].Allergol Immunopathol(Madr),1988,16:1-4.
[23]Helbling A,Reimers A.Immunotherapy in fungal allergy[J].Curr Allergy Asthma Rep,2003,3:447-453.
[24]Tabar AI,Lizaso MT,Garcia BE,et al.Double-blind,placebo-controlled study of Alternaria alternata immunotherapy:clinical efficacy and safety[J].Pediatr Allergy Immunol,2008,19:67-75.
[25]Kuna P,Kaczmarek J,Kupczyk M.Efficacy and safety of immunotherapy for allergies to Alternaria alternata in children[J].JAllergy Clin Immunol,2011,127:502-508.e501-506.
[26]Malling HJ,Dreborg S,Weeke B.Diagnosis and immunotherapy ofmould allergy.V.Clinical efficacy and side effects of immunotherapy with Cladosporium herbarum[J].Allergy,1986,41:507-519.
[27]Dreborg S,Agrell B,Foucard T,et al.A double-blind,multicenter immunotherapy trial in children,using a purified and standardized Cladosporium herbarum preparation. Ⅰ.Clinical results[J].Allergy,1986,41:131-140.
[28]关凯.葎草花粉变应原免疫治疗疗效和安全性评估[J].中华临床免疫和变态反应杂志,2012,4:279-284.
[29]叶世泰.过敏性鼻炎患者在特异性脱敏治疗中血清IgE的动态观察 [J].中华耳鼻喉科杂志,1982,17:147.
[30]李靖.中国特异性免疫治疗的临床实践专家共识[J].中华结核和呼吸杂志,2012,3:163-166.
[31]Zielen S,Kardos P,Madonini E.Steroid-sparing effects with allergen-specific immunotherapy in children with asthma:a randomized controlled trial[J].J Allergy Clin Immunol,2010,126:942-949.
[32]Viswanathan M,Golin CE,Jones CD,et al.Inter-ventions to improve adherence to self-administered medications for chronic diseases in the United States:a systematic review[J].Ann Intern Med,2012,157:785-795.
[33]Tabar AI,Lizaso MT,Garcia BE,et al.Tolerance of immunotherapy with a standardized extract of Alternaria tenuis in patients with rhinitis and bronchial asthma[J].J Investig Allergol Clin Immunol,2000,10:327-333.
[34]Prieto L,Palacios R,Aldana D,et al.Effect of allergen-specific immunotherapy with purified Alt a1 on AMP responsiveness,exhaled nitric oxide and exhaled breath condensate pH:a randomized double blind study[J].Allergy Asthma Clin Immunol,2010,6:27.
[35]Lizaso MT,Tabar AI,Garcia BE,et al.Double-blind,placebo-controlled Alternaria alternata immunotherapy:in vivo and in vitro parameters[J].Pediatr Allergy Immunol,2008,19:76-81.
[36]Adkinson NF Jr,Eggleston PA,Eney D,et al.A controlled trial of immunotherapy for asthma in allergic children[J].N Engl JMed,1997,336:324-331.
[37]乔秉善.变态反应学实验技术 [M].北京:中国协和医科大学出版社,2002.
[38]曹乃清,张宏誉.双向电泳分析链格孢霉过敏原提取液的致敏蛋白组分 [J].中华微生物学和免疫学杂志,2009,8:688-690.
[39]关凯,文昭明.变应原免疫治疗致全身反应 [J].中华临床免疫和变态反应杂志,2011,5:298-302.
[40]文昭明.免疫疗法致不良反应的临床观察:附29例报告 [J].中华微生物学和免疫学杂志,2001,21增刊:63-66.

