气肿疽梭菌胶体金诊断试纸条的研制
任春宇+姜丹丹+车达
摘要:为建立快速、准确、简便的检测气肿疽的胶体金免疫层析试纸条,以免疫层析法为指导,根据抗原-抗体的特性,建立了不需要再加入任何检测试剂且快速简便的检测方法。结果表明,胶体金与该单抗的最佳结合量为 30 μg/mL,最佳 pH 值为8.4,最佳NC膜为Millipore HFB1350220型。将纯化的气肿疽梭菌多抗及羊抗鼠IgG分别以1 ∶4和1 ∶8的稀释倍数喷于硝酸纤维素膜的T线和C线。对胶体金诊断试纸条进行验证,敏感度高,可检测到的最低抗原量为1×105 CFU/mL,特异性强、无假阳性与交叉反應现象、有较好的稳定性。本研究旨在建立快速、准确、简便的检测气肿疽的胶体金免疫层析试纸条。
关键词:气肿疽梭菌;胶体金;免疫层析试纸条
中图分类号: S855.1+2 文献标志码: A
文章编号:1002-1302(2016)11-0283-03
气肿疽又称黑腿病或鸣疽,是由气肿疽梭菌(Clostridium chauvoei)引起的反刍动物的急性、败血性传染病[1]。该菌属细菌纲芽孢杆菌科梭菌属,是土壤中的专性厌氧菌,广泛分布于自然界中,经常发现于牛和绵羊的肠内容物中[2],特别在深部伤口的厌氧环境中[3-4]。该菌为革兰氏阳性棒状大杆菌,对进行疫苗接种的豚鼠腹腔渗出液做涂片观察,可发现该菌以单个形式存在,或几个细菌形成短链,可与呈长链的腐败梭菌做出鉴别,这是形态上的主要区别之一[5]。在进行菌体培养时,需创造严格的厌氧环境,尤其是在固体培养中,当接种于葡萄糖血液琼脂中时,形成半透明圆形菌落、β溶血环,中心略凸起[6]。
该菌繁菌体的抵抗力不强,但芽孢却有很强的抵抗力,可在土壤中存活多年[7],在腐败尸体中仍可存活3个月。若想将组织内的芽孢杀死,经煮沸20 min或0.2%升汞处理 10 min 方可。一旦通过深部创伤或术后而感染[8],或经口感染,经胃肠道肠系膜进入血液最终到达各个器官和肌肉组织内的芽孢将迅速繁殖[9],并很快出现病症,还可形成肠气肿疽,易感动物在感染后12~36 h则出现死亡[10]。
本试验选用气肿疽梭菌标准株制备菌体单克隆抗体,旨在将该单抗与胶体金标记结合,研制出能对气肿疽梭菌做出快速诊断的胶体金免疫层析试纸条,该试纸条研制成功将为气肿疽诊断、流行病学调查及卫生检疫等提供快速、简便、准确的检测手段,更好地应用于生产实践。
1 材料与方法
1.1 试验材料
气肿疽梭菌标准株C54-1,购自于中国兽医药品监察所;氯金酸(HAuCl4·4H2O),购自科兴生物科技有限公司;柠檬酸三钠C6H5Na3O7·2H2O,购自北京华力德科技有限公司;二氯二甲基硅烷(Sigma公司产品);PVC底板、玻璃纤维膜、硝酸纤维素膜、MAX线标签贴纸、色皮标签等,购自杭州隆基生物技术有限公司;BSA,购自Promega公司;样品垫及吸水垫,购自上海金标生物科技有限公司。
1.2 单克隆抗体的制备、纯化及检测
注射经离心洗涤的杂交瘤细胞于8周龄BALB/c小鼠,待有腹水形成后,取腹水并用间接ELISA法检测腹水效价。采用Protein A 亲和层析法对单克隆抗体进行纯化,用紫外光分光光度计测量纯化的单抗浓度,将单抗溶液做50倍稀释,分别于260 nm 和280 nm 波长下测吸光度,并于-20 ℃储存备用。
1.3 胶体金的制备
采用柠檬酸钠还原法制备胶体金,制备胶体金粒径大小为20~25 nm。将100 mL去离子水和1 mL 1%氯金酸溶液加入硅化处理好的锥形瓶中,加热至完全沸腾时,迅速加入1.5 mL 1%柠檬酸三钠,煮沸5~10 min,发现溶液颜色渐变成酒红色后,继续煮沸10 min取下,置于常温自然凉透,补足水分,4 ℃保存备用。
1.4 金标的制备
1.4.1 气肿疽梭菌单抗与胶体金颗粒结合的最适pH值确定
将制备的胶体金加入若干2 mL离心管中,1.5 mL/管。将pH值分别调为5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0。按pH值从低到高分别加50 μL 1 mg/mL 的单抗IgG到离心管中,摇匀30 min后静置约10 min;再将100 μL的10% NaCl溶液加至管中,摇匀20 min后静置约1 h,观察颜色变化情况,记录能保持为红色的最低pH值,即为最适pH值。
1.4.2 单克隆抗体最适用量的确定
分别取金标用抗体5、10、15、20、25、30、35、40、45 μg,加入1 mL胶体金溶液中充分混匀,完成后室温静置约1 h,观察胶体金溶液的颜色变化。
1.4.3 胶体金探针的制备
取已制备好的胶体金溶液 20 mL 加入50 mL离心管中,将胶体金溶液的pH值调整为略高于最适pH值0.2~0.4,在磁力加热搅拌器运行中,将纯化后的单克隆抗体溶液按最佳结合浓度缓慢滴入胶体金溶液中,混匀后室温静置10 min,再置于磁力搅拌器上加入终浓度为2%的BSA,离心弃上清,用TBS将沉淀溶解,即为合成探针。
1.4.4 胶体金探针的纯化
先除去其中未被完全标记的胶体金和在标记的过程中容易产生的多种聚合物[11]。应用低温高速离心纯化方法,将标记好的胶体金先以小转数离心;再将收集的上清液以13 500 r/min离心1 h,此时将上清液缓慢倒出。将沉淀以原体积的胶体金重悬液溶解沉淀,低温重复离心2~3次,沉淀溶于原体积的胶体金重悬液中,4 ℃保存备用。
1.5 试纸条的制备
1.5.1 金标垫的制备
在金标垫处理液Ⅰ与Ⅱ中分别处理玻璃纤维素膜GF-08和Ahlstrom 8964,1 h后取出并于常温中晾干,干燥保存。玻璃纤维素膜处理完毕后剪成50 mm宽的长条,把制备好的金标探针按一定量均匀喷涂于玻璃纤维上,选出最佳玻璃纤维膜及处理液。
1.5.2 样品垫的预处理
将样品垫裁剪成适当尺寸浸入预处理液中浸泡20 min取出,控干液体,置烘干箱,烘干后干燥保存。
1.5.3 NC膜的优选
选择不同流速的Millipore HFB1350220、whatman Immunopore RP、whatman Immunopore FP、Sartorius CN 140、whatman AE 99 (无背衬)硝酸纤维素膜于处理液中,浸泡30 min取出,用PBS冲洗,烘干。进行流速试验,注意其流速和反应背景均匀度,选择层析速度快(3~5 min)且背影小、颜色淡的硝酸纤维膜。
1.5.4 T线及C线条件的优化
将纯化处理好的兔抗气肿疽梭菌血清及羊抗鼠IgG分别按以下比例稀释:1 ∶2、1 ∶4、1 ∶8、1 ∶16、1 ∶32。然后划在NC膜的检测线和质控线上进行优化(做方阵试验),选出效果最好的一组进行包被。
1.5.5 封闭液的优化
将喷涂有肿疽梭菌多抗及羊抗鼠IgG的NC膜分别置于5%犊牛血清、3%脱脂乳和1%BSA中,在封闭液中浸泡30 min,取出用PBS冲洗,晾干,制成试纸条,用标准阳性和阴性血清作试验,筛选出最佳封闭液。
1.5.6 试纸条的组装
将硝酸纤维素膜贴在PVC底板中央,贴后不要有空隙和气泡;金标结合垫平贴于NC膜T线下方压住 NC 膜重叠5 mm、然后粘贴样品板及吸水纸,小心抹平,最后贴上MAX线标贴和色皮标签,即成检测试纸条。
1.6 试纸条的检测方法和结果判定
使试纸条保持竖直方向,将样品垫端放入稀释后的待检样液中(注意液面不可超过MAX 线),室温下作用5~10 min,观察结果。
1.7 敏感性试验
将气肿疽梭菌菌液做1 ∶50、1 ∶100、1 ∶200、1 ∶400倍比稀释,分别将试纸条插入以上不同稀释度的菌液中,观察结果。
1.8 特异性试验
用胶体金试纸条检测选取与气肿疽梭菌种系相近的腐败梭菌、肉毒梭菌进行特异性试验,观察检测结果是否存在交叉反应。
1.9 重复性试验
随机取40支试纸条进行检测试验,10只进行阴性样品检测,30支进行阳性样品检测,测定试纸条的重复性。
1.10 稳定性试验
将胶体金试纸条置于室温和4 ℃冰箱中保存,半年内检测1次/月保存的阳性菌液及阴性对照菌液,观察检测结果,比较符合率。
2 结果与分析
2.1 單克隆抗体的制备、纯化及检测
全菌加强免疫后收集血清,经辛酸-硫酸铵法进行抗体的粗提,并透析除盐处理后,以间接ELISA法检测多抗效价,气肿疽梭菌的抗体效价为1 ∶25 600。
经辛酸-硫酸铵法粗提,再用Protein A 亲和层析法纯化,间接ELISA法测定的单克隆抗体效价为1 ∶102 400,抗体效价升高1倍。测得纯化蛋白的浓度为28.14 mg/mL(紫外分光度计测定)。
2.2 单克隆抗体与胶体金结合的最佳pH值确定
将胶体金溶液的pH值分别调为5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0。按pH值从低到高分别加50 μL 1 mg/mL 单抗IgG和100 μL 10% NaCl溶液至胶体金管中,振摇20 min,室温下静置1 h。根据胶体金的颜色变化,确定了最低pH值为8,再做pH值为7.2、7.4、7.6、7.8、8.0、8.2、8.4、8.6、8.8几个梯度,室温下放置2 h,观测胶体金颜色变化,记录仍保持红色的pH值,稳定胶体金的最适pH值为8.4。
2.3 胶体金标记单克隆抗体最适用量的确定
将胶体金颗粒与气肿疽梭菌单克隆抗体进行标记。观察胶体金溶液的颜色变化,稳定胶体金所需抗体的最低量为 25 μg,而实际标记中使用免疫金抗体的量为最低量再加20%,即为30 μg,确定单克隆抗体与胶体金的的最佳结合浓度应为30 μg/mL。
2.4 金标垫的制备
将已经纯化好的金标探针按一定量均匀喷涂于玻璃纤维上,于室温干燥后观察颜色和均匀度。比较结果为浸泡在金标垫处理液Ⅱ中的Ahlstrom 8964玻璃纤维干燥后的颜色(酒红色)与纯化后的免疫胶体金颜色相同,且均匀度最好;检测样品时,玻璃纤维上的胶体金探针被溶解并带动其向前移动,释放效果最好。所以本试验选用Ahlstrom8964玻璃纤维膜(经金标处理液Ⅱ处理的)为金标垫。
2.5 不同型号NC膜的选择结果
选择5种不同型号的NC膜,用NC 膜处理液于37 ℃浸泡30 min。做流速试验,Millipore HFB1350220型NC膜所用的时间最短,仅为4 min,且扩散均匀不拖带。因此,选择该型号的硝酸纤维素膜作为免疫层析载体膜。
2.6 T线及C线的优化结果
气肿疽梭菌多抗进行1 ∶4倍稀释时,效果较好(颜色清晰且无拖带现象),以1 ∶4稀释后喷于T线;羊抗鼠IgG做 1 ∶2、1 ∶4、1 ∶8稀释时,均能得到理想效果。将羊抗鼠IgG作1 ∶8稀释后喷在C线上;按2.0 μL/cm的喷膜量进行喷膜可达到较好结果,免疫层析显色较快,颜色深且清晰可辨,显色条带无中空效果。
2.7 试纸条的组装和判定
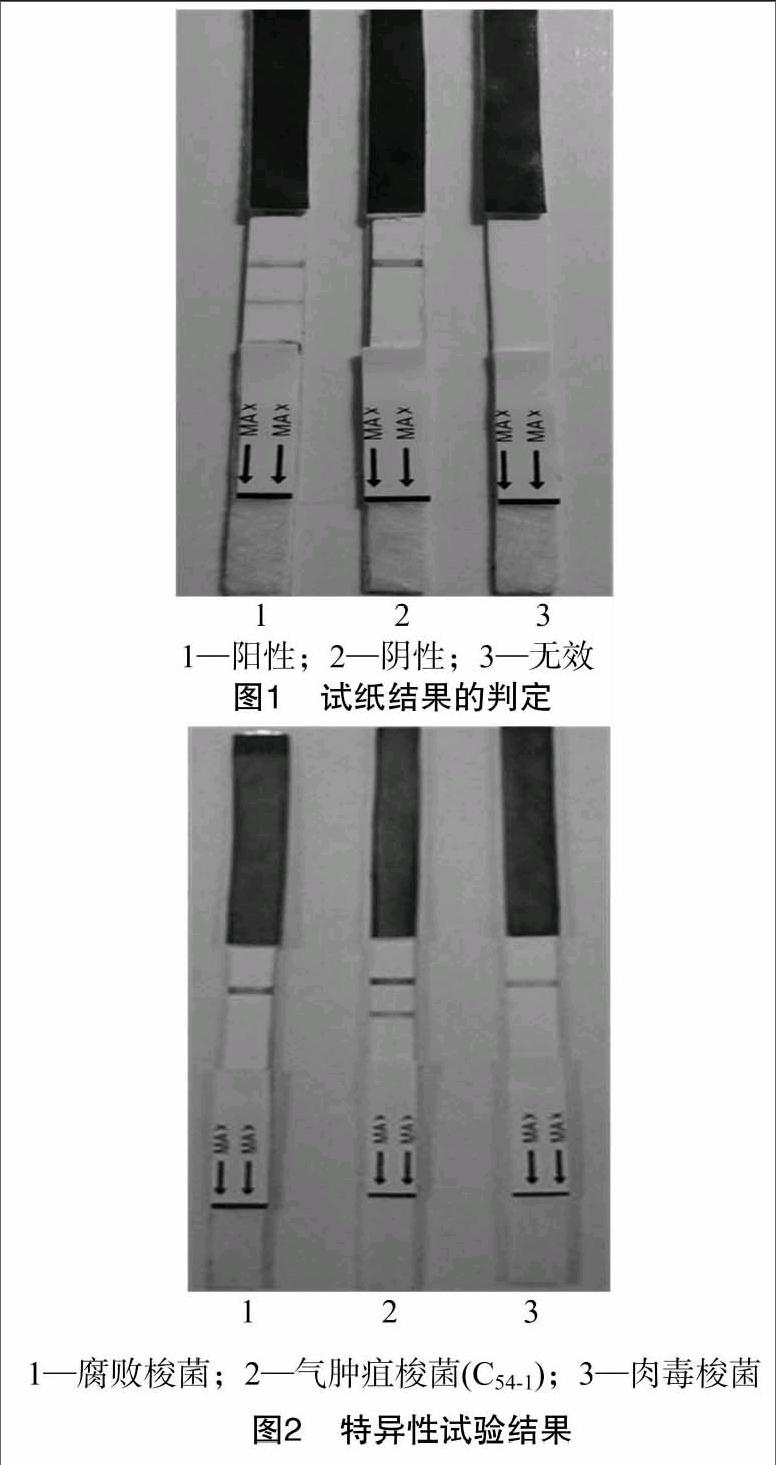
检测样品溶液,在5~10 min内观察检测结果,根据出现红色反应线的情况确定待检样液的阴性、阳性,若出现2条红色反应线则为阳性反应,只出现质控线上1条红线为阴性反应,均不显红色线则试纸条无效(图1)。
2.8 敏感性试验
将气肿疽梭菌菌液做1 ∶50、1 ∶100、1 ∶200、1 ∶400倍稀释,结果显示气肿疽梭菌菌液稀释至1 ∶100倍时,结果仍显示为阳性,检测到的菌液最低抗原量为1×105 CFU/mL。
2.9 特异性试验
用胶体金试纸条检测气肿疽梭菌(C54-1)、腐败梭菌、肉毒梭菌。检测结果显示,气肿疽梭菌呈阳性,试纸条无假阳性与交叉反应现象(图2)。
2.10 重复性试验
10条试纸条进行阴性样品检测结果显示,T线均不出条带,9条试纸条C线显现深红色带,1条的C线为浅红色带;检测阳性样品的30条试纸条,T线C线均出现红色条带,由此得出试纸条的重复性达到100%,重复性好。
2.11 稳定性试验
将试纸条密封后于室温和4 ℃环境存放,5个月内均能正常稳定显色,室温环境中于5个月后略出现胶体金探针释放不完全的现象,4 ℃条件下放置的试纸条在6个月后才出现上述现象,但特异性无变化。
3 讨论
胶体金是氯金酸的水溶胶,可以结合多种生物大分子,现已成为在免疫标记技术中1种常用的非放射性示踪剂。在1971年,Faulk和Taylor首次将胶体金颗粒用抗体来标记,在免疫化学领域中诞生了1项新技术[12]。与ELISA法相比,除了都具有较强的特异性和敏感性之外,在操作上也更加简便快速,无需复杂仪器设备且极易判断,保质期长。随着试剂盒品种和销售量的不断增长,现已发展为生产完全自动化和标准化水平。
胶体金颗粒质量除了受水质、试剂纯度等多种因素的影响之外,还与柠檬酸钠的加入以及搅拌的程度和加入速度有关。制备胶体金溶液玻璃器皿的清洁是成功制备胶体金的前提条件[13]。由胶体金的性质可知,胶体金具有不稳定性,有聚沉的可能,故制备好后尽量在20 d以内进行标记[14],不可长时间放置。在胶体金诊断试纸条的研制过程中,需要对一系列反应条件和材料进行优化和筛选。固相蛋白与NC膜的结合是重中之重,是否能获得灵敏度高、重复性好的检测结果取决于蛋白与膜的结合效果。蛋白与膜的结合力主要为疏水作用力、氢键和静电吸引力,所以在优化蛋白结合膜时应当考虑到这几种力的作用,选择不会使疏水作用力和静电引力下降的缓冲液,使之不影响蛋白结合力。喷完抗体后对NC膜做适当的干燥,使蛋白能够长期而稳定地与膜结合。本试验应用双抗体夹心法,将气肿疽梭菌多抗包被在检测线处,羊抗鼠IgG包被在质控线处,金标单克隆抗体吸附在纤维素膜固相载体上来装备试纸条,检测样品中的抗原。当待检样液中有气肿疽梭菌(C.chauvoei)时,形成“金标单抗-C.chauvoei”复合物,由于毛细虹吸作用,该复合物以及未结合的金标单抗往上走,在检测线上形成“金标单抗-C.chauvoei-多抗”复合物,因有金颗粒在此沉积,故出现肉眼可见红色条带,未结合的金标单抗继续上行,与控制线上的羊抗鼠IgG结合,又形成1条红色条带;若待检样液中不含C.chauvoei,则只出现1条红色条带,只在试纸条上端的C线上出现红色沉淀线。试验证明该试纸条的检测不仅耗时短、操作简单、灵敏度高,而且成本较低,适用于气肿疽的现场检测及鉴别诊断,可以在实践中推广使用。
参考文献:
[1]陆安法,徐官红,简廷安,等. 牛气肿疽的防制[J]. 动物医学进展,2003,24(6):131-131.
[2]Quinn P J,Carter M E,Markey B,et al. Clostridium species[M]//Clinical veterinary microbiology. London:Elsevier,1994:191-208.
[3]Timoney J F,Gillespie J H,Scott F W,et al. The genus Clostridium[M]//Hagan and Bruners microbiology and infectious diseases of domestic animals. 8th ed. New York:Cornell University Press,Comstock Publishing Associates,1988:214-240.
[4]Wierup M,Sandstedt K. Backleg and pulpy kidney disease-two actual clostridial diseases in Sweden[J]. Sv Vet Tidn,1983,35:23-24.
[5]Sasaki Y,Yamamoto K,Kojima A,et al. Rapid identification and differentiation of pathogenic clostridia in gas gangrene by polymerase chain reaction based on the 16S-23S rDNA spacer region[J]. Research in Veterinary Science,2000,69(3):289-294.
[6]Moussa R S. Antigenic formulae for Clostridium septicum and Clostridium chauvoei[J]. The Journal of Pathology and Bacteriology,1959,77(2):341-350.
[7]Songer J G. Clostridial diseases of small ruminants[J]. Veterinary Research,1998,29(3/4):219-232.
[8]Sathish S,Swaminathan K. Molecular characterization of the diversity of Clostridium chauvoei isolates collected from two bovine slaughterhouses:analysis of cross-contamination[J]. Anaerobe,2008,14(3):190-199.
[9]Hatheway C L. Toxigenic clostridia[J]. Clinical Microbiology Reviews,1990,3(1):66-98.
[10]Vilei E M,Johansson A,Schlatter Y,et al. Genetic and functional characterization of the NanA sialidase from Clostridium chauvoei[J]. Veterinary Research,2011,42(1):2.
[11]楊小姣.胶体金免疫层析快速检测氯霉素技术研究[D]. 杨凌:西北农林科技大学,2007.
[12]Faulk M P,Taylor G M.An Immunocolloid method for the electron microscope[J]. Immunochemistry,1971,8(11):1081-1083.
[13]Chandler J,Gurmin T,Robinson N. The place of gold in rapid tests[J]. IVD Technology,2000,6(2):37-49.
[14]蒲 丹. SARS病毒重组核衣壳蛋白胶体金试纸条研制和临床验证[D]. 重庆:重庆医科大学,2004.

