通窍耳聋丸的质量标准研究
王艺纯+唐秋竹

[摘要]目的 建立通窍耳聋丸的质量控制标准。方法 对通窍耳聋丸中各味药材进行显微鉴别,并对柴胡、龙胆进行薄层色谱鉴别;采用HPLC法测定龙胆苦苷含量。采用Phenomenon Luna C18柱(4.6 mm×250 mm,5 μm);流动相为甲醇-水(25∶75);流速为0.8 ml/min;检测波长270 nm;柱温35℃。结果 显微鉴别特征专属,薄层色谱斑点清晰阴性对照无干扰;龙胆苦苷在0.091~0.912 μg与峰面积呈良好的线性关系(r=0.9999,n=6);平均回收率为99.9%(n=6),RSD=1.2%。结论 本方法易于操作,结果准确,重现性良好,可用于通窍耳聋丸制剂的质量控制。
[关键词]通窍耳聋丸;质量控制;显微鉴别;薄层色谱;高效液相色谱法
[中图分类号] R927.11 [文献标识码] A [文章编号] 1674-4721(2017)01(c)-0115-03
[Abstract]Objective To establish quality control standards for Tongqiao Erlong Pills.Methods Microscopical identification was used to qualitative of material medcine prescription,thin layer chromatography (TLC) method were established to identify Bupleuri Radix and Gentianae Radix et Rhizoma,gentiopicroside was determined by HPLC with Phenomenon Luna C18 column (4.6 mm×250 mm,5 μm) used with the mobile phase of mthanol-water (25∶75) at a flow rate of 0.8 ml/min.The detecting wavelength was 270 nm,the column temperature was 35℃.Results Microscopic identification features were exclusive.The spots of TLC were clear and the negative control without interference.The linear range of gentiopicroside was 0.091-0.912 μg(r=0.9999,n=6) with a great linear relationship.The mean recovery rates were 99.9% (n=6),RSD equal to 1.2%.Conclusion This method is simple,rapid,reproducible,precise,reliable and accurate.It can be used for the quantification of Tongqiao Erlong Pills.
[Key words]Tongqiao Erlong Pills;Quality control;Microscopical;Thin layer chromatography;HPLC
通窍耳聋丸由北柴胡、龙胆、芦荟、熟大黄、黄芩、青黛、天南星(矾炙)、木香、青皮(醋炙)、陈皮、当归、栀子(姜炙)12种中药材组成,具有泻火清肝,润便通窍之功效。临床使用病症为肝经热盛,头目眩晕,耳聋蝉鸣,耳底肿痛,目赤口苦,胸膈满闷,大便燥结[1]。通窍耳聋丸现行法定标准收载于《卫生部药品标准》第1册仅有性状及检查项,不能很好地控制其质量。本试验增加了通窍耳聋丸各味药材的显微鉴定,并对龙胆及柴胡进行了薄层色谱鉴别[2-3]。采用HPLC法对方中君药龙胆进行了含量测定[4]。
1仪器与试药
生物显微镜显微镜(日本尼康公司,型号80I,視场22 mm/25 mm);薄层色谱数码相机成像系统(瑞士卡玛公司,型号CAMCAG,光源频率:25~30 kHz);高效液相色谱仪(美国安捷伦公司,型号:1200系列,在线脱气,四元泵,自动进样,DAD检测器);赛多利斯BT-125D电子天平(美国赛多利斯公司,型号:BT125D,1/100 000天平);AE-160电子天平(梅特勒-托利多测量技术有限公司,型号:AE160,1/10 000天平);超纯水机(法国密理博公司,型号:Milli-Q,产水电阻率:>18.2 MΩ·cm)。
龙胆苦苷对照品(中国食品药品检定研究院,批号:110770-201013)、龙胆对照药材(中国食品药品检定研究院,批号:121530-200501)、柴胡对照药材(中国食品药品检定研究院,批号:120992-201108);甲醇(Fisher Scientific,色谱纯),水为超纯水(临用新制),其他试剂试药均为优级纯。
2方法与结果
2.1显微特征鉴别
取通窍耳聋丸,研细,取粉末适量,加水合氯醛透化,置显微镜下观察各药味的显微鉴别特征,结果见图1。
黄芩:纤维淡黄色,梭形,壁厚,孔沟细(图1A)。柴胡:油管含淡黄色或黄棕色条状分泌物(图1B)。木香:木纤维成束,长梭形,直径14~26 μm,纹孔口横裂缝状、十字状或人字状(图1C)。青黛:不规则块片或颗粒蓝色(图1D)。熟大黄:草酸钙簇晶大,直径60~140 μm(图1E)。栀子:种皮石细胞黄色或淡棕色,多破碎,完整者长多角形、长方形或形状不规则,壁厚,有大的圆形纹孔,胞腔棕红色(图1F)。陈皮:草酸钙方晶成片存在于无色薄壁组织中(图1G)[5]。
2.2薄层色谱鉴别
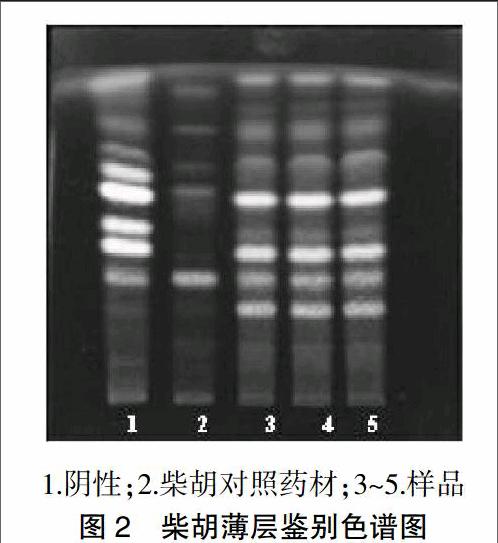
2.2.1柴胡的薄层色谱鉴别
2.2.1.1供试品溶液的制备 取通窍耳聋丸样品5 g,研细,加入甲醇约50 ml,超声波提取30 min,滤过,滤液蒸干,蒸干后的残渣加2%氢氧化钠溶液20 ml,加热使溶解,分次转移至分液漏斗中,用水饱和的正丁醇强力振摇提取2次,每次20 ml,合并正丁醇液,蒸干。蒸干后的残渣再加水5 ml使溶解,溶解后样品通过D101型大孔吸附树脂柱(内径为1.5 cm,柱高为12 cm),分别用水80 ml洗脱,水液弃去,再用80 ml 20%的乙醇洗脱,洗脱液弃去,最后用100 ml 70%的乙醇洗脱,洗脱液置80℃水浴上蒸干,蒸干后的残渣用2 ml甲醇溶解,作为供试品溶液[6]。
2.2.1.2对照药材溶液的制备 柴胡对照药材粉末0.5 g,加入约20 ml甲醇,超声波提取10 min,滤过,滤液蒸干,蒸干后的残渣加2%氢氧化钠溶液20 ml,加热使溶解,分次转移至分液漏斗中,用水饱和的正丁醇强力振摇提取2次,每次20 ml,合并正丁醇液,蒸干。蒸干后的残渣再加水5 ml使溶解,溶解后样品通过D101型大孔吸附树脂柱(内径为1.5 cm,柱高为12 cm),分别用水80 ml洗脱,水液弃去,再用80 ml 20%的乙醇洗脱,洗脱液弃去,最后用100 ml 70%的乙醇洗脱,洗脱液置80℃水浴上蒸干,蒸干后的残渣用2 ml甲醇溶解,作为对照药材溶液。
2.2.1.3阴性样品的制备 按通窍耳聋丸的处方组成、工艺及制法制成缺柴胡的阴性样品5 g,按供试品溶液制备方法,同法制成阴性样品。
2.2.1.4试验方法 吸取上述供试品、对照药材及阴性样品溶液各3 μl,以条带状点样法点于同一以羧甲基纤维素钠为黏合剂制备的硅胶G薄层板上,三氯甲烷-甲醇-水(30∶10∶1)作为展开剂,置于双槽展开缸内,预饱和20 min,展开,取出,晾干,以2%对二甲氨基苯甲醛的40%硫酸溶液作为显色剂,并在置于105℃的烘箱内加热至斑点显色清晰,分别于日光及紫外光灯(365 nm)下检视。
2.2.1.5结果判定 供试品色谱中,在与柴胡对照药材色谱相应的位置上,显相同的红色斑点及相同颜色的荧光斑点,斑点显色清晰,且阴性样品无干扰,证明该方法可行。结果见图2。
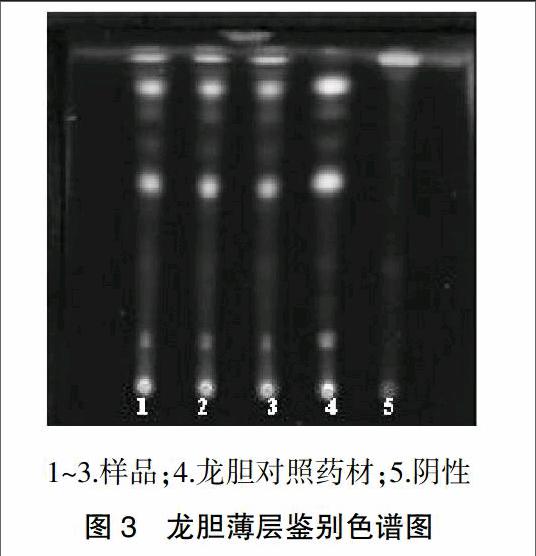
2.2.2龙胆的薄层鉴别
2.2.2.1供试品溶液的制备 取通窍耳聋丸样品5 g,研细,加10 ml 17%氨溶液润湿,加30 ml二氯甲烷,超声提取15 min,滤过,蒸干,残渣加2 ml二氯甲烷溶解,即得[7-9]。
2.2.2.2对照药材溶液的制备 取龙胆对照药材0.5 g,加17%氨溶液1 ml润湿,加10 ml二氯甲烷,超声提取15 min,滤过,蒸干,残渣加1 ml二氯甲烷溶解,即得。
2.2.2.3阴性样品的制备 按通窍耳聋丸的处方组成、工艺及制法制成缺龙胆的阴性对照样品5 g,按“2.2.2.1”项下方法制备,即得。
2.2.2.4试验方法 吸取上述供试品、对照药材及阴性样品溶液各5 μl,分别点于同一以羧甲基纤维素钠为黏合剂制备的硅胶G薄层板上,二氯甲烷-乙醇(15∶1.5)作为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。
2.2.2.5结果判定 供试品色谱中,在与对照药材色谱相应的位置上,显相同绿色荧光斑点。斑点清晰,且阴性样品无干扰,证明该法可行。结果见图3。
2.3龙胆苦苷的含量测定
2.3.1色谱条件与系统适用性试验
色谱柱:Phenomenon Luna C18(4.6 mm×250 mm,5 μm);流动相:甲醇-水(25∶75);检测波长:270 nm;流速:0.8 ml/min;柱温:35℃;进样量:10 μl。在上述条件下龙胆苦苷与其他组分色谱峰可基线分离,与相邻峰分离度均>1.5,按龙胆苦苷峰计算理论板数≤3000。
2.3.2溶液的制备及样品测定
2.3.2.1供试品溶液的制備 取通窍耳聋丸样品10 g,研细,取约1 g,精密称定,置于具塞锥形瓶中,用移液管精密加入20 ml甲醇,称定重量,置于90℃水浴上加热回流15 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,即得[10-15]。
2.3.2.2对照品溶液的制备 取龙胆苦苷对照品10 mg,用1/100 000天平精密称定,转移至100 ml容量瓶中,加甲醇适量使对照品溶解,用甲醇稀释至刻度,即得每1毫升含0.2 mg的龙胆苦苷对照品溶液。
2.3.2.3阴性对照溶液的制备 按通窍耳聋丸的处方组成、工艺及制法制成缺龙胆的阴性对照样品,按上述供试品溶液制备方法,制得阴性对照样品溶液。依正文所述方法进行测定。结果龙胆阴性样品色谱在与龙胆苦苷相应的保留时间附近无干扰峰检出,证明阴性无干扰(图4~6)。
2.3.2.4线性范围的考察 分别精密吸取按上述方法配制好的对照品溶液(浓度为每1毫升溶液含0.0912 mg龙胆苦苷)1、2、4、6、8、10 μl测定,以对照品进样量(x,μg)作为横坐标,以龙胆苦苷峰面积(y)作为为纵坐标,按照偏最小二乘法绘制标准曲线,得到龙胆苦苷进样量与峰面积的线性回归方程为y=2365.09x-4.168(r=0.9999)。结果表明龙胆苦苷在0.091~0.912 μg范围内进样量与峰面积之间具有较好的线性关系,满足外标法进行含量测定的需求。
2.3.2.5精密度试验 精密吸取供试品溶液10 μl,注入液相色谱仪,重复6次,测定其色谱峰面积值,结果其龙胆苦苷峰面积积分值RSD为0.64%,提示所使用的液相色谱仪器进样精密度良好。
2.3.2.6稳定性试验 取同一份供试品溶液,分别考察0、3、6、12、24 h龙胆苦苷峰面积,结果龙胆苦苷峰面积积分值稳定,结果提示该方法制备的供试品溶液在24 h内基本稳定。
2.3.2.7重复性试验 取同一供试品(长春人民药业有限公司,批号:20130406)6份依“2.3.1.1”项下方法提取,进行测定,结果RSD=2.0%,说明本法重复性良好。
2.3.2.8加样回收率试验 采取半量加样回收率测定法,取已知含量的供试品(长春人民药业有限公司,批号:20130406,含龙胆苦苷1.44 mg/g)0.5 g,共6份,分别置具塞锥形瓶中,精密量取龙胆苦苷对照品的甲醇溶液(0.0392 mg/ml)20 ml,依法测定回收率,结果测得龙胆苦苷的平均回收率为99.9%,RSD=1.2%。结果提示本法回收率较好,准确度较高(表1)。
2.3.2.9样品的测定 依正文方法测定9批样品,结果见表2。
3讨论
3.1检测波长的选择
以甲醇溶液为空白,采用1 cm比色池,经紫外-可见分光光度计对龙胆苦苷的甲醇溶液在200~800 nm范围内的吸收度进行扫描,结果龙胆苦苷对照品在272.0 nm波长处有最大吸收,并且同时参考《中国药典》2015年版一部龙胆药材项下的龙胆苦苷的测定方法,选择270 nm为本实验的测定波长。
3.2流动相的选择
参照《中国药典》2015年版一部龙胆项下含量测定方法,采用甲醇∶水(25∶75)为流动相,结果龙胆苦苷与其他色谱峰的分离度均>2.0,且龙胆苦苷色谱峰出峰时间适中。决定采用甲醇∶水(25∶75)作为本试验的流动相。
3.3质量分析评价
通窍耳聋丸现行质量标准不能有效控制本制剂质量。笔者对方中君药龙胆中主成分龙胆苦苷进行了含量测定,并采用显微鉴定和薄层色谱鉴别的方式对方中多数药材进行了鉴别。与原标准比较,本试验可以更好地控制通窍耳聋丸的质量,并为继续研究本制剂的质量控制方法提供了基础。
[参考文献]
[1]卫生部药典委员会.卫生部药品标准中药成方制剂(第一册)[M].北京:卫生部药典委员会出版社,1989:124.
[2]谢东浩,贾晓斌,安益强,等.春柴胡与药典柴胡薄层色谱的比较[J].时针国医医药,2007,18(6):1334-1335.
[3]吴立宏,叶燕,王峥涛.改进《中国药典》2005年版龙胆薄层色谱鉴别方法的建议[J].中国药品标准,2007,8(4):8-9.
[4]国家药典委员会.中国药典[M].2010年版第一增补本.北京:中国医药科技出版社,2012:15.
[5]国家药典委员会.中药材显微鉴别彩色图鉴[M].北京:人民卫生出版社,2008:371.
[6]刘颖,胡琴,陶志国.龙胆泻肝颗粒质量标准研究[J].中成药,2003,35(12):2661-2666.
[7]赵昱玮,于森,司学玲,等.炎热清片中龙胆苦苷的薄层鉴别及含量测定[J].中国实验方剂学杂志,2013,19(3):118-120.
[8]赵顺,孙辉,丁野,等.龙胆泻肝丸(大蜜丸)薄层色谱鉴别方法的建立[J].中国药师,2015,18(1):151-153.
[9]李海兵,张霞,周永妍,等.龙胆配方颗粒的质量标准研究[J].中国药房,2016,27(15):2097-2099.
[10]王琳琳,宋新波,李薇,等.龙胆中龙胆苦苷的分离纯化[J].现代中药研究与实践,2013,27(5):38.
[11]王文月,刘志宏,黄爱文,等.双波长HPLC法测定酸性龙胆合剂中龙胆苦苷和橙皮苷的含量[J].中国药房,2015, 26(9):1241-1243.
[12]徐秋霞,李小芳,舒予,等.干燥方法对龙胆炮制品中龙胆苦苷含量的影响[J].中国药房,2013,24(7):622.
[13]敖茂宏,宋智琴.黔产龙胆不同部位中龙胆苦苷的含量测定[J].西南农业學报,2010,23(5):773.
[14]冯波,朱鹤云,关皎,等.HPLC同时测定龙胆中4种活性成分含量[J].中国实验方剂学杂志,2013,19(13):82.
[15]刘瑞新.HPLC同时测定龙胆泻肝丸中龙胆苦苷和栀子苷的含量[J].中成药,2007,29(8):1170-1172.
(收稿日期:2016-10-15 本文编辑:方菊花)

