塞来昔布在中国治疗骨关节炎的成本效果研究Δ
Bruce C.M.Wang,谢小平,Wesley Furnback,Ronald Caldwell[.亦熙有限公司,纽约 005,美国;.辉瑞投资有限公司(北京分公司),北京 0000;.密歇根大学,密歇根安娜堡 4809,美国]
·药物经济学·
塞来昔布在中国治疗骨关节炎的成本效果研究Δ
Bruce C.M.Wang1*,谢小平2,Wesley Furnback1,Ronald Caldwell3[1.亦熙有限公司,纽约 10053,美国;2.辉瑞投资有限公司(北京分公司),北京 100010;3.密歇根大学,密歇根安娜堡 48109,美国]
目的:评估塞来昔布在中国治疗骨关节炎(OA)的成本效果。方法:采用英国国家卫生与临床优化研究所开发的一种OA成本-效果分析模型结构,对照药包括塞来昔布和双氯芬酸+质子泵抑制剂(PPIs);不良事件的相对风险来自CONDOR试验。以质量调整生命年(QALY)计量有效性;每年以折现率4.76%折减成本和QALY。结果:塞来昔布的成本为$3 591,QALY为8.826年;双氯芬酸+PPIs的成本为$3 674,QALY为8.830年。塞来昔布相对于双氯芬酸+PPIs的增量成本和增量QALY分别为$-83和-0.004 QALY。双氯芬酸+PPIs相对于塞来昔布的增量成本效果比(ICER)为$23 258/QALY。单因素敏感度分析和概率敏感度分析结果显示,药物成本是ICER的主要驱动因素,且两种治疗方案的结果相似。结论:塞来昔布是一种成本低于双氯芬酸+ PPIs的替代药物。两种用药方案之间的QALY差异非常小,因此塞来昔布可能是OA患者更具成本效果优势的选择。
骨关节炎;塞来昔布;双氯芬酸;质子泵抑制剂;成本效果;药物经济学
骨关节炎(Osteoarthritis,OA)是一种关节疾病,以关节磨耗及损伤为特征,最常见于手、颈、腰、膝和髋部。基于不同的定义、累及部位和人群特征等,OA的患病率数据有所差异。例如,45岁及以上成年人的放射学膝盖OA患病率为19.2%~27.8%[1];在山西省农村地区,估计16岁以上居民的OA患病率为24.3%[2]。国外有研究表明,每名患者的OA平均直接医疗成本为$2 600[3],给家庭和社会带来沉重负担;另一方面,OA的间接成本也较高,因为OA会导致患者的劳动能力丧失和生活质量下降[4]。
对OA的治疗通常包括改变生活方式(如减轻体质量、康复治疗和其他支持措施等)、药物治疗[如非甾体抗炎药(Nonsteroidal anti-inflammatory drugs,NSAIDs),包括环氧合酶2(COX-2)抑制剂等]及手术治疗(如椎板切除术、截骨术和全关节置换术等)[5]。其中,药物治疗是最为常见的一种治疗方式,所接受的人群也最多。但不可避免的是,OA的药物治疗也可能会带来一些风险,如胃肠道不良事件(Adverse events,ADEs)或心血管影响等。有研究报道,美国每年有3万余例非选择性NSAIDs所致的消化道(Gastrointestinal,GI)出血住院或死亡病例;而选择性COX-2抑制剂类药物可能与充血性心力衰竭风险增高相关[6],但由其导致的GI事件风险较非选择性NSAIDs更低[7-8]。
药物经济学是应用经济学原理和方法来研究和评估药物治疗的成本与效果的学科,可以通过更全面的视角分析对比不同药物治疗方案的优劣,协助设计合理的临床用药方案,保证有限的社会卫生保健资源发挥最大的效用。本研究中,笔者采用成本-效果分析法,比较了在OA治疗领域非选择性NSAID双氯芬酸[+质子泵抑制剂(PPIs)]与选择性COX-2抑制剂塞来昔布的风险、成本和疗效,希望能从药物经济学角度为临床医师、药师及保险支付方提供一定借鉴。
1 资料与方法
1.1 模型构建
本研究所用模型遵循用于提交给英国国家卫生与临床优化研究所(The National Institute for Health and Care Excellence,NICE)的OA成本-效果分析模型结构。此模型以医疗服务支付者为分析角度,分析了非选择性NSAIDs和选择性COX-2抑制剂治疗OA的疗效、成本、可能的ADEs,以及非选择性NSAIDs与PPIs联用时ADEs的减少情况。模型中包括的ADEs为:GI症状/消化不良;严重的GI事件(症状性溃疡、合并GI出血);心血管(Cardiovascular,CV)事件(心肌梗死、卒中、心力衰竭)等。患者发生严重GI或CV事件时,将默认停止相应的OA药物治疗。由于非选择性NSAIDs和选择性COX-2抑制剂主要用于控制OA症状,不影响手术时间,因此该模型并未考虑OA手术的成本和效果等信息。
此模型已于2012年更新并纳入来自CONDOR试验的数据结果[9],已在多个国家有所应用。CONDOR试验是一项针对32个国家196个研究中心的类风湿性关节炎或OA患者开展的为期6个月的双盲、随机试验。入选该试验的两组患者被分别给予塞来昔布200 mg,bid或双氯芬酸75 mg,bid+奥美拉唑20 mg,qd。研究发现两组患者在上GI和下GI事件的发生率方面有所差异[10]。
从模型结构上看,此模型是合并了与每种健康状态相关的决策树模型和Markov模型[11]。决策树模型是常用的一种反映不同治疗路径随时间变化而产生各种健康结果的动态模型,而本研究中主要比较两条治疗路径(塞来昔布vs.双氯芬酸+PPIs)对应的特定的健康事件发生概率。在模型中,这种概率的评估来自随机对照临床试验(Randomized clinical trial,RCT)数据或真实世界的观察性数据。依据采用的不同治疗方案和患者是否已处于后事件状态(如果之前已发生过某种事件,则再发的概率会高于常人),患者在决策树内发生ADEs的概率有所差异。决策树模型的优点是非常直观地提供各种可能的结果,适合短期内有确定结果的疾病;但不易反映长期健康获益和复发事件的发生情况。Markov模型是一种循环决策树,它将OA按其对健康的影响程度划分为几个不同的健康状态:死亡、无任何并发症或发生ADEs(如消化不良、症状性溃疡、合并GI事件、心肌梗死、卒中和心力衰竭)。对于每种Markov健康状态,患者都可能面临年龄特异性死亡或在不同的状态间发生转换;模型根据各状态在一定时间内相互间的转换概率,结合每个状态上的资源消耗和健康结果,通过循环运算,估计出OA疾病发展的健康结局及费用。为更好地模拟疾病的发生概率和不同疾病状态间的转换,首先需要得知本地化人群健康风险(健康风险是指人群面对不同危险因素时发生某种疾病或健康事件的概率),详见表1。本模型中,相关疾病的风险数据源自CONDOR试验[9],而中国相关数据来自世界卫生组织(World Health Organization,WHO)生命表和国内文献研究。

表1 本地化人群健康风险Tab 1 Localized population health risks
注:*国内消化不良的风险缺少权威数据,此处沿用英国NICE模型中默认数据
Note:*domestic dyspepsia risk lack of anthority data,and default data of British Nice model is used
1.2 成本的确定
此模型所涉及的成本主要包括药物成本、医疗服务成本以及ADEs治疗成本,未考虑疾病所导致的间接成本(如OA引起的劳动力丧失、家人照护损失的成本等)。本研究中的药物价格见表2,医疗服务价格及ADEs管理成本见表3。

表2 药物价格Tab 2 Drug price
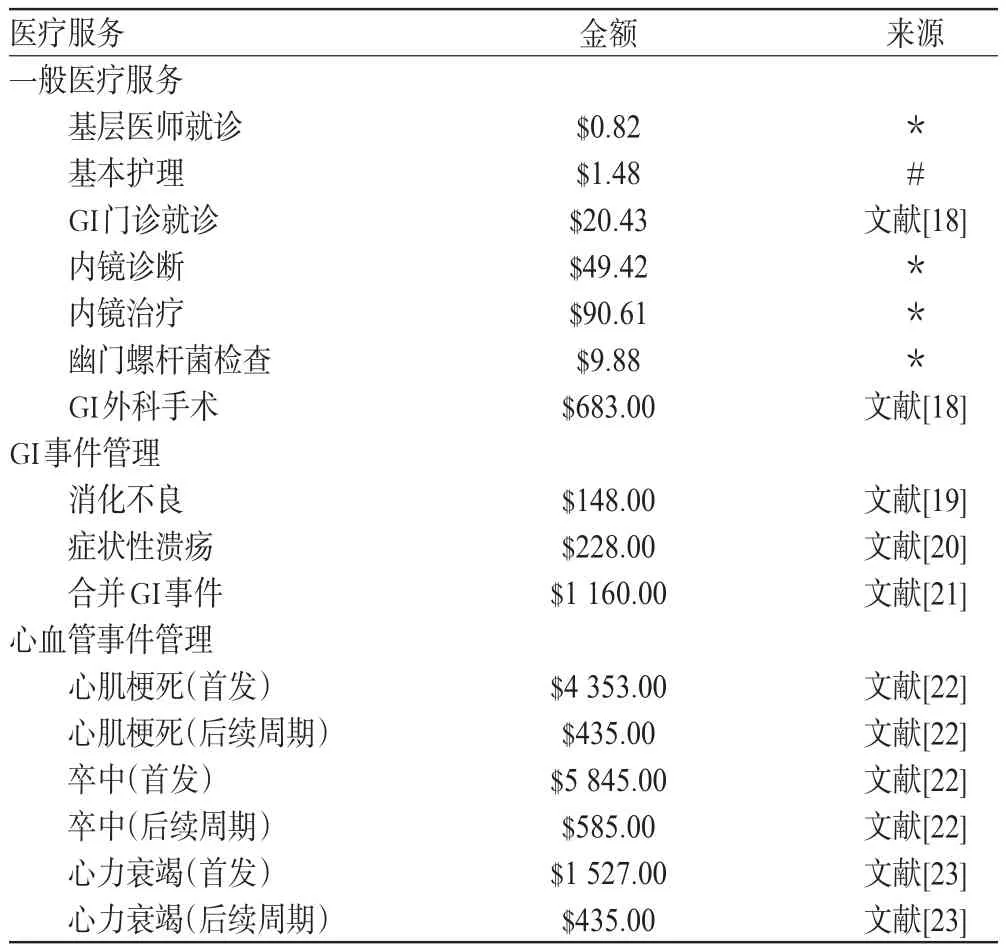
注:*数据来源于北京市发展和改革委员会;#数据来源于2010年10月20日《北京晨报》Note:*data from Beijing Municipal Commission of Development and Refom;#data from Beijing Morning Post issued on Oct.20th,2010
表2和表3中报告的所有成本以美元计算(1美元=6.07元人民币)[24]。使用下列转换公式[11],由CONDOR研究中的西安大略和麦克马斯特大学OA指数(Western Ontario and McMaster Universities Arthritis Index,WOMAC)分数转为欧洲五维健康量表(EQ-5D)分数并计算效用:EQ-5D=0.752 6+0.000 4WOMAC-0.000 1 WOMAC^2。
1.3 产出结果指标的确定
此模型的主要产出结果指标为增量成本效果比(Incremental cost-effectiveness ratio,ICER),该指标由两个治疗组间成本差异和质量调整生命年(Quality adjusted life year,QALY)差异相除获得;计算得到ICER后,通过与某阈值(或界值)比较来评判治疗方案的经济性。该阈值在一些发达国家通常有确定的标准,在发展中国家通常采用3倍(或者更低)人均国内生产总值(GDP)[25]为标准。从根本上讲,这一阈值体现了社会为多获得一个健康生命年而愿意支付的成本。如果研究计算所得ICER小于此阈值,则表明用增量成本所换取的增量效果是经济的;反之,如果计算所得ICER大于此阈值,则认为该治疗方案相对于比较对象而言可能不具备经济学优势。
1.4 敏感度分析及其他
在本研究中,针对主要参数进行了单因素敏感度分析(One-way sensitivity analysis,OWSA)和概率敏感度分析(Probabilistic sensitivity analysis,PSA),以便检验模型结果的稳定性。OWSA是针对关键变量在±10%范围内分别取值,观察分析结果的变化。各参数的分布与此前英国NICE模型的参数分布相同[10]。PSA是指通过分析不确定因素的概率分布,计算在这些不同的概率分布条件下经济学评价指标的期望值,从而检验评估结果的稳定性。
本研究还对模型的应用基础做了一些假设:结合流行病学信息,模型中以55岁OA患者为基准;Markov模型的模拟周期长度为3个月;模拟的患者年龄最高至100岁;成本和QALY均按4.76%折现,这也是《中国药物经济学评价指南》推荐方法计算所得的折现率[26]。
2 结果
2.1 成本和QALY
以55岁患者为例,基于一般治疗情形下模型模拟的结果显示,塞来昔布治疗组的人均治疗成本和QALY分别为$3 591和8.826年;双氯芬酸+PPIs治疗组的人均成本和QALY分别为$3 674和8.830年。塞来昔布的成本比双氯芬酸+PPIs低约$83;两种治疗方案带来的QALY差异较小(0.004年),相应的ICER为$23 258/QALY,约合141 176元/QALY。
2.2 敏感度分析
2.2.1 OWSA 为检验一些关键变量的变化(±10%)对模型结果稳定性的影响,本研究开展了一系列OWSA,结果见图1。图1中显示,模型的ICER对评估中所用药物的成本最敏感:若奥美拉唑的平均成本从$30.69变化为$37.51,则模型产生的ICER范围将会从$18 853变为$27 664,跨度约$8 811;塞来昔布和双氯芬酸的药物成本导致的ICER变化跨度分别为$4 808和$3 272。此外,仅次于药物成本,ADEs成本对ICER也会有一定影响。但总体来看,模型所得的ICER大多高于中国2013年人均GDP(41 908元)[27]的3倍,这意味着从卫生经济学角度来看,并不能认为双氯芬酸+PPIs更具成本效果,相反塞来昔布可能会是更优的方案。
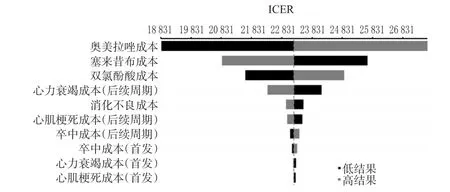
图1 OWSA结果(默认值±10%%)Fig 1 Results of OWSA(base case estimates±10%%)
2.2.2 PSA 1 000次模拟的PSA散点图和成本效果可接受曲线(Cost effectiveness acceptance curve,CEAC)分别见图2、图3。图2中显示,大多数模拟情况下塞来昔布的成本均低于双氯芬酸+PPIs,相对而言两组方案在QALY差异分布方面的概率较为弥散,但总体上双氯芬酸+PPIs的方案有较大的可能性在QALY上长于塞来昔布方案。图3中的CEAC相对平滑,可以看出若支付意愿的阈值为$10 000/QALY,则塞来昔布有约85%的可能性具有成本效果优势;若支付意愿的阈值为$15 000/ QALY,则塞来昔布有约75%的可能性具有成本效果优势;若支付意愿达到$20 000/QALY,塞来昔布仍有接近65%的可能性具有成本效果优势。参考WHO推荐的阈值设定,可以认为在OA治疗方面,相对于双氯芬酸+ PPIs,塞来昔布有可能更符合药物经济学的选择。
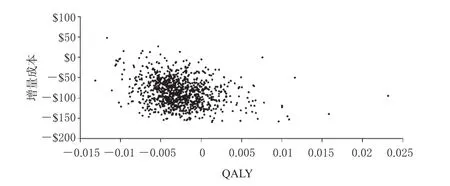
图2 塞来昔布相对于双氯芬酸+PPIs的PSA散点图(1 000次模拟)Fig 2 PSA scatter plot of celecoxib to diclofenac+PPIs(1 000 times of simulation)
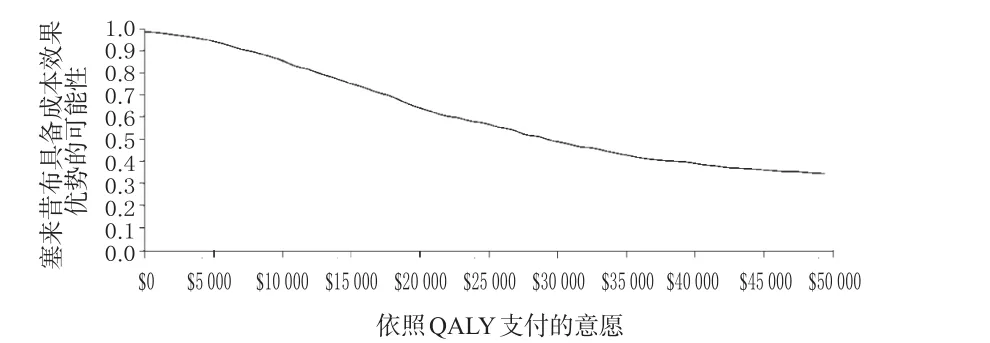
图3 塞来昔布相对于双氯芬酸+PPIs的CEACFig 3 CEAC of celecoxib to diclofenac+PPIs
3 讨论
本文是首次针对中国国内塞来昔布治疗OA的成本效果研究,所得结果类似于其他国家的研究。一项在瑞典采用提交给NICE的OA成本-效果分析模型的研究提示,塞来昔布+PPIs相对于双氯芬酸+PPIs更具有成本效果,ICER=$12 000[28]。一项在阿尔及利亚使用相同模型结构的为期6个月的研究显示,塞来昔布的成本略高于双氯芬酸+PPIs,但QALY更高,ICER=$20 500[29]。另一项使用相似模型结构的研究发现,塞来昔布在巴西和墨西哥的高风险人群中是一种节省成本的策略;而在哥伦比亚、阿根廷和哥斯达黎加,相对于双氯芬酸,塞来昔布是一种具有成本效果优势的选择[30]。
本研究结果显示,双氯芬酸+PPIs治疗OA的效果可能略高于塞来昔布,但治疗成本也比较昂贵,ICER=$23 258,大于2~3倍人均GDP[27],因此倾向于认为塞来昔布可能是更符合成本效果的选择方案;敏感度分析结果支持此结论。本研究结果可能有助于政策制定者在药品准入和报销方面的决策,并有助于医师和药师为患者提出更适当的治疗建议。
本研究也有一定局限性。第一,本研究从支付者的角度开展,因此未纳入与患病率和病死率相关的间接成本,如丧失的劳动力的价值、照护者的时间成本和交通费用等。第二,本研究中ADEs的相对风险来自CONDOR试验,这是一项全球研究,并非专用于中国。虽然笔者已使用本地数据更新了总体人群风险,但是仍需要进一步的分析以更好地确定相对风险。第三,本研究采用的模型基于临床试验,因此临床试验的局限性也反映在本研究中。如:试验中排除了服用阿司匹林的患者,而阿司匹林可能对GI和CV事件都有影响。又如:本试验的效力不足以显示CV事件间的差异,因此需要慎重解读两组间的风险比[9]。第四,随着近年来OA治疗领域引入更新的药物,研究人员可能需要改善模型以允许进行更多药品之间的比较。此模型的其他局限性可参见文献[10]。笔者将开展进一步研究,以逐步解决上述局限点。
4 结语
药物经济学研究最主要的目的之一是促进合理、有效地利用药物资源[31]。本研究采用一种决策分析模型评价塞来昔布相对于双氯芬酸+PPIs治疗OA的成本效果,所用模型基于提交给NICE的OA成本效果分析模型,并进行本土化更新,以反映在中国的成本和流行病学信息。结果显示,塞来昔布的成本低于双氯芬酸+ PPIs,且QALY略低但差异较小。敏感度分析结果显示,药物的成本是ICER的主要驱动因素;PSA模拟显示两种治疗方案的结果相似。综合来看,对于中国OA患者而言,塞来昔布可能是更具成本效果优势的选择。
[1] Zhang Y,Jordan JM.Epidemiology of osteoarthritis[J].Clin Geriatr Med,2010,26(3):355-369.
[2] Zhang JF,Song LH,Wei JN,et al.Prevalence of and risk factors for the occurrence of symptomatic osteoarthritis in rural regions of Shanxi Province,China[J].Int J Rheum Dis,2016,73(8):287-297.
[3] Gabriel SE,Crowson CS,Campion ME,et al.Direct medical costs unique to people with arthritis[J].J Rheumatol,1997,24(4):719-725.
[4] Woo J,Lau E,Lee P,et al.Impact of osteoarthritis on quality of life in a Hong Kong Chinese population[J].J Rheumatol,2004,31(12):2433-2438.
[5] Singh R,Vohra K,Kalra HS.Osteoarthritis(OA)[EB/OL]. [2015-12-11].https://www.lap-publishing.com.
[6] Mamdani M,Juurlink DN,Lee DS,et al.Cyclo-oxygenase-2 inhibitors versus non-selective non-steroidal anti-inflammatory drugs and congestive heart failure outcomes in elderly patients:a population-based cohort study[J].Lancet,2004,363(9423):1751-1756.
[7] Bombardier C,Laine L,Reicin A,et al.Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis.VIGOR Study Group [J].N Engl J Med,2000,343(21):1520-1528.
[8] Blower AL,Afenn GCB,Hill A,et al.Emergency admissions for upper gastrointestinal disease and their relation to NSAID use[J].Aliment Pharmacol Ther,1997,11(2):283-291.
[9] Brereton N,Winn B,Akehurst R.The cost-effectiveness of celecoxib vs diclofenac in the treatment of osteoarthritis in the UK;an update to the NICE model using data from the CONDOR trial[J].Raven Press,1984,19(15):465-472.
[10] Chan FK,Lanas A,Scheiman J,et al.Celecoxib versus omeprazole and diclofenac in patients with osteoarthritis and rheumatoid arthritis(CONDOR):a randomised trial [J].Lancet,2010,376(9736):173-179.
[11] National Collaborating Centre for Chronic Conditions(NCCCC)on behalf of the National Institute for Health and Clinical Excellence.Osteoarthritis:National clinical guideline for care and management in adults[M].London:Royal College of Physicians,2008:Appendix D.
[12] 刁萍萍,杜奕奇,李兆申.NSAIDs与消化性溃疡出血的研究进展[J].实用临床医学,2007,8(7):135-136.
[13] Li Z,Zou D,Ma X,et al.Epidemiology of peptic ulcer disease:endoscopic results of the systematic investigation of gastrointestinal disease in China[J].Am J Gastroenterol,2010,105(12):2570-2577.
[14] Rodríguez LAG,Cattaruzzi C,Troncon MG,et al.Risk of hospitalization for upper gastrointestinal tract bleeding associated with ketorolac,other nonsteroidal anti-inflammatory drugs,calcium antagonists,and other antihypertensive drugs[J].Arch Intern Med,1998,158(1):33-39.
[15] 王清,万征,李永乐,等.天津市市区成人心肌梗死的流行病学特征及相关因素分析[J].中国介入心脏病学杂志,2011,19(3):129-131.
[16] 洪震.脑卒中的流行病学及其危险因素[J].中国卒中杂志,2006,1(8):559-563.
[17] 顾东风,黄广勇,吴锡桂,等.中国心力衰竭流行病学调查及其患病率[J].中华心血管病杂志,2003,31(1):3-6.
[18] 陈文,胡善联,王吉耀,等.非甾体抗炎药致上消化道出血的经济负担研究[J].中华风湿病学杂志,2002,6(1):31-34.
[19] 周忠东,陈劲柏,陈亚媚.三种胃动力药治疗功能性消化不良的成本-效果分析[J].中国药物与临床,2007,7(10):805-806.
[20] 方卫利,黄富宏,严明权,等.5种质子泵抑制剂治疗消化道溃疡的成本-效果分析[J].中国药业,2012,21(17):39-40.
[21] 陈文激,沙卫红,聂玉强,等.不同质子泵抑制剂对消化性溃疡出血的疗效及疗效-费用分析[J].现代消化及介入诊疗,2007,12(2):74-76.
[22] Wu YF,Zhou Q,Xuan JW,et al.A Cost-effectiveness analysis between amlodipine and angiotensin②receptor blockers in stroke and myocardial infarction prevention among hypertension patients in China[J].Value Health,2013,2(1):A631.
[23] 刘媛媛,李长平,崔壮,等.参保心力衰竭患者住院费用及影响因素分析[J].中国公共卫生,2013,29(3):313-315.
[24] Google Finance.US Dollar($):Chinese Yuan(CN¥)[EB/ OL].[2013-12-27].https://www.google.com/finance?q=USDCNY.
[25] World Health Organization(WHO).Cost-effectiveness thresholds.Cost effectiveness and strategic planning(WHOCHOICE)[EB/OL].(2014-11-11)[2015-12-12].http:// www.who.int/choice/costs/CER_levels/en/.
[26]《中国药物经济学评价指南》课题组.中国药物经济学评价指南:2011版[J].中国药物经济学,2011,6(3):8-11.
[27] 国家统计局.2014中国统计年鉴[EB/OL].[2015-12-08]. http://www.stats.gov.cn/tjsj/ndsj/2014/indexch.htm.
[28] Nicholas B,Becky P,Mats E,et al.A cost-effectiveness analysis of celecoxib compared with diclofenac in the treatment of pain in osteoarthritis(OA)within the Swedish health system using an adaptation of the NICE OA model[J].J Med Econ,2014,17(9):677-684.
[29] Mould JF,Meklati M,Khris M,et al.The cost effectiveness of celecoxib versus NSAIDs+PPI in the treatment of osteoarthritis in Algeria;an update to the Nice model using data from the Condor trial[J].Value Health,2012,15(4):A39.
[30] Mould-Quevedo J.Economic outcomes for celecoxib in Latin America:a cost-effectiveness study of Cox-2 inhibitors against NSAIDs+PPI for adult patients with osteoarthritis and rheumatoid arthritis in Brazil,Mexico,Colombia,Argentina and Costa Rica[J].Value Health,2013,16(3):A221.
[31] 陈志军,高文远.药物经济学在我国“新医改”药政管理中的应用[J].中国药房,2012,23(4):292-294.
Cost-effectiveness Study of Celecoxib for Osteoarthritis in China
Bruce C.M.Wang1,XIE Xiaoping2,Wesley Furnback1,Ronald Caldwell3[1.Elysia Group Ltd.,New York 10053,USA;2.Pfizer Inc(Beijing Branch),Beijing 100010,China;3.University of Michigan,Michigan Ann Arbor 48109,USA]
OBJECTIVE:To evaluate cost-effectiveness of celecoxib for osteoarthritis(OA)in China.METHODS:OA cost-effectiveness analysis model developed by National Institute for Health and Clinical Excellence(NICE)was adopted using celecoxib,diclofenac+PPIs as control.Related risk of adverse event was from CONDOR trials.The effectiveness was measured by QALY. Costs and QALYs were discounted annually at 4.76%.RESULTS:Celecoxib had a cost of$3 591 and 8.826 QALYs while diclofenac+PPIs had a cost of$3 674 and 8.830 QALYs.The incremental costs and QALYs of celecoxib to diclofenac+PPIs were-$83 and-0.004 QALYs,respectively.The incremental cost-effectiveness ratio(ICER)for diclofenac+PPIs to celecoxib was$23 258/QALY. The results of single factor sensitivity analysis and probability sensitivity analysis showed that drug cost was driving factor of ICER,and the results of two therapy plans were similar.CONCLUSIONS:Celecoxib is a less costly alternative than diclofenac+ PPIs.The difference in QALYs between celecoxib and diclofenac+PPIs is extremely small,so celecoxib is likely to be cost-effective for OA patients.
Osteoarthritis;Celecoxib;Diclofenac;PPI;Cost-effectiveness;Pharmacoeconomics
R956
A
1001-0408(2017)05-0586-05DOI10.6039/j.issn.1001-0408.2017.05.03
2016-03-24
2016-07-30)
(编辑:胡晓霖)
辉瑞投资有限公司资助课题
*首席执行官,博士。研究方向:卫生经济学、药物经济学。电话:+1-9176602510。E-mail:Bruce.wang@elysiagroup.com

