硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检测方法的建立
戴青,于丽娜,张璐,韩宁宁,徐嫄,赵晖(中国兽医药品监察所,北京 100081)
硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检测方法的建立
戴青,于丽娜,张璐,韩宁宁,徐嫄,赵晖*
(中国兽医药品监察所,北京 100081)
为检测硫酸安普霉素可溶性粉中非法添加的乙酰甲喹,以十八烷基硅烷键合硅胶为填充剂,磷酸盐缓冲液(取磷酸二氢钠3.0 g,加水1000 mL使溶解,加三乙胺0.5 mL,用饱和氢氧化钠溶液调节pH值至7.0)-甲醇为流动相,二极管阵列检测器(PDA),建立了HPLC-PDA检测方法,并采用峰纯度检查和光谱相似度检查辅助对照品比对方法,对非法添加药物进行确证。在此液相色谱条件下,乙酰甲喹与其他物质峰分离良好。按外标法以峰面积计算,乙酰甲喹的平均回收率为98.1%,RSD为0.3%。该检测方法简便、准确、可靠,可用于测定硫酸安普霉素可溶性粉中非法添加的乙酰甲喹。
硫酸安普霉素可溶性粉;乙酰甲喹;峰纯度检查;光谱相似度检查
硫酸安普霉素是一种氨基糖苷类抗生素,其抗菌谱广,兽医临床上广泛用于治疗畜禽大肠杆菌和沙门氏菌引起的腹泻。近年来,有些不法厂家为使兽药达到迅速起效等目的,在兽药产品中非法添加化学药物,从而提高销量来获取更大利润,这种行为不仅扰乱了兽药市场,也为动物源性食品安全埋下隐患[1-2]。乙酰甲喹是我国最早合成的一种喹噁啉类药物,可改变动物肠道菌群,增加动物体内蛋白质合成,具有广谱抗菌活性,主要用于密螺旋体所致的猪痢疾和细菌性肠炎[3]。近年来,由于乙酰甲喹的不合理使用,中毒事件时有发生[4]。在监督抽检中,通过筛查发现有厂家在硫酸安普霉素可溶性粉中非法添加了乙酰甲喹,但目前尚没有现行的标准可用于该项检测。因此,本研究参考已建立的相关检测方法[5],选择乙酰甲喹为测试药物,硫酸安普霉素可溶性粉为目标制剂,建立了硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检查方法。
1 仪器与试药
1.1 仪器与试剂 高效液相色谱仪(Waters 2695);PDA(Waters 996);分析天平(梅特勒AX 205,十万分之一);三乙胺、甲醇为色谱纯。
1.2 试药 乙酰甲喹对照品(批号:H0111505,中国兽医药品监察所,99.6%);供试品空白:经检测合格的某市售硫酸安普霉素可溶性粉;供试品:某企业生产的经初筛含有乙酰甲喹非法添加的硫酸安普霉素可溶性粉。
2 方法与结果
2.1 色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸二氢钠3.0 g,加水1000 mL使溶解,加三乙胺0.5 mL,用饱和氢氧化钠溶液调节pH值至7.0)-甲醇(70∶30)为流动相;PDA;采集波长范围为200~400 nm,分辨率为1.2 nm;记录376 nm波长处的色谱图。乙酰甲喹色谱峰与相邻色谱峰分离度应符合要求。
2.2 溶液配制
2.2.1 供试品溶液和对照品溶液 取供试品1.0 g,置100 mL量瓶中,加甲醇稀释至刻度,摇匀,超声5 min,静置,滤过;取续滤液5.0 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀,作为供试品溶液。另取乙酰甲喹对照品10 mg,置100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为对照品溶液。
2.2.2 系统适用性溶液 取乙酰甲喹对照品适量,加甲醇溶解,制成含乙酰甲喹0.1 mg/mL的溶液,按2.1项方法测定。系统适用性色谱光谱图见图1。
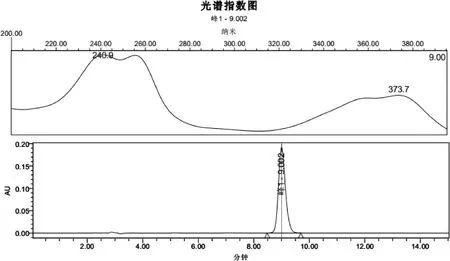
图1 系统适用性色谱光谱图
2.2.3 硫酸安普霉素可溶性粉空白溶液 取供试品空白1.0 g,置100 mL量瓶中,加甲醇稀释至刻度,摇匀,超声5 min,静置,滤过;取续滤液5.0 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀,制备成供试品空白溶液。按2.1项方法进行测定,结果见图2,表明供试品基质对待测物乙酰甲喹没有干扰。
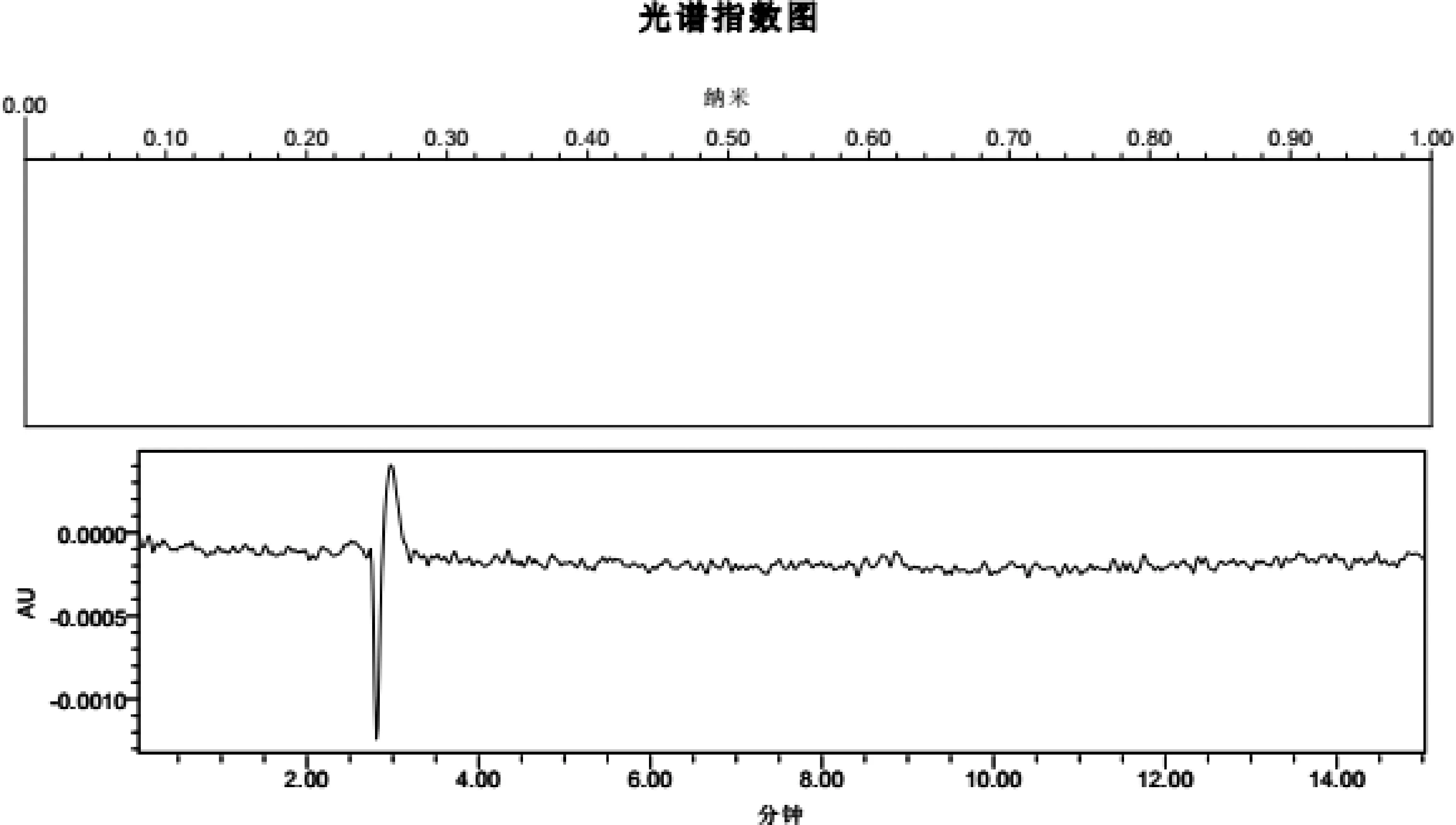
图2 供试品空白溶液色谱图
2.2.4 建立光谱数据库的溶液 以乙酰甲喹对照品溶液作为建立光谱数据库的溶液。
2.3 峰纯度检查 取供试品溶液10 μL注入液相色谱仪,按2.1项色谱条件测定。对供试品溶液色谱图中乙酰甲喹色谱峰进行峰纯度检查,结果见图3和表1。结果显示,乙酰甲喹峰的纯度角度小于纯度阈值,表明在此液相色谱条件下,乙酰甲喹的出峰处无其他干扰峰,为单一物质峰,方法可行。
2.4 光谱相似度检查 对供试品溶液中乙酰甲喹的光谱图与对照品溶液进行匹配,结果见表1与图3~图4。数据显示,供试品溶液中保留时间9.084 min的色谱图与乙酰甲喹对照品保留时间一致,且与对照品的光谱图及最大吸收波长一致,匹配角度小于匹配阈值。表明供试品溶液中相应色谱峰的色谱、光谱与乙酰甲喹对照品的色谱、光谱一致,为同一物质。
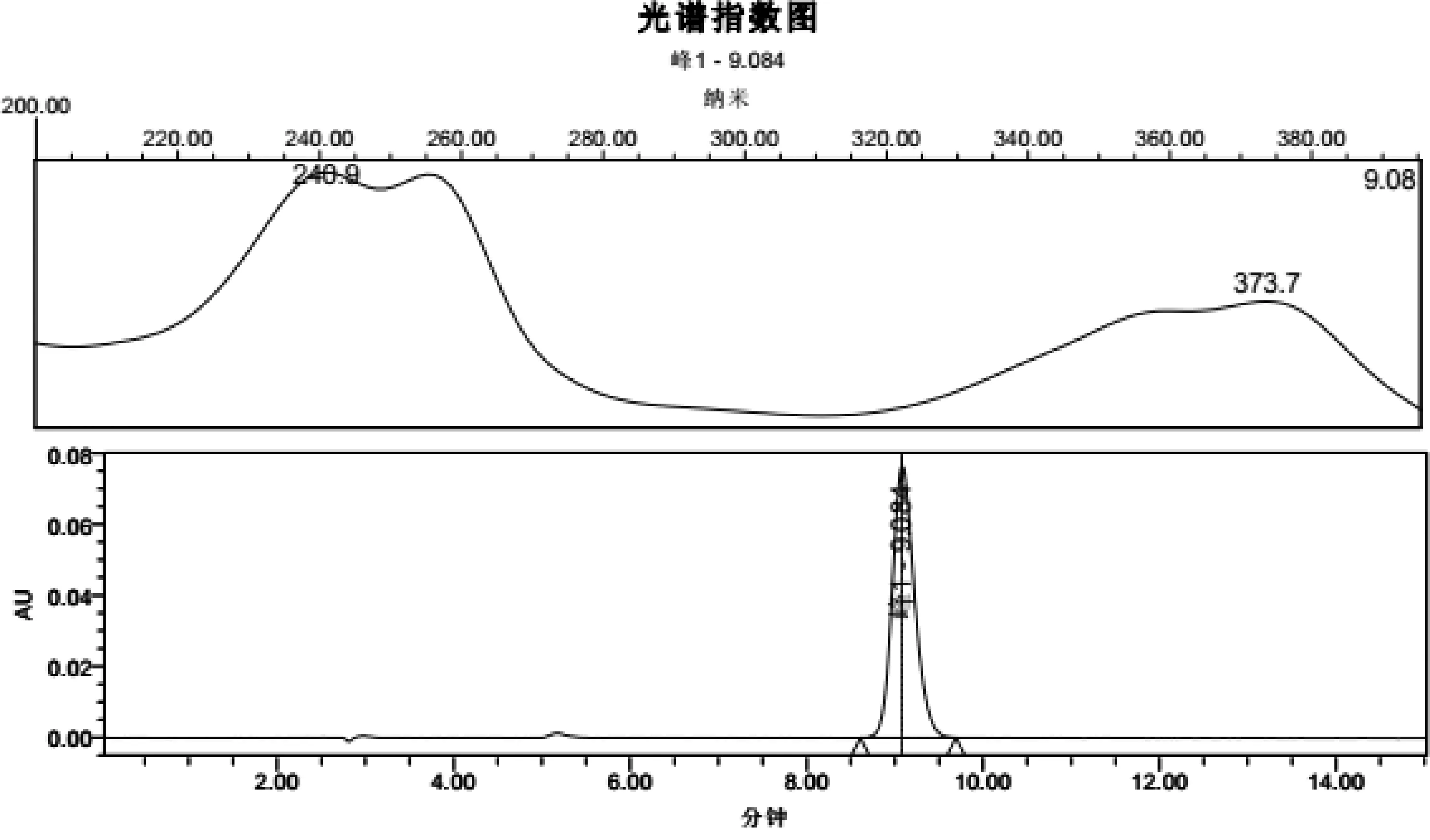
图3 供试品溶液色谱光谱图
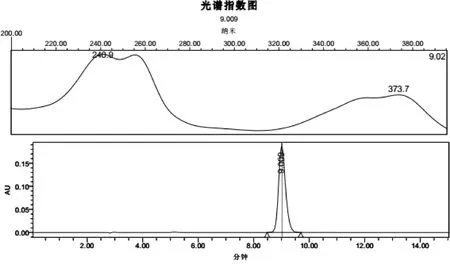
图4 乙酰甲喹对照品色谱光谱图

表1 供试品峰纯度及光谱相似度检查结果
2.5 方法学考察
2.5.1 专属性 通过供试品空白试验排除样品基质对乙酰甲喹的干扰,同时,峰纯度检查结果也显示在此色谱条件下乙酰甲喹的出峰为单一物质峰。
2.5.2 耐用性 从柱温、流动相pH值、色谱柱三个方面考察方法的耐用性。调节柱温分别为20℃、25 ℃、30 ℃,结果显示:随柱温升高,乙酰甲喹保留时间略提前;调节流动相pH值为6.8、7.0、7.2,结果显示:随流动相pH值的增大,乙酰甲喹保留时间基本不变;选择3款不同品牌色谱柱,以系统适用性溶液作为供试溶液,考察不同色谱柱对测定的影响,结果如表2所示:3种品牌色谱柱均可用于该检查,方法耐用性较好。

表2 3种色谱柱耐用性考察结果
2.5.3 检出限 检出限溶液配制:取乙酰甲喹对照品适量,加甲醇稀释至刻度,摇匀,制成浓度为1 mg/mL的储备液,取供试品空白1.0 g,置100 mL
量瓶中,加甲醇适量,超声5 min,冷却至室温,精密加入1 mg/mL的储备液适量(0.1、0.2、0.4、0.6、0.8 mL),用甲醇稀释至刻度,摇匀,即得。以光谱图失真的最大浓度作为方法的检出限,乙酰甲喹检出限为0.6 g/kg。2.5.4 线性与范围 取乙酰甲喹对照品适量,加甲醇稀释至刻度,摇匀,制成浓度为1 mg/mL的储备液,分别量取0.5、1、2、4、8、10 mL于100 mL量瓶中,加甲醇稀释至刻度,摇匀,测定。以峰面积y对浓度x进行线性回归(图5),乙酰甲喹的回归方程分别为:y=33512x+658.4,r2=1。结果表明,乙酰甲喹在5~100 μg/mL范围内线性关系良好。
2.5.5 准确度 以供试品空白加被测物对照品做回收率试验来考察方法的准确度。回收率试验溶液配制:分别称取供试品空白1.0 g,乙酰甲喹对照品5 mg,置100 mL量瓶中,加甲醇稀释至刻度,摇匀,超声5 min,静置,滤过;取续滤液5.0 mL,置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得。平行配制6份,结果见表3。乙酰甲喹回收率为98.1%,RSD为0.3%。
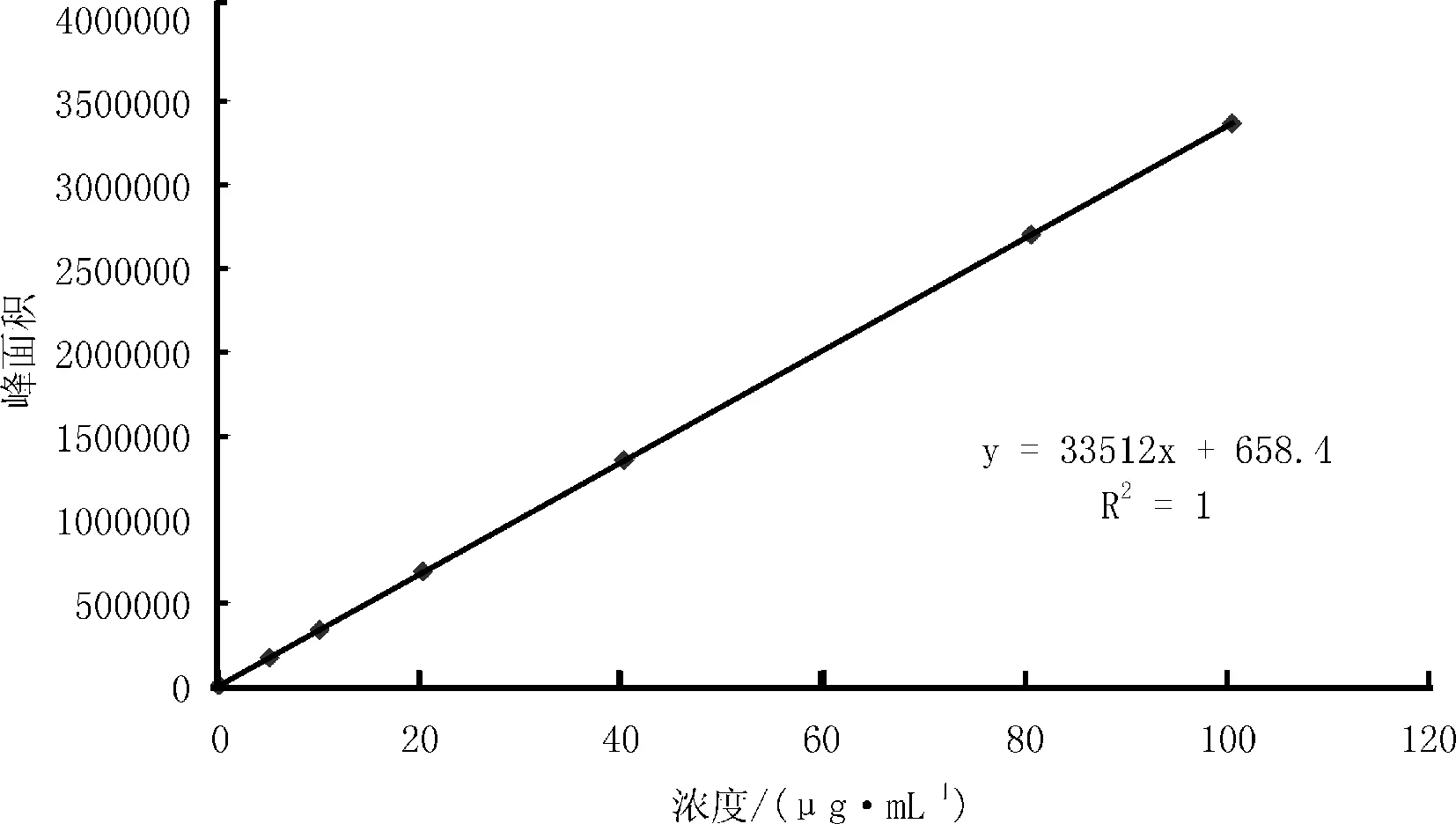
图5 乙酰甲喹线性图
3 讨论与小结
农业部2333号公告硫酸黏菌素预混剂中非法添加乙酰甲喹检查方法中检测波长为376 nm,本试验在200~400 nm波长范围内对乙酰甲喹对照品进行扫描,结果显示乙酰甲喹在376 nm处有较强吸收,因此本试验采用该波长作为检测波长,乙酰甲喹色谱峰与相邻色谱峰分离度好,响应值高,能够很好满足试验要求。此外,向流动相中添加三乙胺,不仅可以调节pH值,增强乙酰甲喹的保留,避免其过快洗脱,还可以改善峰形,减少拖尾。
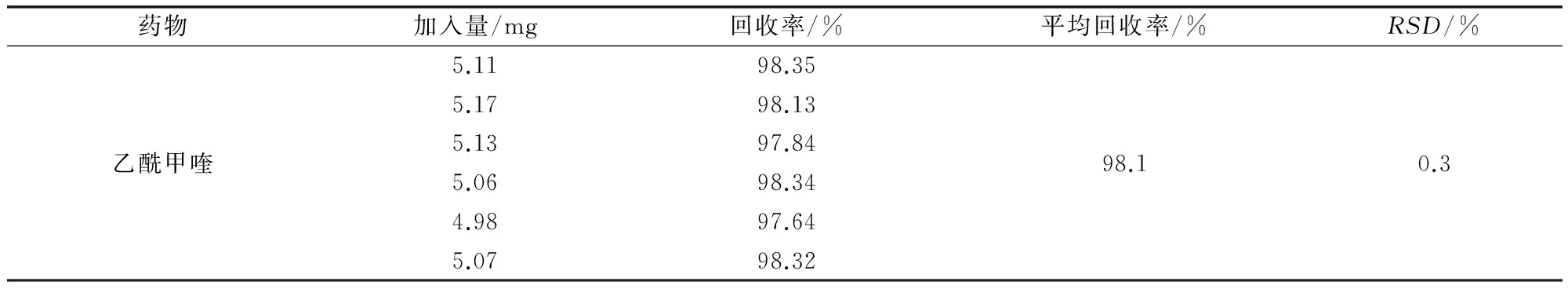
表3 回收率结果
采用本检测方法用于其他兽药制剂中非法添加乙酰甲喹的检查时,需进行空白试验和系统适用性试验,确保供试品溶液中乙酰甲喹色谱峰与相邻色谱峰的分离度应符合要求,从而确定目标分析物以外的成分不会对测定产生干扰,必要时可调整供试品溶液或对照品溶液的浓度,使二者目标分析物的峰面积尽量接近,以便于检测和确认。
目前国外主要采用LC-MS/MS法对乙酰甲喹代谢产物[6]进行研究,国内主要是对兽药制剂和饲料中非法添加乙酰甲喹进行测定,多采用HPLC法[7]。本方法采用高效液相色谱法结合二极管阵列检测器,对检测波长、色谱条件等进行考察,在本检测方法色谱系统中,硫酸安普霉素无紫外吸收,对检出无干扰,因此可通过供试品峰与对照品峰的保留时间、峰纯度及光谱特征的对比来确定硫酸安普霉素可溶性粉中是否添加了乙酰甲喹,方法简便、准确,为有效遏制兽药非法添加行为提供了一定技术支持。
[1] 董玲玲,范强,杨星,等. 氟苯尼考粉中非法添加烟酰胺和氨茶碱的HPLC-PDA检测方法的建立[J]. 中国兽药杂志,2014,48(5):47-50.
[2] 龚旭昊,王静文,董玲玲,等. 鱼腥草注射液中非法添加水杨酸和氧氟沙星HPLC-PDA检测方法的建立[J]. 中国兽药杂志,2016,50(2):37-40.
[3] 李璐璐,骆延波,刘玉庆,等. 乙酰甲喹和喹烯酮药动学研究进展[J]. 中国抗生素杂志,2016,41(2):98-103.
[4] 刘迎春,高怀涛. 乙酰甲喹的合理应用[J]. 养禽与禽病防治,2009,(3):42-43.
[5] 中华人民共和国农业部.公告第2333号[S].
[6] Yanshen Li,Kaili Liu,Rose C Beier. Simultaneous determination of mequindox, quinocetone, and their major metabolites in chicken and pork by UPLC-MS/MS[J]. Food Chemistry,2014,160(10):171-179.
[7] 吴宁鹏,王丽景,李慧素,等. 五种兽药中非法添加喹乙醇和乙酰甲喹的HPLC-PDA检测方法的建立[J]. 中国兽药杂志,2014,48(12):43-49.
(编辑:侯向辉)
A method for the determination of mequindox in the apramycin sulfate soluble powder was developed by the high performance liquid chromatography with photo-diode array detector (HPLC-PDA). It was tested with C18 column, using phosphate buffer solution (taking the sodium dihydrogen phosphate 3.0 g, add 1000 mL water to dissolve, and add 0.5 mL triethylamine, adjusting pH to 7.0 by sodium hydroxide saturated solution) and methanol as the mobile phase. Peak purity test and spectrum similar test were helped to identify the mequindox. The mean recovery of mequindox was 98.1%, andRSDwas 0.3%, respectively. In conclusion, the method is simple, accurate and reliable for the determination of mequindox in apramycin sulfate soluble powder.
apramycin sulfate soluble powder; mequindox; peak purity test; spectrum similar test
戴青,硕士,从事抗生素检验检测工作。
赵晖。E-mail: 171977364@qq.com
2016-09-04
A
1002-1280 (2017) 02-0019-05
S859.83
Determination of Mequindox in Apramycin Sulfate Soluble Powder by HPLC-PDA
DAI Qing,YU Li-na,ZHANG Lu,HAN Ning-ning,XU Yuan,ZHAO Hui*
(ChinaInstituteofVeterinaryDrugControl,Beijing100081,China)

