新型磁性纳米功能材料Fe3O4@g-C3N4的制备及其吸附铀的性能研究*
龙 威,李紫艳,符志鹏,祖 秀,唐 凯,杨星月
(1.南华大学 化学化工学院,湖南 衡阳 421001;2.南华大学 期刊社,湖南 衡阳 421001)
随着核技术的发展和核能的利用,作为自然界最普遍的不可再生的清洁能源核燃料铀(Uranium),已经成为了世界上最重要的战略资源之一[1]。据统计,世界上已知铀总量仅约为500万t,而可用于核反应的天然铀不足5%,并且大多数核工业对核燃料铀的利用率普遍低于10%。由于人类在开发和利用铀资源时不可避免地产生大量放射性废渣和废液,不仅对周围植被、水源和土壤产生不可逆转的危害,而且对人类健康也会产生极大的威胁[2]。因此,无论是从废料中回收微量铀以提高铀资源的利用率还是要减小铀污染对环境的危害,研发和探究铀的新型吸附功能化材料都具有较大的意义[3]。
铀(U)是元素周期表中第七周期第三副族元素,锕系元素之一,是重要的天然放射性元素,半衰期比较长,工业污水中的铀对环境有重大危害[4]。国内对含铀污水的处理有较多的报道[5-8],大都是利用天然矿石、微生物、生物质材料等加工成新型吸附材料,进行直接吸附。近年来,我国科研人员进行了以稻谷壳、酵母菌等相关纤维素为原料对铀的吸附实验,取得了较大的科学研究进展[9-10],但对铀的吸附率仍不理想,吸附材料的稳定性和活性成为继续研究的热点。
国外大多数研究者也同样利用天然矿物、微生物、生物质材料等进行了一系列的对比研究,典型代表如“YuccaMountain”工程[11],直接利用含天然矿石等物质的土壤等对U、Sr、Cs等核素进行吸附实验,从而计算出核素在不同材料中的吸附百分数,同时探讨了溶液组成、核素浓度、温度及固相粒径对核素吸附性的影响。Djimbi等[12]则结合表面络合模型理论,主要对放射性的元素铀、钍等在进行吸附实验水溶液中的表面化学行为进行研究,从而总结出吸附规律,取得了较好的结果。然而,吸附材料的活性和选择性是含铀污水处理的关键,仍未获得一种非常理想的材料用于工业化,其关键是常规性材料吸附效率不高,吸附性高的材料昂贵难制备,因此,探索新型高效吸附除铀的功能材料仍旧是一个非常新兴热门的领域[13]。
新型磁性纳米功能化复合材料采用廉价易得的良好材料为母体,通过特殊的制备技术形成独特的纳米功能化材料,包含着带有磁性的Fe3O4粒子,具有优异的吸附性能已被科学界公认[14]。最近,一种新的非金属材料g-C3N4引起了众多学者的关注,实验表明其具备良好的光生电子和空穴复合率,可直接来源于三聚氰胺的热分解,在光催化、新材料制备领域的运用已获得了成功[15-16]。作者选择制备新型Fe3O4@g-C3N4功能纳米材料用于含铀污水的净化处理,取得了较好的效果,其研究在国内外尚未报道,因此,开发此种新型功能纳米材料具有重要的科学价值和深远的意义。
1 实验部分
1.1 试剂与仪器
硝酸双氧铀、偶氮胂Ⅲ、三聚氰胺、三聚氰酸、尿素、十二烷基苯磺酸钠、三氯化铁、氨水、无水乙醇、乙酸、乙酸钠:分析纯,市售;另自制不同浓度乙酸-乙酸钠的缓冲溶液备用。
超声波清洗器:DF-3510DTH,昆山市超声仪器有限公司;集热式恒温加热磁力搅拌器:DF-101S,郑州长城工贸有限公司;电热鼓风干燥箱:101-2AB,上海精宏实验设备有限公司;精密增力电动搅拌器:JJ-1,巩义市予华仪器有限责任公司;水浴恒温振荡器:SHY-2A,长沙市天恒科学仪器设备有限公司;pH计:pH-3c,上海市仪电科学仪器股份有限公司;真空干燥箱:DZF-6020A,郑州市长城工贸有限公司;红外光谱仪:Prestige-21,美国 Thermo Fisher Scientific Co.,Ltd.;扫描电镜:XL,日本Shimadzu Co.,Ltd.; X射线衍射仪:D8-Advace,日本Rigaku Co.,Ltd.;比表面积分析仪:NOVA 2200e,美国Quantachrome Co.,Ltd.;紫外可见光分光光度计:U-3900,上海驿淼环境技术有限公司;电子天平:FA2004,上海光正医疗仪器有限公司;管式炉:OTF-1200X,合肥科晶材料技术有限公司。
1.2 磁性纳米功能材料Fe3O4@g-C3N4的制备
将三聚氰胺、三聚氰酸和尿素以质量比为30∶10∶1小心混合,经充分研磨均匀后放入管式炉内,在氮气气流的持续保护下以600 ℃的温度煅烧6 h后自然冷却,形成淡黄色的块状固体,经充分研磨后形成粉末状的g-C3N4固体待用。
在一洁净的带有磁石的烧杯中加入少许蒸馏水,添加适当的三氯化铁(约为g-C3N4质量的10%)固体,室温下搅拌均匀使三氯化铁充分溶解形成均匀的黄色液体。称取0.2 g的十二烷基苯磺酸钠加入,投入一定量的g-C3N4粉末后持续搅拌至均匀透明。然后将pH计的传感器连入,小心滴入浓氨水至pH=3.5,搅拌6 h后呈均匀状态。将烧杯移入微波清洗器内室温下振荡清洗1 h后移入鼓风干燥箱于110 ℃干燥一晚,冷却、取出研磨至粉末,小心地用去离子水洗涤固体粉末后,继续放入鼓风干燥箱于110 ℃下持续干燥10 h,冷却后取出研磨至粉末,后置于真空干燥箱45 ℃干燥6 h,冷却、研磨后于管式炉中在N2保护下350 ℃高温焙烧3 h后转入H2氛围内连续还原2 h,再转换在N2保护下降温冷却,形成磁性功能的吸附材料备用。
1.3 吸附铀测定实验
取质量浓度为100 mg/L的铀标准溶液1.00 mL置于1 000 mL容量瓶中,加入超纯水定容,配置成100 μg/L铀储备液,置于聚四氟乙烯瓶内待用。每次实验时取配置好10 mL的铀标准液于50 mL锥形瓶内,加入一定量的缓冲溶液配制成指定pH值的溶液,静止24 h待稳定后,加入一定质量的上述已制备的吸附材料,超声分散30 min后,置于恒温水浴振荡器中以160 r/min的转速连续振荡若干时间,直至反应达到平衡。
取静置3 h的吸附后液体进行离心分离处理,取1 mL的上层清液加入装有偶氮胂Ⅲ的10 mL的容量瓶中,再测定其pH值,如果不合格,可以加入一定量的缓冲溶液调节至10 mL备测。采用分光光度法测定铀酰离子的质量浓度,标准浓度的溶液曲线选择波长为652 nm为最佳测试波长,取不同质量浓度的铀标准溶液测定吸附标准曲线,用于直接判定吸光度和铀质量浓度的线性关系。当吸附平衡后,可直接测吸光度而读出溶液中ρ(铀酰离子),根据吸附前后ρ(铀酰离子)可以计算出该材料对铀酰离子的吸附量Q(mg/g)和吸附率(%),其相关计算公式类似于文献上通用的计算方法[6,14,17],吸附量Q=(ρ0-ρ)V/m;吸附率=(ρ0-ρ)×100%/ρ0,其中ρ0和ρ分别为铀酰离子的初始质量浓度和吸附后的平衡质量浓度,mg/L;V为吸附溶液的体积,L;m为吸附剂的质量,g。
2 结果与讨论
2.1 材料表征
2.1.1 红外表征
将材料g-C3N4与Fe3O4@g-C3N4分别进行红外光谱的表征,结果见图1。

σ/cm-1图1 功能吸附材料的红外光谱图
由图1可见,两图形状轮廓基本一致,在远红外区3 130 cm-1处存在着较大的吸收峰,随着磁性Fe3O4纳米粒子的引入,此吸收峰面积有所减少,这是由于两者相互作用形成的粒子变大振动变小的缘故;近红外的1 340 cm-1区域的峰形基本一致,表明其g-C3N4的基本骨架特征没有发生重大变化,因此,粒子g-C3N4与Fe3O4发生了较好的结合和包合行为。
2.1.2 BET表征分析
固体吸附材料的物理组织结构可以通过BET表征来识别,其多孔性结构和孔径大小、分布等能直接展示材料的吸附性能。材料g-C3N4与Fe3O4@g-C3N4分别进行BET表征,分析结果见表1。

表1 磁性功能纳米粒子的BET分析结果
由表1可见,虽然材料g-C3N4的比表面积较小,但孔径较大,可以容纳和接受磁性的Fe3O4粒子,而两者结合后孔径变小,表明磁性的Fe3O4粒子进入了材料g-C3N4的孔道内部,导致比表面积增加,产生了较多的微孔结构,使得孔容也明显增加,这就直接改良了材料的微观组织结构,有利于更好发挥吸附性能。
BET表征分析得到的N2-吸附脱附图见图2,孔径分布见图3。

p/p0图2 功能吸附材料的N2-吸附脱附图

孔径/nm图3 功能吸附材料的孔径分布图对比
由图2可见,材料g-C3N4的N2回滞环不规则,与磁性纳米Fe3O4粒子结合后N2回滞环明显改善,且出现了其介孔材料的回滞环特征;由图3孔径分布图中可以看出,材料g-C3N4的孔径分布不集中,大多集中在20~45 nm区域,而与磁性纳米Fe3O4粒子结合后,孔径分布主要集中在了4~6 nm区域,这充分说明了Fe3O4@g-C3N4是非常规则且比较优良的多孔性材料。
2.1.3 XRD分析与SEM表征
为了验证已制备的磁性功能纳米材料,对样品进行了XRD表征,其光谱图见图4。由图4可见,样品出现了2θ分别在28.2°、43.4°、63.1°及82.7°等衍射峰,对应的Fe的晶型标于图4中,这属于混合晶型的Fe3O4衍射峰,与文献[8-9]提及的基本一致,而无Fe0、Fe2+、Fe3+的单独衍射峰,进一步说明磁性吸附纳米材料Fe3O4@g-C3N4已制备成功。

2θ/(°)图4 功能吸附材料的XRD光谱图
电子扫描显微镜能进一步观察材料的微观形貌和结构,见图5。

图5 功能吸附材料的SEM图
由图5可见,在放大了5 000倍的扫描电镜图中,得到了半透明且光亮的g-C3N4材料表面,呈近似椭圆形大颗粒状,这表明g-C3N4已经完全包裹了内部的Fe3O4纳米粒子,这也证实了单独的g-C3N4材料具备作为一种良好吸附剂的能力,可以较好地包裹其它纳米粒子。
2.2 吸附性能实验
2.2.1 pH环境对吸附性能的影响
在20 mLρ(铀酰离子)=140 mg/L的溶液中,加入了6 mg的吸附剂,调节溶液不同的pH值,获得了不同的吸附性能实验数据见图6。

pH图6 pH值对铀吸附实验的影响
由图6可见,pH=10时,吸附性能达到最大,而随着pH值的继续增加,吸附剂的吸附量逐渐下降。说明较强的酸性或碱性环境下,吸附行为都得不到理想状态,在中性偏弱碱性的环境下,吸附剂Fe3O4@g-C3N4材料对铀的吸附效率最佳。
2.2.2 吸附剂用量对吸附性能的影响
在上述基础上,选择pH=10、ρ(铀酰离子)=140 mg/L的溶液20 mL中,分别加入不同质量的磁性功能吸附剂,其吸附性能见图7。

m(吸附剂)/mg图7 m(吸附剂)对铀吸附实验的影响
由图7可见,随着吸附剂用量的增加,吸附率在逐步提升,当吸附剂用量在6~7 mg时吸附率达到最大,之后吸附率不再明显增加,而单位吸附量由于投入的吸附剂质量太大而逐步下降,因此,最佳的m(吸附剂)=6~7 mg。
2.2.3 吸附时间对吸附性能的影响
同样,在20 mLρ(铀酰离子)=140 mg/L的的溶液中,加入6.5 mg 吸附剂,加入缓冲溶液体系调节pH=10的条件下,考察了吸附时间对吸附性能的影响,结果见图8。
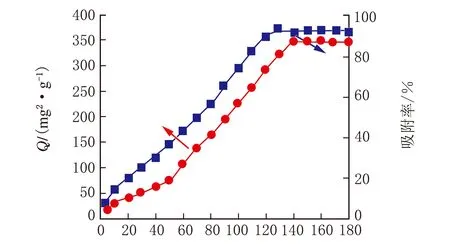
t/min图8 吸附时间对吸附实验的影响
由图8可见,随着时间的不断增多,吸附量和吸附率均增大,当时间达到140 min时,其吸附率已经达到最大稳定值,对应吸附量为352.1 mg/g。虽然吸附速率不快,但是最大吸附率超过90%,因此最佳吸附时间应控制在150 min。
2.2.4 铀初始质量浓度对吸附性能的影响
铀的初始质量浓度对吸附性能也有较大影响,较大的初始浓度下所需的吸附剂质量大、时间长。通过配置ρ(铀酰离子)=20~200 mg/L ,加入缓冲溶液调节pH=10,控制吸附时间为150 min及6.5 mg吸附剂,探究了初始ρ(铀酰离子)对铀吸附性能的影响,结果见图9。

ρ(铀酰离子)/(mg·L-1)图9 初始ρ(铀酰离子)对吸附性能的影响

通常来说,吸附剂的吸附量超过200 mg/g视为优良有效的吸附剂。通过实验探究了活性炭、分子筛、γ-Al2O3、硅胶等作为吸附载体,虽然也引入了磁性的Fe3O4纳米粒子,但效果均不如Fe3O4@g-C3N4材料,这可能是因为载体材料与g-C3N4分子不同,主要与包裹性能有关,可使用分子模拟等手段来证实,且有待进一步探究和验证。
3 结 论
制备了一种新型磁性纳米吸附材料Fe3O4@g-C3N4,通过表征分析了材料的结构和性能,同时通过大量的吸附性能实验探究了外界条件对吸附性能的影响,得到了较好的结果。
(1) g-C3N4材料可以用于包合磁性的Fe3O4纳米粒子,包合后比表面积增加,孔结构分布均匀,吸附性能增加,可用于溶液中的铀的吸附;
(2) 吸附材料Fe3O4@g-C3N4对铀有较好的吸附性能,在pH=10、ρ(铀酰离子)=140 mg/L的20 mL溶液中,吸附的最佳质量为6.5 mg、吸附时间为150 min,最大吸附量可达352.1 mg/g,最佳吸附率可达到90%;
(3) 相较常见的活性炭、分子筛、γ-Al2O3、硅胶等吸附材料,磁性的Fe3O4@g-C3N4材料体现出优良的吸附铀性能,可用于工业污水中铀的吸附和去除,具有重要的科学意义。
致谢
本论文的实验研究过程受到了南华大学“核资源与环境大学生创新训练中心”2016年创新实验项目的大力资助,在此表示感谢。
[1] 张晓峰, 陈迪云,彭燕,等.丁二酸改性茶油树木屑吸附铀的研究[J].环境科学,2015,36(5):1686-1693.
[2] 赖忠俊,张志宾,戴荧,等.碳基吸附材料吸附铀的研究现状[J].湿法冶金,2016,35(3):183-188.
[3] 刘军,张志宾,陈金和,等.钙-铀-碳酸络合物对红土吸附铀性能的影响[J].原子能科学技术,2015,49(8):1359-1365.
[4] 肖方竹,何淑雅,彭国文,等.功能化磁性载体固定耐辐射奇球菌及其对铀的吸附行为与机理[J].中国有色金属学报,2016,26(7):1568-1575.
[5] 胡建邦,袁亚莉,唐琼,等.氨基化改性 Fe3O4@ SiO2复合磁性材料的制备以及对 U(VI) 的吸附研究[J].应用化工,2012,41(12):2067-2070.
[6] 高阳阳,袁亚莉,胡建邦,等.磁性胺肟基功能化 CMC对铀酰离子的吸附行为研究[J].应用化工,2014,43(3):427-431.
[7] WANG G H,LIU J S,WANG X G,et al.Adsorption of uranium (VI) from aqueous solution onto cross-linked chitosan[J].Journal of Hazardous Materials,2009,168(2/3):1053-1058.
[8] LIU J,ZHOU Y,LIU F,et al.One-pot synthesis of mesoporous interconnected carbon-encapsulated Fe3O4nanospheres as superior anodes for Li-ion batteries[J].RSC Advances,2012,2(6):2262-2265.
[9] CHEN X,RAO J,WANG J,et al.A facile enantioseparation for amino acids enantiomers using beta cyclodextrins functionalized Fe3O4nanospheres[J].Chem Commun (Camb),2011,47(37):10317-10319.
[10] DING H L,ZHANG Y X,WANG S,et al.Fe3O4@ SiO2core/shell nanoparticles:the silica coating regulations with a single core for different core sizes and shell thicknesses[J].Chemistry of Materials,2012,24(23):4572-4580.
[11] RECHARD R P,BIRKHOLZER J T,WU Y S,et al.Unsaturated flow modeling in performance assessments for the Yucca Mountain disposal system for spent nuclear fuel and high-level radioactive waste[J].Reliability Engineering & System Safety,2014,122:124-144.
[12] DJIMBI D M,GAUTHERON C,ROQUES J,et al.Impact of apatite chemical composition on (U-Th)/He thermochronometry:an atomistic point of view[J].Geochimica et Cosmochimica Acta,2015,167:162-176.
[13] DAI Y,NIU J,YIN L,et al.Sorption of polycyclic aromatic hydrocarbons on electrospun nanofibrous membranes:sorption kinetics and mechanism[J].Journal of Hazardous Materials,2011,192(3):1409-1417.
[14] CHENG J,WANG B,PARK C M,et al.CNT@Fe3O4@C coaxial nanocables:one-pot,additive-free synthesis and remarkable lithium storage behavior[J].Chemistry-A European Journal,2013,19(30):9866-9874.
[15] 刘建新,王韵芳,王雅文,等.Ag/Ag3PO4/g-C3N4复合光催化剂的合成与再生及其可见光下的光催化性能[J].物理化学学报,2014,30(4):729-737.
[16] 尹竞,廖高祖,朱冬韵,等.g-C3N4/石墨烯复合材料的制备及光催化活性的研究[J].中国环境科学,2016,36(3):735-740.
[17] 张宗波,袁亚莉,周智慧,等.多氨基含氮配体改性有序介孔材料的制备及对铀(VI)的吸附性能研究[J].应用化工,2016,45(4):603-607.

