含氨鲁米特的DTPA双酰胺配体的合成与表征
帅光平,余光勤,袁付明,曹亚萍,袁泽利
(遵义医学院药学院,贵州 遵义 563003)
含氨鲁米特的DTPA双酰胺配体的合成与表征
帅光平,余光勤,袁付明,曹亚萍,袁泽利*
(遵义医学院药学院,贵州 遵义 563003)
以二乙三胺五乙酸(DTPA)、醋酸酐和氨鲁米特为原料,合成了一个含氨鲁米特的DTPA双酰胺配体二乙三胺-N,N″-(二乙酰氨鲁米特)-N,N′,N″-三乙酸(L),并用红外光谱、核磁共振氢谱、核磁共振碳谱、高分辨质谱对配体的组成和结构进行了表征。
二乙三胺五乙酸(DTPA);氨鲁米特;合成;表征
二乙三胺五乙酸(DTPA)及其衍生物因结构中含有多个N、O原子而具有优良的配位性能,在化学和医药学领域有着广泛的应用[1-2]。如临床上常用的小分子造影剂Gd-DTPA、Gd-DTPA-BMA等都是以DTPA为配体制备的,这类造影剂具有低毒和高稳定性的优点,但存在体内循环时间短、弛豫率低、用量大以及功能单一等缺点[3-4]。功能化DTPA配体对于研发DTPA类磁共振成像造影剂具有重要作用[1],经功能化改造的含钆磁共振(MRI)造影剂不仅能有效克服上述造影剂的弊端,还能赋予其特殊的功能[5-6],如刺激响应性、靶向性和载药性等[7-8]。因此,若能将临床一线药物通过化学手段偶联于DTPA分子结构中,再进一步制备具有MRI诊断与化学治疗于一体的单分子双功能化小分子,这对实现诊断与治疗同步意义重大。
为此,作者以DTPA、醋酸酐和氨鲁米特为原料,合成一个含氨鲁米特的DTPA双酰胺配体二乙三胺-N,N″-(二乙酰氨鲁米特)-N,N′,N″-三乙酸(L),并通过红外光谱、核磁共振氢谱、核磁共振碳谱及高分辨质谱对配体的组成和结构进行表征,拟为具有MRI成像诊断与临床药物治疗的诊疗联用的单分子药物研究提供帮助。
1 实验
1.1 试剂与仪器
醋酸酐、DTPA、N,N-二甲基甲酰胺(DMF)、吡啶、乙醚等均为分析纯;氨鲁米特,美仑生物公司。
Agilent400MHz型核磁共振仪,美国安捷伦公司;Varian1000FTIR型红外光谱仪,美国瓦里安公司;MicromassLCTPremierXE型高分辨质谱仪,美国;DZF-6020型真空干燥箱,上海博远实业有限公司。
1.2 合成方法
目标配体L的合成路线如图1所示。
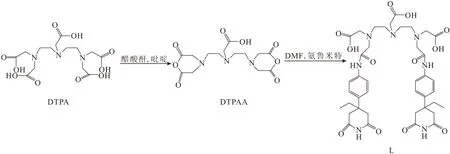
图1 配体L的合成
1.2.1 二乙三胺五乙酸双酸酐(DTPAA)的合成[9]
将10 g DTPA悬浮于30 mL醋酸酐和15 mL吡啶的混合溶液中,于80 ℃搅拌反应5 h,抽滤,依次用醋酸酐洗、少许冷DMF洗2~3次、乙醚搅拌充分洗,用DMF-乙醚(体积比1∶1)重结晶,40 ℃下真空干燥,得白色粉末9.38 g,收率90.1%,m.p.180~182 ℃。1HNMR(D2O),δ:4.00(s,8H,-CH2-,酸酐环),3.65(s,2H,-CH2-COOH),3.48~3.51(t,4H,J=6.3 Hz,-CH2-CH2-N),3.16~3.22(t,4H,J=6.3 Hz,-CH2-CH2-N);13CNMR(D2O),δ:170.54,167.39,109.99,53.53,51.40,49.79,46.91;FTIR(KBr,4 000~400 cm-1),ν:3 433,3 007,1 802,1 772,1 733,1 636,1 400,1 174,1 107,958,904,605。
1.2.2 目标配体L的合成
将1.0 g(2.8 mmol)DTPAA溶解于80 mL DMF中,冷却至0 ℃;再称取氨鲁米特 1.4 g(6 mmol)溶解于5 mL DMF中,搅拌下缓慢滴加到上述反应液中;滴毕,将反应液置于常温下搅拌反应 48 h后倒入100 mL冰水中,减压旋蒸至溶液体积约10~15 mL;加入200 mL丙酮,置于冰箱中过夜,过滤,用氯仿、乙醚洗涤,真空干燥得白色粉末2.0 g,收率90.1%。1HNMR(CD3OD),δ:8.01(s,2H,NH),7.60~7.62(dd,4H,J=8.7 Hz、1.6 Hz, Ar-H),7.22~7.24(d,4H,J=7.7 Hz,Ar-H),3.99(s,2H,-CH2-),3.87(s,2H,-CH2-),3.67(s,2H,-CH2CH2-),3.61(s, 2H,-CH2CH2-),3.28(s,2H,-CH2CH2-),3.03(s,6H,-CH2-),2.90(s,6H,-CH2-),2.56~2.60(d,2H,J=16.5 Hz,-CH2-),2.23(s,2H,-CH2-),1.84~1.89(m,4H,-CH2-),0.82~0.86(t,6H,J=7.7 Hz,-CH3);13CNMR(CD3OD),δ:178.12,175.89,175.25,173.16,171.64,170.70,165.21,138.39,136.59,128.01,121.92,67.06,59.60,56.95,52.73,52.20,51.89,51.55,39.82,39.61,39.40,37.41,33.75,32.07,31.10,30.35,27.94,15.59,9.60;HRMS(ESI-MS),Calcd for C40H52N7O12(M+H+):822.36740, found 822.36943;FTIR(KBr,4 000~400 cm-1),ν:3 395,2 973,2 920,1 589,1 449,1 409,1 326,1 385,1 269,1 092,934,717,589。
2 结果与讨论
2.1 配体L的一般性质
配体L,白色粉末,易溶于甲醇、二甲基亚砜、N,N-二甲基甲酰胺等有机溶剂,难溶于氯仿、苯等有机溶剂,在空气中稳定,无光敏性,长期放置理化性质无变化。
2.2 核磁共振表征
配体L的1HNMR图谱如图2所示。
由图2可以看出,低场δ8.01为氨鲁米特结构中的NH质子化学位移,δ7.22~δ7.62为氨鲁米特结构中的芳环质子化学位移,δ3.99和δ3.87为与氨鲁米特酰胺相连的亚甲基质子化学位移,δ2.23~δ2.60为氨鲁米特分子环上亚甲基质子化学位移,δ1.84~δ1.89为氨鲁米特分子中与甲基相连的亚甲基质子化学位移,δ0.82~δ0.86为氨鲁米特分子中的甲基质子化学位移,δ3.03~δ3.67为其余亚甲基质子化学位移。

图2 配体L的1HNMR图谱
配体L的13CNMR图谱如图3所示。
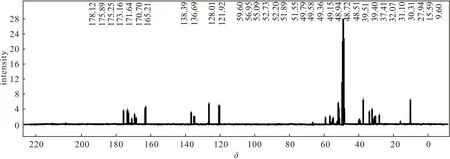
图3 配体L的13CNMR图谱
由图3可以看出,在δ170.70~δ178.12处出现了羰基碳信号,在δ121.92~δ165.21处出现了芳环碳信号,在δ67~δ9.60处出现了亚甲基、甲基碳信号。
2.3 高分辨质谱和红外光谱表征
配体L的高分辨质谱如图4所示。
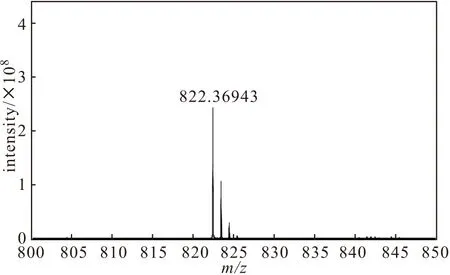
图4 配体L的HRMS(ESI-MS)图谱
由图4可知,配体L的m/z为822.36943,与理论计算值822.36740十分吻合。
配体L的红外光谱如图5所示。
由图5可知,3 395.218 cm-1处为νN-H振动吸收峰[10],2 973.268 cm-1、2 920.346 cm-1处为甲基和亚甲基的特征振动吸收峰[11],1 589.851 cm-1处为νC=O振动吸收峰[10-12],1 269.724 cm-1处为νC-N特征振动吸收峰[9,12]。
3 结论
以二乙三胺五乙酸(DTPA)、醋酸酐和氨鲁米特为原料,合成了一个含氨鲁米特的DTPA双酰胺配体二乙三胺-N,N″-(二乙酰氨鲁米特)-N,N′,N″-三乙酸(L),并用红外光谱、核磁共振氢谱、核磁共振碳谱、高分辨质谱对配体的组成和结构进行了表征。为制备具有MRI成像诊断与临床药物治疗的诊疗联用的单分子药物提供了依据。
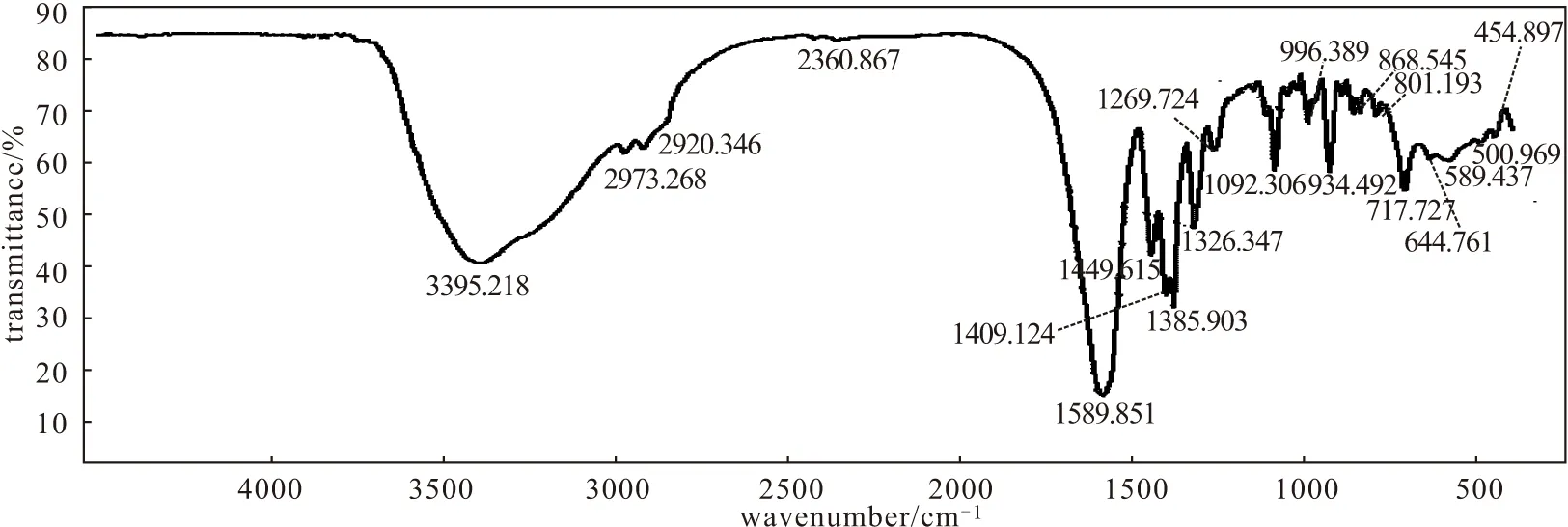
图5 配体L的FTIR图谱
[1] 万福贤,俞开潮.双功能二亚乙基三胺五乙酸系列配体作为磁共振成像造影剂的合成研究进展[J].有机化学,2014,34(4):613-629.
[2] WEN Y,DONG H Q,LI Y,et al.Nano-assembly of bovine serum albumin driven by rare-earth-ion(Gd) biomineralization for highly efficient photodynamic therapy and tumor imaging[J].Journal of Materials Chemistry B,2016,4:743-751.
[3] 李倩,韩林,鄢国平,等.含磺胺嘧啶基团的葡聚糖钆配合物的研究[J].高分子学报,2014(2):263-269.
[4] HUANG J Z,LIAO K,WANG G,et al.Exploitation of the size-exclusion effect of reversed-phase high performance liquid chromatography for the direct analysis of diethylene triamine pentaacetic acid in therapeutic monoclonal antibody formulations[J].Journal of Chromatography A,2016,1455:140-146.
[5] SOUR A,JENNI S,ORT-SUREZ A,et al.Four gadolinium(Ⅲ) complexes appended to a porphyrin:a water-soluble molecular theranostic agent with remarkable relaxivity suited for MRI tracking of the photosensitizer[J].Inorganic Chemistry,2016,55(9):4545-4554.
[6] NI D L,SHEN Z W,ZHANG J W,et al.Integrating anatomic and functional dual-mode magnetic resonance imaging:design and applicability of a bifunctional contrast agent[J].ACS Nano,2016,10(3):3783-3790.
[7] SUN L,LI X,WEI X L,et al.Stimuli-responsive biodegradable hyperbranched polymer-gadolinium conjugates as efficient and biocompatible nanoscale magnetic resonance imaging contrast agents[J].ACS Applied Materials & Interfaces,2016,8(16):10499-10512.
[8] KIM H R,YOU D G,PARK S J,et al.MRI monitoring of tumor-selective anticancer drug delivery with stable thermosensitive liposomes triggered by high-intensity focused ultrasound[J].Molecular Pharmaceutics,2016,13(5):1528-1539.
[9] 张定娃,刘庆奎,吴道伟,等.二乙三胺-N,N″-二(乙酰异烟肼)-N,N′,N″-三乙酸及其中性稀土配合物的合成、表征、驰豫性能研究[J].井冈山大学学报(自然科学版),2010,31(1):40-44.
[10] 刘瑞清,梁爽,江存,等.温度和pH敏感高分子含钆核磁共振成像造影剂的合成及性能[J].高等学校化学学报,2016,37(1):155-160.
[11] 袁泽利,吴庆,杨兴变,等.新型含均三唑席夫碱型大环化合物的合成及其抗菌活性[J].有机化学,2011,31(10):1698-1702.
[12] 郝志峰,吴雅红,汪朝阳,等.酰胺衍生寡聚DTPA钆配合物的合成、表征及弛豫性能[J].高等学校化学学报,2012,33(4):663-667.
Synthesis and Characterization of DTPA Bisamide Ligand Containing Aminoglutethimide
SHUAI Guang-ping,YU Guang-qin,YUAN Fu-ming,CAO Ya-ping,YUAN Ze-li*
(SchoolofPharmacy,ZunyiMedicalUniversity,Zunyi563003,China)
ADTPAbisamideligandcontainingaminoglutethimide,diethylenetriamine-N,N″-bis(acetyl-aminoglutethimide)-N,N′,N″-triaceticacid(L)wassynthesizedbyusingdiethylenetriaminepentaaceticacid(DTPA),aceticanhydride,andaminoglutethimideasrawmaterials.AnditsstructurewascharacterizedbyFTIR,1HNMR,13CNMRandHRMS(ESI-MS).
diethylenetriaminepentaaceticacid(DTPA);aminoglutethimide;synthesis;characterization
国家自然科学基金资助项目(81360471),贵州省国际合作项目([2012]7036),贵州省卫生计生委科学技术基金资助项目(gzwjkj2015-1-001)
2016-10-06
帅光平(1991-),女,贵州瓮安人,硕士研究生,研究方向:新药合成;通讯作者:袁泽利,博士,教授,E-mail:zlyuan2002@126.com。
10.3969/j.issn.1672-5425.2017.02.007
O 641.4
A
1672-5425(2017)02-0029-04
帅光平,余光勤,袁付明,等.含氨鲁米特的DTPA双酰胺配体的合成与表征[J].化学与生物工程,2017,34(2):29-32.

