甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的临床观察
夏松柏,虞冬辉(1.咸宁市中心医院药剂科,湖北咸宁 437100;.咸宁市中心医院神经内科,湖北咸宁437100)
甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的临床观察
夏松柏1*,虞冬辉2(1.咸宁市中心医院药剂科,湖北咸宁 437100;2.咸宁市中心医院神经内科,湖北咸宁437100)
目的:观察甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的疗效和安全性。方法:85例围绝经期抑郁症女性患者随机分为对照组(41例)和观察组(44例)。对照组患者每日早餐后口服盐酸帕罗西汀片20 mg,每日1次;观察组患者在对照组治疗的基础上给予甜梦口服液10 mL,每日早晚各1次。两组均连用8周。观察两组患者的临床疗效,治疗前后围绝经期综合量表(Kupperman)评分、汉密尔顿抑郁量表(HAMD)评分、脑源性神经营养因子(BDNF)水平及不良反应发生情况。结果:对照组和观察组各有1、2例患者失访。两组患者总有效率、不良反应发生率比较,差异均无统计学意义(P>0.05)。治疗后,两组患者Kupperman评分、HAMD评分均显著低于同组治疗前,随时间延长逐渐降低,且观察组患者治疗第8周时Kupperman评分、治疗第2周时HAMD评分均显著低于对照组;两组患者BDNF水平均显著高于同组治疗前,随时间延长逐渐升高,且观察组显著高于对照组,差异均有统计学意义(P<0.05或P<0.01)。结论:甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的疗效和安全性与单用帕罗西汀相当,但在改善症状、升高BDNF方面优于单用帕罗西汀。
围绝经期抑郁症;甜梦口服液;帕罗西汀;疗效;安全性;脑源性神经营养因子
围绝经期是指女性卵巢功能开始衰退至绝经后1年内,因卵巢功能减退和激素波动或下降导致的多系统功能紊乱,除明显的躯体化症状外,50%~60%围绝经期女性有轻度抑郁症,其中1%~3%患有严重抑郁症[1]。临床药物干预多以激素替代疗法、抗抑郁或两者联合用药为主要手段,激素替代疗法具有诸多限制和风险,多数患者不能用或不愿用,抗抑郁药对围绝经期抑郁、焦虑疗效确切,但其副作用使其对部分患者应用受限。帕罗西汀为5-羟色胺再摄取抑制剂(SSRI)类抗抑郁药物,抗胆碱能副作用轻,可用于各种抑郁,影响绝经后女性的雌激素水平,改善情绪和认知功能[2];但常见的不良反应如恶心、厌食、头晕等极大地影响了患者的生活质量,少数患者可出现锥体外系反应[3-4]。甜梦口服液对广泛性焦虑、更年期女性灼口综合征、失眠、脑卒中后遗症、神经衰弱、抑郁症等疗效显著[5-7]。脑源性神经营养因子(BDNF)是神经生长因子家族成员之一,可诱导海马区神经元的生长,BDNF水平可反映抑郁程度,且抑郁程度与BNDF水平呈负相关,女性抑郁患者BDNF水平较男性患者更低[8]。Robinson RG等[9]认为,提高BDNF水平可能成为治疗抑郁症的另一种途径。为此,在本研究中笔者观察了甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的疗效和安全性,旨在为临床提供参考。
1 资料与方法
1.1 研究对象
选择2013年6月—2015年9月我院收治的85例围绝经期抑郁症女性患者,年龄41~60岁。按随机数字表法将所有患者分为观察组(44例)和对照组(41例)。两组患者年龄、病程、围绝经期综合量表(Kupperman)评分、汉密尔顿抑郁量表(HAMD)评分等基本资料比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。本研究方案经医院医学伦理委员会审核通过,所有患者均签署了知情同意书。
1.2 纳入与排除标准
纳入标准:(1)月经不规律>2年;(2)均符合《内分泌病学》中围绝经期综合征的诊断标准[10];(3)均符合《中国精神障碍分类与诊断标准(第3版)》[11]中抑郁症的诊断标准;(4)HAMD的前17项评分>18分。排除标准:(1)伴有严重躯体疾病者;(2)脑器质性疾病者;(3)情感性精神障碍、应激相关的精神障碍、偏执性精神障碍、精神分裂症者;(4)酒精、药物滥用史者。
1.3 治疗方法
对照组患者每日早餐后口服盐酸帕罗西汀片(中美天津史克制药有限公司,规格:20 mg/片,批准文号:国药准字H10950043)20 mg,每日1次;观察组患者在对照组治疗的基础上给予甜梦口服液(烟台荣昌制药股份有限公司,规格:10 mL/支,批准文号:国药准字Z37020040)10 mL,每日早晚各1次。两组均连用8周。治疗时和治疗后第2、4、6、8周随访并接受专业心理咨询师心理疏导。
表1 两组患者基本资料比较(s)Tab 1 Comparison of general information between 2 groups(s)

表1 两组患者基本资料比较(s)Tab 1 Comparison of general information between 2 groups(s)
组别观察组对照组n 44 41年龄,岁49.25±5.63 48.79±6.27病程,月12.04±5.14 11.67±4.92 Kupperman评分,分26.87±6.76 25.65±7.61HAMD评分,分25.99±2.76 25.37±2.43
1.4 观察指标
观察两组患者治疗前后Kupperman评分、HAMD评分、BDNF水平及不良反应发生情况。采用酶联免疫吸附法(ELISA,试剂盒由武汉华美生物工程有限公司提供)以Multiskan MK3型酶标仪和Wellwash 4 MK2型洗板机[均购自赛默飞世尔科技(中国)有限公司]检测BDNF水平。
1.5 疗效判定标准
痊愈:HAMD减分率≥75%;显效:HAMD减分率50%~74%;好转:HAMD减分率25%~49%;无效:HAMD减分率<25%。总有效率=(痊愈例数+显效例数+好转例数)/总例数×100%。HAMD减少率=(治疗前HAMD评分—治疗后HAMD评分)/治疗前HAMD评分×100%。
1.6 统计学方法
采用SPSS 19.0统计软件对数据进行分析。计量资料以s表示,采用t检验;计数资料以率表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者完成治疗情况
对照组有1例患者于治疗第4周时因不良反应退出,共有40例患者完成治疗;观察组有2例患者于治疗第6周时因其他原因退出,共有42例患者完成研究。
2.2 两组患者临床疗效比较
两组患者总有效率比较,差异无统计学意义(P>0.05),详见表2。
2.3 两组患者治疗前后Kupperman评分比较
治疗前,两组患者Kupperman评分比较,差异无统计学意义(P>0.05)。治疗第4、6、8周时,两组患者Kupperman评分均显著低于同组治疗前,随时间延长逐渐降低,且治疗第8周时观察组显著低于对照组,差异均有统计学意义(P<0.05或P<0.01),详见表3。

表2 两组患者临床疗效比较[例(%)]Tab 2 Comparison of clinical efficacy between 2 groups[case(%)]
表3 两组患者治疗前后Kupperman评分比较(s,分)Tab 3 Comparison of Kupperman score between 2 groups before and after treatment(s,score)

表3 两组患者治疗前后Kupperman评分比较(s,分)Tab 3 Comparison of Kupperman score between 2 groups before and after treatment(s,score)
注:与治疗前比较,*P<0.01;对照组比较,#P<0.05Note:vs.before treatment,*P<0.01;vs.control group,#P<0.05
组别观察组对照组治疗第8周时8.76±6.06*#11.97±6.89*n 42 40治疗前26.87±6.76 25.65±7.61治疗第4周时18.03±7.73*19.73±6.89*治疗第6周时13.68±6.59*14.39±7.06*
2.4 两组患者治疗前后HAMD评分比较
治疗前,两组患者HAMD评分比较,差异无统计学意义(P>0.05)。治疗第2、4、6、8周时,两组患者HAMD评分均显著低于同组治疗前,随时间延长逐渐降低,且治疗第2周时观察组显著低于对照组,差异均有统计学意义(P<0.01),详见表4。
表4 两组患者治疗前后HAMD评分比较(s,分)Tab 4 Comparison of HAMD score between 2 groups before and after treatment(s,score)

表4 两组患者治疗前后HAMD评分比较(s,分)Tab 4 Comparison of HAMD score between 2 groups before and after treatment(s,score)
注:与治疗前比较,*P<0.01;与对照组比较,#P<0.01Note:vs.before treatment,*P<0.01;vs.control group,#P<0.01
组别观察组对照组治疗第8周时5.39±0.98*5.68±1.03*n 42 40治疗前25.99±2.76 25.37±2.43治疗第2周时19.26±1.56*#23.85±0.89*治疗第4周时10.65±1.03*11.35±2.09*治疗第6周时7.43±0.97*7.95±1.34*
2.5 两组患者治疗前后BDNF水平比较
治疗前,两组患者BDNF水平比较,差异无统计学意义(P>0.05)。治疗后,两组患者BDNF水平均显著高于同组治疗前,且观察组显著高于对照组,差异均有统计学意义(P<0.01),详见表5。
表5 两组患者治疗前后BDNF水平比较(s,ng/mL)Tab 5 Comparison of BDNF level between 2 groups before and after treatment(s,ng/mL)
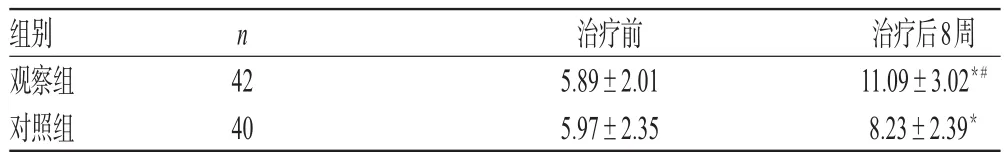
表5 两组患者治疗前后BDNF水平比较(s,ng/mL)Tab 5 Comparison of BDNF level between 2 groups before and after treatment(s,ng/mL)
注:与治疗前比较,*P<0.01;与对照组比较,#P<0.01Note:vs.before treatment,*P<0.01;vs.control group,#P<0.01
组别观察组对照组治疗后8周11.09±3.02*#8.23±2.39*n 42 40治疗前5.89±2.01 5.97±2.35
2.6 不良反应
观察组患者出现1例口干、2例燥热感,不良反应发生率为7.14%;对照组患者出现1例严重恶心、腹泻,2例轻微头晕、头痛,3例口干、便秘,2例乏力伴胃部不适感,不良反应发生率为19.51%。两组患者不良反应发生率比较,差异无统计学意义(P=0.097)。出现不良反应的患者中除1例为严重恶心、腹泻退出治疗外,其他患者症状均较轻微,未中断治疗。治疗期间血尿常规及肝肾功能检查均无明显异常。
3 讨论
现代医学认为,卵巢功能衰退是引起围绝经期综合征临床症状和代谢变化的主要原因,其可产生一系列以自主神经功能失调为主的临床症状,如失眠、抑郁、焦虑、烦躁等多种精神和躯体症状,而抑郁和焦虑是围绝经期常见的精神症状,过激的情绪反应可导致或加重身心疾病[1-2]。
帕罗西汀为典型的抗抑郁药物,可改善神经递质5-羟色胺含量。抑郁、焦虑等精神症状与神经炎症因子白细胞介素-6、BDNF水平密切相关,而BDNF与情绪、认知功能相关,脑卒中后数小时内BDNF急剧降低,其可以预测脑卒中后情绪障碍和预后[9];同时,BDNF还可作为更年期抑郁和抗抑郁疗效的评价指标[8]。营养神经和抗炎治疗有可能是治疗抑郁症未来的方向[9]。李春丽等[12]证实,甜梦口服液可提高睡眠剥夺大鼠的认知功能和行为能力,可能与其提高了海马区的BDNF含量相关。甜梦口服液对改善围绝经期相关症状有积极意义,但与其改善围绝经期患者激素水平无关[13]。
中医认为,围绝经期相关的临床症状以肾虚为根本,肾虚的实质是下丘脑-垂体-卵巢轴的神经内分泌功能失调,免疫系统功能减退,围绝经期抑郁与多系统功能失调相关,而补肾是基础[5]。甜梦口服液具有补肾益气,健脾和胃之功效,其由刺五加、党参等多种中药材组成,方中刺五加健脑安神[14],能够调节大脑单胺氧化酶水平,改善中枢神经系统的功能,配伍党参具镇静、催眠、抗紧张、抗焦虑、抗抑郁的作用[15],对更年期相关症状有良好疗效。孙林琳等[5]认为,甜梦胶囊对更年期女性灼口综合征有良好疗效,通过调节下丘脑-垂体-卵巢轴的功能,促使神经、内分泌的功能恢复,这也可能是甜梦口服液联合帕罗西汀治疗围绝经期抑郁症可提高痊愈率的机制所在。围绝经期抑郁症与多种因素密切相关,BDNF降低为其显著特征之一,而BDNF可改善患者情绪、认知功能。研究发现,甜梦口服液可提高5-羟色氨拮抗大鼠海马区BDNF表达,提高大鼠认知能力[12]。
本研究结果显示,两组患者总有效率、不良反应发生率比较,差异均无统计学意义。治疗后,两组患者Kupperman评分、HAMD评分均显著低于同组治疗前,随时间延长逐渐降低,且观察组治疗第8周时Kupperman评分、治疗第2周时HAMD评分均显著低于对照组,BDNF水平均显著高于同组治疗前,且观察组高于对照组,差异均有统计学意义。这提示,甜梦口服液联合帕罗西汀可提高围绝经期抑郁症患者的生活质量和治疗依从性。
综上所述,甜梦口服液联合帕罗西汀治疗围绝经期抑郁症的疗效和安全性与单用帕罗西汀相当,但在改善症状、升高BDNF水平方面优于单用帕罗西汀。由于本研究纳入的样本量较小,未探讨甜梦口服液对血清BDNF水平的影响及BDNF与大脑海马区中BDNF水平是否平行、甜梦口服液是否影响人体大脑BDNF,故此结论有待大样本、多中心研究进一步证实。
[1] 林禹舜,刘忠杰,王丽彦.围绝经期抑郁症中西医研究进展[J].现代中医临床,2014,21(1):57-60.
[2] 谢双燕,周伯荣,胡佳佳,等.帕罗西汀提高绝经后焦虑/抑郁患者的雌激素水平和认知功能[J].中国神经免疫学和神经病学杂志,2015,22(1):30-33.
[3] 欧阳净,杨佳丹.帕罗西汀的不良反应文献分析[J].中国神经精神疾病杂志,2010,36(8):471-484.
[4] 程丽玲,徐作国.帕罗西汀的不良反应/事件分析[J].中国药物警戒,2012,9(7):431-432.
[5] 孙林琳,刘建伟.甜梦胶囊治疗更年期女性灼口综合征的疗效观察[J].中国药房,2009,20(20):1573-1574.
[6] 梁宏光,王淑莲,雍生满,等.甜梦胶囊治疗广泛性焦虑症的疗效分析[J].宁夏医学杂志,2008,30(9):838-839.
[7] 刘茹.甜梦口服液治疗广泛性焦虑症的疗效观察[J].中草药,2006,37(10):1550-1551.
[8] Karege F,Perret G,Bondolfi G.Decreased serum brainderived neurotrophic factor levels in major depressed patients[J].Psychiatry Res,2002,109(2):143-148.
[9] Robinson RG,Jorge RE.Post-stroke depression:a review [J].Am J Psychiatry,2016,173(3):221-231.
[10] 廖二元,超楚生.内分泌病学[M].北京:人民卫生出版社,2001:1233-1238.
[11] 中华医学会精神病学分会.中国精神障碍分类与诊断标准:第3版[J].中华精神科杂志,2001,34(3):184-188.
[12] 李春丽,徐洋,姜静.甜梦口服液对睡眠剥夺大鼠学习记忆、炎症因子及神经递质的影响[J].中药药理与临床,2015,31(2):147-148.
[13] 曾永青.甜梦胶囊治疗更年期综合征失眠的临床观察[J].亚太传统医药,2010,7(6):29-31.
[14] 张旭东,马杰,李杜燕,等.刺五加制剂的临床运用进展[J].中国药房,2008,19(3):231-233.
[15] 白雪歌,穆洪,张万祥.甜梦口服液治疗冠脉搭桥术后患者焦虑抑郁的临床观察[J].中草药,2007,38(5):747-778.
(编辑:陈 宏)
Clinical Observation of Tianmeng Oral Liquid Combined with Paroxetine in the Treatment of Perimenopausal Depression
XIA Songbai1,YU Donghui2(1.Dept.of Pharmacy,Xianning Central Hospital,Huibei Xianning 437100,China;2.Dept.of Neurology,Xianning Central Hospital,Huibei Xianning 437100,China)
OBJECTIVE:To observe the efficacy and safety of Tianmeng oral liquid combined with paroxetine in the treatment of perimenopausal depression.METHODS:85 patients with perimenopausal depression were randomly divided into control group(41 cases)and observation group(44 cases).Control group received Paroxetine hydrochloride tablet 20 mg after the breakfast,once a day.Observation group was additionally given Tianmeng oral liquid 10 mL,once every morning and evening.They were treated for 8 weeks.The clinical efficacy,Kupperman score,HAMD score,brain-derived neurotrophic factor(BDNF)level before and after treatment,and the incidence of adverse reactions in 2 groups were observed.RESULTS:There were 1 patient lost in follow-up in control group,and 2 in observation group.There were no significant differences in the total effective rate and the incidence of adverse reactions in 2 groups(P>0.05).After treatment,Kupperman score and HAMD score in 2 groups were significantly lower than before,gradually reduced by time extension,Kupperman score after 8 weeks and HAMD score after 2 weeks in ob-servation group were lower than control group,BDNF levels were significantly higher than before,gradually increased by time extension,and observation group was higher than control group,with statistical significances(P<0.05 or P<0.01).CONCLUSIONS:The efficacy and safety of Tianmeng oral liquid combined with paroxetine in the treatment of perimenopausal depression are similar to paroxetine alone,while better than paroxetine alone in terms of improving symptoms and increasing BDNF.
Perimenopausal depression;Tianmeng oral liquid;Paroxetine;Efficacy;Safety;Brain derived neurotrophic factor
R749
A
1001-0408(2017)03-0344-04
2016-07-12
2016-11-22)
*主任药师。研究方向:药事管理。电话:0715-8896142。E-mail:303893537@qq.com
DOI10.6039/j.issn.1001-0408.2017.03.17

