FDP试剂在Sysmex CS5100全自动凝血分析仪上使用的性能评估
陈登锴
【摘要】 目的:验证日本积水(Sekisui)医疗株式会生产的FDP试剂盒在日本Sysmex公司CS5100全自动凝血分析仪检测FDP的分析性能。方法:参照临床和实验室标准协会(Clinical and Laboratory Standars Institute,CLSI)及其他相关文献,检测FDP检测系统的精密度、准确性、分析测量范围、可报告范围、样本针的携带污染、抗干扰能力和参考范围,并与试剂说明书的质量性能进行比较。结果:FDP批内变异系数<5%;批间变异系数<5%。FDP的线性方程为Y=0.9853X+1.4031,r2=0.9993,r2>0.975,在2.5~120 μg/mL范围内,FDP结果呈线性。检测高值标本时稀释倍数不宜超过8倍,以保证结果的准确性。抗干扰实验:在游离型胆红素和结合型胆红素<20.0 mg/dL,溶血血红蛋白<500 mg/dL,乳糜浊度<3000 CM的情况下,对FDP的检测影响均不明显,相对偏差均<10%。参考区间验证:检测20个健康体检者的FDP值结果均在厂商提供的生物参考区间FDP<5.0 μg/mL范围内。结论:日本积水公司生产的FDP试剂盒及标准品和质控品在Sysmex CS5100全自动凝血分析仪上检测FDP系统主要分析性能验证结果与厂家提供的分析性能一致,符合质量目标的要求。
【关键词】 FDP; 全自动凝血分析仪; 性能; 评估
【Abstract】 Objective:To verify the Japanese Sekisui medical strains will produce FDP kit in Japan Sysmex CS5100 Automatic Coagulation Analyzer to detect FDP analysis performance.Method:According to clinical and laboratory standards institute and other relevant documents,the FDP system precision,accuracy,measurement range,reportable range,sample carryover needle,the anti-interference ability and the reference range were detected,and quality performance and kit were compared.Result:The within-run coefficients of variations(CV)were less than 5.0%,between-run coefficients of variations(CV)were less than 5.0%.The linear equation of FDP was Y=0.9853X+1.4031,r2=0.9993,r2>0.975,its linear was 2.5-120 μg/mL.It was not more than 8 times to detect high value samples to ensure the accuracy of the results.Interference test:there was no obvious interference observed when the concentration of free bilirubin or conjugated bilirubin <20.0 mg/dL,hemoglobin<500 mg/dL,and turbidity chyle<3000 CM in the sample.The relative deviation was <10%.Reference range:the measured results of FDP in 20 normal individuals were all in the reference interval of producers.Conclusion:The main performance index of the reagent for the FDP made in Japanese Sekisui on sysmex CS5100 automatic coagulation analyzer consistent with the analysis of the manufacturers performance,and meet the requirements of quality objectives.
【Key words】 FDP; Automatic coagulation analyzer; Performance; Evaluation
First-authors address:Fujian Provincial Maternal and Child Health Hospital,Fuzhou 350001,China
doi:10.3969/j.issn.1674-4985.2016.36.034
纤维蛋白(原)降解产物(fibrin degradation products,FDP)是指当机体纤溶亢进时,血中纤溶酶降解血浆中的纤维蛋白和纤维蛋白原的各种降解产物,包括X、X、Y、Y、A、B、C、H、D、D-二聚体等,统称为FDP,是继发性和原发性纤溶系统亢进的判定指标[1]。作为纤维蛋白特殊降解产物的D-二聚体和FDP较凝血酶原时间、血小板等更早出现,可辅助诊断前期DIC[2]。DIC是在某种致病因素的作用下,全身小血管内广泛微血栓的形成及继发性纤溶亢进的一種综合征[3]。由于现有的检测方法可快速、敏感、特异地检测血中D-二聚体和FDP水平,故在临床应用尤为广泛。本研究应用Sysmex公司CS5100全自动凝血分析仪,根据临床和实验室标准协会(Clinical and Laboratory Standars Institute,CLSI)要求[4-5],对日本Sekisui FDP试剂盒检测FDP的精密度、准确度、灵敏度、分析测量范围、可报告范围、样本针携带污染、抗干扰性能等方面进行临床应用评价。endprint
1 材料与方法
1.1 仪器与试剂 (1)仪器:日本Sysmex公司CS5100全自动凝血分析仪。(2)参数:样本量为10 μL,试剂量为R1∶100 μL,R2∶100 μL。(3)试剂:日本积水(Sekisui)医疗株式会社生产的FDP试剂(批号为817REK);质控品批号为827REJ;干扰物批号为ZS6003。
1.2 标本 本院住院患者或正常体检者新鲜全血,按1∶9的比例与109 mmol/L的枸橼酸钠抗凝剂混匀抗凝,3500 r/min下離心10 min,以取得少血小板血浆,并在2 h内完成检测。
1.3 方法
1.3.1 质量控制 每天开机进行日常保养,检测质控品,所有实验必须在质控结果在控的前提下进行,质控的控制范围为L∶7.1~13.1 μg/mL;
H∶23.8~35.8 μg/mL。
1.3.2 精密度 批内精密度,根据CLSI EP15-A2文件[4-6],取混合血浆(接近参考值/医学决定水平)、高值质控样本、低值质控样本,分别连续测定10次,所有检测在2 h内完成,计算平均值(X)、标准差(SD)和变异系数(CV)。
1.3.3 正确度 (1)不同批标准品的测定:使用厂家提供的有注册证的5个水平配套校准品,各校准品浓度分别测定3次,计算平均值,并与定标值进行比较考核,偏差范围应≤5%。(2)方法学相关性的参考:根据CLSI EP-9A对能力比对与偏差评估的相关要求[6],选取60例以上标本(样本应分为高中低三种浓度,均匀分布在分析测量范围内),在对照检测系统上和考核检测系统上各进行1次测定,进行相关系数曲线的拟合,相关系数应r≥95%。
1.3.4 分析测量范围 根据CLSI EP6-A对分析测量范围的相关要求,取高值血浆标本和接近零值的血浆标本进行配置,按0∶10、1∶10、2∶10、3∶10、4∶10、5∶10、6∶10、7∶10、8∶10、9∶10和10∶10配制成11个浓度梯度,重复检测2次。计算每个浓度的平均值、标准差及变异系数,拟合一条曲线,分别计算每个浓度检测平均值Xs与理论浓度值Xs偏差。
1.3.5 可报告范围 使用定值的高值样本,以仪器自动稀释模式进行2×、4×、5×、8×、10×、20×的测定,稀释模式下的计算结果与理论值进行比较,偏差在20%以内,则可视为可接受的稀释倍数。可接受的稀释倍数×线性上限=临床可接受的最高报告范围。
1.3.6 样本针的携带污染 检测一组样本(3次高值→3次生理盐水→FDP),试验重复5次。计算携带污染的平均污染量,平均污染量≤5%。
1.3.7 抗干扰性能 选用4种已知干扰物质(游离型胆红素,结合型胆红素,溶血血红蛋白及乳糜)和空白液分别与混合血浆进行混合,混合后的两个浓度分别进行配制,形成8组具有6个干扰物浓度梯度的样本(高、低值各4组),每个样本重复测定2次。计算平均值,各平均结果与空白对照样本的偏移量应≤±10%,结果可接受。
1.3.8 参考区间的验证 选取20例正常体检的标本验证参考范围的适用性。
1.4 统计学处理 采用SPSS.19.0软件及Microsoft office Excel软件汇总统计及绘制图表。
2 结果
2.1 质控结果 质控结果均落在x±s范围内,显示在控,可进行后续的实验。
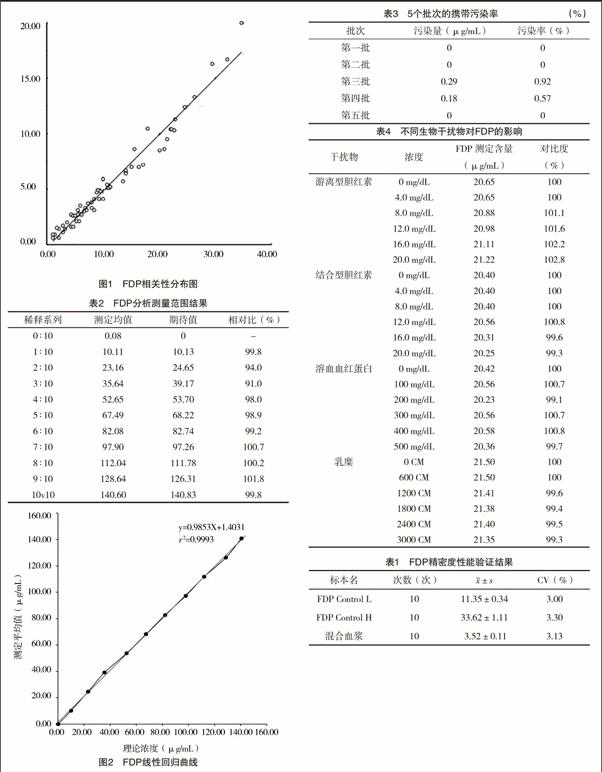
2.2 精密度 Control L为低水平、Control H为高水平,批内CV均<5%,见表1。
2.3 正确度 (1)不同批标准品的测定:检测的5个水平标准品的均值,分别与定标值比较,偏差范围分别为1.01%、1.25%、2.81%、1.85%、4.01%,均≤5%。(2)方法学相关性的参考:本实验用CS5100配套的BIOLINK试剂作对照检测系统,对64例标本进行测定,结果如图1,直线方程Y=0.508X-0.261,相关系数r=0.984。
2.4 分析测量范围 结果分析见表2,回归曲线见图2,线性方程为Y=0.9853X+1.4031。r2=0.9993,r2>0.975,斜率a在0.97~1.03范围内。本实验验证了在2.5~120 μg/mL范围内,FDP结果呈线性。
2.5 可报告范围 实验结果显示,结果偏差范围在20%以内的稀释倍数为8倍,故可报告范围为120×8=960 μg/mL。
2.6 样本针携带污染 结果显示平均污染率为0.30%,小于规定的5%,则样本针携带污染评价为合格,见表3。
2.7 抗干扰性能 在游离型胆红素和结合型胆红素<20.0 mg/dL,溶血血红蛋白<500 mg/dL,乳糜浊度<3000 CM的情况下,对FDP的检测影响均不明显,相对偏差均<10%,见表4。
2.8 参考区间验证 检测20个健康体检者的FDP值均落在0.5~4.0 μg/mL,平均(1.53±0.28)μg/mL,结果均在厂商提供的生物参考区间FDP<5.0 μg/mL范围内。
3 讨论
正常情况下,人体内的促凝与抗凝系统呈动态平衡,各种促凝及抗凝物质的相互作用与相互制约形成了凝血自我调控过程[7-9]。FDP有抗凝血酶及抗血小板聚集功能,在生理情况下可防止微循环形成[2]。血中FDP浓度的高低与机体纤溶系统活性程度成正比,FDP升高,表示纤溶活性增强[10],提示体内存在着频繁的纤维蛋白降解过程。结合D-二聚体检测,可用于原发性和继发性纤溶亢进的鉴别[11]。FDP的增高是诊断弥漫性血管内凝血(DIC)的实验指标之一,是孕期凝血功能监测、术后危重患者、严重感染、恶性肿瘤、羊水栓塞等严重疾病的重要观察指标之一[12-16]。临床上选择快速简便且准确性高的方法检测FDP尤为重要[17]。endprint
FDP的检测由早期的定性、半定量发展为定量分析,方法学由手工操作的ELISA、胶体凝集法到可自动化操作的胶体免疫比浊法[18-19],其检测速度和定量的灵敏度与特异性都明显提高。本实验室使用的日本积水公司的FDP试剂采用乳胶凝集比浊法,标本中的FDP与鼠抗FDP单克隆抗体胶乳粒发生抗原抗体反应,产生凝聚以致浊度上升。通过分光光度计测定浊度变化率,从而测得FDP的浓度。由于其干扰因素少,精密度和准确性高,得到广泛的应用[20]。
本验证结果显示,日本积水公司的FDP试剂在Sysmex CS5100全自动凝血分析仪上批内和批间的變异系数均≤5%,说明该检测系统具有良好的重复性和稳定性。检测下限低于厂家提供的参考范围,提示有较好的灵敏度。在分析测量范围的验证中计算相关系数r=0.9853,提示检测值与预期值相关系数线性良好。当稀释倍数超过8倍时,结果偏差范围超过10%,提示检测高值标本时稀释倍数不宜超过8倍,否则影响准确性。样本针携带污染的验证结果显示平均污染率为0.30%,小于规定的5%,提示样本针携带污染合格,可忽略。抗干扰性能的验证结果提示检测系统有良好的抗干扰能力,则对标本的要求就相对较低。由20例健康体检者的检测结果统计的参考区间落在厂家提供的参考区间内,提示引用的参考区间适用用本实验体系。
本研究对日本积水公司生产的FDP试剂盒及标准品和质控品在Sysmex CS5100全自动凝血分析仪上检测FDP系统进行了质量性能的评价,提示检测FDP的主要分析性能验证结果与厂家提供的分析性能一致,符合质量目标的要求,可供临床使用。
参考文献
[1] Hagiwara S,Oshima K,Aoki M,et al.Usefulness of fibrin degradation products and d-dimer levels as biomarkers that reflect the severity of trauma[J].Trauma Acute Care Surg,2013,74(5):1275-1278.
[2]王敏莉.妊娠晚期孕妇凝血四项、FDP、D-二聚体的变化及临床意义[J].中华全科医学,2013,11(12):1951-1952.
[3]高亚玥,赵永强,王书杰.酶联免疫吸附法检测抗肝素/血小板因子4复合物抗体的临床意义[J].中日友好医院学报,2011,25(6):331-337.
[4] Cuker A,Ortel T L.ASH evidence-based guidelines:is the IgG-specific anti-PF4/heparin ELISA superior to the polyspecific ELISA in the laboratory diagnosis of HIT[J].Hematology,2009,2009(1):250-252.
[5]胡丽涛,王治国.血凝分析仪的性能评估方法的研究进展[J].国际检验医学杂志,2011,32(9):975-976.
[6]杨志钊,缪丽韶,杨山虹,等.利用CLSI EP15-A2指南验证精密度和准确度[J].国际检验医学杂志,2010,31(3):231-232,237.
[7] Ringwala S M,Dibattiste P M,Schneider D J.Effects on platelet function of a direct acting antagonist of coagulation factor Xa[J].J Thromb Thrombolysis,2012,34(3):291-296.
[8] Cramer T J,Gale A J.The anticoagulant function of coagulation factor V[J].Thromb Haemost,2012,107(1):15-21.
[9] Persson E,Olsen O H.Allosteric activation of coagulation factor VIIa[J].Frontiers in Bioscience,2011,16(16):3156-3163.
[10] Kaser A,Brandacher G,Steurer W,et al.Heparin-induced thrombocytopenia[J].Der Internist,2012,51(9):1134-1135.
[11] Kelton J G,Hursting M J,Heddle N,et al.Predictors of clinical outcome in patients with heparin-induced thrombocytopenia treated with direct thrombin inhibition[J].Blood Coagul Fibrinolysis,2008,19(6):471-475.
[12]王兰兰.医学检验项目选择与临床应用[M].北京:人民卫生出版社,2010:76-79.
[13] Kaneko T,Wada H.Evaluation of FDP and D-dimer for the diagnosis of DIC [J]Rinsho Byori,2011,(suppl 147):79.
[14]刘慧英.正常孕妇不同孕期及产后常规凝血功能检测指标参考区间调查[J].河北医学,2012,18(9):1253-1255.
[15]张春荣,张翠波.妊娠期高血压疾病患者凝血功能指标的检测及其临床意义[J].中国妇幼保健,2011,26(3):472-473.
[16]寿玮龄,崔巍.恶性肿瘤出凝血异常机制[J].协和医学杂志,2012,3(4):482-485.
[17]马升俊.STAGO STA-R全自动血凝仪性能验证与评价[J].国际检验医学杂志,2013,34(1):91-93.
[18]刘刚.纤维蛋白(原)降解产物检测及临床研究进展[J].临床和检验医学杂志,2014,13(19):1653-1655.
[19]谭同均,龙琴,彭宇生,等.日立7600-020全自动生化分析仪检测FDP和D-D的性能验证[J].现代检验医学杂志,2012,27(1):91-94.
[20]周雯雯,宋鉴清,丁奇,等.对检测纤维蛋白降解产物的两种试剂评价[J].血栓与止血学杂志,2014,20(4):187-190.
(收稿日期:2016-10-12) (本文编辑:张爽)endprint

