HPLC法测定脑血疏口服液中黄芪甲苷的含量
王庆学+韩琳
[摘要]目的 建立脑血疏口服液中黄芪甲苷的含量测定方法。方法 采用高效液相色谱法(HPLC)定量分析脑血疏口服液中黄芪甲苷的含量。色谱柱:Shimadzu UVP-ODS(5 μm,250 mm×4.6 mm);十八烷基键合硅胶为填充剂;流动相:乙腈-水(17:33)。理论板数按黄芪甲苷峰计应≤4000。结果 黄芪甲苷的进样量在1.78~24.92 μg呈良好的线性关系,r=0.9998;平均回收率为101.02%,相对标准偏差(RSD)=4.03%,在常温下8 h内稳定性较好。结论 HPLC法简便快速、准确、重现性好、结果可靠,该黄芪甲苷含量测定法可作为控制脑血疏口服液质量的方法。
[关键词]脑血疏口服液;黄芪甲苷;高效液相色谱法;含量测定
[中图分类号] R927.2 [文献标识码] A [文章编号] 1674-4721(2016)11(c)-0137-03
[Abatract]Objective To establish an assay method of astragaloside in Naoxueshu Oral Liquid by HPLC.Methods The content of astragaloside in Naoxueshu Oral Liauid was detected by HPLC,and Shimadz UVP-ODS(5 μm,250 mm×4.6 mm)Column was used.18 alkyl bonding silica gel as the filling agent.The mobile phase was a mixture of acetonitrile-water (17∶33).According to the theory of number of astragalus armor plate tower peak computation should not below 4000.Results A good linear relationship of Astragaloside was in the range of injection volume was from 1.78 to 24.92 μg (r=0.9998),the average recovery rate was 101.02%,RSD=4.03%.The constancy was good within 8 hours under common temperature.Conclusion The HPLC method is convenient,sensitive and accurate.It can be a method for quality control of Naoxueshu Oral Liquid in production.
[Key words]Naoxueshu Oral Liquid;Astragaloside;HPLC method;Content determination
脑血疏口服液主要含有黄芪、水蛭、大黄、牡丹皮等,可益气活血,在临床上使用多年,效果良好。主要可以增加脑血流量,改善微循环,促进吞噬细胞的吞噬功能,加速脑血肿的吸收[1-3],因此,该药是治疗出血性中风的首选药物之一。方中君药黄芪为常用中药,素有“补药之长”之称,具有益气固表,利尿托毒等功效,还具有保护缺血性心肌、调节血压、扩张血管、增强免疫力、抗病毒、抗衰老等作用,还具有一定的抗癌作用[4-6]。黄芪的药用价值很高,临床上常被用来治疗非特异性免疫功能低下,乙肝和心血管系统等疾病;黄芪中含有多种化学成分,如多糖类成分、黄芪皂苷Ⅰ~Ⅷ、异黄酮、钙、钾等,其中黄芪甲苷具有强心作用、心肌缺血作用及抑制血小板凝集和抗氧化、衰老等作用[7-8],因此对方中君药黄芪的质量标准研究对脑血疏口服液的质量标准尤其重要。本研究考察多种测定条件,高效液相色谱法(HPLC)具有分离效能高、分析速度快、检测灵敏度高、自动化操作、分析精确度高等优点,故采用HPLC法测定脑血疏中黄芪甲苷的含量,以提高该药品的质量标准。
1仪器与试药
日本岛津1260型高效液相色谱仪,SPD-20A(V)紫外检测器;脑血疏口服液(山东沃华医药科技股份有限公司,批准文号:国药准字Z20070059);黄芪甲苷标准品(批号110781~201402,中国食品药品检定研究院);乙腈为色谱纯(Fisher Scientific);水为纯化水;其余试剂均为分析纯。
2方法与结果
2.1色谱条件
色谱柱:岛津Shimadzu UVP-ODS(5μm,250 mm×4.6 mm);十八烷基键合硅胶为填充剂;流动相:乙腈-水(17∶33);检测波长:200 nm;流速:1.0 ml/min;样品进样量为10 μl。理论板数符合《中国药典》2015年版要求。
2.2溶液配制
精密称取黄芪甲苷标准品9.315 mg,置于10 ml量瓶中,加甲醇溶解稀释至刻度,摇匀,得标准品溶液。
取脑血疏口服液(150101、1501021、150103、150401、150402、150403、150701、151002、151201、151202)样品,精密量取10 ml,置分液漏斗中,分别加20 ml水饱和的正丁醇溶液提取4次,合并正丁醇液;分别取100 ml氨试液洗涤3次,取正丁醇液蒸干。残渣用甲醇溶解并移入5 ml量瓶中,稀释至刻度,摇匀,薄膜过滤,得供试品溶液。
按照药品的制备方法制备缺黄芪的制剂作为空白溶液。
2.3线性试验
配制标准品溶液,浓度分别为0.356 mg/ml、0.712 mg/ml、1.068 mg/ml、1.424 mg/ml、1.780 mg/ml、2.136 mg/ml、2.492 mg/ml,取10 μl分別进样,测定其峰面积分别为110 209、709 820、1 263 252、1 910 580、2 492 408、3 178 988、3 746 508,绘制标准曲线,回归方程y=171312x-523518,r=0.9995,结果显示进样量为3.56~24.92 μg范围内线性关系良好。
2.4精密度试验
精密吸取“2.2”项下标准品溶液,在相同色谱条件下重复进样5次,记录其峰面积分别为1 313 181、1 368 894、1 358 224、1 311 770、1 303 445,RSD为2.26%。
2.5重复性试验
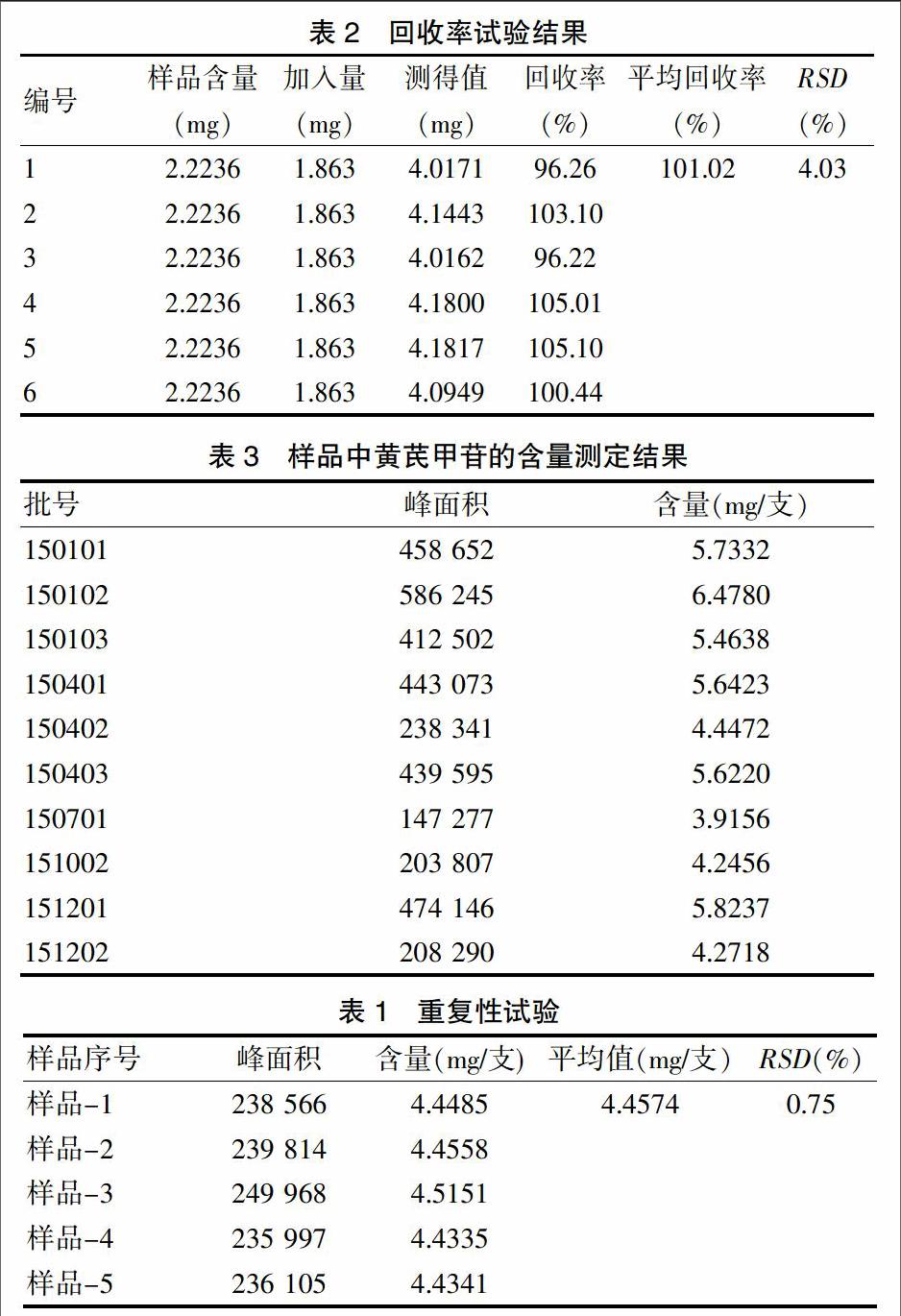
精密量取样品(150402)5 ml共5份,照“2.2”项下供试品溶液制备方法进行处理并测定,结果显示重复性良好(表1)。
2.6稳定性试验
按样品溶液制备方法制得供试品溶液(批号:150402),精密吸取供试品溶液10 μl注入液相色谱仪测定。分别于0、2、4、6、10、16、20、24 h测定1次。峰面积依次为236 851、240 501、239 980、242 697、239 803、 236 654、231 569、235 980,RSD为1.46%,提示供试品溶液在24 h内稳定。
2.7回收率试验
精密量取已知含量的脑血疏口服液(批号:150402)5 ml置分液漏斗中,分别精密量取标准品溶液(0.9 315 mg/ml)各2 ml加入,按2.2项下方法制备供试品溶液并测定,计算其回收率:回收率(%)=(测得量-供试品所含被测成分量)/加入对照品的量×100%。得平均回收率为101.02%,RSD为4.03%,加样回收良好(表2)。
2.8空白试验
取“2.2”项下的空白溶液,按相同色谱条件进样,在与对照品相同时间处无色谱峰出现,表明其他成分对黄芪甲苷的测定无干扰。
2.9样品测定
各样品进样10 μl,按“2.1”项下色谱条件测定,结果见表3。
3讨论
测定黄芪甲苷含量的方法有很多,如比色法[9]、分光光度法[10]及薄层扫描法[11]等,近年来,黄芪甲苷的分析手段有了进一步的提高,有高效液相色谱-蒸发光散射检测器法及在线固相萃取高效液相色谱法等[12-14],但是该方法增加了检验成本,相对提高了药品的成本,HPLC的分辨率较高,重复性好,色谱柱还可以反复使用,节约成本,并能较好的检测黄芪甲苷的含量[15],故本研究仅对该方法进行研究。
由于黄芪甲苷属于四环三萜类皂苷,紫外末端吸收(λmax=200.8 nm),综合考虑多种因素,选择200 nm为本实验的测定波长。另外本研究还考察了甲醇-水及乙腈-水的流动相体系,结果发现,由于黄芪甲苷的最大吸收波长较低,用甲醇-水作为流动相时,黄芪甲苷与其他峰之间的分离效果不好,而乙腈-水(17∶33)作为流动相时,分离度符合药典要求,且分析时间较短,节省成本。
由于黄芪含有多种成分,一般的处理方法无法将多余成分除去,影响分离效果。本实验按照“2.2”项下方法处理样品,能将大部分杂质成分除去,色谱峰中的杂质峰较少,黄芪甲苷与其他非目标峰之间的分离度符合药典要求。
本研究以Shimadz UVP-ODS为色谱柱,乙腈-水(17∶33)为流动相,采用HPLC紫外检测法测定脑血疏口服液中黄芪甲苷的含量,方法简便、结果准确、重现性好,建议用于脑血疏口服液的质量标准控制。
[参考文献]
[1]陈澈,院立新,张根明.脑血疏口服液在脑血管病方面的临床应用和实验研究進展[J].中西医结合心脑血管病杂志,2014,12(8):1005-1006.
[2]王寿先,宋仁兴,王喆,等.脑血疏口服液促进血肿吸收的临床疗效评价[J].中西医结合心脑血管病杂志,2014,12(4):452-453.
[3]张选围,王凌.脑血疏口服液对气虚血瘀型急性脑梗死疗效及炎性指标的影响[J].中西医结合心脑血管病杂志,2016, 14(3):299-300.
[4]吴发宝,陈希元.黄芪药理作用研究综述[J].中药材,2004, 27(3):232-234.
[5]李淑芳.中药黄芪药理作用研究进展[J].湖北中医杂志,2013,35(6):73-75.
[6]左军,张文钊,胡晓阳,等.黄芪现代药理及临床研究进展[J].中医药信息,2014,31(1):111-112.
[7]刘德丽,包华音,刘杨.近5年黄芪化学成分及药理作用研究进展[J].食品与药品,2014,16(1):68-70.
[8]孙秀玲.黄芪药理作用机制的研究进展[J].中国处方药,2015,13(6):29-30.
[9]熊义涛,蒋启明,陶福华.夕阳春口服液中黄芪总皂苷的含量测定[J].中国医院药学杂志,1995,15(2):553.
[10]杜薇.黄芪中黄芪甲苷的提取及含量测定[J].时珍国药研究,1996,7(4):217.
[11]周晶.薄层扫描法测定六味补气胶囊中黄芪甲苷的含量[J].安徽医药,2013,17(1):37-38.
[12]罗丹,罗国安,陈丽,等.HPLC-ELSD测定得力生注射液的黄芪甲苷的含量[J].中药与临床,2014,5(6):21-23.
[13]李效宽,张艳海,冯天辉,等.在线固相萃取法结合电雾式检测器测定黄芪及其复方中黄芪甲苷的含量[J].分析化学,2014,42(12):1791-1796.
[14]葛德洲,邓祖磊.高效液相色谱-蒸发光散射法测定甜梦胶囊中黄芪甲苷含量[J].中国新药杂志,2015,24(5): 31-32.
[15]王希斌,钟小斌,黎渊弘,等.高效液相色谱法测定复方黄龙汤黄芪甲苷含量[J].医药导报,2013,32(8):1069-1071.
(收稿日期:2016-08-05 本文编辑:顾雪菲)

