分光光度法测定全钒液流电池钒电解液中磷含量的不确定度评定
刘月菊 张鹏 姜雪莲(大连博融新材料有限公司,辽宁 大连 116450)
分光光度法测定全钒液流电池钒电解液中磷含量的不确定度评定
刘月菊 张鹏 姜雪莲(大连博融新材料有限公司,辽宁 大连 116450)
本文叙述了铋磷钼蓝分光光度法测定全钒液流电池钒电解液中磷含量测定的不确定度评定方法。通过对溶液配制过程和仪器测定过程的各种不确定度影响因素的评估,建立了全钒液流电池钒电解液中磷含量测定的不确定度评定数学模型,从而为测定的准确性提供了理论基础。
不确定度;分光光度法;全钒液流电池,钒电解液;磷
全钒液流电池(Vanadium Redox Battery,缩写为VRB)[1],是一种液态氧化还原电池,也是一种新型清洁能源存储装置[2]。与其他类型电池相比,具有功率大、寿命长、可靠性高、操作和维修费用少等明显的技术优势[3],因此在储能行业具备无可估量的发展潜力,甚至有可能将改变未来的能源格局。
而钒电解液组成成份含量的高低、杂质的含量,以及添加剂的用量会严重影响电池中膜及电极的寿命。因此其成分检测方法,备受重视。
全钒液流电池电解液是硫酸、硫酸钒(V2(SO4)3)和硫酸氧钒(VOSO4)的混合溶液,在其中添加磷酸可以提高电池电解液的性能。因此准确测定钒电解液中的磷含量,对全钒液流电池的性能提高和商业推广十分重要。
使用铋磷钼蓝分光光度法测定电解液中的磷含量,快速、准确、高效的满足了电解液大规模生产的要求。而测量不确定度是与测量结果相关联的参数,它表征了可以合理的赋予被测对象的数值的分散程度。由于其具有广泛的应用性与实用性,因此对测量不确定度的评定非常重要。
本文主要针对铋磷钼蓝分光光度法测定钒电解液中磷含量的测量结果不确定度进行了分析和评估。
1 实验部分
1.1 原理
在硝酸介质中,磷酸中的磷与铋及钼酸铵生成络合物,以抗坏血酸还原成磷钼蓝,于分光光度计700nm处,测量其吸光度。
测量方法依据标准:GB∕T 24583.5-2009。
1.2 主要仪器设备
T6紫外-可见分光光度计和30mm比色皿;2mL移液管;50mL、500mL、1000mL容量瓶。
1.3 测定过程
磷标准使用溶液的配制:用2mL无分度移液管移取浓度为1000mg∕L的磷标准溶液至500mL容量瓶中,用纯水稀释定容,配成浓度为4.00mg∕L的磷标准使用液。
工作曲线的绘制:取7个50mL容量瓶,分别加入磷标准使用液0.00、1.00、2.00、4.00、6.00、8.00、10.00mL,加入5mL硝酸铋溶液,混匀,加入5mL磷显色溶液,混匀,加入5mL抗坏血酸溶液,加水定容至刻度,摇匀,室温放置10min,用30mm比色皿于分光光度计波长700nm处,测定其吸光度。
样品的测定:准确移取2.00mL钒电解液样品于1000mL容量瓶中,加入2mL硝酸,摇匀至溶液呈纯蓝色,加水定容至刻度;再分取2.00mL稀释后的溶液于50mL容量瓶中,加入1.5mL硝酸,摇匀,加入5mL硝酸铋溶液,混匀。后续步骤与工作曲线的绘制步骤一致。
1.4 计算公式
通过测定工作曲线可以得到一元线性回归方程:
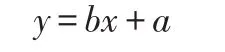
其中y:样品的校正吸光度A;
x:样品的含磷量(ug);
b:回归方程的斜率;
a:回归方程的截距。
计算钒电解液中磷浓度(mol∕L):

其中m:样品的含磷量(ug);
M:磷的相对分子质量(g∕mol);
V:取样体积(mL)。
2 建立数学模型,提出评估方法及程序
根据检测方法和数学模型分析,各输入量估计值彼此不相关,按不确定度传播规律,合成不确定表示为

式中:uc(c)—测定钒电解液中磷的合成标准不确定度;
uc磷—标准贮备液配制引入的不确定度;
uf稀释—标准溶液稀释过程引入的不确定度;
uV取样—样品测量取样引入的不确定度;
um拟合—校准曲线拟合引入的不确定度;
um样品—样品重复性引入的不确定度;
由于在与爱迪生竞争市政照明投标中失败,马克沁不得不在42岁那年远赴英伦重新创业。他无意中发现一种名叫“加特林排枪”的多管武器,有十来根枪管,需要四名射手摇动发射,威力不小,但极其笨重、射速也慢,作战性能不高。不久,马克沁在一次步枪体验中,右肩被射击时的后坐力震得轻一块、紫一块。有了这些经历后,马克沁决心把后坐力与“加特林排枪”的原理结合起来,发明一种新型快速发射的自动武器。
uM磷—磷的相对分子质量引入的不确定度。
根据铋磷钼蓝分光光度法测定钒电解液中磷含量的方法测定程序的操作顺序来逐一进行分析,计算每步骤的不确定度,最后将各不确定度分类进行合成。
3 实例分析给出钒电解液样品中磷含量测定结果
3.1 标准物质引入的不确定度
磷标准贮备液(GSB 04-1741-2004(a))的相对不确定度可由标准物质证书上得到:磷标准贮备液浓度为1000mg∕L,相对不确定度为0.7%,属正态分布,按k=2,置信概率p近似95%,推算出标准物质相对标准不确定度:

3.2 标准使用溶液的稀释配制过程的不确定度
稀释总磷标准贮备液时,用了2mLA级无分度移液管、500mLA级容量瓶,相对不确定度如表1。
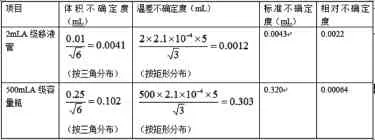
表1 标准使用溶液的稀释配制过程的不确定度
由上述两次稀释造成的标准使用溶液的稀释配制过程的相对不确定度为:
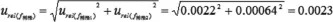
样品取样过程中,分别用了两次2mLA级无分度移液管、50mLA级容量瓶和1000mLA级容量瓶。其相对不确定度如表2。

表2 样品取样过程产生的不确定度
由上述各步骤造成的样品取样过程产生的相对不确定度为:

3.4 曲线拟合产生的不确定度
4.00 mg∕L的磷标准使用溶液通过稀释配制出浓度分别为0、2.0、4.0、8.0、12.0、16.0、20.0ug的7个标准溶液,由于校准标准溶液的不确定度与吸光度测量的不确定度比,小到可以忽略,因此,在采用最小二乘法拟合校正曲线时,计算得到磷的浓度的不确定度仅与吸光度的测量不确定度有关,同时也不考虑七个校准标准溶液之间的相关性。
对七个校准标准溶液各测量三次,共计21次,测量到的吸光度A数据如表3。

表3 磷工作曲线
拟合校准曲线方程为(A取三次平均值)

其中:y:样品的校正吸光度A;
x:样品的含磷量(ug);
b:回归方程的斜率;
a:回归方程的截距。
则吸光度测量的实验标准差为:
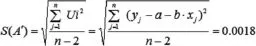
对被测样品测量三次,p=3,测得试液磷的浓度:m=29.02ug
其标准不确定度为:

其中:根据最小二乘法拟合公式
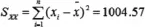
以上式中:i—下标,指第几个工作曲线溶液;
j—下标,指获得工作曲线的测量次数;
n—工作曲线的校准点测量次数,如工作曲线上有7个校准点,每点测量3次,则n=21;
x-——不同工作曲线溶液浓度的平均值。
此时,由曲线拟合带来的标准不确定度为
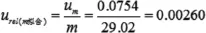
3.5 磷的相对分子质量引入的不确定度
因分子量引入的不确定度较小,可以忽略不计。
3.6 样品重复测量产生的不确定度
实验中对待测样品进行10次独立测量(n=10)得到测定结果如下表4所示,试样磷含量,单位mol∕L。

