UPLC-Q-TOF MS定性定量分析淫羊藿中淫羊藿苷类似物
杨宗林,赵 静
(澳门大学中华医药研究院,中药质量研究国家重点实验室,澳门 999078)
UPLC-Q-TOF MS定性定量分析淫羊藿中淫羊藿苷类似物
杨宗林,赵 静
(澳门大学中华医药研究院,中药质量研究国家重点实验室,澳门 999078)
利用超高效液相色谱-四极杆飞行时间质谱(UPLC-Q-TOF MS)法分析淫羊藿标准药材,并根据淫羊藿苷对照品的裂解规律及相关文献报道对朝鲜淫羊藿中淫羊藿苷类似物进行定性定量分析。采用加压溶剂提取系统提取淫羊藿标准药材中的有效成分,以液相色谱-质谱法进行分析,通过总结对照品淫羊藿苷和朝藿定C的质谱裂解规律,分析检测标准药材中的淫羊藿苷类似物。结果表明,从标准药材朝鲜淫羊藿中检测出42个淫羊藿苷类似物,它们主要集中在15%~70%乙腈洗脱部分,其中有4种化合物是首次发现。该方法通过检测一类标准品进而检测标准药材中的目标成分,可为淫羊藿其他药材中淫羊藿苷类似物的研究及先导药物开发提供必要依据。
超高效液相色谱-四极杆飞行时间质谱(UPLC-Q-TOF MS);淫羊藿;淫羊藿苷;黄酮
淫羊藿是我国常用的中药材,现代实验研究表明,淫羊藿苷是淫羊藿的主要活性成分之一,具有抗炎、抗氧化、抗凋亡和刺激血管生成等多种药理活性[1-7]。多数情况下,化学结构相似意味着化合物在生物合成上可能是同一起源,而在同种植物体内有固定生源合成途径,因此,淫羊藿药材内一定还有其他淫羊藿苷类似物。而这些淫羊藿苷类似物可能具有比淫羊藿苷更好的药理活性,因此,全面分析淫羊藿苷类似物对指导淫羊藿药材精细分离与后期药物开发具有重要意义。
2015版中华人民共和国药典记载,淫羊藿药材是小檗科植物淫羊藿(EpimediumbrevicornumMaxim)、箭叶淫羊藿(Epimediumsagittatum(Sieb.et Zucc.) Maxim)、柔毛淫羊藿(EpimediumpubescensMaxim)或朝鲜淫羊藿(EpimediumkoreanumNakai)的干燥叶。受制于淫羊藿药材的产量多寡,我国法定的国家食品药品生物制品质量最高检验和仲裁机构——中国食品药品生物制品检定院,目前仅能提供朝鲜淫羊藿(EpimediumkoreanumNakai)和淫羊藿(EpimediumbrevicornumMaxim)两种标准药材。
近年来,液相色谱-质谱联用技术发展迅速[8-10],不仅用于淫羊藿药材中化合物的定性分析[11-13],还用于淫羊藿不同种属、不同产地药材的全成分分析[14-17 ]。但是,集中针对淫羊藿苷类似物的研究却不多见。
本研究拟采用超高效液相色谱-四极杆飞行时间质谱法(UPLC-Q-TOF MS),以我国市场上的大宗主流品种——朝鲜淫羊藿为分析对象,通过加压溶剂提取技术富集淫羊藿苷类似物,分析淫羊藿标准药材中淫羊藿苷类似物的结构信息和相对含量,希望为淫羊藿药材中淫羊藿苷类似物的质量控制及药物开发提供理论依据。
1 实验部分
1.1 仪器与试剂
Ultimate 3000 UHPLC系统、加压溶剂萃取系统:美国Thermo Fisher公司产品;Impact HD Q-TOF质谱仪:德国Bruker公司产品。
淫羊藿苷(批号:110737-201516)、朝藿定C(批号:111780-201503)、淫羊藿标准药材(朝鲜淫羊藿EpimediumkoreanumNakai,批号:121032-201302):均购自中国食品药品检定研究院;乙腈、甲酸:均为色谱级,德国Merck公司产品;Milli-Q超纯水(电阻率为18 MΩ·cm):由美国Millipore公司的超纯水仪制得;其他试剂均为分析纯。
1.2 供试品溶液的制备
称取约0.3 g药材粉末,按质量比1∶1加入硅藻土,研磨混匀;用70%乙醇于加压溶剂提取系统120 ℃提取10 min,然后将提取液定容至50 mL,过0.22 μm微孔滤膜,待分析。
精密称取1.04 mg朝藿定C和1.02 mg淫羊藿苷对照品,用甲醇配制并稀释至浓度分别为0.34 mg/L和0.52 mg/L混合对照品溶液,待测。
1.3 实验条件
1.3.1 色谱条件 Waters Acquity UPLC BEH-C18色谱柱(2.1 mm×150 mm, 1.7 μm);柱温25 ℃;流动相:0.05%甲酸水溶液(A),乙腈(B);二元线性梯度洗脱:0~7.5 min(5%~20%B),7.5~30 min(5%~20%B),30~40 min(26%~30%B),40~70 min(30%~77%B),70~72 min(77%~100%B);流速0.3 mL/min;进样量1 μL。
1.3.2 质谱条件 电喷雾正、负离子模式,质量扫描范围m/z50~1 500,干燥气(N2)流速,10 L/min干燥气温度250 ℃,喷雾电压43.5 Pa,毛细管电压3 000 V。二级质谱采用Auto MS/MS模式,实验数据使用Data Analysis Version 4.2分析软件处理。
2 结果与讨论
2.1 对照品的裂解特征
将对照品溶液注入LC/MS仪器中,采集数据并得到二级碎片离子后,总结该类黄酮标准物质的裂解规律和特征碎片离子信息,结果列于表1。可知,对照品淫羊藿苷的保留时间为31.9 min,其准分子离子为m/z721.219 2 [M+HCOOH-H]-、m/z513.164 4 [M-Glu-H]-,说明失去7位葡萄糖;m/z409.118 6 [M-Rha-120-H]-是失去3位鼠李糖后,葡萄糖部分环裂(-C4H8O4)生成的,这与文献[14]报道一致;m/z367.109 5是失去7位葡萄糖和3位鼠李糖得到的母核碎片。在MS/MS模式下,打碎m/z513.164 0得到的碎片离子中,m/z366.100 6是均裂产生的苷元离子减氢的自由基负离子,m/z351.078 0是m/z366.101 2失去4′位CH3生成的,m/z323.083 2是m/z351.078 0失去C环4位CO得到的,此裂解规律与文献[14]报道一致。样品中保留时间为32.0 min化合物的碎片离子与对照品淫羊藿苷一致(表2),因此可确定该化合物为淫羊藿苷。
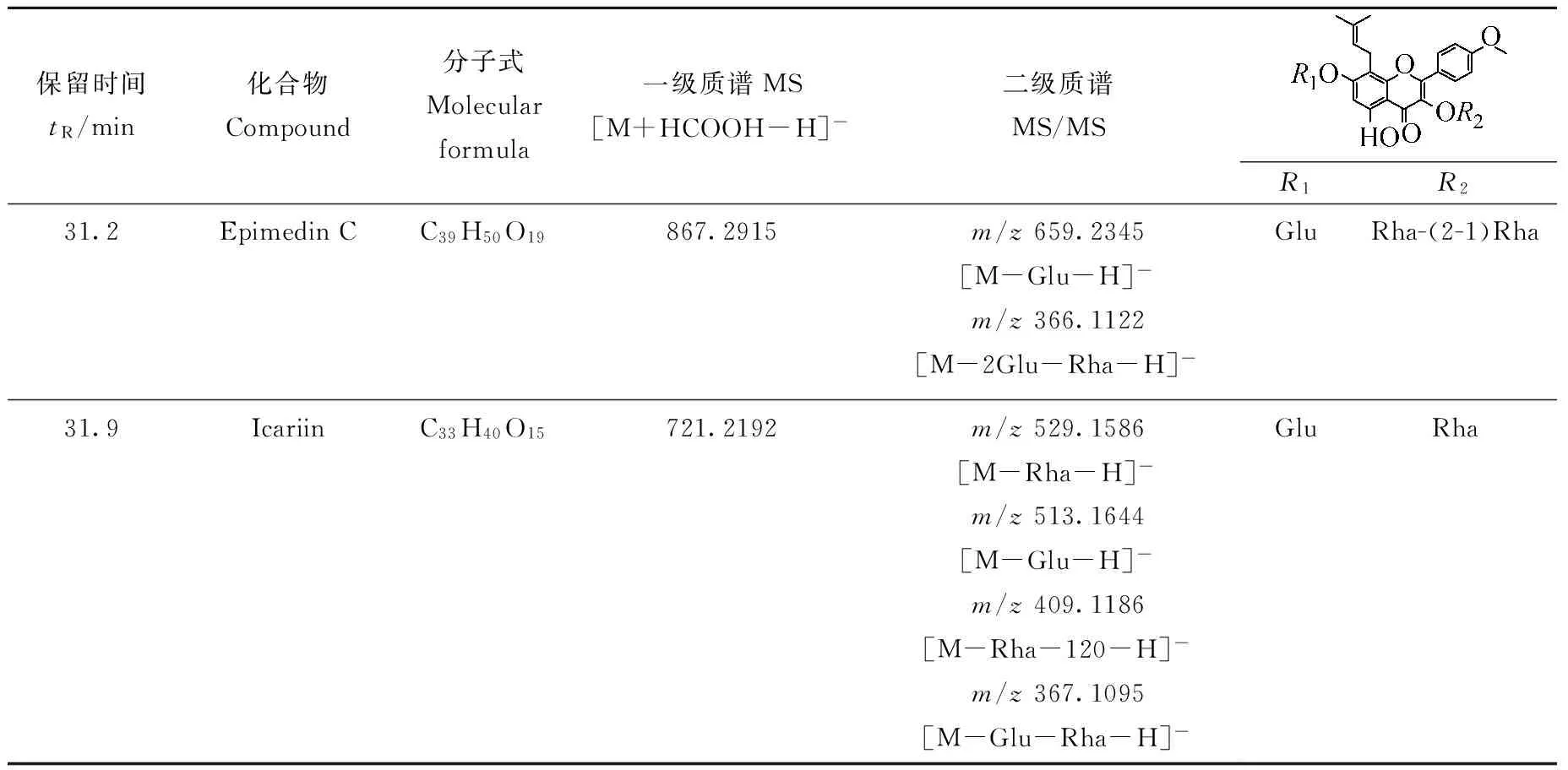
表1 负离子模式下,淫羊藿苷和朝藿定C的质谱信息Table 1 MS data of icariin and epimedin C in negative ion mode
对照品朝藿定C的保留时间为31.2 min,其准分子离子为m/z867.291 5 [M+HCOOH-H]-,m/z659.234 5 [M-Glu-H]-,说明失去7位葡萄糖;m/z366.112 2是在m/z659.234 5基础上失去3位的2个鼠李糖后得到的苷元离子减氢的自由基负离子(均裂),说明连在一起的2个糖基容易同时掉落。样品中保留时间为31.4 min化合物的碎片离子与对照品淫羊藿苷一致(表2),因此可确定该化合物为朝藿定C。
2.2 淫羊藿药材样品中的色谱峰定性分析
朝鲜淫羊藿药材样品的紫外检测谱图,负
离子模式基峰质谱图和42种化合物的提取离子流图示于图1。在负离子模式下,42种淫羊藿苷类似物的分子离子及ESI-MS/MS裂解产生的主要碎片离子列于表2。
根据文献[14-17]报道和对照品裂解规律可知,淫羊藿苷元为m/z367.109 5,提取m/z367.109 5离子可得出,在标准药材中,此类黄酮母核化合物主要集中在15%~70%乙腈洗脱部分(即图1方框内部分)。根据苷元均裂和异裂结果,共检出42种化合物,解析结果也列于表2。
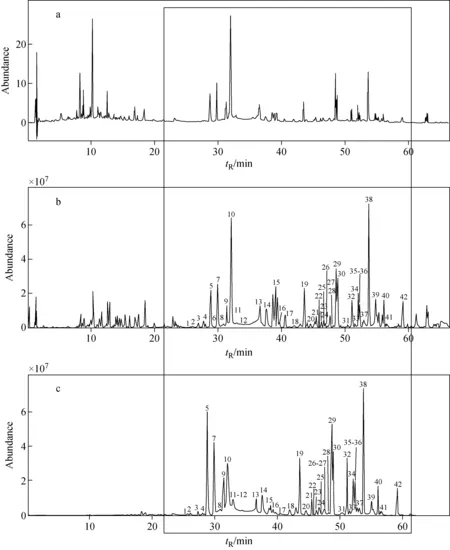
图1 朝鲜淫羊藿的UPLC紫外检测图谱(a)、负离子模式基峰质谱图(b)和基于淫羊藿苷元的MS提取离子流色谱图(c)Fig.1 UPLC couple with UV detection profile (a), BPC (b) and EIC (c) profiles in MS negative ion mode of Epimedium koreanum Nakai


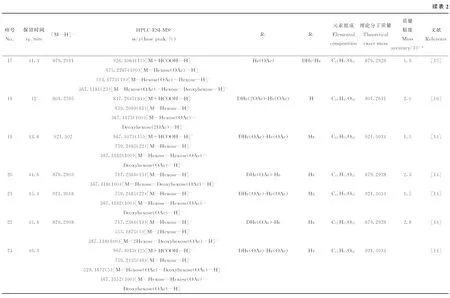
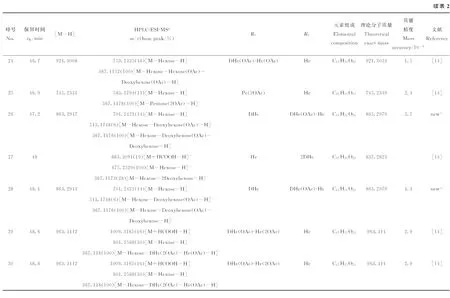

2.2.1 代表性化合物的解析 保留时间为29.9 min的化合物,在正、负离子模式下得到[M+H]+(m/z809.280 5)和[M-H]-(m/z807.263 7)离子,相对分子质量为808,m/z645.213 0 [M-Hexose-H]-为脱去7位己糖,m/z366.108 9 [M-Deoxyhexose-Pentose-Hexose-H]-为脱去3位脱氧己糖和戊糖得到的碎片。这与文献[17]报道的Epimedin B碎裂规律一致。
保留时间为52.3 min的化合物,在正、负离子模式下得到[M-H]+(m/z661.243 0)和[M-H]-(m/z659.232 8)离子,相对分子质量为660,m/z366.112 1 [M-2Deoxyhexose-H]-为7位脱去2个脱氧己糖得到的碎片,推测该化合物为2″-O-rhamnosyl icariside Ⅱ。
保留时间为53.7 min的化合物,在正、负离子模式下得到[M-H]+(m/z515.185 6)和[M-H]-(m/z513.176 3)离子,相对分子质量为514,m/z366.112 1 [M-2Deoxyhexose-H]-为7位脱去2个脱氧己糖得到的碎片,推测为Baohuoside Ⅰ。
2.2.2 新化合物的推断 根据质谱分析和SciFinder检索,在朝鲜淫羊藿中发现4种未见报道的化合物,即1、2、26和28号峰,这些化合物的结构还需后续的实验确认。
以1号峰为例,其保留时间为25.6 min,在正、负离子模式下得到[M-H]+(m/z985.356 3)和[M-H]-(m/z983.337 5)离子,相对分子质量为984,m/z1 029.342 5 [M+HCOOH-H]-、m/z675.228 7 [M-Deoxyhexose-Hexose-H]-、m/z367.117 8 [M-2Hexose-2Deoxy-hexose-H]-为m/z675.228 7脱去7位1个脱氧己糖和1个己糖得到的碎片,m/z352.095 8为继续脱去4′位甲氧基上的甲基后得到的碎片。推测该化合物结构为3位和7位上分别有1个脱氧己糖-己糖,搜索SciFinder未发现此类化合物,说明有可能为新化合物。其他3种新化合物的裂解规律同1号峰。
2.3 相对含量测定
以淫羊藿苷为对照品,采用外标一点法计算朝鲜淫羊藿中主要的淫羊藿苷类似物含量,结果列于表3。
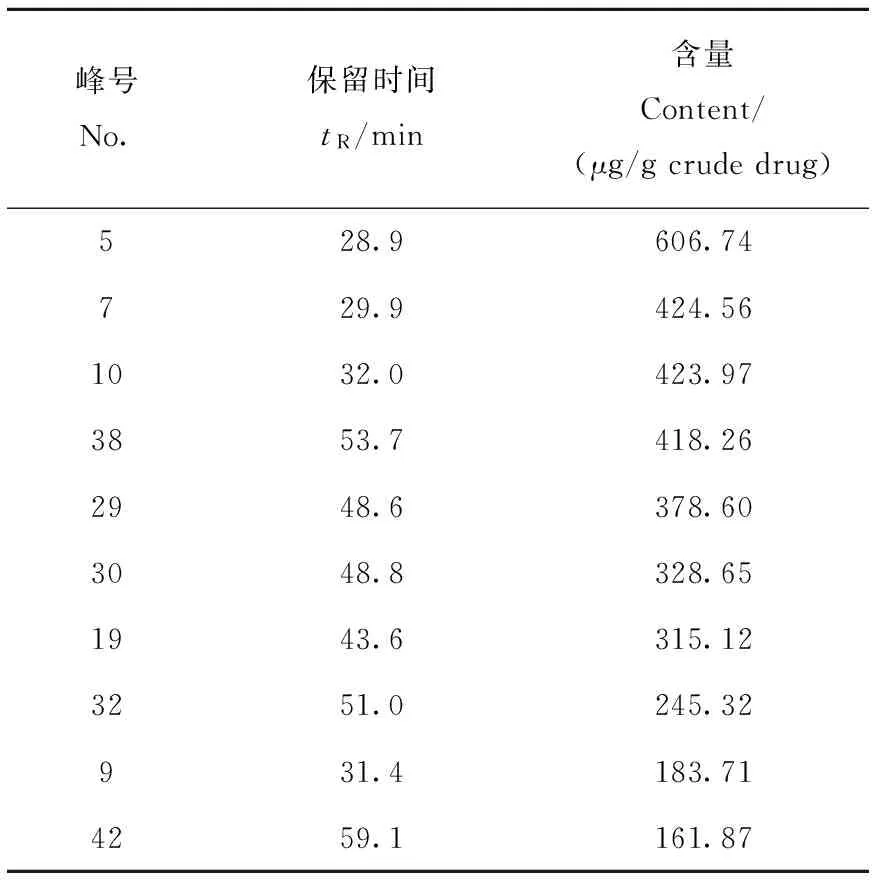
表3 朝鲜淫羊藿中主要的淫羊藿苷类似物含量Table 3 Contents of main icariin analogues in Epimedium koreanum Nakai
3 结论
本研究采用UPLC-Q-TOF MS法分析朝鲜淫羊藿中淫羊藿苷类似物,通过淫羊藿苷和朝藿定C的裂解规律并结合相关文献报道,检出朝鲜淫羊藿标准药材中42种淫羊藿苷类似物。通过分析淫羊藿化学成分可知,淫羊藿苷类似物成分在二级质谱中主要为丢失连接在黄酮骨架上的基团,如糖基、甲基等,而且7位糖基比3位糖基更容易失去,这可能是7位酸性较强[17];黄酮类化合物淫羊藿苷类似物在碎裂行为中均易失去C环的CO,上述特征可为淫羊藿苷类似物的鉴别提供准确、快速的方法。通过对淫羊藿标准药材中淫羊藿苷类似物的鉴定和相对含量的测定,可为发现淫羊藿中淫羊藿苷类似物提供理论依据。
[1] XUE L, JIANG Y, HAN T, et al. Comparative proteomic and metabolomic analysis reveal the antiosteoporotic molecular mechanism of icariin from Epimedium brevicornu maxim[J]. Journal of Ethnopharmacology, 2016, (192): 370-381.
[2] ZHANG Z K, LI J, YAN D X, et al. Icaritin inhibits collagen degradation-related factors and facilitates collagen accumulation in atherosclerotic lesions: a potential action for plaque stabilization[J]. International Journal of Molecular Sciences, 2016, 17(2): 169-175.
[3] LIAO J, LIU Y, WU H, et al. The role of icaritin in regulating Foxp3/IL17a balance in systemic lupus erythematosus and its effects on the treatment of MRL/lpr mice[J]. Clinical Immunology, 2016, (162): 74-83.
[4] JIANG M C, CHEN X H, ZHAO X, et al. Involvement of IGF-1 receptor signaling pathway in the neuroprotective effects of Icaritin against MPP+-induced toxicity in MES23.5 cells[J]. European Journal of Pharmacology, 2016, (786): 53-59.
[5] CUI Z, SHEN Z, YAN X, et al. In silico insight into potential anti-alzheimer’s disease mechanisms of icariin[J]. International Journal of Molecular Sciences, 2016, 17(1): 113-124.
[6] CHEN Y, HAN S, HUANG X, et al. The protective effect of icariin on mitochondrial transport and distribution in primary hippocampal neurons from 3×Tg-AD mice[J]. International Journal of Molecular Sciences, 2016, 17(2): 163-178.
[7] LI W X, DENG YY, LI F, et al. Icariin, a major constituent of flavonoids from Epimedium brevicornum, protects against cognitive deficits induced by chronic brain hypoperfusion via its anti-amyloidogenic effect in rats[J]. Pharmacology Biochemistry and Behavior, 2015, (138): 40-48.
[8] WU L, HAO H P, WANG G J. LC/MS based tools and strategies on qualitative and quantitative analysis of herbal components in complex matrixes[J]. Current Drug Metabolism, 2012, 13(9): 1 251-1 265.
[9] FERRERES F, MAGALHES S C, GIL-IZQUIERDO A, et al. HPLC-DAD-ESI/MSnprofiling of phenolic compounds fromLathyrusciceraL. seeds[J]. Food Chemistry, 2016, (214): 678-685.
[10]ZHOU G, WANG M, LI Y, et al. Comprehensive analysis of 61 characteristic constituents fromSiraitiaefructususing ultrahigh-pressure liquid chromatography with time-of-flight mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2016, (125): 1-14.
[11]WANG C, WU C, ZHANG J, et al. Systematic considerations for a multicomponent pharmacokinetic study ofEpimediiwushanensisherba: from method establishment to pharmacokinetic marker selection[J]. Phytomedicine, 2015, 22(4): 487-497.
[12]LI H F, GUAN X Y, YE M, et al. Qualitative and quantitative analyses of Epimedium wushanense by high-performance liquid chromatography coupled with diode array detection and electrospray ionization tandem mass spectrometry[J]. Journal of Separation Science, 2011, 34(12): 1 437-1 446.
[13]DING X P, WANG X T, CHEN L L, et al. On-line high-performance liquid chromatography-diode array detection-electrospray ionization-mass spectrometry-chemiluminescence assay of radical scavengers in Epimedium[J]. Journal of Chromatography A, 2011, 1 218(9): 1 227-1 235.
[14]ZHAO H Y, SUN J H, FAN M X, et al. Analysis of phenolic compounds in Epimedium plants using liquid chromatography coupled with electrospray ionization mass spectrometry[J]. Journal of Chromatography A, 2008, 1 190(1/2): 157-181.
[15]GUAN X Y, LI H F, YANG W Z, et al. HPLC-DAD-MSnanalysis and HPLC quantitation of chemical constituents in Xian-ling-gu-bao capsules[J]. Journal of Pharmaceutical and Biomedical Analysis, 2011, 55(5): 923-933.
[16]ZHAO H, FAN M, FAN L, et al. Liquid chromatography-tandem mass spectrometry analysis of metabolites in rats after administration of prenylflavonoids from Epimediums[J]. Journal of Chromatography B: Analytical Technologies in the Biomedical and Life Sciences, 2010, 878(15/16): 1 113-1 124.
[17]WANG Y, GUO Z, JIN Y, et al. Identification of prenyl flavonoid glycosides and phenolic acids inEpimediumkoreanumNakai by Q-TOF-MS combined with selective enrichment on “click oligo (ethylene glycol)” column[J]. Journal of Pharmaceutical and Biomedical Analysis, 2010, 51(3): 606-616.
Qualitative and Quantitative Analysis of Icariin Analogues inEpimediumkoreanumby UPLC-Q-TOF MS
YANG Zong-lin, ZHAO Jing
(StateKeyLaboratoryofQualityResearchinChineseMedicine,InstituteofChineseMedicalSciences,UniversityofMacau,Macao999078,China)
HerbEpimedii, the Chinese name is Yinyanghuo, is one of the most well-known and frequently used Chinese herbal medicine with tonic, antirheumatic and aphrodisiac effects. As the major bioactive constituents ofEpimediumplants, the flavonoids compounds showed androgenic, anti-oxidant, antidepressant, anti-osteoporosis, anti-apoptotic, stimulate angiogenesis, and anti-tumor activities. According to the relevant reports, various compounds have been identified inEpimediumspecies, and most of them were phenolic compounds including flavonoids and quinic acids. However, even though the standard crude drugEpimediumkoreanumhas a wildly application in quality control study, the quantity detection of icariin analogues ofEpimediumkoreanumis quietly rare. In this paper, qualitative and quantitative analysis of icariin analogues inEpimediumkoreanumNakai was performed by using ultra performance liquid chromatography and quadrupole time-of-flight mass spectrometry (UPLC-Q-TOF MS) technology based on icariin fragmentation and its analogues fragment pathway. In the experiment, the active components in HerbEpimediumkoreanumwere extracted by accelerated solvent extraction system with 70% acetonitrile at 120 ℃ for 10 min, and the chromatographic separation was used Waters Acquity UPLC BEH-C18 (2.1 mm×150 mm, 1.7 μm), mobile phase was 0.05% formic acid and acetonitrile, then analyzed by Q-TOF-MS. Furthermore, by analyzing the mass spectrometric fragmentations of Icariin and Epimedin C, the fragmentation rules of this kind of compound were summed up. To our knowledge, Icariin and Epimedin C obtained from were 3-O-, 7-O- or 3,7-di-O-glycosides, which frequently contained hexose, deoxyhexose, pentose. Therefore, based on the rules summarized the structures of unknown constituents of the icariin analogues inEpimediumkoreanumcould be detected. The results showed that Q-TOF MS provides abundant and stable information of fragment ions and 42 icariin analogues were identified, which were all eluted by 15%-70% acetonitrile. Among all these compounds, there are 4 compounds were firstly reported. This study is beneficial to discover icariin analogues inEpimediumand explore the leading compounds for drug development.
ultra performance liquid chromatography quadrupole time-of-flight mass spectrometry (UPLC-Q-TOF MS);Epimediumkoreanum; Icariin; flavonoid
2016-03-04;
2016-03-27
澳门大学科学研究基金项目(MYRG2015-00122)资助
杨宗林(1991—),女(汉族),山西人,博士研究生,从事中药活性成分与质量评价。E-mail: yb67535@umac.mo
赵 静(1982—),女(汉族),辽宁沈阳人,助理教授,博士,从事中药活性成分与质量评价。E-mail: jingzhao@umac.mo
O657.63
A
1004-2997(2017)01-0019-11
10.7538/zpxb.2017.38.01.0019

