基于聚合物添加剂谱库的缓冲盐中塑料药品包装材料难挥发可溶出物的快速分析方法研究
邢雪彬,张 云,孙姝琪,杜振霞*,秦孙星,董 彦
(1.北京化工大学 理学院,北京 100029;2.上海乐纯生物技术有限公司,上海 201600)
基于聚合物添加剂谱库的缓冲盐中塑料药品包装材料难挥发可溶出物的快速分析方法研究
邢雪彬1,张 云1,孙姝琪1,杜振霞1*,秦孙星2*,董 彦2
(1.北京化工大学 理学院,北京 100029;2.上海乐纯生物技术有限公司,上海 201600)
采用超高效液相色谱-四极杆飞行时间质谱(UPLC-QTOF-MS),结合基于UNIFI软件建立的174种聚合物添加剂的谱库,实现了塑料药品包装材料中难挥发可溶出物(Extractables)的快速筛查和准确定量。样品经氯仿萃取后,以甲醇和0.1%甲酸水溶液为流动相在CORTECS C18(2.1 mm×100 mm,1.6 μm)色谱柱上进行分离,在质谱电喷雾正离子模式下,UPLC-QTOF-MS进行筛查和定量分析。结果表明,浸泡60 d缓冲盐(25 ℃)中检出4种物质,利用谱库筛查确定其中1种物质是邻苯二甲酸二异癸酯(DIDP),采用外标法定量,测得其溶出量为1.98 μg/L;其余3种物质可通过精确质量数、MSE谱图等进行推断定性,利用结构与质量数相近的邻苯二甲酸二环己酯(DCHP)为内标进行定量,3种提取物的总含量为10.80 μg/L。利用DIDP进行回收率实验,5,10,20 μg/L 3个加标水平的回收率为90.1%~97.1%,相对标准偏差(RSD,n=6)不大于3.7%。该方法快速、准确、灵敏,适用于药品包装材料的安全性考察。
难挥发性可溶出物;药品包装材料;超高效液相色谱-四极杆飞行时间质谱(UPLC-QTOF-MS);谱库筛查
塑料由于其良好的化学稳定性和机械、加工性能,可方便而廉价地替代玻璃或金属等材料,因而在药品包装上应用广泛[1]。然而,塑料的性能是通过许多添加剂的引入而实现,其中部分添加剂显示出极端的遗传毒性、肝毒性或致畸性[2-5]。药品在直接接触包装材料的过程中,包装材料中残留单体、添加剂或降解产物可能会迁移、溶出到药品中,对人体造成危害。美国FDA(the US Food and Drug Administration)从2013年开始,药物召回事件呈爆炸式增长(仅2013年召回药物多达1 225种,而之前9年内,累计召回药物才2 217种),其中由于包装材料导致的药物污染成为召回事件发生的主要原因。基于此,FDA颁布了相关法规对包装材料溶出物进行控制。法规中明确指出,包装材料的制造商需对即将上市的包装材料进行药物相容性试验。因此,包装材料制造商必须要确保材料中迁移物的种类和含量不会对人体产生负面影响[6]。我国也在2015年发布了YBB 00032005-2015《钠钙玻璃输液瓶》等130项直接接触药品的包装材料和容器国家标准的公告(2015年第164号)[7],进一步加强了对药品包装材料的监管。
目前,有关包装材料中溶出物的检测方法主要包括气相色谱法(GC)[8]、高效液相色谱法(HPLC)[9]、气相色谱-质谱法(GC-MS)[10-12]及液相色谱-串联质谱法(LC-MS/MS)[13-15]。现有文献主要研究食品包装材料中溶出物,而药品包装材料溶出物分析鲜见报道。且这些方法只针对特定的某几类添加剂,而在实际的应用中,塑料药品包装材料中的可溶出物可能是未知、多种类的混合物。因此,建立一种快速筛查、检测分析塑料药品包装材料中所有难挥发可溶出物(Extractables)的方法,对保障药品安全有十分重要的意义[16-18]。
本文采用液液萃取作为前处理手段,利用超高效液相色谱-四极杆飞行时间质谱(UPLC-QTOF-MS)检测PBS缓冲盐溶液中的溶出物,利用实验室已建立的聚合物添加剂谱库[19]及Waters UNIFI软件对分析结果进行快速筛查和定量分析,建立了药品包装材料中难挥发可溶出物的快速测定方法,为包装材料厂商以及使用单位合理选择包装材料提供了参考数据。
1 实验部分
1.1 仪器与试剂
超高效液相色谱-四极杆飞行时间质谱(UPLC-QTOF-MS,Waters,美国),涡旋仪,Milli-Q Advantage A10 超纯水系统(Millipore,美国),MTN-2800D 氮吹仪(Auto Science,天津),SHA-BA水浴恒温振荡器(华普达,江苏),采集软件(UNIFI,Waters,美国)。
色谱纯和质谱纯甲醇(Fisher公司,美国),色谱纯甲酸,Milli-Q Ⅰ级超纯水,三氯甲烷(分析纯,北京化工厂),邻苯二甲酸二异癸酯(纯度99.5%,北京华威锐科化工有限公司),邻苯二甲酸二环己酯(纯度99%,北京华威锐科化工有限公司),氯化钠固体、磷酸二氢钾固体(纯度99.5%,阿拉丁,美国),磷酸氢二钠固体(纯度99%,阿拉丁,美国)。储液袋容积为500 mL,由上海乐纯生物技术有限公司提供。
1.2 实验方法
1.2.1 溶出试验PBS缓冲盐体系:1.00 L缓冲盐含NaCl 8.76 g,Na2HPO42.87 g,KH2PO40.31 g,PBS缓冲盐体系的pH值为7.5。
储液袋溶出实验:由储液袋硅胶管入口向储液袋中灌装250 mL PBS缓冲盐溶液,保证储液袋内表面均能接触到溶液,在水浴恒温振荡器中(25±1) ℃振荡60 d后待测。另将250 mL PBS缓冲盐溶液在玻璃瓶中相同条件下储存,作为空白对照。
1.2.2 样品前处理从储液袋中移取5 mL PBS缓冲盐溶液于15 mL具塞玻璃管中,加入2 mL蒸馏氯仿,涡旋10 min使其萃取充分后静置60 min。移去上层水相,有机相在40 ℃下氮吹至干,用0.5 mL甲醇-氯仿(体积比为9∶1)复溶后,进行UPLC-QTOF-MS检测。
1.2.3 UPLC-QTOF-MS条件利用UPLC-QTOF-MS检测实际样品,所用色谱和质谱条件与基于UNIFI软件建立的聚合物添加剂谱库条件完全相同。色谱条件:色谱柱:Waters CORTECS UPLC C18(2.1 mm×100 mm,1.6 μm);流动相:甲醇(A)-0.1%甲酸水溶液(B);梯度洗脱程序:0~3 min,60%~99% A;3~9 min,保持99% A;9~9.1 min,99%~60% A;9.1~11 min,60% A。流速0.3 mL/min,进样量5 μL。
质谱条件:电离模式:ESI+;检测模式:MSE;毛细管电压:3 kV;离子源温度:120 ℃;脱溶剂气温度:450 ℃;脱溶剂气流速:800 L/h;锥孔气流速:50 L/h;锥孔电压:30 V,碰撞能量为20~40 eV;LockSpray:m/z556.277 6,每30 s切换1次进行质量数的校正。
在实际分析时,按此色谱-质谱条件对样品进行检测后,利用谱库对分析结果进行处理,即可完成筛查和匹配定性。
1.2.4 标准溶液的配制准确称取一定量DIDP和DCHP,用蒸馏过的三氯甲烷溶解,配制成10.00 g/L单标储备液,再分别用甲醇稀释成一系列浓度梯度的标准溶液。每次使用前,现配现用。
2 结果与讨论
2.1 萃取溶剂的优化
由于大多数的包材添加剂均为弱极性化合物,且液液萃取的萃取溶剂应与水不互溶。本实验选取3种不同的萃取溶剂(甲苯、氯仿、乙酸乙酯)考察了在不同添加水平(5,10,20 μg/L)下对常见的薄膜添加剂DIDP的萃取效果。按照 “1.2.2 ”方法对样品进行处理,结果表明,以甲苯为萃取溶剂时,回收率为53.1%~58.0%;以乙酸乙酯为萃取溶剂时,由于乙酸乙酯部分溶于水,导致回收率进一步降低为51.1%~51.2%;而以氯仿为萃取溶剂时,回收率为90.1%~97.1%,因此选取氯仿为萃取溶剂。
2.2 聚合物添加剂谱库定性标准
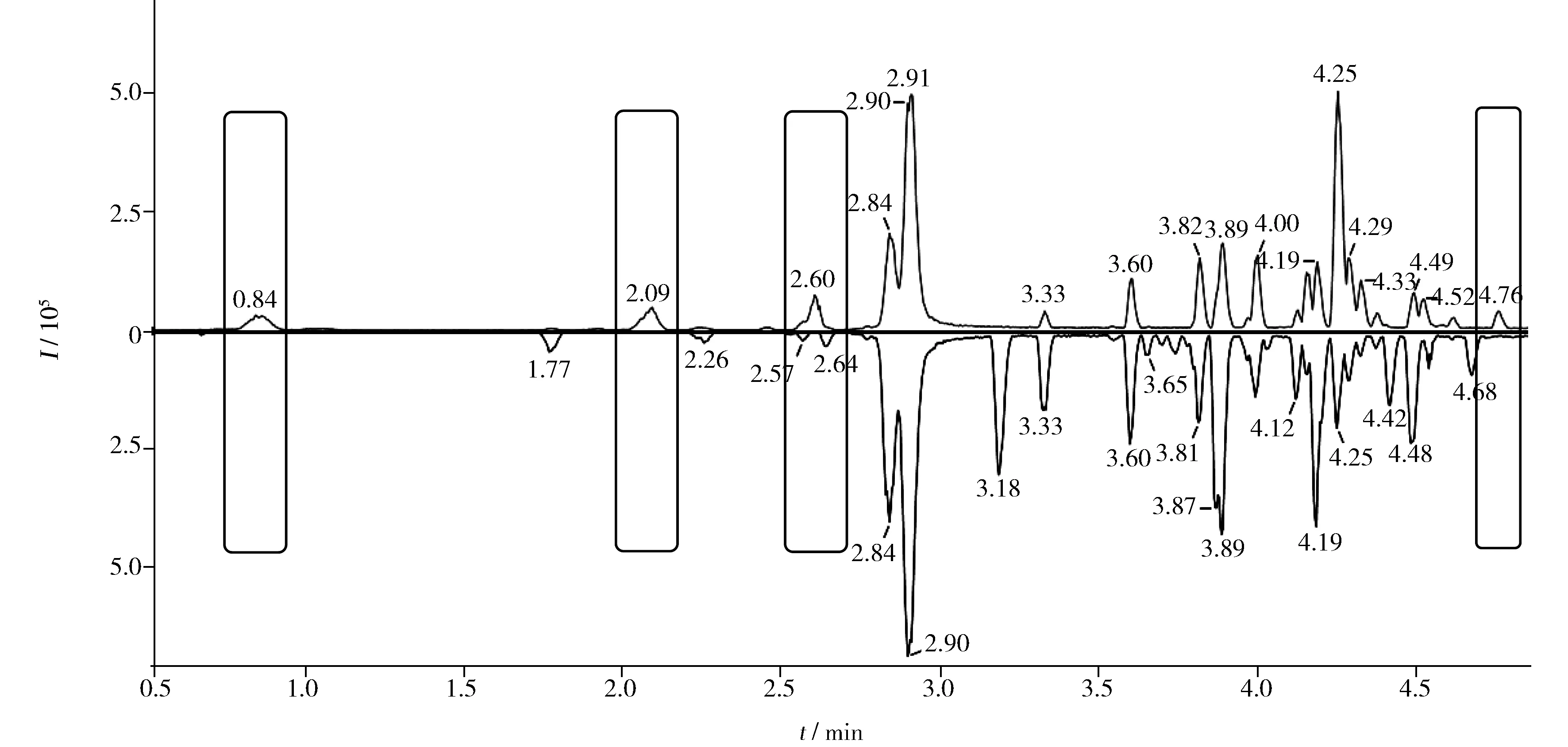
图1 实际样品(上)和空白样品(下)的色谱图Fig.1 Chromatograms of real(top) and blank(below) samples
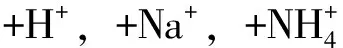
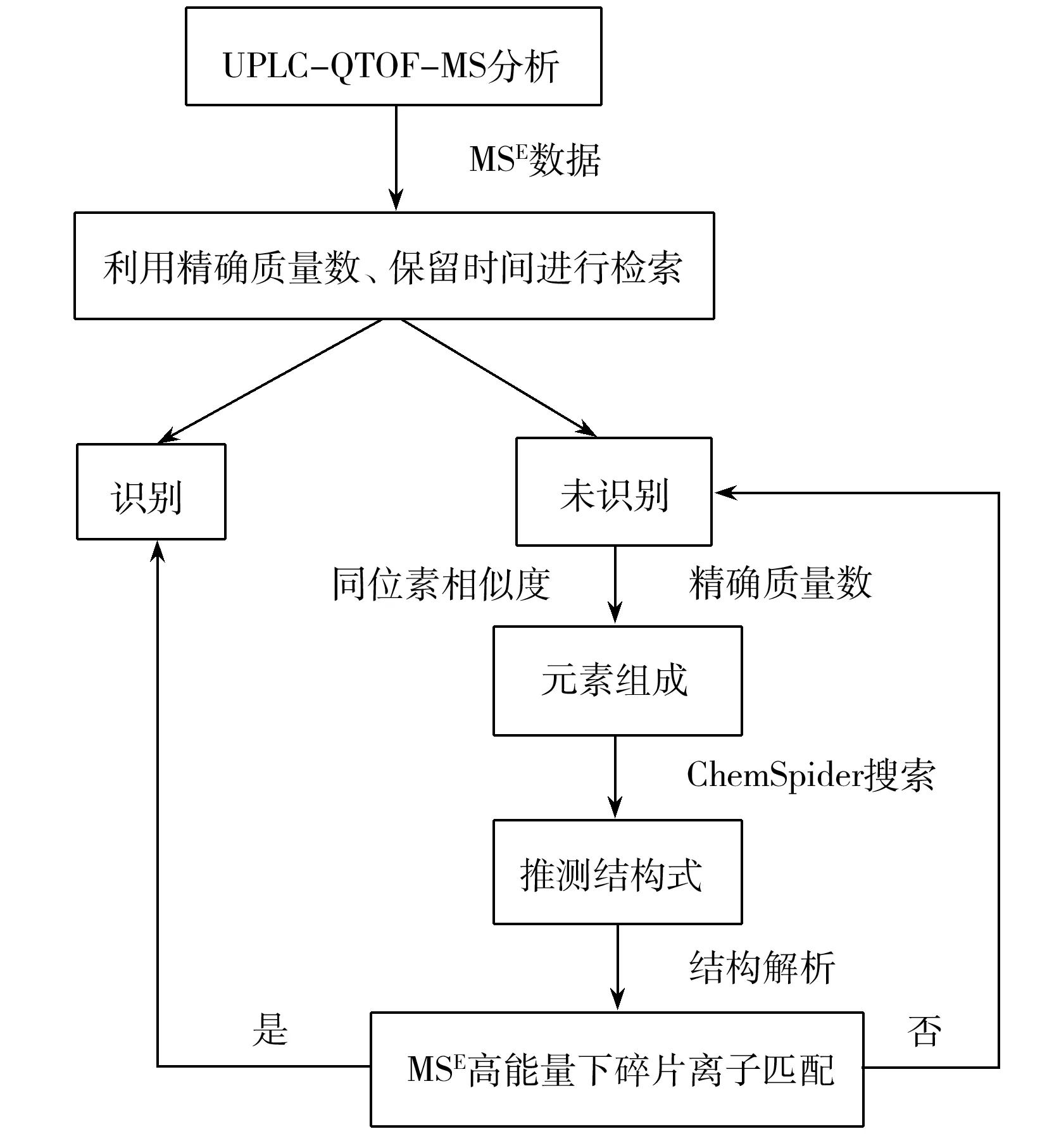
图2 识别目标和非目标塑料包材难挥发可溶出物的流程Fig.2 Workflow for identification targeted and non-targeted extractables
2.3 实际样品的快速筛查方法
用UPLC-QTOF-MS对500 mL储液袋储存的PBS缓冲盐和空白溶液进行测定(25 ℃,60 d)。为保证实验数据的准确性,平行实验6次。对比实际样品和空白样品的色谱图可知,实际样品中有区别于空白样品的4个明显的色谱峰(图1),说明该4个不同保留时间的色谱峰所代表的化合物源于PBS缓冲盐环境下包材的溶出。利用谱库对结果进行分析,结果表明,4.76 min是DIDP溶出。其他色谱峰的识别均不能通过谱库直接检索得到。
对于不能直接利用谱库识别的质荷比所代表的化合物,可利用UNIFI软件进行定性分析,定性流程如图2所示。首先基于精确质量数和同位素的匹配度来推测这些未知化合物的可能元素组成,以2.09 min色谱峰,m/z317.172 3为例。如图3,从MSE低能量的谱图中可知该质荷比所代表的化合物不含卤素,可能含有偶数个氮元素或不含氮元素,根据这些信息可利用“元素组成”功能推测其可能的元素组成,经分析推断出的元素组成为C17H26O4,且其质量数误差低于1 ppm,i-FIT 置信度接近100%,则可确定该化合物的元素组成为C17H26O4。然后利用该元素组成通过软件直接检索网络数据库ChemSpider来推测该元素组成的可能结构:首先选择相似类别或被研究的最多的化合物结构进行结构和谱图的匹配验证,假设此结构正确,利用 “碎片离子匹配” 工具自动判断MSE高能量通道下谱图的碎片离子是否归属于该化合物。如图4所示,MSE高能量通道下的m/z221.115 7是归属于m/z317.172 3的碎片离子(碎片断裂结构合理),多个碎片离子的归属即可确证该化合物结构,具体定性结果见表1。

图3 m/z 317.172 3的元素组成Fig.3 Elemental composition of m/z 317.172 3
2.4 线性关系、方法检出限与定量下限
利用标准品采用外标法定量DIDP;3种推断出的化合物由于无标准品,选择结构式与分子量均相近的DCHP(m/z330.418)对这3种难挥发可溶出物进行定量。取1 g/L的DIDP和DCHP标准溶液,用甲醇分别稀释成质量浓度梯度为1,2,5,10,20,50 μg/L的标准溶液。在聚合物添加剂谱库的色谱质谱条件下利用UPLC-QTOF-MS测定2种标准添加剂,以不同分子离子的响应面积比对相应目标物的浓度绘制标准曲线,以标准样品的3倍信噪比(S/N=3)对应的化合物浓度作为仪器的检出限(LOD),以S/N=10确定仪器的定量下限(LOQ)。结果表明,在1~50 μg/L质量浓度范围内,2种标准添加剂(DCHP,DIDP)呈良好线性,其线性方程分别为:y=1 911.7x+3 365.4(r=0.995),y=488.6x+2 751.2(r=0.994),LOD分别为0.3,0.5 μg/L,LOQ均为1.0 μg/L。表明此方法具有较高的检测灵敏度。
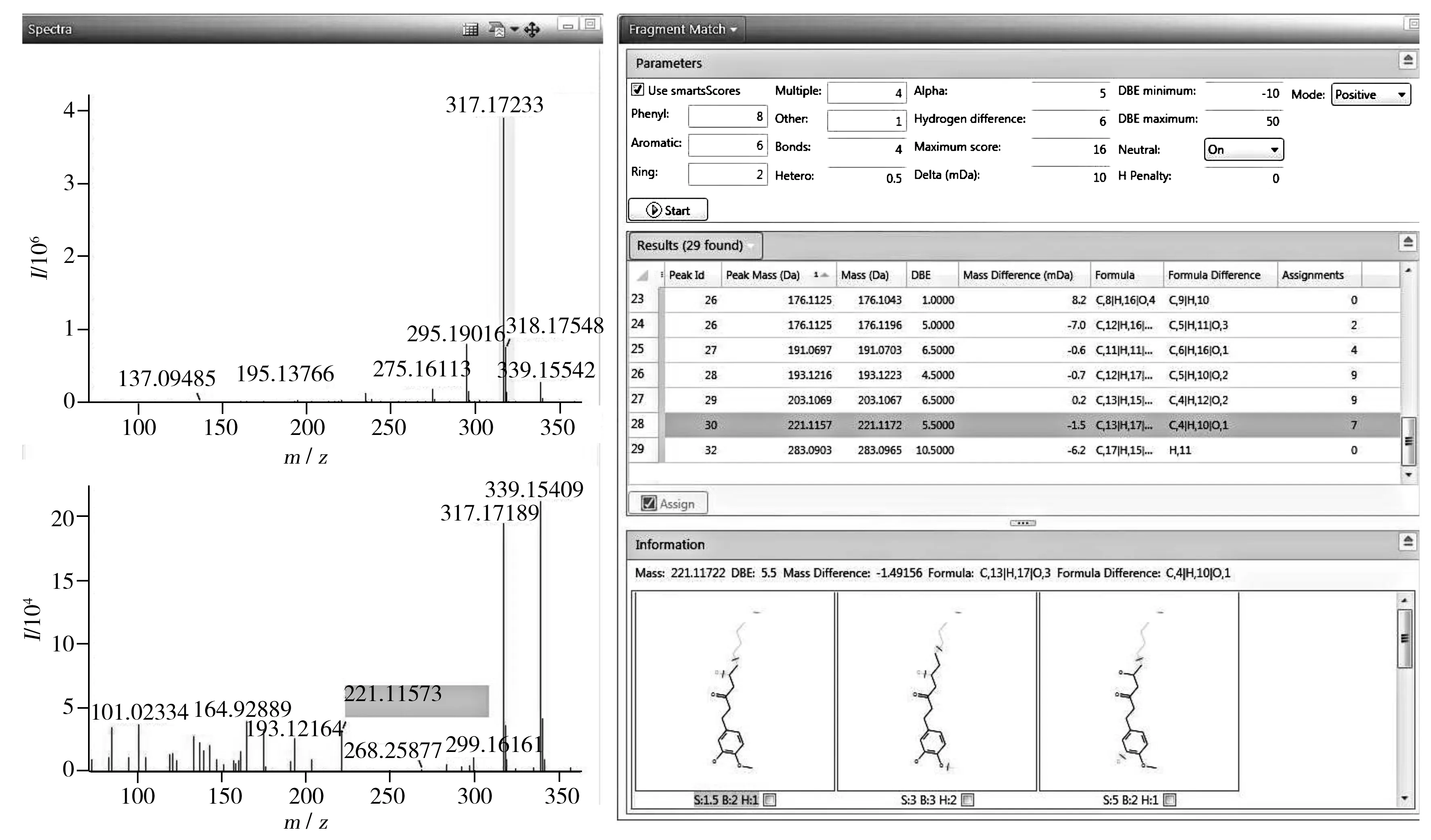
图4 m/z 317.172 3的碎片离子推测
2.5 回收率与精密度
为了考察方法的准确性和可靠性,取DIDP标准溶液采用标准加入法,在空白PBS缓冲盐溶液中加入5,10,20 μg/L 3个浓度水平,每个添加水平重复6次,在聚合物添加剂谱库的色谱-质谱条件下利用UPLC-QTOF-MS进行回收率的测定,并计算方法的精密度。结果表明,添加剂在上述3个浓度水平下的回收率分别为97.1%,90.1%,95.8%,相对标准偏差(RSD,n=6)分别为3.7%,3.6%,2.4%,完全满足实际分析的需求。
2.6 实际样品的定量
利用所建立的方法分析了在PBS缓冲盐溶液环境中药品包装材料的溶出物及其含量,具体筛查结果见表1。结果显示,包材中DIDP溶出浓度为1.98 μg/L,其余3种化合物浓度为3.24~3.97 μg/L,表明该药品包装材料在PBS缓冲盐溶液中的难挥发溶出物含量较低,符合法规要求。
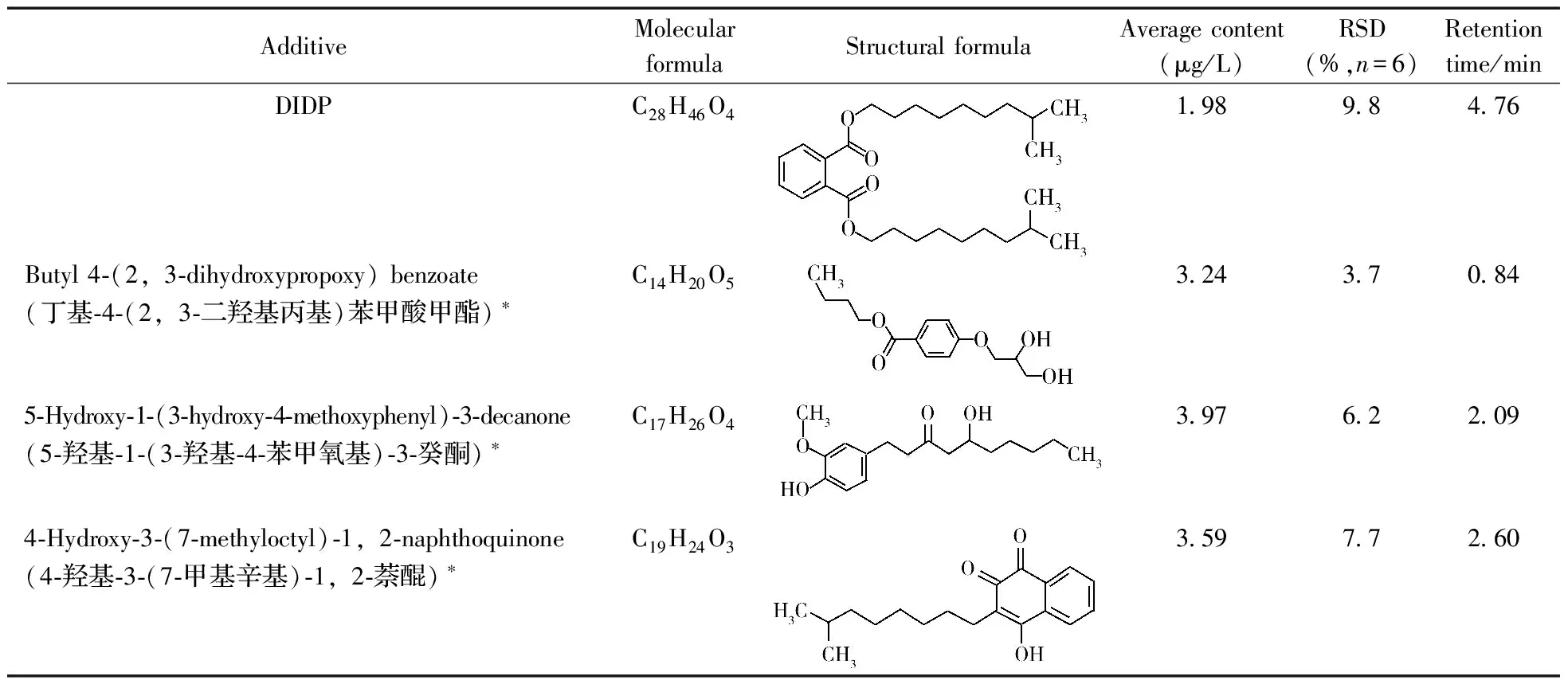
表1 实际样品的筛查结果
*there wasn't the compound in the library,the possible compound could be inferred by the mass spectra and UNIFI software,which was quantified by the standard of DCHP(谱库中不含该化合物,可通过质谱图及UNIFI软件推测其结构,并用DCHP定量)
3 结 论
本文建立了基于聚合物添加剂谱库的PBS缓冲盐中塑料药品包装材料难挥发可溶出物的快速分析方法。采用液液萃取对实际样品进行前处理,UPLC-QTOF-MS分析并利用基于UNIFI软件建立的聚合物添加剂谱库进行检测和筛查,对缓冲盐中的难挥发可溶出物进行定性和定量分析。本方法分析快速、选择性好、灵敏度高、定性定量准确,实现了药品包装材料中难挥发可溶出物的快速筛查与定量,对药品包装材料的安全性考察具有重要意义。
[1] Zhou J Q,Mei D.AdverseDrugReactionsJournal(周健丘,梅丹.药物不良反应杂志),2011,13(1):27-31.
[2] Petrusevski V,Jolevska S T,Ribarska J T,Chachorovska M,Petkovska A,Ugarkovic S.J.Pharm.Biomed.Anal.,2016,124:228-235.
[3] Wakankar A A,Wang Y J,Canova-Davis E,Ma S,Schmalzing D,Grieco J,Milby T,Reynolds T,Mazzarella K,Hoff E,Gomez S,Martin-Moe S.J.Pharm.Sci.,2010,99(5):2209-2218.
[4] Dakwara G R,Kapluna V,Kojukarova L,Gorenbeinb P,Schumacherb I,Kontorovichb D,Försterc C,Beit-Yannaia E,Stepenskya D.Int.J.Pharm.,2012,434(1):20-27.
[5] Pariente J L,Bordenave L,Jacob F,Bareille R,Baquey C,Le Guillou M.Eur.Urol.,2000,38:640-643.
[6] FDA.Comprehensive Regulatory Assistance,Guidance Documents(Medical Devices and Radiation-Emitting Products).[2016-6-9].http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/GuidanceDocuments/default.htm
[7] China Food and Drug Administration.No.164 Bulletin of the China Food and Drug Administration in 2015(国家食品药品监督管理总局.国家食品药品监督管理总局公告2015年第164号).[2016-06-11].http://www.sda.gov.cn/directory/web/WS01/images/MjAxNcTqtdoxNjS6xbmruOa4vbz+MS5kb2N4.docx.
[8] Ma K,Tang F S,He Y J,Liu F.J.Instrum.Anal.(马康,汤福寿,何雅娟,刘菲.分析测试学报),2011,30(3):284-288.
[9] Chen L W,Wu C S,Wang Y,Wu Y L,Wang L,Dong H,Wang B,Luo H Y.J.Instrum.Anal.(陈立伟,吴楚森,汪毅,吴玉銮,王莉,董浩,王斌,罗海英.分析测试学报),2016,35(2):206-212.
[10] Si X X,Zhang R,Zhang F M,Liu Z H,He P,Shen Q P,Su Z B,Zhu R Z.J.Instrum.Anal.(司晓喜,张蓉,张凤梅,刘志华,何沛,申钦鹏,苏钟璧,朱瑞芝.分析测试学报),2015,34(11):1240-1245.
[11] Liu J,Zhu R,Tian Y H,Li F G,Liu H X,Zhang X L,Quan X D,Jiang T.J.Instrum.Anal.(刘俊,朱然,田延河,李锋格,刘宏祥,张旭龙,全小盾,江涛.分析测试学报),2010,29(9):943-947.
[12] Gao J G,Sun Z J,Wang S,Zhang H W,Wang S F,Gao Y G,Gao J,Gao M,Cui H.J.Instrum.Anal.(高建国,孙卓军,王松,张鸿伟,王树峰,高永刚,高见,高玫,崔鹤.分析测试学报),2012,31(S1):127-131.
[13] Wang T J,Lin Q B,Song H,Li B.J.Instrum.Anal.(王天娇,林勤保,宋欢,李波.分析测试学报),2010,29(12):1153-1157.
[14] Ma Q,Li W T,Sun H Y,Yu H M,Li J R,Meng X S,Bai H,Wang X,Wang C.J.Instrum.Anal.(马强,李文涛,孙慧媛,于红梅,李晶瑞,孟宪双,白桦,王星,王超.分析测试学报),2013,32(1):133-137.
[15] Xiao X F,Wang J L,Chen T,Liu T F,He J,Deng H Y,Yang J J.J.Instrum.Anal.(肖晓峰,王建玲,陈彤,刘艇飞,何军,邓弘毅,杨娟娟.分析测试学报),2015,34(9):1021-1026.
[16] Khan M H,Hatanaka K,Sovannarith T,Nivanna N,Casas L C C,Yoshida N,Tsuboi H,Tanimoto T,Kimuraet K.BMC.Pharmacol.Toxicol.,2013,14(1):1145-1150.
[17] Jenke D.Pharm.Res.,2015,32(3):1105-1127.
[18] Xu X Y,He Y,Yin F,Yang H Y.J.Pharm.Anal.(徐晓月,何燕,殷飞,杨海燕.药物分析杂志),2013,(11):1979-1983.
[19] Zhang Y,Sun S Q,Xing X B,Du Z X,Guo Q Z,Yu W L.Anal.Chem.,2016,88(13):6749-6757.
Analysis of Nonvolatile Extractables in Pharmaceutical Packaging Materials in Buffered Saline Based on Polymer Additive Library
XING Xue-bin1,ZHANG Yun1,SUN Shu-qi1,DU Zhen-xia1*,QIN Sun-xing2*,DONG Yan2
(1.College of Science,Beijing University of Chemical Technology,Beijing 100029,China; 2.Shanghai LePure Biotech Co.,Ltd,Shanghai 201600,China)
A rapid method for the determination of extractables in pharmaceutical packaging materials was developed by ultra-performance liquid chromatography-quadrupole time-of-flight-mass spectrometry(UPLC-QTOF-MS) based on UNIFI software and a polymer additive library.The samples were extracted with chloroform,and then the extractables were separated on a CORTECS C18(2.1 mm×100 mm,1.6 μm) column using a binary solvent system composed of methanol and 0.1% formic acid water solution.Screening and quantitative analysis were accomplished by UPLC-QTOF-MS under positive electrospray ion mode.The results showed that four extractables were detected in buffered saline(25 ℃,60 days).Diisodecyl phthalate(DIDP) was identified by library searching and quantitated by external standard method with a concentration of 1.98 μg/L.The other three extractables were inferred and identified by accurate mass and MSE spectra match,and they were quantitated with dicyclohexyl phthalate(DCHP).The total content of the three compounds was 10.80 μg/L.The recovery analysis was carried out to evaluate the method with DIDP.The results indicated that the recoveries of DIDP ranged from 90.1% to 97.1% with relative standard deviation(RSD) no more than 3.7%(n=6) at three spiked concentration levels(5,10,20 μg/L).The method was rapid,accurate and sensitive,and was suitable for the safety investigation on pharmaceutical packaging materials.
nonvolatile extractables;pharmaceutical packaging material;ultra performance liquid chromatography tandem quadrupole-time-of-flight mass spectrometry(UPLC-QTOF-MS);library searching
10.3969/j.issn.1004-4957.2017.01.004
2016-05-18;
2016-07-15
国家质量监督检验检疫总局(201510024)
*通讯作者:杜振霞,教授,研究方向:复杂基质中痕量物质分析方法研究,Tel:010-64433909,E-mail:duzx@mail.buct.edu.cn 秦孙星,工程师,研究方向:药品包装材料检测分析,Tel:021-57791703,E-mail:qinsunxing@lepurechina.com
O657.63;F767.6
A
1004-4957(2017)01-0025-06

